Komplexes regionales Schmerzsyndrom
| Klassifikation nach ICD-10 | |
|---|---|
| G90.5- | komplexes regionales Schmerzsyndrom, Typ I (seit 2019) (bis 2018: M89.0) |
| G90.6- | komplexes regionales Schmerzsyndrom, Typ II (seit 2019) (bis 2018: G56.4 für CRPS II der oberen Extremität, G57.8 für CRPS II der unteren Extremität) |
| ICD-10 online (WHO-Version 2019) | |
Das komplexe regionale Schmerzsyndrom (Complex regional pain syndrome, CRPS) gehört zu den neurologisch-orthopädisch-traumatologischen Erkrankungen. Der international einheitliche Begriff ersetzt zunehmend die früher gebräuchlichen und synonym verwendeten Bezeichnungen Reflexdystrophie, Morbus Sudeck, Sudeck-Dystrophie, Algodystrophie und sympathische Reflexdystrophie.
Die Krankheit ist dadurch gekennzeichnet, dass es nach äußerer Einwirkung (z. B. Traumen, Operationen und Entzündungen) über längere Sicht zu einer Dystrophie und Atrophie von Gliedmaßenabschnitten kommt. Als Symptome treten Schwellungen, Schmerzen, Durchblutungsstörungen, Überempfindlichkeit gegenüber Berührungen und Hautveränderungen auf, im weiteren Verlauf auch Funktionseinschränkungen in Form von Schwäche und eingeschränkter Beweglichkeit. Die Erkrankung tritt bei Erwachsenen öfter an den oberen Gliedmaßen als an den unteren auf; besonders oft nach distalen Radiusfrakturen. Frauen sind häufiger betroffen.
Bei noch nicht zufriedenstellend geklärtem Entstehungsmechanismus wird eine neuronale Entzündungsreaktion, sowohl peripher als auch zentral, in Kombination mit einer kortikalen Reorganisation als Ursache diskutiert. Die Therapie erfordert eine Zusammenarbeit mehrerer Fachdisziplinen.
Das CRPS wurde lange Zeit vorwiegend mit Schmerzmitteln und Nervenblockaden behandelt. 2013 ergab eine umfangreiche Datenanalyse der Cochrane Collaboration eine unzureichende Wirksamkeit der häufig eingesetzten Sympathikusblockade. Seitdem wurden die Therapieempfehlungen erheblich umgestellt. Das warme CRPS, das mit klassischen Entzündungserscheinungen einhergeht, wird vorwiegend antientzündlich behandelt mittels einer Kortison-Stoßtherapie. Das kalte CRPS, welches mehr durch Sensibilitätsstörungen gekennzeichnet ist, wird bevorzugt mit Antineuropathika wie Gabapentin oder Pregabalin behandelt. Zusätzlich ist in allen Fällen von CRPS frühzeitig intensive Physiotherapie und Ergotherapie einzusetzen, um die Schwellungen abzubauen, pathologische Bewegungsmuster und Fehlhaltungen zu kompensieren, schmerzhafte Bewegungsmuster zu reduzieren und die normale Sensibilität wiederherzustellen.[1]
Die Prognose ist stark abhängig vom Zeitpunkt des Behandlungsbeginns. Eine vollständige Heilung ist meist nur bei frühzeitigem Behandlungsbeginn möglich. Häufig werden die Symptome allerdings erst mehrere Monate nach Ausbruch der Erkrankung, in einem späten Stadium, dem richtigen Krankheitsbild zugeordnet, was in der überwiegenden Mehrzahl der Fälle zu lebenslangen Beeinträchtigungen durch Schmerzen und Funktionseinschränkungen führt.
Pathogenese[Bearbeiten | Quelltext bearbeiten]
Die Pathogenese des CRPS ist noch nicht vollständig geklärt. Es wird ein gestörter Heilungsverlauf des betroffenen Gewebes vermutet. Bemerkenswert ist, dass das Auftreten eines CRPS und dessen Schweregrad nicht vom Schweregrad der Ausgangsverletzung abhängt. Folgendes Entstehungsmodell wird aktuell diskutiert: Es kommt zu einer Entzündungsreaktion, bei der Entzündungsmediatoren (Substanz P, CGrP) ausgeschüttet werden, die nicht mehr in ausreichender Menge abgebaut werden und somit die neurogene Entzündungsreaktion verlängern. Diese Ausschüttung der genannten entzündungsvermittelnden Substanzen (Mediatoren) erfolgt auch im zentralen Nervensystem (ZNS), wodurch es zu einer Sensibilisierung der zentralen schmerzverarbeitenden Nervenzellverbände (Neuron) kommt. Die Veränderungen der Durchblutung und Schweißneigung der Haut kommen durch eine zentral bedingte Fehlfunktion des Sympathikus zustande, wobei der genaue Mechanismus hierbei noch im Dunkeln liegt. Durch die Verengung der Gefäße (Vasokonstriktion) und die Ausbildung von arterio-venösen Shunts[2] kommt es zu einer Unterversorgung des Gewebes mit Sauerstoff (Hypoxie), wodurch vermehrt saure Abbauprodukte anfallen (Azidose), die zu einer Schmerzverstärkung beitragen.
Wie beim Phantomschmerz kommt es auch beim CRPS zu einer kortikalen Reorganisation. Dabei handelt es sich um eine Veränderung der einzelnen Repräsentationsbereiche (z. B. der Hand) in der Großhirnrinde, wodurch auch die Ausweitung der Schmerzen über ein bestimmtes Nervenversorgungsgebiet hinaus erklärt werden kann. Es bestehen Hinweise auf eine genetische Disposition.
Die Rolle psychischer Faktoren bei der Entstehung des CRPS wurde lange Zeit kontrovers diskutiert, die Existenz einer sogenannten „CRPS-Persönlichkeit“ wird mittlerweile weitgehend abgelehnt. Jedoch konnten mehrere Studien eine Häufung von belastenden Lebensereignissen vor Auftreten der Erkrankung und eine erhöhte Rate von posttraumatischen Belastungsstörungen nachweisen.[3][4][5] Auch tritt bei CRPS-Patienten gehäuft ein depressives Syndrom auf. Bei diesen Patienten ist eine psychologische Mitbehandlung sinnvoll.[6]
CRPS Typ I nach distaler Radiusfraktur[Bearbeiten | Quelltext bearbeiten]
Die Distale Radiusfraktur ist das häufigste einem CRPS vorausgehende Trauma. Mit einer Inzidenz von 7 % bis 37 %[7] ist es eine häufige Komplikation dieser Fraktur. Allerdings nimmt die Häufigkeit in den letzten 40 Jahren kontinuierlich ab. Der in gleichem Maße ansteigende Anteil an operativ stabilisierten Radiusfrakturen legt den Schluss nahe, dass hierdurch dem CRPS teilweise vorgebeugt werden kann. Es gilt als sicher, dass einige Faktoren die Entstehung eines CRPS begünstigen. Hier sind vor allem zu nennen: Instabile Retention, sekundäre Verschiebung, mehrfache Repositionsversuche und einschnürende, die Beweglichkeit der Finger einschränkende Gipsverbände.
Am häufigsten sind Frauen nach der Menopause betroffen. Die Angaben schwanken hierzu zwischen etwa 70 % bis 90 %. Zudem erleidet diese Patientengruppe auch am häufigsten Radiusfrakturen.
Unterteilung[Bearbeiten | Quelltext bearbeiten]
- CRPS Typ I (M. Sudeck): Trauma ohne Nervenverletzung
- CRPS Typ II (Kausalgie): Trauma mit Nervenverletzung
Stadieneinteilung[Bearbeiten | Quelltext bearbeiten]

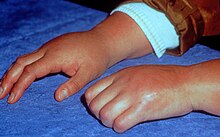
Die Krankheit kann unbehandelt einen chronischen Verlauf nehmen. Es kann eine Einteilung nach dem zeitlichen Verlauf als auch nach Symptomen erfolgen.
Zeitlicher Verlauf[Bearbeiten | Quelltext bearbeiten]
- Akute entzündliche Schwellung (0–3 Monate) mit lokalen Entzündungszeichen (Schwellung, Rötung, Wärme, Schmerz, Funktionsstörung)
- Dystrophie (drei bis sechs Monate) mit Gelenkversteifung
- Atrophie (sechs bis zwölf Monate) = Endstadium (keine Funktion mehr)
Diese Einteilung wurde von Paul Sudeck zu Beginn des 20. Jahrhunderts eingeführt. Sie ist mittlerweile jedoch sehr umstritten, da viele Fälle einen abweichenden Krankheitsverlauf zeigen. In der aktuellen CRPS-Forschung spielt die Stadieneinteilung kaum noch eine Rolle.
Symptome[Bearbeiten | Quelltext bearbeiten]
Die Symptome sind anfangs unspezifisch, so dass die Diagnosestellung verzögert werden kann. Ebenso ist der Krankheitsverlauf individuell stark unterschiedlich, wobei von der spontanen Totalremission bis zur Progression mit nicht unerheblicher Einschränkung der Lebensqualität alle Abstufungen zu finden sind.
Motorische Störungen[Bearbeiten | Quelltext bearbeiten]
Bei mehr als drei von vier Patienten besteht eine Schwäche der betroffenen Extremität, die im Akutstadium durch Schmerzen und das Ödem bedingt ist, im chronischen Stadium durch Kontrakturen und Fibrosen. Bei der Hälfte der Patienten besteht ein Tremor und bei jedem Dritten kommt es zu Myoklonien.
Sensorische Störungen[Bearbeiten | Quelltext bearbeiten]
Bei vielen Patienten kommt es zur sogenannten Hyperalgesie, also zu einer stark erhöhten Schmerzempfindlichkeit meist auf mechanische Reize oder zur Allodynie, d. h. Schmerzen bei einer eigentlich nicht schmerzhaften Empfindung (z. B. Bestreichen der Haut mit einem Wattebausch). Bei ca. drei von vier Patienten besteht ein Ruheschmerz, der individuell sehr unterschiedlich ausfällt (bzw. brennend oder prickelnd). In selteneren Fällen kommt es zu einer Taubheit oder einem Fremdheitsgefühl der betroffenen Extremität.
Autonome Störungen[Bearbeiten | Quelltext bearbeiten]
Fast immer kommt es im Anfangsstadium zu Rötung, Schwellung (Ödem) und Erhitzung der Haut (Zeichen der Entzündung), die sich bei längerem Fortbestehen (Chronifizierung) zu einer Blaufärbung und Kältegefühl verändern. In der Hälfte der Fälle besteht eine erhöhte Schwitzneigung (Hyperhidrose).
Veränderungen im Röntgenbild[Bearbeiten | Quelltext bearbeiten]
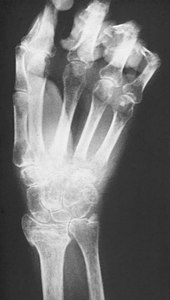
Beim Übergang in das chronische Stadium einige Monate nach Beginn der Erkrankung sind im Röntgenbild meist fleckige Aufhellungen zu erkennen, die durch eine Verringerung des Kalksalzgehaltes im Knochen bedingt sind, wodurch dieser durchlässiger für Röntgenstrahlung wird. Die Entkalkung der Knochen nimmt mit fortschreitender Chronifizierung zu, bis das Bild einer hochgradigen Inaktivitätsosteoporose vorliegt.
Trophische Störungen[Bearbeiten | Quelltext bearbeiten]
In vielen Fällen kommt es im akuten Stadium zu einem vermehrten Nagel- und Haarwachstum, im chronischen Stadium wechselt es ins Gegenteil. In schweren Fällen kann es zum Abbau der Muskulatur (Atrophie) mit der Ausbildung von Kontrakturen und folglicher Bewegungseinschränkung kommen.
Diagnostik[Bearbeiten | Quelltext bearbeiten]
Die Diagnose des CRPS erfolgt primär nach klinischen Gesichtspunkten. Apparative Verfahren (z. B. Röntgenbild, Szintigraphie) können zusätzliche Informationen liefern, jedoch ein CRPS weder beweisen noch ausschließen.[8]
Klinische Diagnosestellung[Bearbeiten | Quelltext bearbeiten]
Die klinische Diagnosestellung erfolgt heute nach den revidierten Kriterien der IASP (International Association for the Study of Pain), die 2003 in Budapest erstellt wurden und daher auch als „Budapest-Kriterien“ oder „Harden-Bruehl-Kriterien“ (nach den Autoren der Veröffentlichung) bezeichnet werden. Hierzu werden die Symptome des CRPS in vier Kategorien eingeteilt. Anamnestisch (in der Krankengeschichte) muss aus drei der vier Kategorien jeweils ein Symptom vorhanden sein, bei der Untersuchung müssen Symptome aus zwei Kategorien nachweisbar sein.
| Modifizierte Budapest-Kriterien | |||
| A | Anhaltender Schmerz, der durch das Anfangstrauma nicht mehr erklärt wird. | ||
| B | mindestens ein Symptom aus 3 der 4 folgenden Kategorien sowohl in
der Anamnese als auch zum Zeitpunkt der Untersuchung: | ||
| 1. | Hyperalgesie (Überempfindlichkeit gegenüber Schmerzreizen) oder | Hyperästhesie (Überempfindlichkeit gegenüber Berührungen) oder | Allodynie |
| 2. | Asymmetrie der Hauttemperatur oder | Veränderung der Farbe | |
| 3. | Asymmetrie im Schwitzen oder | Ödem | |
| 4. | reduzierte Beweglichkeit, Dystonie oder | Tremor, „Paresen“, Schwäche oder | Veränderungen von Haar- oder Nagelwachstum. |
| C | Eine andere Erkrankung erklärt die Symptome nicht hinreichend. | ||
Für die klinische Diagnose eines CRPS müssen alle Punkte A, B und C erfüllt sein.[9]
Labor[Bearbeiten | Quelltext bearbeiten]
Routine-Laborwerte zeigen beim CRPS keine Auffälligkeiten. Laboruntersuchungen sind nur zum Ausschluss anderer Erkrankungen angezeigt (z. B. Infektion).
Röntgenbild[Bearbeiten | Quelltext bearbeiten]
Im Röntgenbild zeigen sich klassischerweise gelenknahe fleckförmige Entkalkungen. Diese treten jedoch frühestens zwei Monate nach Erkrankungsbeginn auf und können auch völlig fehlen. In späteren Stadien sind die Veränderungen nicht sicher von anderen Knochenatrophien unterscheidbar. Daher spielt das Röntgenbild nur eine untergeordnete Rolle in der Diagnostik.
Kernspintomogramm[Bearbeiten | Quelltext bearbeiten]
Im Kernspintomogramm können Weichteilödeme, Hautverdickungen, Gelenkergüsse und später auch fibrotische Veränderungen sichtbar sein. Die Sensitivität ist jedoch gering, d. h., es werden viele CRPS-Fälle nicht erkannt. Die Bedeutung des Kernspintomogramms liegt daher hauptsächlich in der Differentialdiagnose (Ausschluss anderer Erkrankungen).
Skelettszintigrafie[Bearbeiten | Quelltext bearbeiten]
Der Wert der Skelettszintigrafie liegt darin, dass bereits relativ frühzeitig (maximale Sensitivität nach etwa sechs Wochen) charakteristische Veränderungen (bandförmige gelenknahe Mehrspeicherungen) sichtbar sind. Sensitivität und Spezifität sind besser als bei den vorgenannten Verfahren, genügen aber ebenfalls nicht für eine sichere Diagnosestellung. Im Krankheitsverlauf (nach mehr als 12 Wochen) nimmt der diagnostische Wert der Szintigraphie erheblich ab.
Therapie[Bearbeiten | Quelltext bearbeiten]
Die Behandlung ist oft langwierig und kann für Patienten und Therapeuten frustrierend sein. Die Prognose ist am besten, wenn die Krankheit zeitig erkannt und behandelt wird. Chronische schwere Verläufe sind insgesamt mit weniger als 2 % der Fälle eher selten.
- Physiotherapie: Die krankengymnastische Übungsbehandlung ist in der Prophylaxe nach frischen Verletzungen unumstritten, jedoch hilft in der Therapie nur stadiengerecht angepasste Krankengymnastik. Übungen der betroffenen Extremität sollen im akuten, von Ödem, Rötung und Schmerz betroffenen Abschnitt unterlassen werden. In diesem Stadium wird durch Ruhigstellung und Hochlagerung, gegebenenfalls auf einer Lagerungsschiene behandelt. Zur Behandlung des Ödems kommen Lymphdrainage, lokale Kühlung und eventuell „absteigende Bäder“ zur Anwendung. Am Ende dieses Stadiums kann auch mit kontralateraler aktiver Übungsbehandlung begonnen werden. Die krankengymnastische Aktivierung der betroffenen Gelenke erfolgt erst, wenn die abklingenden Schmerzen dies zulassen. Ärztliche Überwachung des Effekts und ggf. Anpassung der Verordnung sind notwendig.
- Die Ergotherapie dient der Wiederherstellung der Alltagsfunktion, zunächst beginnend mit der Reduktion schmerzhafter Bewegungsmuster. Zur Herstellung einer möglichst normalen Sensibilität erfolgt eine aktive Desensibilisierung der betroffenen Hautareale mit dem Ziel der Gewöhnung an alltägliche Berührungen. Die Feinmotorik wird zunächst ohne, später auch mit Widerstand trainiert, zuletzt kann, falls nötig, die Stellungskorrektur der Gelenke allmählich erfolgen.
- Bisphosphonate wie Pamidronat, Neridronat und Alendronat werden häufig verwendet. Die Wirkung ist gut bewiesen bei CRPS nach Frakturen. Mehrere Studien zeigen innerhalb 4 bis 10 Tagen gute Wirkung und eine deutliche Verbesserung innerhalb Wochen oder Monaten.[10][11] Vier 100 mg Infusionen Neridronat über 4 bis 10 Tage (400 mg Gesamtdosis) sind jetzt Standardbehandlung in den Universitätskliniken von Norditalien. Es ist jedoch zu beachten, dass Bisphosphonate für diese Anwendung nicht zugelassen sind. Das häufig diskutierte Risiko von Knochenschäden (z. B. am Kiefer) ist allerdings nur in der Hochdosis-Therapie von Bedeutung.
- Corticoide in Tablettenform (z. B. Prednisolon) werden vor allem in der Frühphase eingesetzt. Die Studienlage hierzu ist nicht ganz eindeutig, es tritt jedoch sehr oft eine schnelle Besserung von Schmerz, Schwellung und Bewegung ein.
- Schmerztherapie: trizyklische Antidepressiva, Nichtopioid-Analgetika (NSAID, z. B. Ibuprofen, Diclofenac oder Metamizol) oder Opioide (wie Morphin).
- Bei neurologischen Symptomen werden Antiepileptika wie z. B. Gabapentin oder Pregabalin eingesetzt, hierzu existieren aber kaum Studien.
- In zwei placebokontrollierten Studien zeigte Ketamin eine positive Wirkung, daher wird die Anwendung in der aktuellen Version der DGN-Leitlinie (2018) empfohlen, sofern andere Therapien nicht ausreichend wirksam sind. Die Therapie ist jedoch relativ aufwendig und nebenwirkungsreich, Leberschäden wurden beobachtet. Ketamin besitzt keine Zulassung für das CRPS.
- lokale Anwendung von steroidhaltiger Salbe oder DMSO (Dimethylsulfoxid[12] als Radikalfänger).[13]
- In bestimmten Fällen (Harden/Swan) ist eine Blockade des sympathischen Ganglion stellatum angezeigt. Sie sollte nach Möglichkeit innerhalb der ersten sechs Monate der Krankheitsdauer erfolgen, da nur dann Besserungsraten von bis zu 70 % erzielt werden können.
- Der frühzeitige Einsatz von Calcitonin (Nasenspray) kann möglicherweise den Verlauf positiv beeinflussen. Die Studienergebnisse hierzu sind jedoch widersprüchlich. Calcitonin steht in Deutschland als Nasenspray nicht mehr zur Verfügung und muss gespritzt werden.
- Rheologika wie Haes werden manchmal eingesetzt, hierfür gibt es jedoch keine wissenschaftliche Grundlage.
- Zur Behandlung von chronischen Schmerzen kann die Rückenmarkstimulation oder TENS eingesetzt werden.[14][15]
Die Therapie gehört auf jeden Fall in die Hände von in der Schmerztherapie erfahrenen Fachärzten für Orthopädie und Unfallchirurgie, Physikalische und Rehabilitative Medizin, Neurologie und Anästhesiologie im interdisziplinären Austausch.
Prognose[Bearbeiten | Quelltext bearbeiten]
Der Krankheitsverlauf des CRPS ist höchst unterschiedlich und reicht von völliger Ausheilung bis zum schweren chronischen Verlauf mit bleibender Behinderung und Schmerz.
Es herrscht weitgehend Einigkeit darüber, dass ein möglichst frühzeitiger Therapiebeginn die Prognose verbessert; gesicherte Daten hierzu fehlen jedoch.
In einer Langzeituntersuchung[16] an über 100 Patienten besserten sich im Verlauf einiger Jahre fast 85 % der Patienten so weit, dass die Diagnosekriterien des CRPS nicht mehr erfüllt waren. Jedoch waren in 41 % der Fälle noch Schmerzen unterschiedlichen Ausmaßes vorhanden. Die mediane Zeit bis zur „Ausheilung“ betrug 11 Monate, jedoch kamen auch nach drei Jahren noch Besserungen vor. Es handelt sich hier jedoch nur um Daten eines einzelnen Zentrums, größere Untersuchungen fehlen.
Vorbeugung[Bearbeiten | Quelltext bearbeiten]
Seit langem ist die klinische Beobachtung bekannt, dass ein CRPS nach Operationen in Regionalanästhesie seltener auftritt als nach OP in Vollnarkose. Eine Beobachtungsstudie[17] bestätigt dies, randomisierte Untersuchungen existieren jedoch nicht. Dennoch wird üblicherweise der Einsatz von Regionalanästhesie empfohlen.
Durch mehrere Studien bewiesen ist jedoch der vorbeugende Effekt von Vitamin C bei Operationen an Hand oder Fuß (500–1.000 mg täglich über 50 Tage ab dem OP-Tag). In einer zusammenfassenden Analyse[18] zeigte sich eine Verminderung des CRPS-Risikos um ca. drei Viertel. Damit stellt die Vitamin-C-Therapie eine wirksame Vorbeugungsmaßnahme dar.
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Literatur[Bearbeiten | Quelltext bearbeiten]
- Leitlinie „Diagnostik und Therapie komplexer regionaler Schmerzsyndrome (CRPS)“ der DGN
- R. N. Harden, M. Swan u. a.: Treatment of Complex Regional Pain Syndrome: Functional Restoration. In: Clinical Journal of Pain. 2006 Jun, 22 (5), S. 420–424.
- D. V. Nelson, B. R. Stacey: Interventional Therapies in the Management of Complex Regional Pain Syndrome. In: Clinical Journal of Pain. 2006 Jun, 22 (5), S. 438–442.
- J. Klingelhöfer, M. Rentrop: Klinikleitfaden „Neurologie, Psychiatrie“. S. 252.
- Interne Fortbildung der Abteilung für Neurologie. Landgrebe, Krankenhaus der BB R., April 2005.
- F. U. Niethard, J. Pfeil: Orthopädie. 4. Auflage. 2003, ISBN 3-13-130814-1.
- Thomas von Rothkirch, Walter Blauth, Bodo Helbig: Das Sudeck-Syndrom der Hand. Überblick, Behandlungskonzept und Ergebnisse. Handchirurgie, Mikrochirurgie und Plastische Chirurgie 21 (1989), S. 115–126.
- G. Wasner, J. Schattschneider u. a.: Das komplexe regionale Schmerzsyndrom. In: Der Anaesthesist. 2003 Oct, 0(10), S. 883–895.
- M. Rizzo, S. S. Balderson, D. H. Harpole, L. S. Levin: Thoracoscopic sympathectomy in the management of vasomotor disturbances and complex regional pain syndrome of the hand. In: Orthopedics. Januar 2004, 27 (1), S. 49–52.
- Heilung am Rande des Todes. In: Bild der Wissenschaft. 8/2006.
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Morbus Sudeck - Funktionelle Therapie ist das A und O, abgerufen am 12. Juli 2018.
- ↑ E. Scola: Diagnostik und Therapie der Algodystrophie. In: Trauma und Berufskrankheit. 2006, 8, Suppl. 2;, S. 225–228, doi:10.1007/s10039-005-1088-5.
- ↑ J. H. Geertzen u. a.: Stressful life events and psychological dysfunction in Complex Regional Pain Syndrome type I. In: Clin J Pain. 1998 Jun, 14(2), S. 143–147.
- ↑ H. Brehmer u. a.: CRPS bei Kindern: Welche Rolle spielen psychische Faktoren und kritische Lebensereignisse? In: Schmerz. 26, 2012, Suppl.1 (Poster beim deutschen Schmerzkongress 2012)
- ↑ V. Speck u. a.: Erhöhte Prävalenz der posttraumatischen belastungsstörung bei Patienten mit CRPS. In: Schmerz. 26, 2012, Suppl.1 (Poster beim deutschen Schmerzkongress 2012)
- ↑ Rommel, O., Willweber-Strumpf, A., Wagner, P. et al.: Psychische Veränderungen bei Patienten mit komplexem regionalem Schmerzsyndrom (CRPS). In: Springer Link. August 2005, abgerufen am 4. Februar 2022.
- ↑ R. M. Atkins, T. Duckworth, J. A. Kanis: Algodystrophy following Colles’ fracture. In: J Hand Surg. (Br) 1989; 14, S. 161–164.
- ↑ E. Peltz, F. Seifert, C. Maihöfner: Leitfaden zur Diagnostik des komplexen regionalen Schmerzsyndroms. In: Akt Rheumatol. 36, 2011, S. 28–34.
- ↑ Andreas Böger: Morbus Sudeck. Diagnose ohne Apparate möglich. In: Deutsches Ärzteblatt. Band 116, Nr. 1, 1. Februar 2019, S. A204-A205.
- ↑ Massimo Varenna, F. Zucchi, D. Ghiringhelli, L. Binelli, M. Beviacqua, P. Bettica, L. Sinigaglia: Intravenous clodronate in the treatment of reflex sympathetic dystrophy syndrome. A randomized, double blind, placebo controlled study. In: J Rheumatol. Band 27, Nr. 6, Juni 2000, S. 1477–1483, PMID 10852274.
- ↑ Massimo Varenna, S. Adami, M. Rossini, D. Gatti, L. Idolazzi, F. Zucchi, N. Malavolta, L. Sinigaglia: Treatment of complex regional pain syndrome type I with neridronate: a randomized, double-blind, placebo-controlled study. In: Rheumatology. Band 52, Nr. 3, März 2013, S. 534–542, doi:10.1093/rheumatology/kes312, PMID 23204550.
- ↑ In Deutschland nicht zugelassen
- ↑ W. W. A. Zuurmond u. a.: Treatment of acute reflex sympathetic dystrophy with DMSO 50 % in a fatty cream. In: Acta Anaesthesiologica Scandinavica. 40/1996, S. 364–367, doi:10.1111/j.1399-6576.1996.tb04446.x.
- ↑ Komplexes regionales Schmerzsyndrom (CRPS). Abgerufen am 4. Februar 2022 (deutsch).
- ↑ Wolfgang Rössy, Yaren Acar: TENS-Therapie. In: sankt-rochus-kliniken.de. Abgerufen am 4. Februar 2022.
- ↑ A. Rácz, L. Göderer, S. Dworsky, F. Birklein, V. Speck, C. Maihöfner: Langzeitprognose des CPRS – eine Follow-up-Studie. In: Schmerz. 26, 2012, Suppl.1 (Poster beim deutschen Schmerzkongress 2012)
- ↑ S. S. Reuben, R. Pristas, D. Dixon, S. Faruqi, L. Madabhushi, S. Wenner: The incidence of complex regional pain syndrome after fasciectomy for Dupuytren’s contracture: a prospective observational study of four anesthetic techniques. In: Anesthesia and Analgesia. 2006 Feb, 102(2), S. 499–503.
- ↑ N. Shibuya, J. M. Humphers, M. R. Agarwal, D. C. Jupiter: Efficacy and safety of high-dose vitamin C on complex regional pain syndrome in extremity trauma and surgery--systematic review and meta-analysis. In: J Foot Ankle Surg. 2013 Jan-Feb, 52(1), S. 62–66.