„Meningokokken“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
→Nebenwirkungen: + NW MenB |
Aktualisierung der STIKO-Impfempfehlungen sowie der Einreisebestimmungen Saudi-Arabien. Ergänzung relevanter Quellen und Rechtschreibkorrekturen. |
||
| Zeile 21: | Zeile 21: | ||
== Merkmale == |
== Merkmale == |
||
Meningokokken sind Bakterien der Art ''Neisseria meningitidis'', die zu den [[Aerobie|aerob]] und fakultativ anaerob wachsenden, gramnegativen Kokken gehört. Die Bakterien können sich durch die Hochregulation von nitrat- statt sauerstoffabhängigen Enzymen ihres Zuckerstoffwechsels an die anaeroben Verhältnisse im infizierten Gewebe anpassen.<ref>E. Bartolini et al.: ''Role of FNR and FNR-regulated, sugar fermentation genes in Neisseria meningitidis infection.'' In: ''Molecular Microbiology.'' (2006); 60, S. 963–972. [[doi:10.1111/j.1365-2958.2006.05163.x]]</ref> In flüssigen Nährmedien (sowie auch in der Gehirn- und Rückenmarksflüssigkeit) lagern sich die Bakterien in Pärchen zusammen (Diplokokken), bei denen die Längsachsen der beiden Bakterien nebeneinander gelagert sind. Die Enden der Bakterien sind dabei abgerundet, |
Meningokokken sind Bakterien der Art ''Neisseria meningitidis'', die zu den [[Aerobie|aerob]] und fakultativ anaerob wachsenden, gramnegativen Kokken gehört. Die Bakterien können sich durch die Hochregulation von nitrat- statt sauerstoffabhängigen Enzymen ihres Zuckerstoffwechsels an die anaeroben Verhältnisse im infizierten Gewebe anpassen.<ref>E. Bartolini et al.: ''Role of FNR and FNR-regulated, sugar fermentation genes in Neisseria meningitidis infection.'' In: ''Molecular Microbiology.'' (2006); 60, S. 963–972. [[doi:10.1111/j.1365-2958.2006.05163.x]]</ref> In flüssigen Nährmedien (sowie auch in der Gehirn- und Rückenmarksflüssigkeit) lagern sich die Bakterien in Pärchen zusammen (Diplokokken), bei denen die Längsachsen der beiden Bakterien nebeneinander gelagert sind. Die Enden der Bakterien sind dabei abgerundet, sodass ein einzelnes Bakterium an eine Kaffeebohne, ein Pärchen jeweils entfernt an ein Brötchen erinnert (daher die Beschreibung als semmelförmige gramnegative Diplokokken). Bei einer durch diese Bakterien ausgelösten [[Meningitis]] findet man in der Gehirn- und Rückenmarksflüssigkeit ([[Liquor cerebrospinalis]]) zusätzlich fast immer zahlreiche weiße Blutkörperchen ([[Granulozyten]]). |
||
Meningokokken wurden erstmals 1887 durch [[Anton Weichselbaum]] kultiviert (aus Patienten mit einer Meningitis).<ref name=":2" /> Sie wachsen im Labor auf reichhaltigen Nährböden wie z. B. [[Blutagar|Kochblutagar]] oder Columbia-Blutagar sowie aufgrund ihrer [[Resistenz]] gegen [[Colistin]] auch auf Spezialnährböden zur Anzucht von [[Pathogenität|pathogenen]] Neisserienarten wie z. B. [[Thayer-Martin-Agar]]. Am besten gelingt die Kultur in einer Atmosphäre, die einen erhöhten [[Kohlenstoffdioxid|Kohlendioxid]]-Gehalt (ca. 5–10 %) aufweist.<ref name=":2" /> Die [[Kolonie (Biologie)|Kolonien]] sind nach 24 Stunden Wachstum klein (ca. 1 mm Durchmesser), glatt, rund und von gräulicher Farbe. Sie bilden [[Cytochrom c Oxidase|Cytochrom-c-Oxidase]] und reagieren daher im [[Oxidase-Test]] positiv. In der Literatur sind auch flüssige Nährmedien beschrieben.<ref>{{Literatur |Autor=Ivan D. Frantz |Titel=Growth Requirements of the Meningococcus |Hrsg= |Sammelwerk=Journal of Bacteriology |Band=43 |Nummer=6 |Datum=1942-06 |PMID=16560537 |Seiten=757–761}}</ref><ref>{{Literatur |Autor=Jeffrey Fu et al. |Titel=Recent Advances in the Large Scale Fermentation of Neisseria meningitidis Group B for the Production of an Outer Membrane Protein Complex |Hrsg= |Sammelwerk=Bio/Technology |Band=13 |Nummer=2 |Auflage= |Datum=1995-02 |DOI=10.1038/nbt0295-170 |Seiten=170–174}}</ref> |
Meningokokken wurden erstmals 1887 durch [[Anton Weichselbaum]] kultiviert (aus Patienten mit einer Meningitis).<ref name=":2" /> Sie wachsen im Labor auf reichhaltigen Nährböden wie z. B. [[Blutagar|Kochblutagar]] oder Columbia-Blutagar sowie aufgrund ihrer [[Resistenz]] gegen [[Colistin]] auch auf Spezialnährböden zur Anzucht von [[Pathogenität|pathogenen]] Neisserienarten wie z. B. [[Thayer-Martin-Agar]]. Am besten gelingt die Kultur in einer Atmosphäre, die einen erhöhten [[Kohlenstoffdioxid|Kohlendioxid]]-Gehalt (ca. 5–10 %) aufweist.<ref name=":2" /> Die [[Kolonie (Biologie)|Kolonien]] sind nach 24 Stunden Wachstum klein (ca. 1 mm Durchmesser), glatt, rund und von gräulicher Farbe. Sie bilden [[Cytochrom c Oxidase|Cytochrom-c-Oxidase]] und reagieren daher im [[Oxidase-Test]] positiv. In der Literatur sind auch flüssige Nährmedien beschrieben.<ref>{{Literatur |Autor=Ivan D. Frantz |Titel=Growth Requirements of the Meningococcus |Hrsg= |Sammelwerk=Journal of Bacteriology |Band=43 |Nummer=6 |Datum=1942-06 |PMID=16560537 |Seiten=757–761}}</ref><ref>{{Literatur |Autor=Jeffrey Fu et al. |Titel=Recent Advances in the Large Scale Fermentation of Neisseria meningitidis Group B for the Production of an Outer Membrane Protein Complex |Hrsg= |Sammelwerk=Bio/Technology |Band=13 |Nummer=2 |Auflage= |Datum=1995-02 |DOI=10.1038/nbt0295-170 |Seiten=170–174}}</ref> |
||
Innerhalb der Art ''Neisseria meningitidis'' sind aufgrund der Zusammensetzung der Kapselpolysaccharide 12 verschiedene [[Serotyp|Serogruppen]] bekannt: A, B, C, E (ehemals 29E), H, I, K, L, W (ehemals W-135), X, Y und Z.<ref name=":2">{{Literatur |Autor=Lee H. Harrison, Dan M. Granoff, und Andrew J. Pollard |Titel=Meningococcal Capsular Group A, C, W, and Y Conjugate Vaccines |Hrsg=Stanley A. Plotkin et al. |Sammelwerk=Plotkin's Vaccines |Band= |Nummer= |Auflage=7 |Verlag=Elsevier |Ort=Philadelphia |Datum=2017 |ISBN=978-0-323-35761-6 |DOI=10.1016/B978-0-323-35761-6.00038-9 |Seiten=619ff.}}</ref><ref name=":3">{{Internetquelle |autor= |url=https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Meningokokken.html |titel=Meningokokken, invasive Erkrankungen (Neisseria meningitidis) |titelerg=RKI-Ratgeber |werk=RKI |hrsg= |datum=2014-02-01 |abruf=2020-12-02 |sprache=}}</ref> Die ehemalige Gruppe D hat sich als unbekapselte Variante der Gruppe C herausgestellt.<ref name=":2" /> Bei Erkrankten werden in der Regel nur die Serogruppen A (vor allem im afrikanischen „Meningitisgürtel“), B, C, W, Y und selten auch X (ebenfalls vorwiegend in Afrika) nachgewiesen. Bei Meningokokken-Infektionen in Deutschland wird am häufigsten die Serogruppe B nachgewiesen, gefolgt von C. Die Serogruppen unterscheiden sich |
Innerhalb der Art ''Neisseria meningitidis'' sind aufgrund der Zusammensetzung der Kapselpolysaccharide 12 verschiedene [[Serotyp|Serogruppen]] bekannt: A, B, C, E (ehemals 29E), H, I, K, L, W (ehemals W-135), X, Y und Z.<ref name=":2">{{Literatur |Autor=Lee H. Harrison, Dan M. Granoff, und Andrew J. Pollard |Titel=Meningococcal Capsular Group A, C, W, and Y Conjugate Vaccines |Hrsg=Stanley A. Plotkin et al. |Sammelwerk=Plotkin's Vaccines |Band= |Nummer= |Auflage=7 |Verlag=Elsevier |Ort=Philadelphia |Datum=2017 |ISBN=978-0-323-35761-6 |DOI=10.1016/B978-0-323-35761-6.00038-9 |Seiten=619ff.}}</ref><ref name=":3">{{Internetquelle |autor= |url=https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Meningokokken.html |titel=Meningokokken, invasive Erkrankungen (Neisseria meningitidis) |titelerg=RKI-Ratgeber |werk=RKI |hrsg= |datum=2014-02-01 |abruf=2020-12-02 |sprache=}}</ref> Die ehemalige Gruppe D hat sich als unbekapselte Variante der Gruppe C herausgestellt.<ref name=":2" /> Bei Erkrankten werden in der Regel nur die Serogruppen A (vor allem im afrikanischen „Meningitisgürtel“), B, C, W, Y und selten auch X (ebenfalls vorwiegend in Afrika) nachgewiesen. Bei Meningokokken-Infektionen in Deutschland wird am häufigsten die Serogruppe B nachgewiesen, gefolgt von C. Die Serogruppen unterscheiden sich in ihrer Oberflächenstruktur, welche unter anderem aus speziellen [[Lipopolysaccharide|Zuckermolekülen]] besteht. Diese und andere [[Molekül]]e bilden eine dicke Kapsel um die Bakterien, die diese vor den Angriffen des [[Immunsystem]]s schützt. Durch molekulare Feintypisierung der variablen Regionen äußerer Membranproteine ([[Porine]] PorA und FetA bzw. PorB<ref name=":2" />) lassen sich Meningokokken ferner in Serosubtypen mit unterschiedlichen Virulenzeigenschaften klassifizieren (z. B. B:P1.7–2,4:F1–5).<ref name=":0" /><ref name=":3" /> |
||
== Übertragungswege == |
== Übertragungswege == |
||
Meningokokken werden durch [[Tröpfcheninfektion]] von Mensch zu Mensch beispielsweise beim [[Husten|Anhusten]], [[Niesen]] oder [[Küssen]] übertragen. Begünstigt wird dies durch enge Unterkünfte oder Kindergärten bzw. Schulen.<ref name=":0" /> Sie heften sich |
Meningokokken werden durch [[Tröpfcheninfektion]] von Mensch zu Mensch beispielsweise beim [[Husten|Anhusten]], [[Niesen]] oder [[Küssen]] übertragen. Begünstigt wird dies durch enge Unterkünfte oder Kindergärten bzw. Schulen.<ref name=":0" /> Sie heften sich mithilfe kleiner Fortsätze ([[Pilus|Pili]]) an die [[Schleimhaut|Schleimhäute]] des [[Nasopharynx|Nasenrachenraumes]], wo sie wochen- oder monatelang bleiben können. Häufig verläuft die Besiedelung asymptomatisch.<ref name=":0" /> Vor allem, wenn das [[Immunsystem]] geschwächt ist, etwa durch andere [[Infektion]]en, und abhängig vom Virulenzfaktor<ref name=":2" />, vermehren sich die Bakterien, durchdringen die Schleimhäute (Mukosabarriere) und lösen [[Hirnhautentzündung]]en und [[Blutvergiftung]]en aus. Hierbei wirkt die Bekapselung einer [[Opsonisierung]] und [[Phagocytose|Phagozytose]] des Immunsystems entgegen. Wenn die Bakterien im Blutstrom zirkulieren, ist die [[Milz]] an der Entfernung beteiligt. Daher besteht die Gefahr für Patienten mit eingeschränkter Milzfunktion, dass eine invasive Meningokokken-Infektion schwerer verläuft.<ref name=":2" /> |
||
Der Mensch ist das einzige Erregerreservoir für Meningokokken.<ref name=":0" /> |
Der Mensch ist das einzige Erregerreservoir für Meningokokken.<ref name=":0" /> |
||
| Zeile 39: | Zeile 39: | ||
Am Ende der [[Trockenzeit]] (März/April) kommen Meningokokken-[[Epidemie]]n überwiegend der Serogruppe A im afrikanischen „Meningitisgürtel“ vor (zwischen südlicher [[Sahara]] und Äquatorialwäldern wie bei [[Senegal]], [[Ghana]], [[Nigeria]], bis nach [[Sudan]]).<ref name=":0" /> Von November bis Mai treten sie auch gehäuft in [[Indien]], vor allem Nordindien, und [[Nepal]] auf. In [[Gemäßigte Zone|gemäßigten Zonen]] werden epidemische Häufungen im späten Winter bzw. frühen Frühling verzeichnet.<ref name=":0" /> Dies lässt darauf schließen, dass eine geringe [[Luftfeuchtigkeit]] eine Infektion begünstigt, da die Schleimhäute durch Austrocknen vorgeschädigt werden können.<ref name=":0" /> |
Am Ende der [[Trockenzeit]] (März/April) kommen Meningokokken-[[Epidemie]]n überwiegend der Serogruppe A im afrikanischen „Meningitisgürtel“ vor (zwischen südlicher [[Sahara]] und Äquatorialwäldern wie bei [[Senegal]], [[Ghana]], [[Nigeria]], bis nach [[Sudan]]).<ref name=":0" /> Von November bis Mai treten sie auch gehäuft in [[Indien]], vor allem Nordindien, und [[Nepal]] auf. In [[Gemäßigte Zone|gemäßigten Zonen]] werden epidemische Häufungen im späten Winter bzw. frühen Frühling verzeichnet.<ref name=":0" /> Dies lässt darauf schließen, dass eine geringe [[Luftfeuchtigkeit]] eine Infektion begünstigt, da die Schleimhäute durch Austrocknen vorgeschädigt werden können.<ref name=":0" /> |
||
Im Jahr 2012 wurde in der Gruppe der [[Männer, die Sex mit Männern haben]], erstmals ein erhöhtes Infektionsrisiko in Metropolen wie [[New York City|New York]] und [[Berlin]] festgestellt.<ref name="zeit20130720" /> Verschiedene Ausbrüche unter anderem in Deutschland legen zudem nahe, dass Meningokokken sexuell übertragbar sein könnten.<ref>{{Literatur |Titel=Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen.(II) Impfen bei 1. Primären Immundefekterkrankungen und 2. HIV-Infektion |Sammelwerk=Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz |Band=61 |Nummer=8 |Datum=2018-08 |ISSN=1436-9990 |DOI=10.1007/s00103-018-2761-8 |Seiten=1034–1051 |Online=http://link.springer.com/10.1007/s00103-018-2761-8 |Abruf=2021-10-13}}</ref> |
|||
== {{Anker|Meningokokkenmeningitis}} Krankheitsbild (Symptome) == |
== {{Anker|Meningokokkenmeningitis}} Krankheitsbild (Symptome) == |
||
| Zeile 46: | Zeile 46: | ||
| 01-BEZEICHNUNG = Meningokokkeninfektion}} |
| 01-BEZEICHNUNG = Meningokokkeninfektion}} |
||
[[Datei:Charlotte Cleverley-Bisman.jpg |mini|Charlotte Cleverley-Bisman, ein neuseeländisches Kind, das im Alter von sieben Monaten eine Meningokokken-Infektion überlebte, dem aber alle vier [[Gliedmaßen|Extremitäten]] teilweise amputiert werden mussten<ref>{{cite web|url=http://www.biocsl.co.nz/docs/957/642/NorthSouth_case-for-accination.pdf|title=The case for vaccination|date=2010-06|accessdate=2015-07-03|last=|first=|archiveurl=http://web.archive.org/web/20180202234741/http://www.seqirus.co.nz/docs/957/642/NorthSouth_case-for-accination.pdf|archivedate=2018-02-02|last1=Wane|first1=Joanna|website=North & South}}</ref>]] |
[[Datei:Charlotte Cleverley-Bisman.jpg |mini|Charlotte Cleverley-Bisman, ein neuseeländisches Kind, das im Alter von sieben Monaten eine Meningokokken-Infektion überlebte, dem aber alle vier [[Gliedmaßen|Extremitäten]] teilweise amputiert werden mussten<ref>{{cite web|url=http://www.biocsl.co.nz/docs/957/642/NorthSouth_case-for-accination.pdf|title=The case for vaccination|date=2010-06|accessdate=2015-07-03|last=|first=|archiveurl=http://web.archive.org/web/20180202234741/http://www.seqirus.co.nz/docs/957/642/NorthSouth_case-for-accination.pdf|archivedate=2018-02-02|last1=Wane|first1=Joanna|website=North & South}}</ref>]] |
||
Die [[Inkubationszeit]] beträgt in der Regel |
Die [[Inkubationszeit]] beträgt in der Regel 3–4 Tage, kürzere und längere Inkubationszeiten (2–10 Tage) werden ebenfalls beobachtet. |
||
Das Spektrum der Erkrankung reicht von leichten Verläufen mit spontaner Abheilung bis hin zu einem hoch[[akut]]en Ausbruch, der trotz Behandlung in wenigen Stunden zum Tod führt. Bezeichnend für eine [[Meningitis|Entzündung der Hirnhäute]] ([[Hirnhaut|Pia mater]] und Arachnoidea)<ref name=":0" /> ist die sogenannte '''Meningokokkenmeningitis''', genannt auch ''Meningitis cerebrospinalis epidemica'' und ''übertragbare Genickstarre''<ref>Karl Wurm, A. M. Walter: ''Infektionskrankheiten.'' In: [[Ludwig Heilmeyer]] (Hrsg.): ''Lehrbuch der Inneren Medizin.'' 1961, S. 177.</ref>. Sie beginnt mit starkem Krankheitsgefühl wie Abgeschlagenheit, hohem [[Fieber]], Übelkeit und Erbrechen, [[Schüttelfrost]], Gelenk- und Muskelschmerzen, [[Krampf|Krämpfen]] oder [[Bewusstseinsstörung]]en. Als typisches Zeichen einer Hirnhautentzündung tritt die ''[[Meningismus|Nackensteifigkeit]]'' auf; diese bewirkt dann das |
Das Spektrum der Erkrankung reicht von leichten Verläufen mit spontaner Abheilung bis hin zu einem hoch[[akut]]en Ausbruch, der trotz Behandlung in wenigen Stunden zum Tod führt. Bezeichnend für eine [[Meningitis|Entzündung der Hirnhäute]] ([[Hirnhaut|Pia mater]] und Arachnoidea)<ref name=":0" /> ist die sogenannte '''Meningokokkenmeningitis''', genannt auch ''Meningitis cerebrospinalis epidemica'' und ''übertragbare Genickstarre''<ref>Karl Wurm, A. M. Walter: ''Infektionskrankheiten.'' In: [[Ludwig Heilmeyer]] (Hrsg.): ''Lehrbuch der Inneren Medizin.'' 1961, S. 177.</ref>. Sie beginnt mit starkem Krankheitsgefühl wie Abgeschlagenheit, hohem [[Fieber]], Übelkeit und Erbrechen, [[Schüttelfrost]], Gelenk- und Muskelschmerzen, [[Krampf|Krämpfen]] oder [[Bewusstseinsstörung]]en. Als typisches Zeichen einer Hirnhautentzündung tritt die ''[[Meningismus|Nackensteifigkeit]]'' auf; diese bewirkt dann das sogenannte ''Kissenbohren'': wenn der Patient liegt, zeigt sich ein überstrecktes Hohlkreuz und der Kopf drückt sich in das Kissen ([[Opisthotonus]]). Ungefähr die Hälfte der Patienten hat [[Petechie]]n wegen der hämatogenen Erregerstreuung ([[Bakteriämie]] oder [[Sepsis]]).<ref name=":0" /> |
||
Bei Säuglingen kann neben dem fast immer auftretenden Fieber die [[Symptomatik]] zunächst wenig eindeutig sein: [[Apathie]] oder Unruhe, Nahrungsverweigerung und Berührungsempfindlichkeit. Lichtempfindlichkeit ist ein mögliches Begleitsymptom. |
Bei Säuglingen kann neben dem fast immer auftretenden Fieber die [[Symptomatik]] zunächst wenig eindeutig sein: [[Apathie]] oder Unruhe, Nahrungsverweigerung und Berührungsempfindlichkeit. Lichtempfindlichkeit ist ein mögliches Begleitsymptom. |
||
| Zeile 54: | Zeile 54: | ||
[[Bewusstseinstrübung]], punktförmige Hautblutungen und [[Kreislaufkollaps]] sind Hinweise auf einen lebensbedrohenden Krankheitsverlauf ([[Waterhouse-Friderichsen-Syndrom]]). In schweren Fällen tritt der Tod schon innerhalb weniger Stunden ein. |
[[Bewusstseinstrübung]], punktförmige Hautblutungen und [[Kreislaufkollaps]] sind Hinweise auf einen lebensbedrohenden Krankheitsverlauf ([[Waterhouse-Friderichsen-Syndrom]]). In schweren Fällen tritt der Tod schon innerhalb weniger Stunden ein. |
||
Treten die Bakterien in die Blutbahn über und überschwemmen den Körper mit ihren Giftstoffen, spricht |
Treten die Bakterien in die Blutbahn über und überschwemmen den Körper mit ihren Giftstoffen, spricht man von einer Sepsis. Sie ist lebensbedrohlich. Bei schnellem Verlauf hin zur Sepsis müssen die „meningitischen“ Symptome nicht auftreten; die Schock- und toxisch bedingten Symptome stehen dann im Vordergrund. Bei nicht zeitnaher Behandlung kann es durch die Sepsis zum Verlust von Gliedmaßen kommen.<ref>[http://www.taz.de/Gericht-verurteilt-Asylheimbeschaeftigte-/!136884/ ''Kein Taxi, kein Anruf, keine Hilfe.''] In: ''taz.de''</ref> |
||
Entscheidend ist eine möglichst frühe Behandlung mit [[Antibiotika]]. Trotz Behandlung können Komplikationen und Spätfolgen wie Hörverlust, [[Blindheit]], [[Lähmung]]en oder [[Epilepsie|Krampfleiden]] auftreten und für jeden zehnten Patienten kommt jede Hilfe zu spät. Deshalb ist die vorbeugende Schutzimpfung für gefährdete Personen |
Entscheidend ist eine möglichst frühe Behandlung mit [[Antibiotika]]. Trotz Behandlung können Komplikationen und Spätfolgen wie Hörverlust, [[Blindheit]], [[Lähmung]]en oder [[Epilepsie|Krampfleiden]] auftreten und für jeden zehnten Patienten kommt jede Hilfe zu spät. Deshalb ist die vorbeugende Schutzimpfung für gefährdete Personen |
||
(beispielsweise aufgrund eines angeborenen oder erworbenen [[Immundefekt|Immundefekts]]) besonders wichtig. |
|||
Enge Kontaktpersonen sollten eine vorbeugende Therapie mit einem Antibiotikum (etwa [[Rifampicin]]) erhalten. |
|||
Enge Kontaktpersonen von Patienten mit einer invasiven Meningokokken-Infektion (IME) sollten eine vorbeugende Therapie mit einem Antibiotikum (etwa [[Rifampicin]]) sowie eine [[Postexpositionsprophylaxe#Meningokokkenmeningitis|postexpositionelle Impfung]] erhalten, sofern sie über keinen aktuellen Impfschutz gegen die entsprechende [[Serotyp|Serogruppe]] verfügen.<ref name=":10">{{Literatur |Titel=Epidemiologisches Bulletin |Hrsg=Robert Koch-Institut |Auflage=34 |Datum=2021 |Online=https://www.rki.de/DE/Content/Infekt/EpidBull/Archiv/2021/Ausgaben/34_21.pdf?__blob=publicationFile}}</ref> |
|||
== Therapie == |
== Therapie == |
||
| Zeile 64: | Zeile 66: | ||
== Chemoprophylaxe == |
== Chemoprophylaxe == |
||
Um bei Kontaktpersonen von Infizierten einer Erkrankung mit Meningokokken vorzubeugen, wird eine Chemoprophylaxe empfohlen. Die Prophylaxe ist indiziert, falls der Kontakt in den letzten sieben Tagen vor der Erkrankung stattgefunden hat. Die Behandlung sollte möglichst bald nach der Diagnosestellung beim Indexfall erfolgen, ist aber bis zu 10 Tage nach der letzten Exposition sinnvoll. Hierbei einsetzbare Chemotherapeutika sind [[Rifampicin]] und dessen Alternativen [[Ciprofloxacin]], Ceftriaxon sowie [[Azithromycin]]. Auch der Erkrankte sollte, wenn er zur Behandlung nicht ein Cephalosporin der dritten Generation intravenös erhalten hatte, nach Abschluss seiner Therapie eine Prophylaxe mit Rifampicin erhalten.<ref>Marianne Abele-Horn (2009), S. 320 f.</ref><ref name=":10" /> |
|||
== Impfung (Immunprophylaxe) == |
== Impfung (Immunprophylaxe) == |
||
Erste Versuche der Impfstoffherstellung wurden Beginn des 20. Jahrhunderts mit abgetöteten Zellen des Erregers unternommen. Zwischen 1900 und 1940 gab es zwar viele Studien zur Wirksamkeit, diese waren aber von schlechter Qualität, was die Aussagekraft erheblich gesenkt hatte.<ref name=":2" /> Durch die Entdeckung von [[Antibiotikum|Antibiotika]] wurde die Entwicklung geeigneter Impfstoffe zunächst zurückgestellt. Das Auftreten erster [[Sulfonamide|Sulfonamid]]-resistenter Stämme in den 1960er-Jahren stellte gerade für Militärrekruten während des [[Vietnamkrieg]]es ein ernstzunehmendes Problem dar, was die Impfstoffentwicklung wieder bestärkte.<ref name=":2" /> Ende der 1960er Jahre konnte durch die Arbeiten von [[Emil C. Gotschlich]] und Mitarbeitern Polysaccharide aus ''N. meningitidis'' isoliert und gereinigt werden, die sicher und ausreichend [[immunogen]] waren.<ref name=":2" /> Aufgrund gewisser Limitationen der Polysaccharid-Impfstoffe (z. B. fehlende T-Zell-abhängige Immunantwort, keinen Einfluss auf den Trägerstatus der entsprechenden Meningokokkenserogruppen im Nasen-Rachen-Raum<ref name=":0" />) wurde aufgrund der guten Erfahrungen von [[HIB-Impfung|Hib-Impfstoffen]] ebenfalls an Konjugatimpfstoffen für Meningokokken geforscht. Dies mündete 1999, auch auf Druck der Öffentlichkeit, in der Zulassung eines ersten, monovalenten Konjugatimpfstoffes gegen Meningokokken der Gruppe C in Großbritannien auf Grundlage von [[Immunogenität|Immunogentiäts]]- und Verträglichkeitsdaten – ein [[Therapeutische Wirksamkeit|Wirksamkeitsnachweis]] war vorher nicht erfolgt.<ref name=":2" /><ref name=":0" /> |
Erste Versuche der Impfstoffherstellung wurden Beginn des 20. Jahrhunderts mit abgetöteten Zellen des Erregers unternommen. Zwischen 1900 und 1940 gab es zwar viele Studien zur Wirksamkeit, diese waren aber von schlechter Qualität, was die Aussagekraft erheblich gesenkt hatte.<ref name=":2" /> Durch die Entdeckung von [[Antibiotikum|Antibiotika]] wurde die Entwicklung geeigneter Impfstoffe zunächst zurückgestellt. Das Auftreten erster [[Sulfonamide|Sulfonamid]]-resistenter Stämme in den 1960er-Jahren stellte gerade für Militärrekruten während des [[Vietnamkrieg]]es ein ernstzunehmendes Problem dar, was die Impfstoffentwicklung wieder bestärkte.<ref name=":2" /> Ende der 1960er Jahre konnte durch die Arbeiten von [[Emil C. Gotschlich]] und Mitarbeitern Polysaccharide aus ''N. meningitidis'' isoliert und gereinigt werden, die sicher und ausreichend [[immunogen]] waren.<ref name=":2" /> Aufgrund gewisser Limitationen der Polysaccharid-Impfstoffe (z. B. fehlende T-Zell-abhängige Immunantwort, keinen Einfluss auf den Trägerstatus der entsprechenden Meningokokkenserogruppen im Nasen-Rachen-Raum<ref name=":0" />) wurde aufgrund der guten Erfahrungen von [[HIB-Impfung|Hib-Impfstoffen]] ebenfalls an Konjugatimpfstoffen für Meningokokken geforscht. Dies mündete 1999, auch auf Druck der Öffentlichkeit, in der Zulassung eines ersten, monovalenten Konjugatimpfstoffes gegen Meningokokken der Gruppe C in Großbritannien auf Grundlage von [[Immunogenität|Immunogentiäts]]- und Verträglichkeitsdaten – ein [[Therapeutische Wirksamkeit|Wirksamkeitsnachweis]] war vorher nicht erfolgt.<ref name=":2" /><ref name=":0" /> |
||
Zur Vorbeugung, etwa |
Zur Vorbeugung einer Meningokokkeninfektion, etwa vor einer geplanten [[Splenektomie|Milzentfernung]], Konjugatimpfstoffe gegen den Serotyp C zur Verfügung, der beispielsweise in England, Spanien oder auch in einigen Regionen Deutschlands gehäuft auftritt, zudem gegen die Typen A, W und Y. Außerdem wurden ab 2013 erste Impfstoffe gegen ''N. meningitidis'' der Gruppe B in Europa zugelassen. In [[Kuba]] wurde bereits 1988 ein Impfstoff gegen die Gruppe B eingesetzt<ref>{{Der Spiegel |ID=13918399 |Titel=Bioboom in der Karibik |Jahr=1999 |Nr=27 |Seiten=}}</ref><ref>{{Webarchiv|url=http://www.granma.cu/aleman/kuba/3marzo-Eine%20Revolution.html |wayback=20111110220705 |text=''50 Jahre Impfprogramm in Kuba – Eine Revolution in Sachen Gesundheit.'' }} In: ''Digital Granma International.'' 3. März 2011; abgerufen 26. April 2011.</ref>. Auch in [[Neuseeland]] gab es ab 2004 einen Impfstoff (''MeNZB'') gegen einen speziellen Erregertyp der Gruppe B, der damals nur dort vorgekommen ist; der Impfstoff wird heute nicht mehr hergestellt.<ref name=":6" /><ref>{{Internetquelle |autor=Petra Jungmayr |url=https://www.deutsche-apotheker-zeitung.de/daz-az/2017/daz-30-2017/zwei-fliegen-mit-einem-impfstoff |titel=Zwei Fliegen mit einem Impfstoff |werk=Deutsche Apothekerzeitung |hrsg= |datum=2017-07-27 |abruf=2020-12-29}}</ref> |
||
Die Impfung ist die zuverlässigste Maßnahme zur Prävention invasiver Meningokokkeninfektionen.<ref name=":0">{{Literatur |Autor=Ulrich Heininger |Titel=Meningokokken |Hrsg=Heinz Spiess, Ulrich Heininger, Wolfgang Jilg |Sammelwerk=Impfkompendium |Band= |Nummer= |Auflage=8 |Verlag=Georg Thieme Verlag |Datum=2015-11-04 |ISBN=978-3134989083 |DOI=10.1055/b-0035-127590 |Seiten=220ff.}}</ref> |
Die Impfung ist die zuverlässigste Maßnahme zur Prävention invasiver Meningokokkeninfektionen.<ref name=":0">{{Literatur |Autor=Ulrich Heininger |Titel=Meningokokken |Hrsg=Heinz Spiess, Ulrich Heininger, Wolfgang Jilg |Sammelwerk=Impfkompendium |Band= |Nummer= |Auflage=8 |Verlag=Georg Thieme Verlag |Datum=2015-11-04 |ISBN=978-3134989083 |DOI=10.1055/b-0035-127590 |Seiten=220ff.}}</ref> |
||
=== Polysaccharid-Impfstoffe === |
=== Polysaccharid-Impfstoffe === |
||
Bei Polysaccharid-Impfstoffen verwendet man gereinigte, gruppenspezifische Kapsel[[polysaccharide]] (PS), damit Teile der Bakterienhülle.<ref name=":0" /> Bei den früher erhältlichen Polysaccharid-Impfstoffen wurde ein Schutz gegen die Serotypen A und C (''AC-Impfstoff'', etwa Meningokokken-Impfstoff ''A+C Mérieux'', nicht mehr vermarktet<ref name=":1">{{Internetquelle |autor= |url=https://www.pei.de/DE/arzneimittel/impfstoffe/meningokokken/meningokokken-node.html?cms_tabcounter=0&cms_tabcounter=0#anchor |titel=Meningokokken-Impfstoffe |werk=Paul-Ehrlich-Institut |hrsg= |datum=2020-11-02 |abruf=2020-11-29}}</ref>) bzw. gegen die Serotypen A, C, W und Y (etwa der ehemalige Impfstoff ''Mencevax ACWY'', dessen Vermarktung 2013 endete und nicht mehr ausgeliefert wird<ref>{{Internetquelle |autor= |url=https://www.aerzteblatt.de/archiv/138329/Kurz-informiert |titel=Kurz informiert |titelerg=Vermarktung von Mencevax® ACWY eingestellt |werk=Deutsches Ärzteblatt |hrsg= |datum=2013-05-10 |abruf=2020-11-29}}</ref><ref name=":0" />) aufgebaut. Zwar stimulieren PS der Gruppe A im Gegensatz zu den PS der Gruppen C, W und Y im Säuglingsalter bereits das T-Zell-Immunsystem, |
Bei Polysaccharid-Impfstoffen verwendet man gereinigte, gruppenspezifische Kapsel[[polysaccharide]] (PS), damit Teile der Bakterienhülle.<ref name=":0" /> Bei den früher erhältlichen Polysaccharid-Impfstoffen wurde ein Schutz gegen die Serotypen A und C (''AC-Impfstoff'', etwa Meningokokken-Impfstoff ''A+C Mérieux'', nicht mehr vermarktet<ref name=":1">{{Internetquelle |autor= |url=https://www.pei.de/DE/arzneimittel/impfstoffe/meningokokken/meningokokken-node.html?cms_tabcounter=0&cms_tabcounter=0#anchor |titel=Meningokokken-Impfstoffe |werk=Paul-Ehrlich-Institut |hrsg= |datum=2020-11-02 |abruf=2020-11-29}}</ref>) bzw. gegen die Serotypen A, C, W und Y (etwa der ehemalige Impfstoff ''Mencevax ACWY'', dessen Vermarktung 2013 endete und nicht mehr ausgeliefert wird<ref>{{Internetquelle |autor= |url=https://www.aerzteblatt.de/archiv/138329/Kurz-informiert |titel=Kurz informiert |titelerg=Vermarktung von Mencevax® ACWY eingestellt |werk=Deutsches Ärzteblatt |hrsg= |datum=2013-05-10 |abruf=2020-11-29}}</ref><ref name=":0" />) aufgebaut. Zwar stimulieren PS der Gruppe A im Gegensatz zu den PS der Gruppen C, W und Y im Säuglingsalter bereits das T-Zell-Immunsystem, sodass nach einmaliger Gabe [[Immunglobulin G|IgG]]-Antikörper gebildet werden. Jedoch erreichen die Serumantikörper selbst nach Booster nach einem Jahr wieder die Ausgangswerte vor der Impfung. Zudem hat man bei einer Impfung unter zwei Jahren mit PS der Gruppe C beobachtet, dass sich eine anhaltende, einen Boostereffekt inhibierende [[Immuntoleranz]] bildet. Daher schützen beide Polysaccharid-Impfstoffe am besten ab einem Alter von zwei Jahren, da erst ab diesem Alter eine T-zellunabhängige B-Zellaktivierung möglich ist. Die altersabhängige Wirksamkeit der Impfung gegenüber Gruppe-C-Infektionen wurde aufgrund eines Meningokokkenausbruchs in [[Québec|Quebec]] ermittelt: Sie beträgt 41 % bei Kindern von 2–9 Jahren, 75 % bei Kindern von 10–14 Jahren und 83 % bei Kindern und jungen Erwachsenen von 15–20 Jahren.<ref name=":0" /> |
||
Polysaccharid-Impfstoffe werden unter die Haut gespritzt. Der Impfschutz hält mindestens drei Jahre. Für Erwachsene und Kinder genügt eine einmalige Injektion. Der AC-Impfstoff kann ab einem Alter von 18 Monaten eingesetzt werden. Der ACWY-Impfstoff ist ab zwei Jahren wirksam. Bei jüngeren Kindern ist ein Schutz gegen die Gruppen C, W und Y nicht gesichert und der Impfschutz hält höchstens zwei Jahre an. Um einen besseren Impfschutz zu erreichen, können Kinder unter zwei Jahren im Abstand von drei Monaten auch ein zweites Mal geimpft werden. Die Schutzwirkung der Impfung setzt etwa nach zwei Wochen ein. Bei bestehendem Infektionsrisiko ist nach drei Jahren eine Wiederholungsimpfung ratsam. |
Polysaccharid-Impfstoffe werden unter die Haut gespritzt. Der Impfschutz hält mindestens drei Jahre. Für Erwachsene und Kinder genügt eine einmalige Injektion. Der AC-Impfstoff kann ab einem Alter von 18 Monaten eingesetzt werden. Der ACWY-Impfstoff ist ab zwei Jahren wirksam. Bei jüngeren Kindern ist ein Schutz gegen die Gruppen C, W und Y nicht gesichert und der Impfschutz hält höchstens zwei Jahre an. Um einen besseren Impfschutz zu erreichen, können Kinder unter zwei Jahren im Abstand von drei Monaten auch ein zweites Mal geimpft werden. Die Schutzwirkung der Impfung setzt etwa nach zwei Wochen ein. Bei bestehendem Infektionsrisiko ist nach drei Jahren eine Wiederholungsimpfung ratsam. |
||
| Zeile 83: | Zeile 85: | ||
Speziell für Kinder im Alter zwischen zwei Monaten und zwei Jahren sind sogenannte ''[[Konjugierter Impfstoff|Konjugatimpfstoffe]]'' entwickelt worden. Sie können bei Bedarf aber auch bei älteren Kindern, Jugendlichen oder Erwachsenen eingesetzt werden. Bei einem Konjugatimpfstoff sind die Teile der Bakterienhülle zusätzlich an ein Eiweiß ([[Protein]]) gebunden, wodurch eine bessere T-Zell-abhängige Immunantwort erzielt wird. Die Kapselantigene können beispielsweise an der ungiftigen Variante des [[Diphtherietoxin]]s CRM<sub>197</sub> aus ''[[Corynebacterium diphtheriae]]'' (z. B. bei ''Menveo''<ref>{{Internetquelle |autor= |url=https://www.ema.europa.eu/en/medicines/human/EPAR/menveo |titel=European public assessment report von Menveo |werk=EMA |hrsg= |datum=2020-01-23 |abruf=2020-11-29 |sprache=en}}</ref>) oder an ein [[Tetanospasmin|Tetanustoxoid]]-Trägerprotein konjugiert sein (z. B. bei ''Nimenrix''<ref>{{Internetquelle |url=https://www.ema.europa.eu/en/medicines/human/EPAR/nimenrix |titel=European public assessment report von Nimenrix |werk=EMA |datum=2020-07-23 |abruf=2020-11-29 |sprache=en}}</ref>). |
Speziell für Kinder im Alter zwischen zwei Monaten und zwei Jahren sind sogenannte ''[[Konjugierter Impfstoff|Konjugatimpfstoffe]]'' entwickelt worden. Sie können bei Bedarf aber auch bei älteren Kindern, Jugendlichen oder Erwachsenen eingesetzt werden. Bei einem Konjugatimpfstoff sind die Teile der Bakterienhülle zusätzlich an ein Eiweiß ([[Protein]]) gebunden, wodurch eine bessere T-Zell-abhängige Immunantwort erzielt wird. Die Kapselantigene können beispielsweise an der ungiftigen Variante des [[Diphtherietoxin]]s CRM<sub>197</sub> aus ''[[Corynebacterium diphtheriae]]'' (z. B. bei ''Menveo''<ref>{{Internetquelle |autor= |url=https://www.ema.europa.eu/en/medicines/human/EPAR/menveo |titel=European public assessment report von Menveo |werk=EMA |hrsg= |datum=2020-01-23 |abruf=2020-11-29 |sprache=en}}</ref>) oder an ein [[Tetanospasmin|Tetanustoxoid]]-Trägerprotein konjugiert sein (z. B. bei ''Nimenrix''<ref>{{Internetquelle |url=https://www.ema.europa.eu/en/medicines/human/EPAR/nimenrix |titel=European public assessment report von Nimenrix |werk=EMA |datum=2020-07-23 |abruf=2020-11-29 |sprache=en}}</ref>). |
||
In Deutschland sind drei ''C-Konjugat-Impfstoffe'' ab dem Alter von 2 Monaten zugelassen: ''Meningitec, Menjugate'' und ''NeisVac-C''.<ref name=":1" /> Sie schützen vor Infektionen |
In Deutschland sind drei ''C-Konjugat-Impfstoffe'' ab dem Alter von 2 Monaten zugelassen: ''Meningitec, Menjugate'' und ''NeisVac-C''.<ref name=":1" /> Sie schützen vor Infektionen mit Meningokokken des Serotyps C, der in Deutschland etwa jede fünfte Erkrankung verursacht. Die Impfung mit solchen Konjugatimpfstoffen kann bei Bedarf ab dem dritten Lebensjahr mit einem Polysaccharidimpfstoff ergänzt werden. Als [[Adjuvans]] enthalten C-Konjugat-Impfstoffe [[Aluminiumhydroxid]].<ref name=":0" /> Die Wirksamkeit der Impfung wurde anhand von [[Fall-Kontroll-Studie|Fall-Kontrollstudien]] in Großbritannien ermittelt, das als erstes Land ein nationales Impfprogramm gegen Meningokokken 1999 initiiert hatte.<ref name=":0" /> Für Kinder im Alter von 1–2 Jahren und Jugendlichen im Alter von 15–17 Jahren wurde eine Wirksamkeit von 92 % bzw. 97 % ermittelt. Dies erklärt auch den schnellen und signifikanten Rückgang invasiver Meningokokkeninfektionen der Gruppe C.<ref name=":0" /> Epidemiologische [[Beobachtungsstudie]]n anderer Länder bestätigten die hohe Wirksamkeit des Konjugatimpfstoffes. Zudem reduzieren Konjugatimpfstoffe auch die entsprechenden Meningokokkenserogruppen im Nasen-Rachen-Raum.<ref name=":0" /> |
||
Im Oktober 2010 wurde in Europa ein tetravalenter Konjugatimpfstoff gegen A, C, W und Y (''Menveo'') zugelassen, ursprünglich für 11- bis 55-Jährige, ab 2011 auch für 2- bis 10-jährige Kinder.<ref>{{Internetquelle |autor= |url=https://www.rki.de/DE/Content/Infekt/EpidBull/Archiv/2012/32/Tabelle.html |titel=Epidemiologisches Bulletin Nr. 32/2012 |werk=RKI |hrsg= |datum=2012-08-13 |abruf=2020-11-30}}</ref> 2012 folgte ein zweiter tetravalenter Konjugatimpfstoff, ''Nimenrix'', welcher ab einem Alter von 6 Wochen zugelassen ist.<ref>{{Internetquelle |autor= |url=https://www.pei.de/SharedDocs/arzneimittel/impfstoffe/Mono/Meningokokken/EU-1-12-767-001-007.html |titel=Nimenrix |werk=Paul-Ehrlich-Institut |hrsg= |datum= |abruf=2020-11-30}}</ref> Diese beiden Impfstoffe sind nicht nur früher als der entsprechende Polysaccharidimpfstoff einsetzbar, sondern zudem auch auffrischbar, da hier – im Gegensatz zu Polysaccharidimpfstoffen – ein immunologisches Gedächtnis gebildet wird. Zudem erlaubt die T-Zellhilfe einen [[Klassenwechsel]], sodass auch IgA gebildet werden kann (Polysaccharidimpfstofe nur IgM) und damit der Trägerstatus vermindert werden sollte. Sie weisen damit eine bessere Immunogenität auf.<ref name=":0" /> |
|||
Seit dem Januar 2013 ist in Europa ein wirksamer rekombinanter Adsorbatimpfstoff (''Bexsero''<ref>{{Internetquelle |url=https://www.ema.europa.eu/en/medicines/human/EPAR/bexsero |titel=European public assessment report von Bexsero |werk=EMA |datum=2020-07-02 |abruf=2020-11-30 |sprache=en}}</ref>) gegen den Serotyp B zugelassen. Er basiert nicht auf Kapsel-Antigenen wie bei den Serotypen A, C, W und Y, da die Kapsel des Serotyps B dem menschlichen neuronalen Zelladhäsionsprotein 1 ([[Neurales Zelladhäsionsmolekül 1|NCAM-1]]) ähnelt, sondern auf vier immunogene Oberflächenantigene („4CMenB“ bzw. „MenB-4C“).<ref>{{Literatur |Autor=Dan M.Granoff et al. |Titel=Meningococcal Capsular Group B Vaccines |Hrsg=Stanley A. Plotkin et al. |Sammelwerk=Plotkin's Vaccines |Auflage=7 |Verlag=Elsevier |Ort=Philadelphia |Datum=2017 |ISBN=978-0-323-35761-6 |DOI=10.1016/B978-0-323-35761-6.00053-5 |Seiten=646}}</ref><ref name=":8" /> Diese wurde durch sogenannte reverse Vakzinologie entwickelt (umgekehrte Impfstoffentwicklung). Hierbei wurden besonders immunogene, potenzielle Oberflächenproteinantigene mit Hilfe einer Computeranalyse des ''N.-meningitidis''-Genoms identifiziert, anschließend [[Genexpression|exprimiert]] und dann Mäusen immunisiert: Es sind das Faktor-H-Bindungsprotein fHbp („factor H binding protein“), das Neisseria Adhäsin A NadA („Neisserial adhesin A“), das Neisseria-Heparin-Bindungsantigen NHBA („Neisserial Heparin Binding Antigen“) sowie das PorA-Protein („Porin A P1.4“).<ref name=":8" /><ref>{{Literatur |Autor=Cynthia Burman et al. |Titel=A review of the immunogenicity, safety and current recommendations for the meningococcal serogroup B vaccine, MenB-FHbp |Hrsg= |Sammelwerk=Journal of Clinical Pharmacy and Therapeutics |Band=45 |Nummer=2 |Auflage= |Datum=2020-04 |DOI=10.1111/jcpt.13083 |Seiten=270–281}}</ref> Die Oberflächenproteine werden vom Großteil aller zirkulierenden MenB-Stämmen exprimiert (beziehungsweise wenigstens zu einem ausreichenden Grad).<ref name=":8" /> ''Bexsero'' ist für die aktive Immunisierung im Alter ab 2 Monaten und älter gegen invasive Meningokokken-Erkrankungen indiziert. |
Seit dem Januar 2013 ist in Europa ein wirksamer rekombinanter Adsorbatimpfstoff (''Bexsero''<ref>{{Internetquelle |url=https://www.ema.europa.eu/en/medicines/human/EPAR/bexsero |titel=European public assessment report von Bexsero |werk=EMA |datum=2020-07-02 |abruf=2020-11-30 |sprache=en}}</ref>) gegen den Serotyp B zugelassen. Er basiert nicht auf Kapsel-Antigenen wie bei den Serotypen A, C, W und Y, da die Kapsel des Serotyps B dem menschlichen neuronalen Zelladhäsionsprotein 1 ([[Neurales Zelladhäsionsmolekül 1|NCAM-1]]) ähnelt, sondern auf vier immunogene Oberflächenantigene („4CMenB“ bzw. „MenB-4C“).<ref>{{Literatur |Autor=Dan M.Granoff et al. |Titel=Meningococcal Capsular Group B Vaccines |Hrsg=Stanley A. Plotkin et al. |Sammelwerk=Plotkin's Vaccines |Auflage=7 |Verlag=Elsevier |Ort=Philadelphia |Datum=2017 |ISBN=978-0-323-35761-6 |DOI=10.1016/B978-0-323-35761-6.00053-5 |Seiten=646}}</ref><ref name=":8" /> Diese wurde durch sogenannte reverse Vakzinologie entwickelt (umgekehrte Impfstoffentwicklung). Hierbei wurden besonders immunogene, potenzielle Oberflächenproteinantigene mit Hilfe einer Computeranalyse des ''N.-meningitidis''-Genoms identifiziert, anschließend [[Genexpression|exprimiert]] und dann Mäusen immunisiert: Es sind das Faktor-H-Bindungsprotein fHbp („factor H binding protein“), das Neisseria Adhäsin A NadA („Neisserial adhesin A“), das Neisseria-Heparin-Bindungsantigen NHBA („Neisserial Heparin Binding Antigen“) sowie das PorA-Protein („Porin A P1.4“).<ref name=":8" /><ref>{{Literatur |Autor=Cynthia Burman et al. |Titel=A review of the immunogenicity, safety and current recommendations for the meningococcal serogroup B vaccine, MenB-FHbp |Hrsg= |Sammelwerk=Journal of Clinical Pharmacy and Therapeutics |Band=45 |Nummer=2 |Auflage= |Datum=2020-04 |DOI=10.1111/jcpt.13083 |Seiten=270–281}}</ref> Die Oberflächenproteine werden vom Großteil aller zirkulierenden MenB-Stämmen exprimiert (beziehungsweise wenigstens zu einem ausreichenden Grad).<ref name=":8" /> ''Bexsero'' ist für die aktive Immunisierung im Alter ab 2 Monaten und älter gegen invasive Meningokokken-Erkrankungen indiziert. |
||
| Zeile 94: | Zeile 96: | ||
Die [[Ständige Impfkommission]] (STIKO) empfiehlt seit 2006<ref name=":4">{{Internetquelle |autor=Celine Müller |url=https://www.deutsche-apotheker-zeitung.de/news/artikel/2020/07/17/meningokokken-b-auf-dem-vormarsch |titel=Meningokokken B auf dem Vormarsch? |werk=[[Deutsche Apothekerzeitung]] |datum=2020-07-17 |abruf=2020-12-08}}</ref> die Impfung gegen Meningokokken der Serogruppe C mit dem ''C-Konjugat-Impfstoff'' standardmäßig für alle Kinder ab 12 Monate (Beginn des 2. Lebensjahres).<ref name="eb2012-30">[http://www.rki.de/DE/Content/Infekt/EpidBull/Archiv/2012/Ausgaben/30_12.pdf?__blob=publicationFile Epidemiologisches Bulletin 2012, Nr. 30 (30. Juli 2012)] (PDF) </ref><ref name=":3" /> Dabei werden die Reduzierung der Morbidität invasiver Meningokokken-Erkrankungen durch diese Serogruppe und der resultierenden Folgen wie Hospitalisierung, schwere Komplikationen, Behinderung und Tod als primäres Ziel angesehen. Für noch nicht geimpfte Kinder und Jugendliche wird das Nachholen der Impfung bis zum 18. Lebensjahr empfohlen.<ref name="eb2012-30" /> 2011 betrug die Impfquote von Kleinkindern etwa 80 %<ref name=":3" />, diese stieg 2017 auf fast 90 %.<ref name=":5" /> |
Die [[Ständige Impfkommission]] (STIKO) empfiehlt seit 2006<ref name=":4">{{Internetquelle |autor=Celine Müller |url=https://www.deutsche-apotheker-zeitung.de/news/artikel/2020/07/17/meningokokken-b-auf-dem-vormarsch |titel=Meningokokken B auf dem Vormarsch? |werk=[[Deutsche Apothekerzeitung]] |datum=2020-07-17 |abruf=2020-12-08}}</ref> die Impfung gegen Meningokokken der Serogruppe C mit dem ''C-Konjugat-Impfstoff'' standardmäßig für alle Kinder ab 12 Monate (Beginn des 2. Lebensjahres).<ref name="eb2012-30">[http://www.rki.de/DE/Content/Infekt/EpidBull/Archiv/2012/Ausgaben/30_12.pdf?__blob=publicationFile Epidemiologisches Bulletin 2012, Nr. 30 (30. Juli 2012)] (PDF) </ref><ref name=":3" /> Dabei werden die Reduzierung der Morbidität invasiver Meningokokken-Erkrankungen durch diese Serogruppe und der resultierenden Folgen wie Hospitalisierung, schwere Komplikationen, Behinderung und Tod als primäres Ziel angesehen. Für noch nicht geimpfte Kinder und Jugendliche wird das Nachholen der Impfung bis zum 18. Lebensjahr empfohlen.<ref name="eb2012-30" /> 2011 betrug die Impfquote von Kleinkindern etwa 80 %<ref name=":3" />, diese stieg 2017 auf fast 90 %.<ref name=":5" /> |
||
Außerdem empfiehlt die STIKO die Immunisierung mit einem Meningokokken-ACWY-Konjugatimpfstoff sowie mit einem Meningokokken-B-Impfstoff für alle [[Risikogruppe|Risikogruppen]]. Dazu zählen neben beruflich exponierten Personen (etwa Laborpersonal) insbesondere Menschen mit angeborener oder erworbener Immunschwäche.<ref name=":10" /> Diese erkranken durchschnittlich häufiger an Infektionskrankheiten und erleiden öfter einen schweren Verlauf.<ref name=":10" /><ref name=":11">{{Literatur |Autor=Norbert Wagner, Frauke Assmus, Gabriele Arendt, Erika Baum, Ulrich Baumann |Titel=Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen. (IV) Impfen bei Autoimmunkrankheiten, bei anderen chronisch-entzündlichen Erkrankungen und unter immunmodulatorischer Therapie |Sammelwerk=Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz |Band=62 |Nummer=4 |Datum=2019-04 |ISSN=1436-9990 |DOI=10.1007/s00103-019-02905-1 |Seiten=494–515 |Online=http://link.springer.com/10.1007/s00103-019-02905-1 |Abruf=2021-10-13}}</ref> Da der Impfschutz gegen alle Meningokokken-Serogruppen mittels [[Totimpfstoff|Totimpfstoffen]] erzeugt wird, besteht in der Regel kein erhöhtes Risiko für Komplikationen bei immungeschwächten Personen.<ref name=":11" /><ref>{{Literatur |Autor=Tim Niehues, Christian Bogdan, Jane Hecht, Thomas Mertens, Miriam Wiese-Posselt |Titel=Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen(I) Grundlagenpapier |Sammelwerk=Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz |Band=60 |Nummer=6 |Datum=2017-06 |ISSN=1436-9990 |DOI=10.1007/s00103-017-2555-4 |Seiten=674–684 |Online=http://link.springer.com/10.1007/s00103-017-2555-4 |Abruf=2021-10-13}}</ref> |
|||
Ferner gibt es eine risikobasierte Empfehlung seit August 2015: So ist Impfung mit einem Meningokokken-ACWY-Konjugatimpfstoff sowie mit einem Meningokokken-B-Impfstoff allen Personen mit erhöhtem Infektionsrisiko angezeigt, etwa bei beruflich oder individuell erhöhtem Risiko sowie als Reiseimpfung.<ref name=":4" /><ref name="eb2012-30" /> Besonders gefährdet sind zum Beispiel Personen mit [[Immunsystem|Immundefekten]] oder fehlender beziehungsweise funktionsuntüchtiger [[Milz]]. Auch Reisende in Gebiete, in denen Meningokokken-Infektionen häufig auftreten, tragen ein erhöhtes Infektionsrisiko, wenn sie sich dort länger aufhalten oder engen Kontakt zur Bevölkerung haben. Schließlich sollten Säuglinge, Kinder oder Jugendliche bei Vorliegen eines erhöhten Risikos für invasive Meningokokken-Erkrankungen entsprechend geimpft werden.<ref name=":3" /> |
|||
Ursachen für die Immunschwäche können unter anderem sein: |
|||
| ⚫ | Der Berliner Impfbeirat empfiehlt seit Juli 2013 [[Männer, die Sex mit Männern haben|Männern, die Sex mit Männern haben]] (MSM), sich mit einem Impfstoff impfen zu lassen, der eine Komponente gegen Meningokokken der Gruppe C enthält und für Erwachsene zugelassen ist. Anlass für die |
||
* Primäre oder erworbene Immundefekte, z. B. [[Mikrodeletionssyndrom 22q11|DiGeorge-Syndrom]], [[Variables Immundefektsyndrom|Common Variable Immunodeficiency (CVID)]], [[Hypogammaglobulinämie]], Defekte des [[Toll-like-Rezeptoren|Toll-like Rezeptor Signalwegs]], [[HIV]]-Infektion, [[AIDS]], [[Komplementsystem|Komplement]]-/Properdin-Defizienz, [[Asplenie]]<sup>[A]</sup><ref name=":10" /> |
|||
[[Saudi-Arabien]] verlangt während der [[Mekka]]-[[Wallfahrt]]en von [[Pilger]]n und Besuchern eine Impfbescheinigung, die maximal drei Jahre und minimal zehn Tage vor dem Eintreffen in Saudi-Arabien ausgestellt worden sein darf. Pflicht ist der ''Vierfach-Impfstoff A,C,W,Y''. Pilger, die aus [[Endemie]]gebieten einreisen, werden untersucht und bei Verdacht auf Meningitis beobachtet. Alle anderen Reisenden müssen nicht geimpft sein. |
|||
* Autoimmunerkrankungen wie Erkrankungen des [[Rheuma|rheumatischen Formenkreises]] und [[chronisch-entzündliche Darmerkrankungen]]<ref name=":10" /><ref name=":11" /> |
|||
* [[Immunmodulation|Immunmodulatorische Therapie]], z. B. Behandlung mit C5-Komplement-Inhibitoren oder Therapie bei [[Schuppenflechte|Psoriasis]] oder [[Krebs (Medizin)|onkologischer Erkrankungen]]; mindestens 2 Wochen vor Beginn einer medikamentös hervorgerufenen [[Immunsuppression]] sollte der Impfschutz aktualisiert und bei längerfristiger Behandlung alle fünf Jahre aufgefrischt werden.<ref name=":10" /><ref name=":11" /><ref name=":12">{{Literatur |Autor=Hans-Jürgen Laws, Ulrich Baumann, Christian Bogdan, Gerd Burchard, Maximilian Christopeit |Titel=Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen. (III) Impfen bei hämatologischen und onkologischen Erkrankungen (antineoplastische Therapie, Stammzelltransplantation), Organtransplantation und Asplenie |Sammelwerk=Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz |Band=63 |Nummer=5 |Datum=2020-05 |ISSN=1436-9990 |DOI=10.1007/s00103-020-03123-w |PMC=7223132 |PMID=32350583 |Seiten=588–644 |Online=https://link.springer.com/10.1007/s00103-020-03123-w |Abruf=2021-10-13}}</ref> |
|||
* [[Transplantation]]: Es wird ein erhöhtes Risiko für invasive Meningokokken-Erkrankungen (IME) nach Gewebe- oder Organtransplantationen angenommen, weshalb vor der Operation ein Impfschutz aufgebaut und anschließend alle fünf Jahre aufgefrischt werden sollte.<ref name=":12" /> |
|||
* [[Dialyse#H%C3%A4modialyse|Hämodialyse]] als Nierenersatzverfahren: Die amerikanischen [[Centers for Disease Control and Prevention]] (CDC) empfehlen die Impfung für Erwachsene unter einer Dialyse-Behandlung, wenn zusätzliche Risikofaktoren vorliegen.<ref>{{Literatur |Titel=Recommended Adult Immunization Schedule for ages 19 years or older |Hrsg=Centers for Disease Control and Prevention |Datum=2021 |Online=https://www.cdc.gov/vaccines/schedules/downloads/adult/adult-combined-schedule.pdf}}</ref> |
|||
| ⚫ | Auch Reisende in Gebiete, in denen Meningokokken-Infektionen häufig auftreten, tragen ein erhöhtes Infektionsrisiko, wenn sie sich dort länger aufhalten oder engen Kontakt zur Bevölkerung haben. Schließlich sollten Säuglinge, Kinder oder Jugendliche bei Vorliegen eines erhöhten Risikos für invasive Meningokokken-Erkrankungen entsprechend geimpft werden.<ref name=":3" />Der Berliner Impfbeirat empfiehlt seit Juli 2013 [[Männer, die Sex mit Männern haben|Männern, die Sex mit Männern haben]] (MSM), sich mit einem Impfstoff impfen zu lassen, der eine Komponente gegen Meningokokken der Gruppe C enthält und für Erwachsene zugelassen ist. Anlass für die Impfempfehlung sind gehäufte Erkrankungsausbrüche im MSM-Kreis mit schweren, auch tödlichen Verläufen, wie sie jüngst auch aus New York, Paris und Berlin beschrieben wurden.<ref name="zeit20130720">[http://www.zeit.de/wissen/gesundheit/2013-07/meningokokken-homosexualitaet-berlin/komplettansicht ''Berlin empfiehlt schwulen Männern Impfung''.] [[Die Zeit|Zeit Online]], 20. Juli 2013.</ref><ref>[http://www.berlin.de/sen/gessoz/presse/archiv/20130718.1630.387129.html ''Empfehlung des Berliner Impfbeirates zur Impfung gegen Meningokokken-Erkrankungen''.] Berliner Senatsverwaltung für Gesundheit und Soziales, Pressemitteilung vom 18. Juli 2013.</ref><ref>[https://www.berlin.de/sen/gesundheit/_assets/themen/gesundheitsschutz-und-umwelt/infektionsschutz/rundschreiben-vom-07012015.pdf Rundschreiben über die öffentlich empfohlene Meningokokken-Schutzimpfung] (PDF) Berliner Senatsverwaltung für Gesundheit und Soziales, 7. Dezember 2014.</ref><ref>{{Literatur |Autor=Wiebke Hellenbrand, Heike Claus, Susanne Schink, Ulrich Marcus, Ole Wichmann |Titel=Risk of Invasive Meningococcal Disease in Men Who Have Sex with Men: Lessons Learned from an Outbreak in Germany, 2012—2013 |Sammelwerk=PLOS ONE |Band=11 |Nummer=8 |Datum=2016-03-08 |ISSN=1932-6203 |DOI=10.1371/journal.pone.0160126 |PMC=4972413 |PMID=27486669 |Seiten=e0160126 |Online=https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0160126 |Abruf=2021-10-13}}</ref> |
||
[[Saudi-Arabien]] verlangt während der [[Mekka]]-[[Wallfahrt]]en von [[Pilger]]n und Besuchern eine aktuelle Impfbescheinigung. Die Impfung muss mindestens zehn Tage vor der Einreise erfolgen. Konjugatimpfstoffe haben eine Gültigkeit von fünf Jahren, bei fehlender Angabe des Impfstofftyps oder Verwendung des Polysaccharidimpfstoffs beträgt die Gültigkeit drei Jahre.<ref>{{Internetquelle |url=https://www.crm.de/transform.asp?Domain=CRM&Sprache=de&Bereich=laender&Klientel=laie&Auspraegung=kurz&HTMLfragmente=no&RGI=&NN=&land=168 |titel=Reisemedizinische Länderinformationen Saudi-Arabien (2021) |hrsg=Centrum für Reisemedizin |datum=2021 |sprache=de |abruf=2021-10-13}}</ref> Pflicht ist der ''Vierfach-Impfstoff A,C,W,Y''. |
|||
| ⚫ | |||
| ⚫ | Ein Schutz wird nur gegen die jeweils genannten [[Serotyp|Serogruppen]] aufgebaut. Die Impfung gegen die weltweit, auch in Europa, häufiger vorkommende Meningitis durch Meningokokken der Serogruppe B<ref>{{Literatur |Autor=Ali Purmohamad, Elham Abasi, Taher Azimi, Sareh Hosseini, Hossein Safari |Titel=Global estimate of Neisseria meningitidis serogroups proportion in invasive meningococcal disease: A systematic review and meta-analysis |Sammelwerk=Microbial Pathogenesis |Band=134 |Datum=2019-09 |DOI=10.1016/j.micpath.2019.103571 |Seiten=103571 |Online=https://linkinghub.elsevier.com/retrieve/pii/S088240101930467X |Abruf=2021-10-13}}</ref> wird zurzeit von der Ständigen Impfkommission noch nicht allgemein empfohlen, da die vorliegenden Studiendaten und die daraus resultierende [[Evidenz]] dafür noch nicht ausreichen.<ref name=":9">{{Internetquelle |autor= |url=https://www.rki.de/SharedDocs/FAQ/Impfen/Meningokokken/faq_ges.html |titel=Schutzimpfung gegen Meningokokken: Häufig gestellte Fragen und Antworten |werk=RKI |datum=2021-06-01 |abruf=2021-10-11}}</ref> Die STIKO weist aber darauf hin, dass eine Impfung {{"|für Personen mit erhöhtem Erkrankungsrisiko nach individueller Nutzen-Risiko-Abwägung sinnvoll sein kann}}.<ref name="STIKO_Bexsero_2013-12-09">{{Internetquelle |url=http://www.rki.de/DE/Content/Infekt/EpidBull/Archiv/2013/Ausgaben/49_13.html |titel=Ständige Impfkommission (STIKO) am RKI: Stellungnahme zum neuen Meningokokken-B-Impfstoff |werk=[[Epidemiologisches Bulletin]] 49/2013 |hrsg=Robert-Koch-Institut |datum=2013-12-09 |seiten=495–498 |zugriff=2014-05-17}}</ref> Falls mit ''Bexsero'' geimpft wird, dann sollen für die Grundimmunisierung Kinder im Alter von 2 bis 5 Monaten drei Impfstoffdosen (Mindestabstand ein Monat) oder zwei Impfstoffdosen (Mindestabstand zwei Monate) erhalten, Kinder von 6 bis 23 Monaten zwei Impfstoffdosen (Mindestabstand 2 Monate) und alle Kinder/Erwachsene ab 2 bis 50 Jahren zwei Impfstoffdosen (Mindestabstand 1 Monat).<ref name=":5" /> Bei der Grundimmunisierung mit ''Trumenba'' werden Kinder über 10 Jahren zweimal geimpft (Mindestabstand 6 Monate); alternativ erhalten diese drei Impfstoffdosen (erster Mindestabstand 1 Monat, dann 4 Monate). Die Meningokokken-Impfung kann meistens gleichzeitig mit anderen Schutzimpfungen vorgenommen werden. |
||
Die Meningokokken-Impfung kann meistens gleichzeitig mit anderen Schutzimpfungen vorgenommen werden. Zeitabstände zu anderen Impfungen sind nicht einzuhalten. |
|||
=== Nebenwirkungen === |
=== Nebenwirkungen === |
||
Version vom 13. Oktober 2021, 10:36 Uhr
| Meningokokken | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
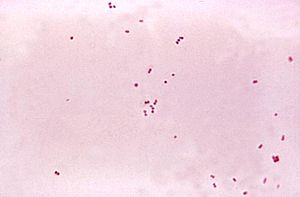
Neisseria meningitidis | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Neisseria meningitidis | ||||||||||||
| (Albrecht & Ghon 1901) Murray 1929 |
Meningokokken (Neisseria meningitidis, früher Meningococcus meningitis) sind gramnegative intrazelluläre Bakterien, die als Diplokokken auftreten. Sie besiedeln beim Menschen den Nasenrachenraum und können schwere Krankheiten auslösen. Etwa zehn Prozent der europäischen Bevölkerung tragen diese Bakterien im Nasenrachenraum, ohne dabei Krankheitsanzeichen zu entwickeln.
Merkmale
Meningokokken sind Bakterien der Art Neisseria meningitidis, die zu den aerob und fakultativ anaerob wachsenden, gramnegativen Kokken gehört. Die Bakterien können sich durch die Hochregulation von nitrat- statt sauerstoffabhängigen Enzymen ihres Zuckerstoffwechsels an die anaeroben Verhältnisse im infizierten Gewebe anpassen.[1] In flüssigen Nährmedien (sowie auch in der Gehirn- und Rückenmarksflüssigkeit) lagern sich die Bakterien in Pärchen zusammen (Diplokokken), bei denen die Längsachsen der beiden Bakterien nebeneinander gelagert sind. Die Enden der Bakterien sind dabei abgerundet, sodass ein einzelnes Bakterium an eine Kaffeebohne, ein Pärchen jeweils entfernt an ein Brötchen erinnert (daher die Beschreibung als semmelförmige gramnegative Diplokokken). Bei einer durch diese Bakterien ausgelösten Meningitis findet man in der Gehirn- und Rückenmarksflüssigkeit (Liquor cerebrospinalis) zusätzlich fast immer zahlreiche weiße Blutkörperchen (Granulozyten).
Meningokokken wurden erstmals 1887 durch Anton Weichselbaum kultiviert (aus Patienten mit einer Meningitis).[2] Sie wachsen im Labor auf reichhaltigen Nährböden wie z. B. Kochblutagar oder Columbia-Blutagar sowie aufgrund ihrer Resistenz gegen Colistin auch auf Spezialnährböden zur Anzucht von pathogenen Neisserienarten wie z. B. Thayer-Martin-Agar. Am besten gelingt die Kultur in einer Atmosphäre, die einen erhöhten Kohlendioxid-Gehalt (ca. 5–10 %) aufweist.[2] Die Kolonien sind nach 24 Stunden Wachstum klein (ca. 1 mm Durchmesser), glatt, rund und von gräulicher Farbe. Sie bilden Cytochrom-c-Oxidase und reagieren daher im Oxidase-Test positiv. In der Literatur sind auch flüssige Nährmedien beschrieben.[3][4]
Innerhalb der Art Neisseria meningitidis sind aufgrund der Zusammensetzung der Kapselpolysaccharide 12 verschiedene Serogruppen bekannt: A, B, C, E (ehemals 29E), H, I, K, L, W (ehemals W-135), X, Y und Z.[2][5] Die ehemalige Gruppe D hat sich als unbekapselte Variante der Gruppe C herausgestellt.[2] Bei Erkrankten werden in der Regel nur die Serogruppen A (vor allem im afrikanischen „Meningitisgürtel“), B, C, W, Y und selten auch X (ebenfalls vorwiegend in Afrika) nachgewiesen. Bei Meningokokken-Infektionen in Deutschland wird am häufigsten die Serogruppe B nachgewiesen, gefolgt von C. Die Serogruppen unterscheiden sich in ihrer Oberflächenstruktur, welche unter anderem aus speziellen Zuckermolekülen besteht. Diese und andere Moleküle bilden eine dicke Kapsel um die Bakterien, die diese vor den Angriffen des Immunsystems schützt. Durch molekulare Feintypisierung der variablen Regionen äußerer Membranproteine (Porine PorA und FetA bzw. PorB[2]) lassen sich Meningokokken ferner in Serosubtypen mit unterschiedlichen Virulenzeigenschaften klassifizieren (z. B. B:P1.7–2,4:F1–5).[6][5]
Übertragungswege
Meningokokken werden durch Tröpfcheninfektion von Mensch zu Mensch beispielsweise beim Anhusten, Niesen oder Küssen übertragen. Begünstigt wird dies durch enge Unterkünfte oder Kindergärten bzw. Schulen.[6] Sie heften sich mithilfe kleiner Fortsätze (Pili) an die Schleimhäute des Nasenrachenraumes, wo sie wochen- oder monatelang bleiben können. Häufig verläuft die Besiedelung asymptomatisch.[6] Vor allem, wenn das Immunsystem geschwächt ist, etwa durch andere Infektionen, und abhängig vom Virulenzfaktor[2], vermehren sich die Bakterien, durchdringen die Schleimhäute (Mukosabarriere) und lösen Hirnhautentzündungen und Blutvergiftungen aus. Hierbei wirkt die Bekapselung einer Opsonisierung und Phagozytose des Immunsystems entgegen. Wenn die Bakterien im Blutstrom zirkulieren, ist die Milz an der Entfernung beteiligt. Daher besteht die Gefahr für Patienten mit eingeschränkter Milzfunktion, dass eine invasive Meningokokken-Infektion schwerer verläuft.[2]
Der Mensch ist das einzige Erregerreservoir für Meningokokken.[6]
Epidemiologie
Weltweit werden mehr als 90 Prozent der Meningokokken-Infektionen durch bestimmte Serotypen, Typ A, B, C, W und Y, hervorgerufen. In Deutschland wurden vor 2004 etwa 700 bis 800 invasive Meningokokken-Erkrankungen jährlich registriert.[7] Einige Fälle werden von Reisenden aus dem europäischen Ausland eingeschleppt. Die Inzidenz ist seit 2004 rückläufig: Sie sank auf jährlich 0,4 pro 100.000 Einwohnern (Stand 2014).[5] Etwa 60 Prozent werden durch den Serotyp B verursacht, gefolgt von den Serotypen C, W und Y. Der Anteil der Erkrankungen vom Serotyp C, insbesondere bei Kleinkindern, ist seit Einführung der Meningokokken-C-Impfung zurückgegangen: 2006 wurden 137 Krankheitsfälle gemeldet, 2010 dann 76, 2015 noch 41 und 2019 schließlich 27 Erkrankungen.[8][5]
40 Prozent aller Patienten sind Kinder unter vier Jahren, mit Abstand am häufigsten sind Säuglinge im ersten Lebensjahr betroffen. Auch heute noch sterben etwa zehn Prozent der Patienten. Insgesamt liegt die Letalität bei etwa 8–10 %.[6]
Am Ende der Trockenzeit (März/April) kommen Meningokokken-Epidemien überwiegend der Serogruppe A im afrikanischen „Meningitisgürtel“ vor (zwischen südlicher Sahara und Äquatorialwäldern wie bei Senegal, Ghana, Nigeria, bis nach Sudan).[6] Von November bis Mai treten sie auch gehäuft in Indien, vor allem Nordindien, und Nepal auf. In gemäßigten Zonen werden epidemische Häufungen im späten Winter bzw. frühen Frühling verzeichnet.[6] Dies lässt darauf schließen, dass eine geringe Luftfeuchtigkeit eine Infektion begünstigt, da die Schleimhäute durch Austrocknen vorgeschädigt werden können.[6]
Im Jahr 2012 wurde in der Gruppe der Männer, die Sex mit Männern haben, erstmals ein erhöhtes Infektionsrisiko in Metropolen wie New York und Berlin festgestellt.[9] Verschiedene Ausbrüche unter anderem in Deutschland legen zudem nahe, dass Meningokokken sexuell übertragbar sein könnten.[10]
Krankheitsbild (Symptome)
| Klassifikation nach ICD-10 | |
|---|---|
| A39 | Meningokokkeninfektion |
| ICD-10 online (WHO-Version 2019) | |

Die Inkubationszeit beträgt in der Regel 3–4 Tage, kürzere und längere Inkubationszeiten (2–10 Tage) werden ebenfalls beobachtet.
Das Spektrum der Erkrankung reicht von leichten Verläufen mit spontaner Abheilung bis hin zu einem hochakuten Ausbruch, der trotz Behandlung in wenigen Stunden zum Tod führt. Bezeichnend für eine Entzündung der Hirnhäute (Pia mater und Arachnoidea)[6] ist die sogenannte Meningokokkenmeningitis, genannt auch Meningitis cerebrospinalis epidemica und übertragbare Genickstarre[12]. Sie beginnt mit starkem Krankheitsgefühl wie Abgeschlagenheit, hohem Fieber, Übelkeit und Erbrechen, Schüttelfrost, Gelenk- und Muskelschmerzen, Krämpfen oder Bewusstseinsstörungen. Als typisches Zeichen einer Hirnhautentzündung tritt die Nackensteifigkeit auf; diese bewirkt dann das sogenannte Kissenbohren: wenn der Patient liegt, zeigt sich ein überstrecktes Hohlkreuz und der Kopf drückt sich in das Kissen (Opisthotonus). Ungefähr die Hälfte der Patienten hat Petechien wegen der hämatogenen Erregerstreuung (Bakteriämie oder Sepsis).[6]
Bei Säuglingen kann neben dem fast immer auftretenden Fieber die Symptomatik zunächst wenig eindeutig sein: Apathie oder Unruhe, Nahrungsverweigerung und Berührungsempfindlichkeit. Lichtempfindlichkeit ist ein mögliches Begleitsymptom.
Bewusstseinstrübung, punktförmige Hautblutungen und Kreislaufkollaps sind Hinweise auf einen lebensbedrohenden Krankheitsverlauf (Waterhouse-Friderichsen-Syndrom). In schweren Fällen tritt der Tod schon innerhalb weniger Stunden ein.
Treten die Bakterien in die Blutbahn über und überschwemmen den Körper mit ihren Giftstoffen, spricht man von einer Sepsis. Sie ist lebensbedrohlich. Bei schnellem Verlauf hin zur Sepsis müssen die „meningitischen“ Symptome nicht auftreten; die Schock- und toxisch bedingten Symptome stehen dann im Vordergrund. Bei nicht zeitnaher Behandlung kann es durch die Sepsis zum Verlust von Gliedmaßen kommen.[13]
Entscheidend ist eine möglichst frühe Behandlung mit Antibiotika. Trotz Behandlung können Komplikationen und Spätfolgen wie Hörverlust, Blindheit, Lähmungen oder Krampfleiden auftreten und für jeden zehnten Patienten kommt jede Hilfe zu spät. Deshalb ist die vorbeugende Schutzimpfung für gefährdete Personen
(beispielsweise aufgrund eines angeborenen oder erworbenen Immundefekts) besonders wichtig.
Enge Kontaktpersonen von Patienten mit einer invasiven Meningokokken-Infektion (IME) sollten eine vorbeugende Therapie mit einem Antibiotikum (etwa Rifampicin) sowie eine postexpositionelle Impfung erhalten, sofern sie über keinen aktuellen Impfschutz gegen die entsprechende Serogruppe verfügen.[14]
Therapie
Sind Meningokokken als Erreger nachgewiesen worden, ist das Antibiotikum der Wahl Penicillin G oder ein Cephalosporin der 3. Generation (Ceftriaxon). Der Vorteil von Ceftriaxon ist das Erfassen weiterer bakterieller Meningitiserreger. Wichtig ist das frühzeitige Therapieren. Daher ist es in der Praxis üblich, bei Verdacht auf eine eitrige Meningitis sofort, noch vor dem Erregernachweis, Cephalosporine der 3. Generation zu verabreichen; zusätzlich ist die Gabe von Ampicillin zu erwägen, um auch eine Listerien-Meningitis antibiotisch abzudecken.
Chemoprophylaxe
Um bei Kontaktpersonen von Infizierten einer Erkrankung mit Meningokokken vorzubeugen, wird eine Chemoprophylaxe empfohlen. Die Prophylaxe ist indiziert, falls der Kontakt in den letzten sieben Tagen vor der Erkrankung stattgefunden hat. Die Behandlung sollte möglichst bald nach der Diagnosestellung beim Indexfall erfolgen, ist aber bis zu 10 Tage nach der letzten Exposition sinnvoll. Hierbei einsetzbare Chemotherapeutika sind Rifampicin und dessen Alternativen Ciprofloxacin, Ceftriaxon sowie Azithromycin. Auch der Erkrankte sollte, wenn er zur Behandlung nicht ein Cephalosporin der dritten Generation intravenös erhalten hatte, nach Abschluss seiner Therapie eine Prophylaxe mit Rifampicin erhalten.[15][14]
Impfung (Immunprophylaxe)
Erste Versuche der Impfstoffherstellung wurden Beginn des 20. Jahrhunderts mit abgetöteten Zellen des Erregers unternommen. Zwischen 1900 und 1940 gab es zwar viele Studien zur Wirksamkeit, diese waren aber von schlechter Qualität, was die Aussagekraft erheblich gesenkt hatte.[2] Durch die Entdeckung von Antibiotika wurde die Entwicklung geeigneter Impfstoffe zunächst zurückgestellt. Das Auftreten erster Sulfonamid-resistenter Stämme in den 1960er-Jahren stellte gerade für Militärrekruten während des Vietnamkrieges ein ernstzunehmendes Problem dar, was die Impfstoffentwicklung wieder bestärkte.[2] Ende der 1960er Jahre konnte durch die Arbeiten von Emil C. Gotschlich und Mitarbeitern Polysaccharide aus N. meningitidis isoliert und gereinigt werden, die sicher und ausreichend immunogen waren.[2] Aufgrund gewisser Limitationen der Polysaccharid-Impfstoffe (z. B. fehlende T-Zell-abhängige Immunantwort, keinen Einfluss auf den Trägerstatus der entsprechenden Meningokokkenserogruppen im Nasen-Rachen-Raum[6]) wurde aufgrund der guten Erfahrungen von Hib-Impfstoffen ebenfalls an Konjugatimpfstoffen für Meningokokken geforscht. Dies mündete 1999, auch auf Druck der Öffentlichkeit, in der Zulassung eines ersten, monovalenten Konjugatimpfstoffes gegen Meningokokken der Gruppe C in Großbritannien auf Grundlage von Immunogentiäts- und Verträglichkeitsdaten – ein Wirksamkeitsnachweis war vorher nicht erfolgt.[2][6]
Zur Vorbeugung einer Meningokokkeninfektion, etwa vor einer geplanten Milzentfernung, Konjugatimpfstoffe gegen den Serotyp C zur Verfügung, der beispielsweise in England, Spanien oder auch in einigen Regionen Deutschlands gehäuft auftritt, zudem gegen die Typen A, W und Y. Außerdem wurden ab 2013 erste Impfstoffe gegen N. meningitidis der Gruppe B in Europa zugelassen. In Kuba wurde bereits 1988 ein Impfstoff gegen die Gruppe B eingesetzt[16][17]. Auch in Neuseeland gab es ab 2004 einen Impfstoff (MeNZB) gegen einen speziellen Erregertyp der Gruppe B, der damals nur dort vorgekommen ist; der Impfstoff wird heute nicht mehr hergestellt.[7][18]
Die Impfung ist die zuverlässigste Maßnahme zur Prävention invasiver Meningokokkeninfektionen.[6]
Polysaccharid-Impfstoffe
Bei Polysaccharid-Impfstoffen verwendet man gereinigte, gruppenspezifische Kapselpolysaccharide (PS), damit Teile der Bakterienhülle.[6] Bei den früher erhältlichen Polysaccharid-Impfstoffen wurde ein Schutz gegen die Serotypen A und C (AC-Impfstoff, etwa Meningokokken-Impfstoff A+C Mérieux, nicht mehr vermarktet[19]) bzw. gegen die Serotypen A, C, W und Y (etwa der ehemalige Impfstoff Mencevax ACWY, dessen Vermarktung 2013 endete und nicht mehr ausgeliefert wird[20][6]) aufgebaut. Zwar stimulieren PS der Gruppe A im Gegensatz zu den PS der Gruppen C, W und Y im Säuglingsalter bereits das T-Zell-Immunsystem, sodass nach einmaliger Gabe IgG-Antikörper gebildet werden. Jedoch erreichen die Serumantikörper selbst nach Booster nach einem Jahr wieder die Ausgangswerte vor der Impfung. Zudem hat man bei einer Impfung unter zwei Jahren mit PS der Gruppe C beobachtet, dass sich eine anhaltende, einen Boostereffekt inhibierende Immuntoleranz bildet. Daher schützen beide Polysaccharid-Impfstoffe am besten ab einem Alter von zwei Jahren, da erst ab diesem Alter eine T-zellunabhängige B-Zellaktivierung möglich ist. Die altersabhängige Wirksamkeit der Impfung gegenüber Gruppe-C-Infektionen wurde aufgrund eines Meningokokkenausbruchs in Quebec ermittelt: Sie beträgt 41 % bei Kindern von 2–9 Jahren, 75 % bei Kindern von 10–14 Jahren und 83 % bei Kindern und jungen Erwachsenen von 15–20 Jahren.[6]
Polysaccharid-Impfstoffe werden unter die Haut gespritzt. Der Impfschutz hält mindestens drei Jahre. Für Erwachsene und Kinder genügt eine einmalige Injektion. Der AC-Impfstoff kann ab einem Alter von 18 Monaten eingesetzt werden. Der ACWY-Impfstoff ist ab zwei Jahren wirksam. Bei jüngeren Kindern ist ein Schutz gegen die Gruppen C, W und Y nicht gesichert und der Impfschutz hält höchstens zwei Jahre an. Um einen besseren Impfschutz zu erreichen, können Kinder unter zwei Jahren im Abstand von drei Monaten auch ein zweites Mal geimpft werden. Die Schutzwirkung der Impfung setzt etwa nach zwei Wochen ein. Bei bestehendem Infektionsrisiko ist nach drei Jahren eine Wiederholungsimpfung ratsam.
Polysaccharid-Impfstoffe wurden größtenteils durch Konjugatimpfstoffe ersetzt.[2]
Konjugatimpfstoffe
Speziell für Kinder im Alter zwischen zwei Monaten und zwei Jahren sind sogenannte Konjugatimpfstoffe entwickelt worden. Sie können bei Bedarf aber auch bei älteren Kindern, Jugendlichen oder Erwachsenen eingesetzt werden. Bei einem Konjugatimpfstoff sind die Teile der Bakterienhülle zusätzlich an ein Eiweiß (Protein) gebunden, wodurch eine bessere T-Zell-abhängige Immunantwort erzielt wird. Die Kapselantigene können beispielsweise an der ungiftigen Variante des Diphtherietoxins CRM197 aus Corynebacterium diphtheriae (z. B. bei Menveo[21]) oder an ein Tetanustoxoid-Trägerprotein konjugiert sein (z. B. bei Nimenrix[22]).
In Deutschland sind drei C-Konjugat-Impfstoffe ab dem Alter von 2 Monaten zugelassen: Meningitec, Menjugate und NeisVac-C.[19] Sie schützen vor Infektionen mit Meningokokken des Serotyps C, der in Deutschland etwa jede fünfte Erkrankung verursacht. Die Impfung mit solchen Konjugatimpfstoffen kann bei Bedarf ab dem dritten Lebensjahr mit einem Polysaccharidimpfstoff ergänzt werden. Als Adjuvans enthalten C-Konjugat-Impfstoffe Aluminiumhydroxid.[6] Die Wirksamkeit der Impfung wurde anhand von Fall-Kontrollstudien in Großbritannien ermittelt, das als erstes Land ein nationales Impfprogramm gegen Meningokokken 1999 initiiert hatte.[6] Für Kinder im Alter von 1–2 Jahren und Jugendlichen im Alter von 15–17 Jahren wurde eine Wirksamkeit von 92 % bzw. 97 % ermittelt. Dies erklärt auch den schnellen und signifikanten Rückgang invasiver Meningokokkeninfektionen der Gruppe C.[6] Epidemiologische Beobachtungsstudien anderer Länder bestätigten die hohe Wirksamkeit des Konjugatimpfstoffes. Zudem reduzieren Konjugatimpfstoffe auch die entsprechenden Meningokokkenserogruppen im Nasen-Rachen-Raum.[6]
Im Oktober 2010 wurde in Europa ein tetravalenter Konjugatimpfstoff gegen A, C, W und Y (Menveo) zugelassen, ursprünglich für 11- bis 55-Jährige, ab 2011 auch für 2- bis 10-jährige Kinder.[23] 2012 folgte ein zweiter tetravalenter Konjugatimpfstoff, Nimenrix, welcher ab einem Alter von 6 Wochen zugelassen ist.[24] Diese beiden Impfstoffe sind nicht nur früher als der entsprechende Polysaccharidimpfstoff einsetzbar, sondern zudem auch auffrischbar, da hier – im Gegensatz zu Polysaccharidimpfstoffen – ein immunologisches Gedächtnis gebildet wird. Zudem erlaubt die T-Zellhilfe einen Klassenwechsel, sodass auch IgA gebildet werden kann (Polysaccharidimpfstofe nur IgM) und damit der Trägerstatus vermindert werden sollte. Sie weisen damit eine bessere Immunogenität auf.[6]
Seit dem Januar 2013 ist in Europa ein wirksamer rekombinanter Adsorbatimpfstoff (Bexsero[25]) gegen den Serotyp B zugelassen. Er basiert nicht auf Kapsel-Antigenen wie bei den Serotypen A, C, W und Y, da die Kapsel des Serotyps B dem menschlichen neuronalen Zelladhäsionsprotein 1 (NCAM-1) ähnelt, sondern auf vier immunogene Oberflächenantigene („4CMenB“ bzw. „MenB-4C“).[26][27] Diese wurde durch sogenannte reverse Vakzinologie entwickelt (umgekehrte Impfstoffentwicklung). Hierbei wurden besonders immunogene, potenzielle Oberflächenproteinantigene mit Hilfe einer Computeranalyse des N.-meningitidis-Genoms identifiziert, anschließend exprimiert und dann Mäusen immunisiert: Es sind das Faktor-H-Bindungsprotein fHbp („factor H binding protein“), das Neisseria Adhäsin A NadA („Neisserial adhesin A“), das Neisseria-Heparin-Bindungsantigen NHBA („Neisserial Heparin Binding Antigen“) sowie das PorA-Protein („Porin A P1.4“).[27][28] Die Oberflächenproteine werden vom Großteil aller zirkulierenden MenB-Stämmen exprimiert (beziehungsweise wenigstens zu einem ausreichenden Grad).[27] Bexsero ist für die aktive Immunisierung im Alter ab 2 Monaten und älter gegen invasive Meningokokken-Erkrankungen indiziert.
Ebenfalls zugelassen gegen N. meningitidis der Gruppe B ist Trumenba[29] („rLP2086“) für Personen ab einem Alter von 10 Jahren. Die fHbp-Komponenten sind lipidiert, da die Antigene in dieser Form zu einer verbesserten Immunantwort geführt hatten.[27]
Impfempfehlungen
Die Ständige Impfkommission (STIKO) empfiehlt seit 2006[30] die Impfung gegen Meningokokken der Serogruppe C mit dem C-Konjugat-Impfstoff standardmäßig für alle Kinder ab 12 Monate (Beginn des 2. Lebensjahres).[31][5] Dabei werden die Reduzierung der Morbidität invasiver Meningokokken-Erkrankungen durch diese Serogruppe und der resultierenden Folgen wie Hospitalisierung, schwere Komplikationen, Behinderung und Tod als primäres Ziel angesehen. Für noch nicht geimpfte Kinder und Jugendliche wird das Nachholen der Impfung bis zum 18. Lebensjahr empfohlen.[31] 2011 betrug die Impfquote von Kleinkindern etwa 80 %[5], diese stieg 2017 auf fast 90 %.[8]
Außerdem empfiehlt die STIKO die Immunisierung mit einem Meningokokken-ACWY-Konjugatimpfstoff sowie mit einem Meningokokken-B-Impfstoff für alle Risikogruppen. Dazu zählen neben beruflich exponierten Personen (etwa Laborpersonal) insbesondere Menschen mit angeborener oder erworbener Immunschwäche.[14] Diese erkranken durchschnittlich häufiger an Infektionskrankheiten und erleiden öfter einen schweren Verlauf.[14][32] Da der Impfschutz gegen alle Meningokokken-Serogruppen mittels Totimpfstoffen erzeugt wird, besteht in der Regel kein erhöhtes Risiko für Komplikationen bei immungeschwächten Personen.[32][33]
Ursachen für die Immunschwäche können unter anderem sein:
- Primäre oder erworbene Immundefekte, z. B. DiGeorge-Syndrom, Common Variable Immunodeficiency (CVID), Hypogammaglobulinämie, Defekte des Toll-like Rezeptor Signalwegs, HIV-Infektion, AIDS, Komplement-/Properdin-Defizienz, Asplenie[A][14]
- Autoimmunerkrankungen wie Erkrankungen des rheumatischen Formenkreises und chronisch-entzündliche Darmerkrankungen[14][32]
- Immunmodulatorische Therapie, z. B. Behandlung mit C5-Komplement-Inhibitoren oder Therapie bei Psoriasis oder onkologischer Erkrankungen; mindestens 2 Wochen vor Beginn einer medikamentös hervorgerufenen Immunsuppression sollte der Impfschutz aktualisiert und bei längerfristiger Behandlung alle fünf Jahre aufgefrischt werden.[14][32][34]
- Transplantation: Es wird ein erhöhtes Risiko für invasive Meningokokken-Erkrankungen (IME) nach Gewebe- oder Organtransplantationen angenommen, weshalb vor der Operation ein Impfschutz aufgebaut und anschließend alle fünf Jahre aufgefrischt werden sollte.[34]
- Hämodialyse als Nierenersatzverfahren: Die amerikanischen Centers for Disease Control and Prevention (CDC) empfehlen die Impfung für Erwachsene unter einer Dialyse-Behandlung, wenn zusätzliche Risikofaktoren vorliegen.[35]
Auch Reisende in Gebiete, in denen Meningokokken-Infektionen häufig auftreten, tragen ein erhöhtes Infektionsrisiko, wenn sie sich dort länger aufhalten oder engen Kontakt zur Bevölkerung haben. Schließlich sollten Säuglinge, Kinder oder Jugendliche bei Vorliegen eines erhöhten Risikos für invasive Meningokokken-Erkrankungen entsprechend geimpft werden.[5]Der Berliner Impfbeirat empfiehlt seit Juli 2013 Männern, die Sex mit Männern haben (MSM), sich mit einem Impfstoff impfen zu lassen, der eine Komponente gegen Meningokokken der Gruppe C enthält und für Erwachsene zugelassen ist. Anlass für die Impfempfehlung sind gehäufte Erkrankungsausbrüche im MSM-Kreis mit schweren, auch tödlichen Verläufen, wie sie jüngst auch aus New York, Paris und Berlin beschrieben wurden.[9][36][37][38]
Saudi-Arabien verlangt während der Mekka-Wallfahrten von Pilgern und Besuchern eine aktuelle Impfbescheinigung. Die Impfung muss mindestens zehn Tage vor der Einreise erfolgen. Konjugatimpfstoffe haben eine Gültigkeit von fünf Jahren, bei fehlender Angabe des Impfstofftyps oder Verwendung des Polysaccharidimpfstoffs beträgt die Gültigkeit drei Jahre.[39] Pflicht ist der Vierfach-Impfstoff A,C,W,Y.
Ein Schutz wird nur gegen die jeweils genannten Serogruppen aufgebaut. Die Impfung gegen die weltweit, auch in Europa, häufiger vorkommende Meningitis durch Meningokokken der Serogruppe B[40] wird zurzeit von der Ständigen Impfkommission noch nicht allgemein empfohlen, da die vorliegenden Studiendaten und die daraus resultierende Evidenz dafür noch nicht ausreichen.[41] Die STIKO weist aber darauf hin, dass eine Impfung „für Personen mit erhöhtem Erkrankungsrisiko nach individueller Nutzen-Risiko-Abwägung sinnvoll sein kann“.[42] Falls mit Bexsero geimpft wird, dann sollen für die Grundimmunisierung Kinder im Alter von 2 bis 5 Monaten drei Impfstoffdosen (Mindestabstand ein Monat) oder zwei Impfstoffdosen (Mindestabstand zwei Monate) erhalten, Kinder von 6 bis 23 Monaten zwei Impfstoffdosen (Mindestabstand 2 Monate) und alle Kinder/Erwachsene ab 2 bis 50 Jahren zwei Impfstoffdosen (Mindestabstand 1 Monat).[8] Bei der Grundimmunisierung mit Trumenba werden Kinder über 10 Jahren zweimal geimpft (Mindestabstand 6 Monate); alternativ erhalten diese drei Impfstoffdosen (erster Mindestabstand 1 Monat, dann 4 Monate). Die Meningokokken-Impfung kann meistens gleichzeitig mit anderen Schutzimpfungen vorgenommen werden.
Nebenwirkungen
Bei den Polysaccharid- und Konjugatimpfstoffen werden ähnliche Nebenwirkungen beobachtet wie bei den Standardimpfungen anderer Totimpfstoffe, daher treten lokale Reaktionen, Fieber und andere unspezifische, systemische Nebenwirkungen ähnlich häufig auf.[6]
Nach der Impfung mit Konjugatimpfstoffen bei Säuglingen und Kleinkindern wurde häufig bis sehr häufig von geringgradigen Rötungen und Schwellungen an der Impfstelle sowie von Fieber (≥ 38 °C) berichtet. Es wird empfohlen, nach der Impfung die Temperatur zu überwachen, bevor es zu einem Fieberkrampf (> 39,5 °C) kommen kann.[43] Ferner traten Symptome wie Reizbarkeit, Schläfrigkeit oder Appetitlosigkeit auf.[43] In Zulassungsstudien wurden bei Jugendlichen, die den tetravalenten Konjugat- oder den Polysaccharidimpfstoff erhalten hatten, Schmerzen an der Impfstelle (49–56 %) und Kopfschmerzen (37–49 %) beobachtet. Auch Muskelschmerzen können eine mögliche Folge sein.[43]
Falls der Impfstoff gegen den Serotyp B zusammen mit dem Sechsfach- und dem Pneumokokkenimpfstoff verabreicht wird, wurden häufiger Nebenwirkungen, insbesondere Fieber, beobachtet.[41] Dieses lässt sich prophylaktisch durch die Gabe von Paracetamol abmildern, ohne dass die Bildung von Antikörpern beeinträchtigt wird.
Insgesamt liegt eine gute Verträglichkeit bei Meningokokken-Impfstoffen vor.[6]
Meldepflicht
In Deutschland ist Meningokokken-Meningitis eine meldepflichtige Krankheit nach § 6 Absatz 1 Nummer 1 des Infektionsschutzgesetzes (IfSG). Die namentliche Meldepflicht besteht bei Verdacht, Erkrankung und Tod. Meldepflichtig sind hinsichtlich der Erkrankung die feststellenden Ärzte usw. (§ 8 IfSG). Zudem ist der direkte Nachweis von Neisseria meningitidis namentlich meldepflichtig nach § 7 IfSG. Die Meldepflicht gilt nur für den direkten Nachweis aus Liquor, Blut, hämorrhagischen Hautinfiltraten oder anderen normalerweise sterilen Substraten. Meldepflichtig sind hinsichtlich des Nachweises des Erregers die Labore usw. (§ 8 IfSG).
In der Schweiz ist der positive laboranalytische Befund von Neisseria meningitidis für Laboratorien meldepflichtig und zwar nach dem Epidemiengesetz (EpG) in Verbindung mit der Epidemienverordnung und Anhang 3 der Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen. Zudem ist eine invasive Meningokokken-Erkrankung meldepflichtig für Ärzte, Spitäler usw. Grundlage sind die soeben genannten Normen und Anhang 1 der genannten Verordnung des EDI. Meldekriterien sind klinischer Verdacht und Veranlassung einer erregerspezifischen Labordiagnostik.
Literatur
- Ulrich Vogel, Matthias Frosch: Gramnegative aerobe und fakultativ anaerobe Kokken. In: Birgid Neumeister, Heinrich K. Geiss, Rüdiger W. Braun, Peter Kimmig (Hrsg.): Mikrobiologische Diagnostik. Georg Thieme Verlag, Stuttgart/ New York 2009, ISBN 978-3-13-743602-7, S. 419–425.
- Marianne Abele-Horn: Antimikrobielle Therapie. Entscheidungshilfen zur Behandlung und Prophylaxe von Infektionskrankheiten. Unter Mitarbeit von Werner Heinz, Hartwig Klinker, Johann Schurz und August Stich, 2., überarbeitete und erweiterte Auflage. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4, S. 320 f. und 327–329.
- Karl Wurm, A. M. Walter: Infektionskrankheiten. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 9–223, hier: S. 177–184.
Weblinks
Meningokokken-Erkrankungen – Informationen des Robert Koch-Instituts
- Meningokokken, invasive Erkrankungen (Neisseria meningitidis). In: RKI-Ratgeber. Robert Koch-Institut, 1. Februar 2014, abgerufen am 27. März 2020.
- www.meningococcus.de – Nationales Referenzzentrum für Meningokokken, Institut für Hygiene und Mikrobiologie, Universität Würzburg
- EpiscanGIS – Web-basiertes Geographisches Informationssystem zur Überwachung der Meningokokken-Erkrankungsfälle in Deutschland
- Meningokokken-Netz – Vergleichende Genomanalyse zur Erfassung, Bewertung und Verhütung von Meningokokken-Erkrankungen
Einzelnachweise
- ↑ E. Bartolini et al.: Role of FNR and FNR-regulated, sugar fermentation genes in Neisseria meningitidis infection. In: Molecular Microbiology. (2006); 60, S. 963–972. doi:10.1111/j.1365-2958.2006.05163.x
- ↑ a b c d e f g h i j k l Lee H. Harrison, Dan M. Granoff, und Andrew J. Pollard: Meningococcal Capsular Group A, C, W, and Y Conjugate Vaccines. In: Stanley A. Plotkin et al. (Hrsg.): Plotkin's Vaccines. 7. Auflage. Elsevier, Philadelphia 2017, ISBN 978-0-323-35761-6, S. 619 ff., doi:10.1016/B978-0-323-35761-6.00038-9.
- ↑ Ivan D. Frantz: Growth Requirements of the Meningococcus. In: Journal of Bacteriology. Band 43, Nr. 6, Juni 1942, S. 757–761, PMID 16560537.
- ↑ Jeffrey Fu et al.: Recent Advances in the Large Scale Fermentation of Neisseria meningitidis Group B for the Production of an Outer Membrane Protein Complex. In: Bio/Technology. Band 13, Nr. 2, Februar 1995, S. 170–174, doi:10.1038/nbt0295-170.
- ↑ a b c d e f g Meningokokken, invasive Erkrankungen (Neisseria meningitidis). RKI-Ratgeber. In: RKI. 1. Februar 2014, abgerufen am 2. Dezember 2020.
- ↑ a b c d e f g h i j k l m n o p q r s t u v w Ulrich Heininger: Meningokokken. In: Heinz Spiess, Ulrich Heininger, Wolfgang Jilg (Hrsg.): Impfkompendium. 8. Auflage. Georg Thieme Verlag, 2015, ISBN 978-3-13-498908-3, S. 220 ff., doi:10.1055/b-0035-127590.
- ↑ a b Lebensgefährliche Meningokokken. In: Pharmazeutische Zeitung. 13. Dezember 2004, abgerufen am 29. Dezember 2020.
- ↑ a b c Celine Müller: Warum ist der Meningokokken-B-Schutz keine Standardimpfung? In: Deutsche Apothekerzeitung. 24. August 2020, abgerufen am 29. Dezember 2020.
- ↑ a b Berlin empfiehlt schwulen Männern Impfung. Zeit Online, 20. Juli 2013.
- ↑ Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen.(II) Impfen bei 1. Primären Immundefekterkrankungen und 2. HIV-Infektion. In: Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz. Band 61, Nr. 8, August 2018, ISSN 1436-9990, S. 1034–1051, doi:10.1007/s00103-018-2761-8 (springer.com [abgerufen am 13. Oktober 2021]).
- ↑ The case for vaccination. In: North & South. Juni 2010, archiviert vom am 2. Februar 2018; abgerufen am 3. Juli 2015.
- ↑ Karl Wurm, A. M. Walter: Infektionskrankheiten. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. 1961, S. 177.
- ↑ Kein Taxi, kein Anruf, keine Hilfe. In: taz.de
- ↑ a b c d e f g Robert Koch-Institut (Hrsg.): Epidemiologisches Bulletin. 34. Auflage. 2021 (rki.de [PDF]).
- ↑ Marianne Abele-Horn (2009), S. 320 f.
- ↑ Bioboom in der Karibik. In: Der Spiegel. Nr. 27, 1999 (online).
- ↑ 50 Jahre Impfprogramm in Kuba – Eine Revolution in Sachen Gesundheit. ( vom 10. November 2011 im Internet Archive) In: Digital Granma International. 3. März 2011; abgerufen 26. April 2011.
- ↑ Petra Jungmayr: Zwei Fliegen mit einem Impfstoff. In: Deutsche Apothekerzeitung. 27. Juli 2017, abgerufen am 29. Dezember 2020.
- ↑ a b Meningokokken-Impfstoffe. In: Paul-Ehrlich-Institut. 2. November 2020, abgerufen am 29. November 2020.
- ↑ Kurz informiert. Vermarktung von Mencevax® ACWY eingestellt. In: Deutsches Ärzteblatt. 10. Mai 2013, abgerufen am 29. November 2020.
- ↑ European public assessment report von Menveo. In: EMA. 23. Januar 2020, abgerufen am 29. November 2020 (englisch).
- ↑ European public assessment report von Nimenrix. In: EMA. 23. Juli 2020, abgerufen am 29. November 2020 (englisch).
- ↑ Epidemiologisches Bulletin Nr. 32/2012. In: RKI. 13. August 2012, abgerufen am 30. November 2020.
- ↑ Nimenrix. In: Paul-Ehrlich-Institut. Abgerufen am 30. November 2020.
- ↑ European public assessment report von Bexsero. In: EMA. 2. Juli 2020, abgerufen am 30. November 2020 (englisch).
- ↑ Dan M.Granoff et al.: Meningococcal Capsular Group B Vaccines. In: Stanley A. Plotkin et al. (Hrsg.): Plotkin's Vaccines. 7. Auflage. Elsevier, Philadelphia 2017, ISBN 978-0-323-35761-6, S. 646, doi:10.1016/B978-0-323-35761-6.00053-5.
- ↑ a b c d Aktualisierte Stellungnahme der Ständigen Impfkommission (STIKO) am Robert Koch-Institut (RKI). (PDF) In: Epidemiologisches Bulletin 03/2018. Robert-Koch-Institut, 18. Januar 2018, S. 35–48, abgerufen am 31. Juli 2021.
- ↑ Cynthia Burman et al.: A review of the immunogenicity, safety and current recommendations for the meningococcal serogroup B vaccine, MenB-FHbp. In: Journal of Clinical Pharmacy and Therapeutics. Band 45, Nr. 2, April 2020, S. 270–281, doi:10.1111/jcpt.13083.
- ↑ European public assessment report von Trumenba. In: EMA. 28. Mai 2020, abgerufen am 30. November 2020 (englisch).
- ↑ Celine Müller: Meningokokken B auf dem Vormarsch? In: Deutsche Apothekerzeitung. 17. Juli 2020, abgerufen am 8. Dezember 2020.
- ↑ a b Epidemiologisches Bulletin 2012, Nr. 30 (30. Juli 2012) (PDF)
- ↑ a b c d Norbert Wagner, Frauke Assmus, Gabriele Arendt, Erika Baum, Ulrich Baumann: Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen. (IV) Impfen bei Autoimmunkrankheiten, bei anderen chronisch-entzündlichen Erkrankungen und unter immunmodulatorischer Therapie. In: Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz. Band 62, Nr. 4, April 2019, ISSN 1436-9990, S. 494–515, doi:10.1007/s00103-019-02905-1 (springer.com [abgerufen am 13. Oktober 2021]).
- ↑ Tim Niehues, Christian Bogdan, Jane Hecht, Thomas Mertens, Miriam Wiese-Posselt: Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen(I) Grundlagenpapier. In: Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz. Band 60, Nr. 6, Juni 2017, ISSN 1436-9990, S. 674–684, doi:10.1007/s00103-017-2555-4 (springer.com [abgerufen am 13. Oktober 2021]).
- ↑ a b Hans-Jürgen Laws, Ulrich Baumann, Christian Bogdan, Gerd Burchard, Maximilian Christopeit: Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen. (III) Impfen bei hämatologischen und onkologischen Erkrankungen (antineoplastische Therapie, Stammzelltransplantation), Organtransplantation und Asplenie. In: Bundesgesundheitsblatt - Gesundheitsforschung - Gesundheitsschutz. Band 63, Nr. 5, Mai 2020, ISSN 1436-9990, S. 588–644, doi:10.1007/s00103-020-03123-w, PMID 32350583, PMC 7223132 (freier Volltext) – (springer.com [abgerufen am 13. Oktober 2021]).
- ↑ Centers for Disease Control and Prevention (Hrsg.): Recommended Adult Immunization Schedule for ages 19 years or older. 2021 (cdc.gov [PDF]).
- ↑ Empfehlung des Berliner Impfbeirates zur Impfung gegen Meningokokken-Erkrankungen. Berliner Senatsverwaltung für Gesundheit und Soziales, Pressemitteilung vom 18. Juli 2013.
- ↑ Rundschreiben über die öffentlich empfohlene Meningokokken-Schutzimpfung (PDF) Berliner Senatsverwaltung für Gesundheit und Soziales, 7. Dezember 2014.
- ↑ Wiebke Hellenbrand, Heike Claus, Susanne Schink, Ulrich Marcus, Ole Wichmann: Risk of Invasive Meningococcal Disease in Men Who Have Sex with Men: Lessons Learned from an Outbreak in Germany, 2012—2013. In: PLOS ONE. Band 11, Nr. 8, 8. März 2016, ISSN 1932-6203, S. e0160126, doi:10.1371/journal.pone.0160126, PMID 27486669, PMC 4972413 (freier Volltext) – (plos.org [abgerufen am 13. Oktober 2021]).
- ↑ Reisemedizinische Länderinformationen Saudi-Arabien (2021). Centrum für Reisemedizin, 2021, abgerufen am 13. Oktober 2021.
- ↑ Ali Purmohamad, Elham Abasi, Taher Azimi, Sareh Hosseini, Hossein Safari: Global estimate of Neisseria meningitidis serogroups proportion in invasive meningococcal disease: A systematic review and meta-analysis. In: Microbial Pathogenesis. Band 134, September 2019, S. 103571, doi:10.1016/j.micpath.2019.103571 (elsevier.com [abgerufen am 13. Oktober 2021]).
- ↑ a b Schutzimpfung gegen Meningokokken: Häufig gestellte Fragen und Antworten. In: RKI. 1. Juni 2021, abgerufen am 11. Oktober 2021.
- ↑ Ständige Impfkommission (STIKO) am RKI: Stellungnahme zum neuen Meningokokken-B-Impfstoff. In: Epidemiologisches Bulletin 49/2013. Robert-Koch-Institut, 9. Dezember 2013, S. 495–498, abgerufen am 17. Mai 2014.
- ↑ a b c Meningokokken: die Krankheit und der Impfstoff. In: Infovac. 27. November 2020, abgerufen am 1. Januar 2021.