Leberzirrhose
| Klassifikation nach ICD-10 | |
|---|---|
| K74 | Fibrose und Zirrhose der Leber |
| K74.0 | Leberfibrose |
| K74.1 | Lebersklerose |
| K74.2 | Leberfibrose mit Lebersklerose |
| K74.3 | Primäre biliäre Zirrhose, chronische nichteitrige destruktive Cholangitis |
| K74.4 | Sekundäre biliäre Zirrhose |
| K74.5 | Biliäre Zirrhose, nicht näher bezeichnet |
| K74.6 | Sonstige und nicht näher bezeichnete Zirrhose der Leber |
| K70.3 | Alkoholische Leberzirrhose |
| ICD-10 online (WHO-Version 2019) | |
Die Leberzirrhose, veraltet Lebercirrhose (von griechisch κίρρωσις kírrosis, von kirrós ‚gelb-orange‘, ‚zitronengelb‘, ‚gelb‘, nach der durch Verfettung manchmal gelben Schnittfläche,[1] von René Laënnec geprägter Begriff[2]), ist das Endstadium chronischer Leberkrankheiten. Dieses Stadium gilt als irreversibel, auch wenn einzelne Berichte über Heilungen existieren. Typischerweise entwickelt sich eine Zirrhose über Jahre bis Jahrzehnte, seltener sind schnellere Verläufe von unter einem Jahr. Fast alle chronischen Leberkrankheiten führen im Endstadium zu einer Leberzirrhose. In Europa sind Alkoholmissbrauch, Nicht-alkoholische Fettleber und chronische Virushepatitis die häufigsten Ursachen.[3][4]
Durch den chronischen Ablauf von Untergang und Regeneration des Lebergewebes entsteht eine gestörte Gewebearchitektur mit knotigen Veränderungen. Zusätzlich bildet sich übermäßig Bindegewebe (Fibrosierung). Diese narbigen Areale können mehr als 50 % des gesamten Gewebes einer zirrhotischen Leber einnehmen. Dadurch ist die Durchblutung der Leber gestört, im Bereich der Pfortader staut sich das Blut vor der Leber (portale Hypertension).
Die Inzidenz, d. h. die Anzahl der Neuerkrankungen, beträgt in den Industrieländern 250 pro 100.000 Einwohner im Jahr. Das Verhältnis erkrankter Männer zu Frauen liegt bei 2:1. Schätzungen zufolge leiden rund eine Million Menschen in Deutschland an einer Leberzirrhose. Die Leberzirrhose ist die häufigste Ursache für Leberkrebs, an dem in Deutschland jährlich etwa 9.000 Menschen erkranken. Zu den Risikopatienten zählen dabei Menschen mit einer chronischen Hepatitis-C-Virus-Infektion und diejenigen, die an einer nicht-alkoholbedingten Fettlebererkrankung leiden.[5]
Ursachen[Bearbeiten | Quelltext bearbeiten]
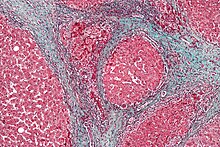
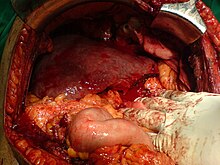
Alkoholische Leberzirrhose[Bearbeiten | Quelltext bearbeiten]
Die Alkoholkrankheit ist in Industrieländern mit ca. 50 % der Fälle die häufigste Ursache für Leberzirrhosen. Der massive Alkoholkonsum und die dadurch entstehende hohe Metabolisierungsrate von Ethanol zu Ethanal führen zu einem starken Anstieg des NADH/NAD-Quotienten im Körper. Die Erhöhung des Redoxpotentials der Pyridinnukleotide hemmt den Zitronensäure-Zyklus. Das Acetyl-CoA dient in dieser Situation vor allem in der Leber in erhöhtem Umfang zur Fettsäuresynthese und schließlich zu Anlagerung von Triglyceriden (Fett). Diese Leberverfettung ist anfangs voll reversibel, führt bei fortgesetztem Alkoholkonsum allerdings zu einer Fettleber und damit letztendlich zur Ausbildung einer Leberzirrhose.[6]
Fettleber (Steatosis hepatis)[Bearbeiten | Quelltext bearbeiten]
Die Fettleber stellt in Deutschland den häufigsten Leberbefund dar. Diese Lebererkrankung zeichnet sich durch eine Fetteinlagerung in den Leberzellen aus, die im anfänglichen Verlauf noch reversibel ist. Eine einfache Fettleber, die lediglich das Befinden beeinträchtigt, führt noch nicht zu einem Leberschaden. Sie kann sich jedoch entzünden; dabei unterscheidet man zwischen einer durch Alkoholkonsum hervorgerufenen, alkoholischen Steatohepatitis (ASH) und der nicht-alkoholischen Steatohepatitis (NASH). Beide Formen können zu einer Vernarbung der Leber führen, womit das Risiko, an einer Leberzirrhose zu erkranken, steigt.[7] Bei der ASH ist Interleukin-8 im Lebergewebe erhöht, wodurch sich neutrophile Granulozyten (weiße Blutkörperchen) in die Leber einlagern können.[8][9] Ein weiterer Mechanismus ist die Bildung von Leukotrien-B4 aus Arachidonsäure, welches ebenfalls Entzündungszellen anzieht.[10]
Weitere Ursachen[Bearbeiten | Quelltext bearbeiten]
- Leberzirrhose bei chronischer Virushepatitis (in Industrieländern mit 20–25 % zweithäufigste Ursache, in Afrika mit 90 % häufigste)[11] – meist Hepatitis C, die in 85 % chronisch bleibt und in 35 % zur Zirrhose führt
- kryptogene Leberzirrhose (ohne nachweisbare Ätiologie)
- Stauungszirrhose (Cirrhose cardiaque), typisch bei Rechtsherzinsuffizienz
- Autoimmunhepatitis
- seltene Zirrhoseformen mit definierter Ätiologie
- Hämochromatose
- Morbus Wilson
- Galaktosämie
- hereditäre Fruktoseintoleranz
- Mukoviszidose
- Glykogenspeicherkrankheit
- cholangiodysplastische Leberzirrhose
- primär sklerosierende Cholangitis
- Budd-Chiari-Syndrom
- Tropenkrankheiten
- Zirrhose bei Alpha-1-Antitrypsin-Mangel
- primär biliäre Cholangitis (früher: primär biliäre Zirrhose)
- sekundär biliäre Zirrhose
- Hepatopathie bei Zöliakie (glutensensitive Enteropathie)
- Leberzirrhose durch lebertoxische Substanzen wie Tetrachlormethan (Metallverarbeitung) und selten auch durch Medikamente wie beispielsweise Methotrexat
| Alkoholabusus | ca. 30–40 % |
| chronische Virushepatitis B, C und D | ca. 30 % |
| kryptogene Leberzirrhose | ca. 10 % |
| seltenere Ursachen der Leberzirrhose | ca. 10 % |
Pathogenese[Bearbeiten | Quelltext bearbeiten]
Die Ursache der Zirrhose ist die Nekrose (Absterben) von Leberzellen, verursacht z. B. durch Viren oder Gifte. Die Zellen setzen dabei Zytokine frei, die einerseits Leber-Makrophagen (Kupffer-Zellen) und Fettspeicherzellen der Leber (Ito-Zellen) und andererseits Monozyten und Granulozyten aus dem Blut aktivieren. Durch diese Zellen wird die Organstruktur mit Parenchym-Nekrosen, Herausbildung von Regeneratknoten (Pseudolobuli) und Bindegewebssepten destruktiv umgebaut. Durch diese Bindegewebsknoten werden die Kanäle der Leber unterbrochen, welche die Galle über die Gallenkanälchen (Canaliculi und Ductus) zur Gallenblase bringen, Nährstoffe aus dem portalen Blut in den Körper führen, den Hepatozyten Schadstoffe zum Entgiften anschwemmen und die Leber mit sauerstoffreichem Blut versorgen. Gallenkanäle bilden sich zwar neu aus, enden aber blind. Als Folge entsteht ein Blutstau zwischen Leber und Verdauungstrakt (Portale Hypertension), durch welchen sich Aszites bildet und die Milz sich vergrößert. Im schlimmsten Fall kommt es zu Ösophagusvarizenblutungen. Der Ausfall der Hepatozyten bedingt auch die hepatische Enzephalopathie: Bei einer Leberzirrhose ist die Ammoniakverstoffwechselung um bis zu 80 % reduziert, wobei das im Darm gebildete Ammoniak über Gefäßkollateralen an der Leber vorbeigeleitet wird. Durch den mangelnden Abbau steigt die Toxinkonzentration im Blut und Ammoniak passiert die Blut-Hirn-Schranke. Die Astrozyten im Gehirn schwellen an und es kann ein Hirnödem entstehen, was zu meist episodisch verlaufenden kognitiven Defiziten führen kann.[13][14] Letztlich kann die unzureichende Entgiftungsfunktion einer zirrhotischen Leber bis hin zum Leberkoma führen.[15] Dabei gilt die Hepatische Enzephalopathie als Prädiktor für einen besonders schwerwiegenden Verlauf der Leberzirrhose.[16] So starben in einer Studie nahezu die Hälfte aller Leberzirrhose-Patienten mit hepatischer Enzephalopathie innerhalb eines Monats nach Diagnosestellung.[17] Studiendaten zeigen im Rahmen einer Therapie der hepatischen Enzephalopathie auch eine Risikosenkung für weitere Leberzirrhose-Komplikationen wie spontan bakterielle Peritonitis (SBP) oder Varizenblutungen.[18]
Der Pathologe unterscheidet nach dem äußeren Erscheinungsbild des Organs die mikronoduläre, die makronoduläre und die gemischtknotige Zirrhose. Die Leber schrumpft („Schrumpfleber“), ihre Oberfläche wird runzlig und knotig. Mikroskopisch lassen sich aktive oder floride (d. h. voranschreitende) und inaktive Zirrhosen unterscheiden. Die Vorstufe der Leberzirrhose ist die Leberfibrose.
Symptome[Bearbeiten | Quelltext bearbeiten]
Frühe, allerdings unspezifische Symptome der Leberzirrhose können Leistungsminderung, Konzentrationsschwäche und Müdigkeit sein. Hinzu können die so genannten Leberhautzeichen auftreten, welche sich unter anderem durch rot gefärbte Kleinfingerballen, durch eine gelbliche Haut (Ikterus) sowie Spider naevi bemerkbar machen. Eine Leberzirrhose beeinträchtigt das subjektive Empfinden des betroffenen Patienten häufig erst in einem recht späten Stadium der Erkrankung. Die Leberfunktion kann dabei hinsichtlich der Synthesefunktion (Gerinnungsfaktoren, Albumin) und der Entgiftungsfunktion (Leberkoma) sehr unterschiedlich beeinträchtigt sein. Bis zur Ausbildung von Komplikationen spricht man dabei von einer kompensierten Leberzirrhose. Eine dekompensierte Leberzirrhose liegt vor, sobald klinisch relevante Komplikationen wie portale Hypertension (daraus folgende Ösophagusvarizen = Krampfadern in der Speiseröhre), Aszites, ein größerer Pleuraerguss (bzw. hepatischer Hydrothorax)[19] oder Milzvergrößerung (Mangel an Thrombozyten) und hepatische Enzephalopathie auftreten.[20] Letztere ist eine Gehirnfunktionsstörung, bei der es infolge der gestörten Leberfunktion zu einem Anstieg an toxischen Metaboliten kommt, die Hirnzellen zum Anschwellen bringen. Zu den Symptomen der hepatischen Enzephalopathie zählen auch Schwindel, Desorientierung, Müdigkeit, Konzentrationsschwierigkeiten, Gedächtnisverluste, Veränderung der Persönlichkeit bis hin zum Leberkoma.[21][22] Andere typische Symptome der Leberzirrhose sind Rötungen der Handinnenflächen (Palmarerythem), Caput medusae, Spider-Naevi (Naevus araneus), Rhagaden, Lackzunge und Ödeme. In der sogenannten Child-Pugh-Score-Klassifikation werden mehrere dieser Faktoren einbezogen (Bilirubin, Quick-Wert, Albumin, hepatische Enzephalopathie und Aszites) und daraus ein Score errechnet; die daraus resultierende Einteilung in die Stadien A bis C erlaubt eine Aussage über die Prognose der Erkrankung, Patienten im Stadium C nach Child-Pugh haben eine sehr schlechte Prognose hinsichtlich der Überlebenszeit. Die hepatische Enzephalopathie und der Aszites werden nur in drei Schweregrade eingeschätzt, was zu mehr oder weniger subjektiven, ungenauen Werten führt. Darum nutzt man seit 2002 auch den MELD-Score, der nach einer bestimmten Formel aus Laborparametern (Kreatinin, Bilirubin und INR) berechnet wird. Leberzirrhosen gelten als fakultative Präkanzerose, d. h., dass sich auf dem Boden einer Leberzirrhose ein bösartiger Tumor entwickeln kann, das hepatozelluläre Karzinom (HCC).
Diagnose[Bearbeiten | Quelltext bearbeiten]
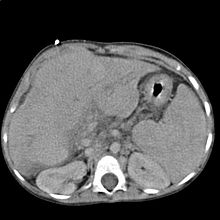

Bei der Untersuchung fallen oft ein Ikterus, ein größerer Bauchumfang (Aszites-bedingt), Ödeme, eine Gynäkomastie, Hautblutungen sowie bei einer hepatischen Enzephalopathie ein flapping tremor und Bewusstseinsstörungen auf. Typisch, allerdings erst spät auftretend, sind die sogenannten Leberhautzeichen: Spider Naevi (Gefäßspinne), „Milchglasnägel“ (Opake Weißverfärbung der Fingernägel mit distaler longitudinaler Rot-braun-Färbung,[23] auch „Terry-Nägel“ genannt), Prurigo (Juckreiz), Lackzunge, Hautatrophie („Geldscheinhaut“) sowie Palmar- bzw. Plantarerytheme (Rötung der Handflächen bzw. der Fußsohle). Diese Zeichen sind allerdings nicht nur für die Leberzirrhose spezifisch, sondern können auch in diskreter Form bei anderen Leberstörungen, wie z. B. der Fettleber, auftreten. Dies kann z. B. auch temporär während einer Schwangerschaft der Fall sein. Weitere Leberzeichen sind Caput medusae, Dupuytren-Kontrakturen sowie eine fehlende Bauchbehaarung beim Mann (Abdominalglatze, „Bauchglatze“).
Im Labor fallen durch die eingeschränkte Syntheseleistung der Leber verminderte Werte für die Cholinesterase, Albumin und einige Gerinnungsfaktoren (erniedrigter Quick-Wert) auf. Die Leberenzyme AST (GOT), ALT (GPT) sowie γ-GT, Bilirubin und Ammoniak können erhöht sein. Allerdings hat die Höhe des Ammoniakwerts allein keine Aussagekraft zum Vorliegen einer hepatischen Enzephalopathie.
Im Ultraschall stellt sich die Leber inhomogen dar. Der Leberrand ist wellig, die Binnengefäße sind rarefiziert. Der Lobus caudatus kann vergrößert sein. Sehr gut können mit dem Ultraschall ein Aszites und eine Milzvergrößerung (Splenomegalie) erkannt werden. Eine verbesserte Form der Sonographie stellt der sogenannte Fibroscan, auch bekannt als transiente Elastografie, dar. Hiermit kann die Fibrosierung, also der Bindegewebsumbau, der Leber ermittelt werden, was ein sehr zuverlässiges Ergebnis zur Diagnosestellung liefert und zukünftig die Leberbiopsie (s. u.) ersetzen könnte. Mit der Farbduplex sonographie lassen sich in den Lebervenen eine verminderte Elastizität der Leber, in der Pfortader ein verminderter Fluss sowie in der Leberarterie ein erhöhter peripherer Widerstand messen.
Die definitive Diagnose wird durch eine Leberbiopsie gestellt.
Aus verschiedenen Untersuchungsbefunden wird der Child-Pugh-Score erstellt, der sowohl zur Stadieneinteilung (Child A–C) als auch zur Prognoseabschätzung dient.
Infektionen[Bearbeiten | Quelltext bearbeiten]
Patienten mit Leberzirrhose infizieren sich leichter und haben eine schlechtere Immunabwehr.[24][25] Die Sterblichkeit im Falle von Infektionen ist bei bestehender Leberzirrhose um den Faktor 4 erhöht.[26] Verschiedene Faktoren begünstigen bei Leberzirrhose eine Infektion und verschlechtern deren Abwehr. Neben dem verschlechterten Gallenabfluss wird eine Veränderung des enteralen Mikrobioms dafür verantwortlich gemacht. Die verschlechterte Infektionsabwehr betrifft sowohl die angeborene als auch die adaptive Immunantwort. Auch die Barrierefunktion des Darms ist vermindert.[27]
Therapie[Bearbeiten | Quelltext bearbeiten]
Die Basis der Therapie bilden ernährungstherapeutische Allgemeinmaßnahmen wie das Weglassen aller potenziell lebertoxischen Substanzen (Alkohol, Medikamente), Ausgleich eines Vitaminmangels (z. B. Vitamin B1 bei Alkoholismus) und eine ausreichende Energiezufuhr. Mangelernährte Patienten haben sowohl eine erhöhte Mortalität im spontanen Krankheitsverlauf als auch eine erhöhte Komplikationsrate. Die Nahrungszufuhr sollte bevorzugt als orale Trinknahrung erfolgen, insbesondere Patienten mit fortgeschrittener Leberzirrhose profitieren auch von parenteraler Ernährung. Im frühen Stadium ist dies noch nicht angezeigt.[28] Die Energiezufuhr sollte etwa 145–167 kJ (35–40 kcal) pro Kilogramm Körpergewicht betragen. Befindet sich die Leberzirrhose im Endstadium, ist das Leben des Patienten akut bedroht. Aufgrund der knappen Verfügbarkeit von Spenderorganen, der Schwere des Eingriffs und der anschließenden Einnahme von Medikamenten, die das Immunsystem unterdrücken, ist die Lebertransplantation die letztmögliche Therapieoption, um den Patienten zu retten. Ein passendes Spenderorgan ersetzt dabei die zirrhotische Leber.
Kohlenhydratzufuhr[Bearbeiten | Quelltext bearbeiten]
Eine unzureichende Kohlenhydratzufuhr kann eine bestehende katabole Stoffwechselsituation verschlechtern. Dies ist dadurch zu erklären, dass in dieser Situation neben Fetten auch Proteine zur Energiegewinnung verstoffwechselt werden. Die DDG rät Diabetikern mit Leberzirrhose grundsätzlich von kohlenhydratreduzierten Diäten ab.[28]
Proteinzufuhr[Bearbeiten | Quelltext bearbeiten]
Empfohlen wird eine tägliche Eiweißmenge von 1,2–1,5 g Protein pro kg Körpergewicht. Proteinrestriktion darf ausschließlich bei Patienten mit therapierefraktärer chronischer hepatischer Enzephalopathie erfolgen. Gegebenenfalls sollte bei diesen Patienten Leucin, Isoleucin und Valin substituiert werden (verzweigtkettige Aminosäuren).[28]
Osteoporoseprophylaxe[Bearbeiten | Quelltext bearbeiten]
Bei allen Patienten sollte frühzeitig eine Osteoporoseprophylaxe eingeleitet werden. Dies geschieht durch Calcium-Substitution (1200–1500 mg/d). Bei Patienten mit cholestatischen Lebererkrankungen wird zusätzlich Vitamin D3 substituiert (400–800 IE/d). Bei Patienten fortgeschrittenen Alters (> 65 Jahre), untergewichtigen Patienten und Rauchern sollte eine Basisdiagnostik früh erfolgen.[28]
Vitaminsubstitution[Bearbeiten | Quelltext bearbeiten]
Eine Vitamin-K-Substitution ist angezeigt bei erhöhtem Blutungsrisiko und niedrigen Quick-Werten. Da die enterale Resorption dieses lipophilen Vitamins bei Cholestase vermindert ist, sollte die Substitution hier in gesteigerter Dosis (10 mg alle 10 Wochen) oral oder parenteral erfolgen. Bei alkoholkranken Patienten liegt zu 50 % ein Vitamin-B1-Mangel vor. Dieses ist – besonders bei fortgesetztem Alkoholkonsum zur Prophylaxe einer Wernicke-Enzephalopathie – ebenfalls zu substituieren.[28]
Nicht-ernährungstherapeutische Maßnahmen[Bearbeiten | Quelltext bearbeiten]
Die Grunderkrankung muss behandelt werden, bei Alkoholabhängigkeit wird eine Entzugsbehandlung versucht, Patienten mit Autoimmunhepatitis werden mittels Immunsuppression behandelt, bei einer chronischen Hepatitis B kann eine Viruselimination mit Interferonen versucht werden. Bei Hepatitis C führt eine antivirale Therapie bei über 90 % der Betroffenen zur Viruselimination (keine Viren mehr im Blut nachweisbar). Komplikationen der Leberzirrhose werden mit spezifischen Maßnahmen behandelt. Bei Blutungen aus Ösophagusvarizen ist das primäre Ziel die Blutstillung, da ansonsten ein tödlicher Blutverlust drohen kann. Liegt eine schwere Form des Aszites vor, so kann das Bauchwasser durch eine gezielte Punktion abgeleitet werden. Eine hepatische Enzephalopathie wird medikamentös therapiert; vornehmliches Ziel ist dabei, die weitere Produktion von Ammoniak und anderen Giftstoffen zu reduzieren. Als eine mögliche Therapieoption steht für die Rezidivprophylaxe das darmselektive Antibiotikum Rifaximin zur Verfügung. Es tötet unter anderem die ammoniakproduzierenden Bakterien im Darm ab und reduziert das relative Risiko wiederauftretender Episoden der hepatischen Enzephalopathie.[29] Ein weiteres Medikament ist Laktulose, ein synthetisches Disaccharid, das die Darmflora zugunsten milchsäurebildender Bakterien beeinflusst, womit ammoniakbildende Darmbakterien zurückgedrängt werden. Zur Behandlung der hepatischen Enzephalopathie kann auch L-Ornithin-L-Aspartat verwendet werden, welches die Umwandlung von Ammoniak zum unschädlichen Harnstoff fördert. Folgend kann der Harnstoff über den Urin ausgeschieden werden.
Wichtig sind regelmäßige Untersuchungen zur Früherkennung eines Leberkarzinoms. Eine Ultima Ratio ist in vielen Fällen die Lebertransplantation.
Es gibt Hinweise darauf, dass der Konsum von Koffein in Form von Kaffee die Leber vor der Bildung einer Zirrhose schützen oder seine Entwicklung verzögern kann.[30] Dabei könnten die Polyphenole, eine Gruppe von pflanzlichen Stoffen, die in besonders hohen Mengen im Kaffee vorkommen, eine große Rolle spielen.[31]
Die Prognose ist abhängig von der Ursache, der erfolgreichen ursächlichen Behandlung, den Komplikationen und dem Stadium. So sind die Ein-Jahres-Überlebensraten für Patienten im Stadium Child A fast 100 %, bei Child B etwa 85 % und bei Child C 35 %. Mit dem MELD-Score lassen sich Aussagen für das Überleben in den nächsten drei Monaten treffen. So hat ein Patient im Krankenhaus mit einem Score von 20–30 ein Risiko von 25 %, in den nächsten drei Monaten zu sterben. Ein Zirrhotiker mit einem MELD von 40 ist in drei Monaten höchstwahrscheinlich verstorben.[32]
Geschichte[Bearbeiten | Quelltext bearbeiten]
Die erste makroskopische Beschreibung einer Leberzirrhose in der Medizingeschichte findet sich in den Anmerkungen zur Zeichnung del vecchio von Leonardo da Vinci (1452–1519). Die Zeichnungen zur Gefäßanatomie der Leber basieren auf einer Autopsie, die Leonardo da Vinci 1508 in Florenz an einem über 100-Jährigen vornahm.
Literatur[Bearbeiten | Quelltext bearbeiten]
- Herbert Renz-Polster, Steffen Krautzig: Basislehrbuch Innere Medizin. 4. Auflage. 2006, S. 708 ff.
- Gerd Herold: Innere Medizin. 2009, S. 518 ff.
- Deutsche Leberstiftung (Hrsg.): Innere Medizin. 2009, S. 518 ff.
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Hans Adolf Kühn: Lebercirrhose. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 863–868, hier: S. 863.
- ↑ Hans-Werner Altmann: Krankheitsnamen als Spiegelbild medizinischer Erkenntnisse. In: Würzburger medizinhistorische Mitteilungen. Band 3, 1985, S. 225–241, hier: S. 228 f.
- ↑ Roeb et al. In: Z Gastroenterol, 2015, 53, S. 668–723
- ↑ Leberzirrhose und ihre Komplikationen. (Memento vom 2. Juli 2010 im Internet Archive) Lebertransplantation.de, 2001; abgerufen am 22. Oktober 2010
- ↑ Barbara Schellhaas, Thomas Bernatik, Wolfram Bohle, Fanny Borowitzka, Johannes Chang: Contrast-Enhanced Ultrasound Algorithms (CEUS-LIRADS/ESCULAP) for the Noninvasive Diagnosis of Hepatocellular Carcinoma – A Prospective Multicenter DEGUM Study. In: Ultraschall in Der Medizin. 14. Juli 2020, ISSN 1438-8782, doi:10.1055/a-1198-4874, PMID 32663881.
- ↑ Gertrud Rehner, Hannelore Daniel: Biochemie der Ernährung. 3. Auflage. Spektrum Akademischer Verlag, 2010, ISBN 978-3-8274-2041-1, S. 491.
- ↑ Deutsche Leberhilfe e. V., Fettleber (NASH/ASH). Leberhilfe.org; abgerufen am 2. August 2017
- ↑ Thomas Zilker: Alkoholische Leberzirrhose. Die Sicht des Toxikologen. In: Klinikarzt. Band 41, Nr. 6+7, 2012, S. 310–314.
- ↑ N Sheron, G Bird, J Koskinas et al.: Circulating and tissue levels of the neutrophil chemotoxin interleukin-8 are elevated in severe acute alcoholic hepatitis, and tissue levels correlate with neutrophil infiltration. In: Hepatology. Band 18, 1993, S. 41–46.
- ↑ FJ Roll, HD Perez, LN Serhan: Charactrization of a novel arachidonic acid-derived neutrophil chemoatractant. In: Biochemical and Biophysical Research Communications. Band 186, 1992, S. 268–276.
- ↑ H. Renz-Polster, S. Krautzig: Basislehrbuch Innere Medizin 4. Aufl., 2006, S. 709.
- ↑ hepatitisandmore.de (PDF; 2,1 MB)
- ↑ JS Bajaj, CM Schubert, DM Heuman, JB Wade, DP Gibson, A Topaz, K Saeian, M Hafeezullah, DE Bell, RK Sterling, RT Stravitz, V Luketic, MB White, AJ Sanyal: Persistence of cognitive impairment after resolution of overt hepatic encephalopathy. In: Gastroenterology, 2010, 138, S. 2332–2340, doi:10.1053/j.gastro.2010.02.015
- ↑ H. Grüngreiff: Thieme-Refresher Innere Medizin. 2014, R1-R16
- ↑ K. J.Bühling, J. Lepenies, K. Witt: Intensivkurs – Allgemeine und spezielle Pathologie. 3. Auflage. 2004, S. 233 ff
- ↑ Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften. S2k-Leitlinie: Komplikationen der Leberzirrhose. November 2018 [Abruf: 3. Mai 2019].
- ↑ P Jepsen et al. In: Hepatology, 2010, 51, S. 1675–1682
- ↑ SH Kang et al. In: Aliment Pharmacol Ther, 2017,46, S. 845–855.
- ↑ Berthold Jany, Tobias Welte: Pleuraerguss des Erwachsenen – Ursachen, Diagnostik und Therapie. In: Deutsches Ärzteblatt, Jahrgang 116, Heft 21/2019, 24. Mai 2019, S. 377–386, hier: S. 379 und 382.
- ↑ In: Dtsch med Wochenschr, 2015, 140(20), S. 1514–1516
- ↑ H Vilstrup et al.: Hepatic Encephalopathy in Chronic Liver Disease. In: J Hepatol, 2014; 61(3), S. 642–659
- ↑ T Zhan, W. Stremmel: The diagnosis and treatment of minimal hepatic encephalopathy. In: Dtsch Ärztebl. Int, 2012, 109(10), S. 180–187, doi:10.3238/arztebl.2012.0180
- ↑ Amir M. Nia, Stefan Ederer, Kristina M. Dahlem, Natig Gassanov, Fikret Er: Terry’s nails: a window to systemic diseases. In: The American Journal of Medicine. Band 124, Nr. 7. Elsevier, Juli 2011, S. 602–604, doi:10.1016/j.amjmed.2010.11.033, PMID 21683827.
- ↑ Jasmohan S. Bajaj, Patrick S. Kamath, K. Rajender Reddy: The Evolving Challenge of Infections in Cirrhosis. In: New England Journal of Medicine. Band 384, Nr. 24, 17. Juni 2021, ISSN 0028-4793, S. 2317–2330, doi:10.1056/NEJMra2021808.
- ↑ Alexander R. Bonnel, Chalermrat Bunchorntavakul, K. Rajender Reddy: Immune Dysfunction and Infections in Patients With Cirrhosis. In: Clinical Gastroenterology and Hepatology. Band 9, Nr. 9, September 2011, S. 727–738, doi:10.1016/j.cgh.2011.02.031 (elsevier.com [abgerufen am 1. August 2021]).
- ↑ Vasiliki Arvaniti, Gennaro D’Amico, Giuseppe Fede, Pinelopi Manousou, Emmanuel Tsochatzis: Infections in Patients With Cirrhosis Increase Mortality Four-Fold and Should Be Used in Determining Prognosis. In: Gastroenterology. Band 139, Nr. 4, Oktober 2010, S. 1246–1256.e5, doi:10.1053/j.gastro.2010.06.019 (elsevier.com [abgerufen am 1. August 2021]).
- ↑ Agustín Albillos, Margaret Lario, Melchor Álvarez-Mon: Cirrhosis-associated immune dysfunction: Distinctive features and clinical relevance. In: Journal of Hepatology. Band 61, Nr. 6, Dezember 2014, S. 1385–1396, doi:10.1016/j.jhep.2014.08.010 (elsevier.com [abgerufen am 1. August 2021]).
- ↑ a b c d e Hans Konrad Biesalski, Stephan Bischoff, Christoph Puchstein: Ernährungsmedizin. 4., vollständig überarbeitete und erweiterte Auflage. Georg Thieme, Stuttgart 2010, ISBN 978-3-13-100294-5, S. 674 f.
- ↑ Bass NM et al. N Engl J Med 2010; 362(12):1071-81
- ↑ Coffee, Cirrhosis, and Transaminase Enzymes. In: Archives of Internal Medicine, 12. Juni 2006
- ↑ C Taguchi et al.: Estimated Dietary Polyphenol Intake and Major Food and Beverage Sources among Elderly Japanese. In: Nutrients, 2015, 7(12), S. 10269–10281; doi:10.3390/nu7125530
- ↑ Christian Müller: Leber und Operationsrisiko. In: Journal für Gastroenterologische und Hepatologische Erkrankungen. Fachzeitschrift für Erkrankungen des Verdauungstraktes. Band 2, Nr. 2. Krause & Pachernegger, 2004, ISSN 1728-6263, S. 36–39 (kup.at [PDF]).