Brenzcatechin
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||
| Allgemeines | ||||||||||
| Name | Brenzcatechin | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C6H6O2 | |||||||||
| Kurzbeschreibung |
farblose Kristalle[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 110,11 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
1,34 g·cm−3 [1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
245 °C [1] | |||||||||
| Dampfdruck | ||||||||||
| Löslichkeit | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| MAK |
Schweiz: 5 ml·m−3 bzw. 23 mg·m−3[4] | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Brenzcatechin, 1,2-Dihydroxybenzol, englisch: Catechol (Kurzform von Pyrocatechol), – nach IUPAC 1,2-Dihydroxybenzen oder Benzen-1,2-diol genannt – ist ein zweiwertiges Phenol, ein aromatischer Alkohol. Es besitzt zwei benachbarte, sich in sogenannter ortho-Position befindende Hydroxygruppen an einem Benzolring.
Außer Brenzcatechin (1,2-Dihydroxybenzol) existieren zwei weitere stellungsisomere Formen, nämlich das Resorcin (1,3-Dihydroxybenzol) und das Hydrochinon (1,4-Dihydroxybenzol).
Geschichte und Vorkommen
Der Trivialname der chemischen Verbindung geht auf die Gerber-Akazie (Acacia catechu) zurück. Aus deren Pflanzensaft, der Catechin enthält, wurde sie erstmals 1839 von dem Chemiker K. Reinsch durch trockene Destillation, sogenanntes Brenzen (altertümliche Bezeichnung für Pyrolyse), isoliert. Außerdem sind für Brenzcatechin die Bezeichnungen Pyrocatechin und Pyrocatechol geläufig.
Brenzcatechin ist im Pflanzenreich verbreitet und kann durch Pyrolyse (Brenzreaktion) natürlicher Rohstoffe wie Holz, Kohle und Lignin erhalten werden. Es ist mehrheitlich in Baumharz und Buchenholzteer, früher wurde es auch aus den Schwelwässern[5] der Braunkohle gewonnen.[6]
Gewinnung und Darstellung
Brenzcatechin lässt sich mit Hilfe einer Alkalischmelze[7] von o-Chlorphenol oder o-Phenolsulfonsäure darstellen.
Auch durch Hydrolyse von 2-Chlorphenol mit Natronlauge bei höherer Temperatur in Gegenwart von Kupfersulfat, auch in Gegenwart von Bariumhydroxid und Kupfer(I)-chlorid[6] oder durch den oxidativen Abbau von Salicylaldehyd mit Wasserstoffperoxid und Natronlauge (Dakin-Reaktion).[8] Ebenso ist eine Etherspaltung von Guajacol mit Bromwasserstoff möglich.
Eigenschaften
Brenzcatechin bildet farblose Kristalle, die mit Wasserdampf leicht flüchtig sind. An der Luft und bei Lichteinfall wird es instabil und oxidiert zu 1,2-Benzochinon (Autoxidation).
Eine wässrige Lösung, besonders bei pH-Werten über 7, ist braun gefärbt. In neutraler Lösung ergibt die Kombination mit Eisen(III)-chlorid eine Grünfärbung. Diese Reaktion kann zur Unterscheidung der Dihydroxybenzole dienen: Resorcin gibt eine violette Färbung, Hydrochinon eine Blaufärbung, die nach kurzer Zeit wieder verschwindet, da das Hydrochinon vom Eisen(III)-chlorid zum p-Benzochinon oxidiert wird, das keine Farbreaktion zeigt.[9] Mit Blei(II)-acetat bildet sich dagegen ein farbloser Niederschlag. Eine blaugrüne Färbung gibt die Reaktion von Brenzcatechin mit „Vanadinschwefelsäure“ → Mandelin-Reagenz.[10][11] Ebenfalls eine blaugrüne Färbung gibt die Reaktion mit Chlorkalk.[11] Brenzcatechin ist ein starkes Reduktionsmittel, das Fehlingsche Lösung, Benedicts Reagenz und ammoniakalische Silbernitratlösung zu reduzieren vermag.
Verwendung
Die Verwendungsmöglichkeiten von Brenzcatechin liegen in der Fototechnik als Entwickler. Zum Einsatz kommt es als Antioxidations- und Desinfektionsmittel. In der organischen Synthese spielt es eine Rolle als Ausgangsmaterial für Farbstoffe, Riechstoffe und Arzneimittel sowie als Schutzgruppe für Carbonylverbindungen. Etwa 50 % des synthetischen hergestellten Brenzcatechins wird zur Herstellung von Pestiziden verwendet, wobei der Rest als Vorstufe zu Chemikalien zur Herstellung von Parfüms und Arzneimitteln dient.[12]
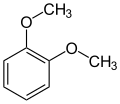
Das Hydroborierungsmittel Catecholboran[13] ist ein Derivat von Brenzcatechin. Methylierungen ergeben Guajacol (Monomethylether) und Veratrol (Dimethylether):
Naturstoffe
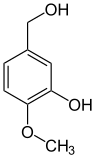
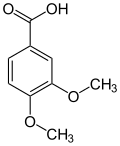
Vom Brenzcatechin und seinen Methylethern Guajacol und Veratrol leiten sich zahlreiche Naturstoffe ab, darunter das bekannte Vanillin. Die vorgenannten drei Basisverbindungen entstehen durch Decarboxylierung aus den entsprechenden Säuren: z. B. Veratrol aus Veratrumsäure. Veratrumaldehyd wird wiederum aus Veratrol mittels Vilsmeier-Formylierung dargestellt.[14]
Nachweis
Zum qualitativ-analytischen Nachweis entsteht bei der Bromierung mit Kaliumbromid und Brom[15] das Tetrabromderivat mit einem Schmelzpunkt von 192 °C.[16]
Sicherheitshinweise
Die Dihydroxybenzole reizen Augen, Haut und Atemwege. Sie sind gesundheitsschädlich bei Berührung mit der Haut und beim Verschlucken. Brenzcatechin ist giftig für Wasserorganismen und daher als umweltgefährlich in Wassergefährdungsklasse 2 eingestuft.[1]
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Brenzcatechin in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ Eintrag zu Brenzcatechin. In: Römpp Online. Georg Thieme Verlag
- ↑ Eintrag zu Pyrocatechol im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA) Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte
- ↑ Schwelwasser auf universal_lexikon.deacademic.com, abgerufen am 1. August 2016.
- ↑ a b Hans R. Schweizer: Künstliche Organische Farbstoffe und Ihre Zwischenprodukte, Springer-Verlag, 13. März 2013, ISBN 978-3-642-87245-7, S. 142.
- ↑ Alkalischmelze auf spektrum.de, abgerufen 1. August 2016.
- ↑ Brenzcatechin auf spektrum.de, abgerufen 1. August 2016.
- ↑ Uni Regensburg: Versuchsanleitung zum Nachweis von Dihydroxybenzolen (Peter Keusch).
- ↑ K. F. Mandelin, St. Petersburg: Über Vanadinschwefelsäure, ein neues Reagens für Alkoloide, E. Wienecke, 1883.
- ↑ a b Dissertation, Joseph Schomacker: "Beitrag zum forensisch-chemischen Nachweise des Resorcin und Brenzcatechin im Thierkörper", 1886, Universität Dorpat. (PDF; 1,3 MB)
- ↑ Fiegel, Helmut et al.: Phenol Derivatives, In: Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 15 Juni 2000, doi:10.1002/14356007.a19_313.
- ↑ 6327445
- ↑ Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 345.
- ↑ Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 331.
- ↑ Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 653.