Herpes simplex
| Klassifikation nach ICD-10 | |
|---|---|
| B00 | Infektionen durch Herpesviren [Herpes simplex] |
| ICD-10 online (WHO-Version 2019) | |
Als Herpes simplex (zu lateinisch simplex ‚einfach‘) bezeichnet man verschiedene durch Herpes-simplex-Viren hervorgerufene Virusinfektionen. Umgangssprachlich wird für eine spezielle Lokalisation auf der Haut meist die verkürzte Form (Lippen-)Herpes verwendet. Das Wort stammt vom altgriechischen ἕρπειν herpein (‚kriechen‘), womit die kriechende Ausbreitung der Hautläsionen bei einer Herpes-simplex-Infektion (auch in Form des Herpes febrilis mit Fieberbläschen) gemeint sei.
Herpes simplex gehört zu den sexuell übertragbaren Krankheiten.
Die Erreger von Herpes-simplex-Infektionen sind zwei verschiedene Virusspezies: das Herpes-simplex-Virus 1 (HSV-1) und das Herpes-simplex-Virus 2 (HSV-2). Sie zeigen hinsichtlich ihrer Krankheitsbilder und der Krankheitslokalisation geringfügige Abweichungen. Nach dem Auftreten sowie der Lokalisation der Krankheitssymptome werden klinisch verschiedene HSV-Infektionen bezeichnet, von denen vor allem der Herpes simplex labialis (Lippenherpes) und der Herpes simplex genitalis (Genitalherpes) verbreitet sind. Neben diesen Formen gibt es auch seltene, schwer verlaufende HSV-Infektionen wie die generalisierte HSV-Sepsis bei Patienten mit Immundefizienz, die Herpes-simplex-Enzephalitis und die generalisierte HSV-Infektion des Neugeborenen (Herpes neonatorum).
Nach einer (auch symptomlosen) Erstinfektion verbleibt das Virus in einem Ruhezustand (Latenz) stets lebenslang im Organismus, was als persistierende Infektion bezeichnet wird. Diese Eigenschaft der Persistenz ist bei allen Mitgliedern der Familie Herpesviridae zu finden. Die Therapie von HSV-Infektionen vermag diese Persistenz nicht zu beenden, sondern sie versucht die Vermehrung des Virus nach einer erfolgten Reaktivierung aus dem Ruhestadium zu verhindern. Für die HSV-Therapie stehen mehrere Virostatika zur Verfügung, die hoch spezifisch sind.
Geschichte
Die genitale Manifestation des Herpes simplex wurde bereits von Hippokrates um 400 v. Chr. als Symptom einer sich ausbreitenden Bläschenkrankheit beschrieben.[1][2] Dass die Erkrankung auch übertragbar ist, war spätestens in der römischen Antike bekannt, da Kaiser Tiberius das Küssen bei öffentlichen Zeremonien verbot, da die Ausbreitung einer Bläschenerkrankung an den Lippen beobachtet wurde. Dies wurde von Aulus Cornelius Celsus als erste Epidemie einer möglichen Herpeserkrankung dokumentiert. Im Europa des 16. und 17. Jahrhunderts war der Herpes labialis ebenfalls weit verbreitet und seine Übertragung durch Küssen allgemein bekannt. So schreibt William Shakespeare in seiner bekannten Tragödie Romeo und Julia: “O’er ladies’ lips, who straight on kisses dream, Which oft the angry Mab with blisters plagues, because their breaths with sweetmeats tainted are.” (Übersetzung: „Der Schönen Lippen, die von Küssen träumen, Oft plagt die böse Mab mit Bläschen diese, Weil ihren Odem Näscherei verdarb“; erg. Erläuterung: Der im Zitat vorkommende Name Mab bezieht sich auf die Fee „Queen Mab“, die in dem Werk in einer Rede Mercutios vorkommt).[3]

Jean Astruc erkannte 1736 den Herpes genitalis als eigene Krankheit, und nicht wie zuvor angenommen als Variante der Gonorrhoe oder der Syphilis.[4] Der deutsche Dermatologe Paul Gerson Unna beschrieb 1883 die Häufigkeit der Erkrankung und ihr gemeinsames Auftreten zusammen mit weiteren Geschlechtskrankheiten.[5] Er führte auch die ersten histologischen Untersuchungen über den Herpes simplex durch. Nachdem 1913 Wilhelm Gürtler den Erreger der Herpes-Keratitis (Herpes corneae) experimentell auf ein Kaninchenauge übertragen konnte, fand Ernst Löwenstein mit der Übertragung von Bläscheninhalt des Herpes labialis auf ein Kaninchenauge die Identität des Erregers beider Erkrankungen. Das HSV wurde schließlich erstmals von Slavin und Gavett 1946 aus Bläscheninhalt eines Patienten isoliert und charakterisiert.[6] Die erste elektronenmikroskopische Darstellung von Herpes-simplex-Viren gelang Coriell 1950.[7] Erst in den 1960er Jahren wurde durch Andre Nahmias und besonders Karl Eduard Schneweis entdeckt, dass die Herpes-simplex-Infektionen von zwei verschiedenen Virusspezies verursacht werden, die die Forscher aufgrund ihrer verschiedenen Antigenität unterscheiden konnten.[8][9]
Erreger
Herpes-simplex-Viren
Die beiden Erreger von Herpes-simplex-Infektionen – die Herpes-simplex-Viren 1 und 2 – die taxonomisch und korrekter auch als Humanes Herpesvirus 1 und 2 (HHV-1/2) bezeichnet werden, gehören zur Gattung Simplexvirus der Familie Herpesviridae. Den Herpes-simplex-Viren verwandte Mitglieder dieser Gattung sind auch bei Tieren zu finden, wo diese Viren beispielsweise bei Rindern oder Klammeraffen, Makaken und anderen Meerkatzenverwandten ähnliche Erkrankungen hervorrufen. Obwohl Herpesviren im Allgemeinen streng auf ihren jeweiligen Wirt spezialisiert sind, kann selten das dem HSV-1 ähnliche Cercopithecine Herpesvirus 1 (Herpesvirus simiae) der Makaken auf den Menschen übertragen werden, wo es schwere, generalisierte Infektionen hervorrufen kann.
Die Herpes-simplex-Viren gehören mit einem Durchmesser von 140 bis 180 nm zu den großen Viren.[10] In einem ikosaedrischen Kapsid befindet sich eine lineare, doppelsträngige DNA als Genom. Das Kapsid wiederum ist von einer Virushülle umgeben, was zu einer Empfindlichkeit der Viren gegenüber Seifen, Detergenzien oder bereits milden Desinfektionsmitteln führt. Zwischen Kapsid und Virushülle befindet sich eine Vielzahl von Virusproteinen, die sogenannten Tegumentproteine, die unter anderem für die Regulation der Genexpression in der Wirtszelle und den Übergang des Virus in ein ruhendes Latenzstadium verantwortlich sind. Als doppelsträngiges DNA-Virus sind die Herpes-simplex-Viren genetisch stabil, Mutationen und die Entstehung natürlicher Varianten sind eher selten.
Übertragung und Verbreitung
Herpes-simplex-Viren sind weltweit verbreitet, der Mensch ist für sie als Reservoir der einzige natürliche Wirt. Da das HSV-1 bereits durch Speichelkontakt und Schmierinfektion ab dem Säuglingsalter im normalen familiären Umgang erworben wird, ist es in der Bevölkerung häufig. Das Virus zeigt eine altersabhängige Seroprävalenz, die etwa am Ende der Pubertät hohe Prozentzahlen erreicht und dann nur noch gering weiter ansteigt. In Deutschland konnten bei 84 bis 92 % der Personen einer altersnormalisierten Stichprobenuntersuchung Antikörper gegen HSV-1 nachgewiesen werden.[11]
Das HSV-2 wird durch engen Schleimhautkontakt übertragen, wenn beim Virusträger das Virus gerade reaktiviert und sich in Epithelzellen erneut vermehrt. Die Virusausscheidung kann auch ohne sichtbare Läsionen geschehen. Die Prävalenz von Antikörpern gegen das HSV-2 ist unterschiedlich verteilt. Sie wird besonders vom Alter und der sexuellen Aktivität beeinflusst; ebenfalls ist die geographische Verbreitung unterschiedlich. Bei gesunden Blutspendern oder Gesundheitsüberwachungen gab es Häufigkeiten von 3 bis 23 % in den USA. Diese Zahl ist signifikant höher bei Patienten, die wegen einer anderen sexuell übertragbaren Krankheit einen Arzt konsultierten (bis 55 %) oder gewerbliche Prostitution betrieben haben (bis 75 %).[12]
Infektionsmechanismen
Die HS-Viren dringen bei einer Primärinfektion über die Schleimhautzellen des Mund-Rachen-Raumes (überwiegend das HSV-1) und des Genitaltraktes (überwiegend das HSV-2) ein. Bereiche am Übergang von Schleimhaut zu normaler Haut werden bevorzugt infiziert. Hier vermehren sich die Viren in den Epithelzellen. Die Ausbreitung der Herpes-simplex-Viren innerhalb des Epithels geschieht durch Zerstörung der Wirtszellen und Freisetzung neuer Virionen oder durch Verschmelzen benachbarter Zellen, wobei die unbehüllten Viruskapside die neue Zelle infizieren. Die Zerstörung der Epithelzellen äußert sich klinisch in einer Entzündungsreaktion, oft bildet sich durch Gewebszerstörung ein Ulcus oder ein entzündliches Hautbläschen. Die Bläschenflüssigkeit ist ein Exsudat, in dem sich Herpes-simplex-Viren in einer hohen Konzentration (>100.000 PFU/µl[13]) anreichern.
Durch direkten Zell-Zell-Kontakt oder durch Virionen in der Zwischenzellflüssigkeit gelangt das HSV zu den Nervenenden sensibler Neurone, von denen es spezifisch aufgenommen und entlang den Mikrotubuli und Intermediärfilamenten des Axons zum Zellkörper des Nervs transportiert wird. Dieser retrograde axonale Transport geschieht durch Bindung des Virus (als nacktes Viruskapsid, eventuell mit Restanteilen von Tegumentproteinen und Hüllproteinen) an kinesin-ähnliche Proteine und Dynein. Die Wanderungsgeschwindigkeit in Richtung Zellkörper beträgt etwa 0,7 µm pro Sekunde.[14]
Erkrankungsformen
Herpes labialis
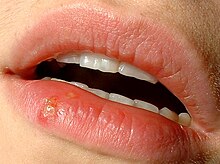

Bei dieser Form treten meist rund um den Mund wunde Stellen mit Bläschen („Fieberblasen“) auf. Meistens zeigt sich eine Herpes-simplex-Infektion in der Form der Herpes labialis (Lippenherpes, Herpes simplex labialis) als Reaktivierung einer schon bestehenden HSV-Infektion; das HSV-1 ist mit 80 bis 90 % der Fälle deutlich häufiger als HSV-2. Etwa 40 % der erwachsenen Bevölkerung erleben mindestens einmal im Leben eine als Bläschen sichtbare Reaktivierung.[15] Etwa 10–20 % vor allem der jüngeren Erwachsenen berichten von mehrfachen oder gelegentlichen Rückfällen (Rezidive, Herpes simplex rezidivans). Eine bevorzugte Stelle des Rezidivs ist der Übergangsbereich zwischen Haut und Lippenrot oder die Mundwinkel. Die Gründe dafür sind die hohe Dichte an sensorischen Nervenenden an der Lippe und das Offenliegen jener Epithelschichten, die für die Vermehrung des Virus besonders günstig sind. Zu den Ursachen für ein Herpes-Rezidiv gehören akuter emotionaler Stress und Sonnenstrahlung.[16][17][18][19]
Fiebrige Infektionskrankheiten können von der Reaktivierung eines Herpes labialis begleitet werden. Da die Bläschen schon im Prodromalstadium oder im frühen akuten Stadium einer zusätzlich auftretenden Infektionskrankheit sichtbar werden und diese Stadien meist mit hohem Fieber einhergehen, wird das Herpes-labialis-Rezidiv dann als Herpes febrilis („Fieberbläschen“) bezeichnet. Eine oft beobachtete Reaktivierung des Herpes labialis kurz vor oder während der Menstruation wird gelegentlich auch Herpes menstrualis genannt.
Der Herpes labialis kann bei einer Erstinfektion mit milden oder fehlenden Symptomen verlaufen. Bilden sich Bläschen, so stehen sie – im Gegensatz zum Rezidiv – über ein größeres Hautareal weiter verstreut auseinander. Eine HSV-Erstinfektion als Herpes labialis kann bei Kindern klinisch schwerer verlaufen und mit einem allgemeinen Krankheitsgefühl, Fieber und Kopfschmerzen einhergehen. Die Bläschen können zu größeren Ulzerationen zusammenfließen und zusätzlich mit Bakterien (häufig Staphylococcus aureus) superinfiziert sein. Gelegentlich sind zusätzlich die Mundschleimhaut und das Zahnfleisch in die Infektion einbezogen, wo sich schmerzhafte Bläschen (Aphthen) und Ulzera bilden. Diese typische Erstmanifestation wird auch als Gingivostomatitis herpetica, Stomatitis herpetica oder Mundfäule bezeichnet.
Andere Lokalisationen
Eine Herpes-simplex-Infektion kann durch ein Verschleppen der Viren auch in solchen Hautarealen auftreten, in denen primär eine Erstinfektion nicht zu erwarten ist. Dies geschieht nach einem Kontakt der Hände mit den offenen Bläschen eines Herpes labialis oder Herpes genitalis durch ein Einreiben der Erreger in verletzte oder empfängliche Hautpartien (Autoinokulation). Es folgen danach Bläschenbildung an der Nase (Herpes nasalis), der Wange (Herpes buccalis, Herpes facialis), dem Augenlid oder anderen Körperstellen (Herpes corporis). Eine Sonderform ist die Infektion sonst wenig empfänglicher Hautpartien durch Gewalteinwirkung, wie sie bei speziellen Sportarten passiert. Die Form eines Herpes gladiatorum wurde zuerst bei Ringern beobachtet.[20] Bei jugendlichen Ringern können Erstinfektionen in größerem Maße ausbrechen, z. B. in Trainingslagern.[21] Bei Rugby-Spielern wurde Ähnliches beobachtet.[22]
Aufgrund der typischen Bläschen kann das Auftreten von Herpes-simplex-Infektionen auf verschiedenen Hautpartien klinisch einem Herpes zoster (Gürtelrose), also einer Reaktivierung des Varizella-Zoster-Virus, ähnlich sein. Dies ist besonders dann der Fall, wenn die HSV-Läsionen der Haut zufällig in den für Herpes zoster üblichen Hautdermatom auftreten. Man spricht dann von einem „Zosteriformen Herpes simplex“. Umgekehrt kann eine atypisch lokalisierte Gürtelrose als HSV-Infektion missgedeutet werden, dies ist der sogenannte „Herpetiforme Zoster“.
Sonderformen und generalisierte Erkrankungen
Ekzema herpeticatum
Auf dem Boden einer chronischen Hauterkrankung wie beispielsweise dem atopischen Ekzem, der Schuppenflechte oder dem Morbus Darier kann es zu einer zusätzlichen Herpes-simplex-Infektion größerer Hautareale kommen. Dieses sogenannte Ekzema herpeticatum (oder auch Ekzema herpeticum) ist im Rahmen einer Primärinfektion oder einer Reaktivierung der Herpes-simplex-Viren möglich; häufiger Erreger ist das HSV-1. Das klinische Bild erscheint als verteilte, teils in Gruppen angeordnete Bläschen, die konfluieren und rasch platzen. Das Ekzema herpeticatum geht oft mit einem schweren Krankheitsgefühl einher und birgt als generalisierte Herpes-simplex-Infektion die Gefahr einer Herpes-simplex-Enzephalitis oder bei immundefizienten Patienten einer Herpes-Sepsis. Ein Ekzema herpeticatum bei Kindern kann ebenfalls zu einer sehr ernsten Sepsis führen und ist dringend medikamentös zu behandeln.[23]
Herpes-simplex-Retinitis
Eine besondere Form der Infektion in Nervengewebe ist die Infektion der Netzhaut des Auges (Retina), die sogenannte Herpes-simplex-Retinitis.[24] Sie gehört zu den endogenen, intraokulären Infektionen, das bedeutet, dass die Infektion immer durch eine Reaktivierung des Virus und nicht durch fortschreitende Infektion über eine andere, äußere HSV-Infektion des Auges (Herpes corneae) erfolgt. Bei der HSV-Retinitis findet man Exsudate in der Retina sowie lokale Entzündungsherde, die sich rasch zu einem Untergang von Netzhautgewebe (Retinanekrose) entwickeln können und damit zur Erblindung führen. Eine HSV-Retinitis wird auch unmittelbar oder Jahre nach einer Herpes-simplex-Enzephalitis beobachtet.[25][26] In diesen Fällen gelangt das Virus über den Sehnerv in die Netzhaut, die beide anatomisch als Hirnbestandteile gelten.
Herpes-simplex-Enzephalitis
Die Herpes-simplex-Enzephalitis ist eine sehr gefährliche Erkrankung mit Befall des Zentralnervensystems und hoher Sterblichkeit (unbehandelt ca. 70 %). Schon bei Verdacht ist eine antiviral-medikamentöse Behandlung angezeigt. Sehr oft verbleiben auch anhaltende neurologische Defizite nach durchgemachter Erkrankung.
Bell-Lähmung
Eine Infektion mit HSV-1 wird als häufige Ursache einer besonderen Form einer Lähmung des Gesichtsnerven (Nervus facialis) diskutiert.[27] Diese sogenannte Bell-Lähmung, eine idiopathische periphere Fazialislähmung, ist ursächlich noch nicht vollständig geklärt. Möglicherweise findet eine Demyelinisierung der HSV-infizierten Nervenscheiden statt, die nicht durch die Vermehrung des Virus selbst hervorgerufen wird, sondern auf einer viral induzierten Immunantwort beruht.[28] Dies würde auch die Unwirksamkeit von Virostatika trotz nachgewiesener HSV-1-Infektion erklären, da diese nur die Virusvermehrung, nicht aber die fehlgeleitete Immunantwort unterdrücken.
Herpes-simplex-Ösophagitis
Eine HSV-Infektion der Schleimhaut der Speiseröhre (Ösophagitis) kann im Rahmen einer Reaktivierung aus den Neuronen des Mund-Rachen-Raumes auftreten.[29] Typischerweise findet man bei dieser Form keine zusätzlichen Lippenbläschen als Zeichen der Reaktivierung, in 2/3 der Fälle ist der untere Ösophagusabschnitt betroffen. Charakteristisch bei der endoskopischen Untersuchung sind scharf begrenzte, kleine, flache Ulzera der Schleimhaut. Die Auslöser für die HSV-Ösophagitis sind meist schwere Grunderkrankungen oder eine immunsupprimierende Therapie mit Corticosteroiden oder Zytostatika. Begünstigt wird diese Lokalisation durch eine Schädigung der Speiseröhre, beispielsweise bei einer Strahlentherapie, einer schweren Refluxösophagitis, dem Liegen einer Magensonde oder nach chemischen Schädigungen (Verätzung). Liegen keine erkennbaren Ursachen vor, ist der Immunstatus des Patienten zu überprüfen. Eine HSV-Ösophagitis im Rahmen einer HIV-Infektion gilt als AIDS-definierende Erkrankung.
Sehr selten kann eine HSV-Ösophagitis auch als Begleiterkrankung einer klinisch stark ausgeprägten HSV-Erstinfektion auftreten. Diese Form ist auch bei immunkompetenten, nicht-vorerkrankten Patienten möglich, häufiger bei Männern als Frauen. Bei diesen Fällen der Erstinfektion liegt immer gleichzeitig eine Stomatitis herpetica vor.[30] Die HSV-Ösophagitis beim Immunkompetenten ist meist selbstlimitierend, neben einer symptomatischen Behandlung der Beschwerden ist eine antivirale Therapie meist nicht notwendig.
Generalisierter Herpes simplex
Die Herpes-simplex-Viren können auch Erkrankungen hervorrufen, die nicht primär über eine neuronale Ausbreitung entstehen, sondern über die Blutbahn als vorübergehende oder dauerhafte Virämie. Eine Abgrenzung zu zusätzlichen Symptomen einer Erstinfektion oder einer Reaktivierung ist nicht immer streng möglich. Die schwerste Form der generalisierten Infektion ist die „Herpes-simplex-Sepsis“, oder – da die Bezeichnung Sepsis strenggenommen nicht für Viren verwendet wird – die disseminierte Herpes-simplex-Infektion.
Herpes-simplex-Infektionen in der Schwangerschaft
Die generalisierte Herpes-simplex-Infektion des Neugeborenen, der Herpes neonatorum, ist eine sehr schwere und dringend behandlungsbedürftige Erkrankung. Ursache ist meist eine Übertragung des HSV-2 (weniger HSV-1) von der Mutter auf das Kind während des Geburtsvorganges. Bei Gebärenden mit einer Erstinfektion mit HSV-2 und einer Manifestation des genitalen Herpes im 3. Trimester (ab der 34. Schwangerschaftswoche), ist das Risiko eines Herpes neonatorum besonders hoch. Eine Entbindung durch Kaiserschnitt kann die Infektion des Kindes jedoch vermeiden. Der Herpes neonatorum betrifft beim Neugeborenen die Haut (lokal begrenzt oder großflächig verteilt), den Mund-Rachen-Raum, innere Organe und in der gravierendsten Form auch das Zentralnervensystem als Herpes-simplex-Enzephalitis.
HSV-2 und HIV
Bei dem Typ 2 der Herpes-simplex-Infektion, welche durch Geschlechtsverkehr übertragbar ist, tritt oft ein Befall der Schleimhäute von Geschlechtsorganen auf. Infektionen mit HSV-2 verlaufen beim Menschen in der Regel harmlos. Bei Personen mit bereits geschwächtem Immunsystem wie beispielsweise bei Aidspatienten kann sich die HSV-2-Infektion auch auf andere Körperteile ausbreiten und lebensbedrohlich werden.
Diagnostik
Bei der Mehrzahl der einfachen HSV-Infektionen wird die Diagnose durch das klinische Bild gestellt, ein kostenintensiver Erregernachweis oder eine wenig aussagekräftige Untersuchung auf Anti-HSV-Antikörper ist dann nicht anzustreben. Neben neurologischen und internistischen Diagnoseverfahren, die jeweils für eine spezielle HSV-Erkrankung von Nutzen sind (Bildgebende Verfahren, Magnetresonanztomographie bei Enzephalitis, Spiegelung des Augenhintergrundes bei Retinitis, Endoskopie bei Ösophagitis u. a.), ist der Nachweis des spezifischen Erregers nur bei schweren Erkrankungen von Bedeutung. Bei Immundefizienz beispielsweise im Rahmen einer Chemotherapie oder einer Immunsuppression nach Organtransplantation hat die HSV-Diagnostik einen hohen Stellenwert, da gerade diese Patienten von gefährlichen, generalisierten Infektionen bedroht sind.
Serologie und Erregernachweis
Der serologische Nachweis von Antikörpern gegen HSV-1 und HSV-2 ist klinisch nur sehr eingeschränkt von Bedeutung.[31] Lediglich für epidemiologische Untersuchungen ist der Antikörpernachweis sinnvoll. Die Problematik des HSV-Antikörpernachweises beruht zum einen auf der sehr hohen Prävalenz der Antikörper bei klinisch Gesunden, einer unzuverlässigen Unterscheidung zwischen HSV-1 und HSV-2 in den meisten verfügbaren Testsystemen und einer späten oder ausbleibenden Antikörperproduktion bei schweren HSV-Erkrankungen. Selbst bei einer generalisierten, disseminierten HSV-Infektion können Anti-HSV-IgG und -IgM Antikörper nicht oder nur sehr spät nachweisbar sein.[32]
Der Nachweis von Anti-HSV-IgM-Antikörpern hat klinisch keine Bedeutung, da eine Erstinfektion bei nicht nachgewiesenen IgM-Antikörpern nicht ausgeschlossen werden kann, andererseits der erfolgte Nachweis nicht zwingend eine Erstinfektion beweist. IgM-Antikörper gegen HSV können für Monate und Jahre persistieren, bei einer Reaktivierung erneut auftreten, bei einer Erstinfektion nicht nachweisbar sein oder auf einer relativ häufigen Unspezifität der kommerziellen Testverfahren beruhen. Eine nacheinander erfolgende Infektion mit den beiden HSV-Spezies erschwert zusätzlich die Interpretation des Befundes.[33] Die nicht ausreichende Spezifität der Antikörper-Suchtests bedarf einer Bestätigung mittels Western Blot oder eines indirekten Immunfluoreszenztests.
Eine Erstinfektion mit HSV kann serologisch nur durch eine Serokonversion des Anti-HSV-IgG nachgewiesen werden, wenn eine zeitlich ausreichend nahe abgenommene Vorprobe negativ ist und im Verlauf eine Folgeprobe nach ein bis zwei Wochen eindeutig positiv wird. Es muss sichergestellt sein, dass die Antikörper nicht passiv erworben wurden, d. h. die Positivität beruht nicht auf der Gabe anti-HSV-positiver Blutprodukte (Hyperimmunglobulin, Thrombozytenkonzentrat etc.) oder mütterlicher Antikörper bei Neugeborenen und Säuglingen. Schwankende Mengen von HSV-IgG oder sich ändernde positive Anti-HSV-Titer besitzen klinisch keine Aussagekraft. Bei immundefizienten Personen ist zudem die Aussagekraft der Antikörperbestimmung eingeschränkt, da bei diesen Patienten nicht ausreichend oder nur verzögert Antikörper gebildet werden können.
Die höchste Aussagekraft bei HSV-Infektionen bietet der direkte Erregernachweis in betroffenem Gewebe oder Gewebsflüssigkeiten (Liquor, Augenkammerwasser, Bläscheninhalt etc.). Dieser wird meist durch Nachweis der viralen DNA mittels Polymerase-Kettenreaktion (PCR) oder seltener durch Nachweis virusspezifischer Antigene im Immunfluoreszenztest durchgeführt. Als hoch spezifische, direkte Nachweismethode ist auch die Virusisolierung in Zellkulturen möglich, die durch eine nachfolgende Differenzierung der produzierten Viren jedoch mehrere Tage in Anspruch nimmt. Ein Nachweis von Viren bei elektronenoptischer Untersuchung von infiziertem Material ist möglich, jedoch kann morphologisch nicht zwischen verschiedenen Spezies der Virusfamilie Herpesviridae differenziert werden.
Resistenztestung
Bei schweren HSV-Infektionen, die nicht signifikant innerhalb weniger Tage auf eine korrekt durchgeführte antivirale Therapie mit Aciclovir ansprechen, besteht der Verdacht einer Resistenzentwicklung. Diagnostisch ist es möglich, die Resistenz der isolierten Virusstämme zu testen. Dazu wird das Virus auf Zellkulturen vermehrt und eine Bestimmung der noch wirksamen Aciclovirkonzentration (Minimale Hemm-Konzentration) durchgeführt. Die wirksame Hemmung der Virusvermehrung in der Zellkultur kann über einen Plaque-Reduktionstest oder einer Bestimmung der TCID50 in Verdünnungsreihen bestimmt werden. Virusstämme, die nur bei Aciclovirkonzentrationen von über 3 µM hemmbar sind, gelten als resistent.
Behandlung
Spezifische Therapie
Nukleosid-Analoga
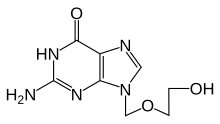

Der erste spezifisch wirksame Wirkstoff gegen HSV-1 und HSV-2 war das Aciclovir, das auch noch gegenwärtig bei der lokalen Anwendung als auch bei schweren HSV-Infektionen als Infusion verabreicht wird und als wirksamstes spezifisches Virustatikum bei Herpes-simplex-Viren gilt. Nur Zellen, in denen das Virus aktiv repliziert, können das Aciclovir phosphorylieren und es damit in seine aktiv wirksame Form umwandeln. Das phosphorylierte Aciclovir wird von der viralen Thymidinkinase während der Vermehrung des Virusgenoms in den DNA-Strang eingebaut und führt damit zum Abbruch der viralen DNA-Synthese. Es ist der erste Vertreter aus der Gruppe der Nukleosidanaloga. Als Valaciclovir, das erst im Organismus in Aciclovir umgewandelt wird (Prodrug), verfügt es bei einigen Anwendungen wie der oralen Therapie über eine verbesserte Bioverfügbarkeit, der antivirale Wirkmechanismus ist jedoch derselbe. Wie Valaciclovir ist auch Famciclovir eine Alternative zu Aciclovir (etwa bei der Behandlung des Herpes genitalis[34]).
Aciclovir-resistente Mutationen der Herpes-simplex-Viren können sich selten unter einer Therapie entwickeln. Bei schwersten Verlaufsformen und nachgewiesener Aciclovir-Resistenz gilt Foscarnet als Alternative, das jedoch erhebliche Nebenwirkungen verursacht. Eine vollständige und dauerhafte Beendigung der Infektion (also dem Verbleib der Viren im Körper) ist bisher nicht möglich, denn die Einwirkung auf infizierte Stellen der Hauteffloreszenz erreicht nicht die Viren, die im Zellkern der Nervenganglien persistieren.
Nur zur äußeren, lokalen Therapie zugelassen ist das dem Aciclovir strukturähnliche Nukleosidanalogon Penciclovir, das ebenfalls von der viralen Thymidinkinase phosphoryliert wird und zum Kettenabbruch während der DNA-Synthese führt.
Hautcremes mit Aciclovir oder Penciclovir können den Heilungsprozess von Lippenherpes, der durchschnittlich bei fünf bis fünfeinhalb Tagen liegt, um rund einen halben Tag verkürzen. Die Wirksamkeit von Cremes und Salben mit Foscarnet, Docosanol, Tromantadin, Idoxuridin oder Zinksulfat konnte nicht nachgewiesen werden.[35]
Andere spezifische Virustatika
Außer den spezifischen Nuklosidanaloga wird zur lokalen Anwendung gelegentlich auch Tromantadin verwendet.[36] Tromantadin ist ein Adamantan-Derivat, das als häufigste Nebenwirkung zu allergischen Reaktionen der Haut oder Entzündungen (Balanitis) führen kann.[37][38]
Ein essenzielles Protein der Herpesviren bei der viralen DNA-Replikation ist der Helikase-Primase-Enzymkomplex. Antivirale Wirkstoffe wie Helikase-Primase-Inhibitoren zeigen im Tierversuch (z. B. BAY 57-1293) eine antivirale Aktivität.[39] Erste Entwicklungskandidaten werden derzeit in klinischen Studien (PhaseI/II) getestet.
Symptomatische Therapie
Bei der symptomatischen Therapie des dermalen Herpes simplex wird versucht, Hautirritationen, Bläschenbildung oder eine bakterielle Superinfektion der Bläschen und des Wundsekrets zu vermindern. Dies wird durch verschiedene austrocknende oder antibakterielle Wirkstoffe, die Salben und Cremes zugegeben werden, versucht. Alternativ gibt es ferner Hydrokolloid-Pflaster („Herpes-Patches“). Sie enthalten keine antiviralen Wirkstoffe, sondern schaffen ein feuchtes Wundheilungsmilieu, wodurch die Läsionen ohne Krustenbildung schneller abheilen sollen. Zudem sollen die Patches durch das Abdecken der Bläschen und das Aufnehmen des Bläschensekrets ein Verbreiten der Herpesviren unterbinden.[40]
Bei häufigen Ausbrüchen, etwa mehrmals im Jahr, geben einige Betroffene an, das frühzeitige Aufstechen der Bläschen beschleunige den Heilungsverlauf und vermindere die Ansteckungsgefahr durch das geringere Volumen der auslaufenden Flüssigkeit. Tatsächlich erhöht sich durch das Aufstechen jedoch das Risiko, zusätzlich an einer bakteriellen Infektion des Gebiets, einer sog. Superinfektion, zu erkranken. Da die Flüssigkeit in den Bläschen nur ein Symptom und nicht die Ursache der Erkrankung ist, tritt die Heilung durch das Aufstechen auch keineswegs schneller ein; das Risiko, andere Menschen zu infizieren, wird durch das dauerhafte Aussickern der Flüssigkeit aus dem Wundgebiet jedoch erhöht. Die Flüssigkeit in den Bläschen enthält Viren in höchster Konzentration (>1 Milliarde pro ml).
Hausmittel und alternative Behandlungsmöglichkeiten
Unterschiedlichen Hausmitteln wird ein Nutzen in der Behandlung von Herpes zugeschrieben. Die Wirksamkeit von Hausmitteln konnte bisher wissenschaftlich nicht nachgewiesen werden. Zu diesen Methoden gehört das Betupfen mit einer frisch aufgeschnittenen Knoblauchzehe, Zahnpasta, Honig, Melissengeist, mit heißem, frisch abgekochtem Wasser, mit Alkohol oder Isopropanol, das Einreiben mit feingemahlenem schwarzen Pfeffer und das lokale Erwärmen von betroffenen Hautpartien, etwa mithilfe eines erhitzten Teelöffels. Auch konnten Wirkung und Sicherheit von Sonnenhut, Taigawurzel, L-Lysin, Zink (als Verbindung), Bienenprodukten und Aloe vera während eines Herpesausbruchs nicht sicher belegt werden. Die Erforschung der antiviralen Wirksamkeit von Teebaumöl oder Ähnlichem hat ebenfalls noch keine Hinweise auf eine Wirkung am Menschen erbracht. Bei Teebaumöl gibt es inzwischen Hinweise auf Hautirritationen nach mehrfacher Anwendung.
Nach einigen Publikationen, die vorwiegend aus den 1980er Jahren stammen, kann das Antioxidationsmittel Butylhydroxytoluol (BHT) die Dauer der Bläschenbildung von durchschnittlich 2,4 auf 2,0 Tage verkürzen.[41] Die Häufigkeit und Schwere des Auftretens von Herpeserkrankungen wurden jedoch nicht vermindert. Zusätzlich wurden bei systemischer Einnahme des BHT Vergiftungserscheinungen und Pseudoallergien beobachtet,[42] so dass von dieser Behandlung abgeraten wurde.
Vorbeugung
Vorbeugemöglichkeiten, ein Herpes-simplex-Rezidiv zu verhindern, werden kontrovers diskutiert. Eine Vielzahl unbelegter Empfehlungen kursieren. Dazu zählen die allgemeine Stärkung der Abwehrkräfte durch gesunde Ernährung, Bewegung und ausreichend Schlaf.
Die Vermeidung von Sonnenexposition (z. B. durch das Auftragen von Sunblocker auf die Lippen) ist laut folgender Studien mit geringerer Rezidiv-Inzidenz verbunden.[43][44]
Impfstoffentwicklung
Verschiedene Versuche zur Impfstoffentwicklung wurden unternommen, die ersten schon in den 1920er Jahren, blieben aber bislang erfolglos.[45] Aufgrund der antigenischen Ähnlichkeit beider Virusspezies (HSV-1 und HSV-2) stellt die Entwicklung einer Impfung gegen eine Spezies gleichzeitig die Basis für die Impfstoffentwicklung der anderen dar.
Der Erfolg des Windpocken-Impfstoffes zeigt, dass ein abgeschwächtes aktives α-Herpesvirus prinzipiell verwendet werden könnte, um einer herpesviralen Infektion beim Menschen vorzubeugen. Die Attenuierung kann somit auf HSV-1 und HSV-2 erweitert werden, wie im Falle eines ICP0-Protein-negativen Impfstoffs dargelegt ist.[46] 2019 befinden sich verschiedene Impfstoffe in unterschiedlichen Phasen klinischer Studien.[47][48]
Die folgende Tabelle führt Impfstoffe gegen HSV auf. Bis zum Jahr 2019 war kein HSV-Impfstoff kommerziell erhältlich.[49][50] Daneben wird untersucht, die Viruslatenz und die daraus folgende Reaktivierung des HSV durch die CRISPR/Cas-Methode zu unterbinden.[51]
| Vaccine | Firma und Forschungsleiter | Vakzintyp | Status | Ergebnisse |
|---|---|---|---|---|
| Anteris HSV-2 therapeutischer Impfstoff[52][53] / COR-1 | Anteris Technologies Ltd (ehemals Admedus) | DNA-Impfstoff | Phase II, wahrscheinlich eingestellt[54] | 58 % Minderung der Virusfreisetzung, Schutz bei 81 % der Geimpften nach zwei Impfungen[55] |
| dl5-29 / ACAM-529 / HSV-529 | Sanofi Pasteur
David Knipe[56] |
HSV-2 replikationsdefizient, mit Deletion der Gene UL5 und UL29 | Phase I | HSV529-induzierte neutralisierende und ADCC-Antikörper, zelluläre Immunantwort aber nur in Seronegativen[57] |
| VC2 | Louisiana State University
Gus Kousoulas |
attenuiert mit kleinen Deletionen in UL20 und UL53 | Präklinisch | hemmt Infektion und Viruslatenz bei Mäusen, Meerschweinen und Rhesusaffen[58][59][60] |
| R2 | Thyreos LLC[61]
Gregory Smith, Gary Pickard, Ekaterina Heldwein |
attenuiert mit Mutationen in der R2-Region von UL37 | Präklinisch | hemmt Infektion bei Mäusen und Ratten nach einer Impfung[62] |
| HSV-2 ΔgD-2 | Albert Einstein College of Medicine William Jacobs Jr & Betsy Harold | attenuiertes HSV-2 mit Deletion von US6 (gD) | Präklinisch | hemmt HSV-1 und HSV-2 bei Mäusen[63] |
| HSV-2 Trivalenter Impfstoff[64] | Perelman School of Medicine at the University of Pennsylvania
Harvey Friedman[65] & Sita Awasthi |
HSV-2 trivalenter Untereinheitenimpfstoff mit gC2, gD2, gE2 | Präklinisch | hemmt Virusfreisetzung um 98,8 % bei Mäusen[66] |
| G103[67] | Immune Design | HSV-2 trivalenter Untereinheitenimpfstoff mit gD, pUL19, pUL25 | Präklinisch | Schutz vor letaler intravaginaler HSV-2-Infektion bei Mäusen[68] |
| GV2207[69] | GenVec | ? | Präklinisch[69] | ? |
| NE-HSV2[70] | NanoBio[71] | ? | Präklinisch | ? |
| PBSVax[72] | Profectus BioSciences | DNA-Impfstoff | Antigenermittlungsphase | Nicht verfügbar |
| HSV-2 ICP0‾ HSV-2 0ΔNLS[73] | Rational Vaccines RVx
William Halford[74] |
attenuiert | Kontroverse um Einverständniserklärung der Geimpften[75] | Schutz vor Erkrankung bei 65 % der Geimpften[76] |
| Vitaherpavac & Herpovax | Russland | ? | ? | ? |
| Vakzin | Organisation | Vakzintyp | Grund | Ergebnisse | |
|---|---|---|---|---|---|
| Herpevac, Simplirix | GlaxoSmithKline | Untereinheitenimpfstoff gD2t mit Adjuvans AS04[77][78] | In Phase III durchgefallen[79] | keine statistisch signifikanten Ergebnisse[80], keine Auswirkung auf HSV-2, teilweiser Schutz gegen HSV-1 bestätigt[81] | |
| Unbenannt[82] | PaxVax | Vektorimpfstoff[83] | Abbruch in der präklinischen Phase[84] | - | |
| ImmunoVEX HSV2 vaccine | Amgen, BioVex | attenuiert[85] | Abbruch in Phase I[86] | - | |
| Gen-003 | Genocea | Untereinheitenimpfstoff gD2/ICP4 mit Matrix M2 | Abbruch nach Phase II | 58 % Minderung der Virusfreisetzung, 69 % Schutz[87] | |
| AuRx Herpes Vaccine | AuRx[88] | Vektorimpfstoff[89] | Inaktiv | - | |
| DISC vaccine[90] | Cantab Pharmaceuticals | attenuiert mit Deletion von gH | Abbruch in Phase I | kein Nutzen | |
| Unnamed[91] | Mymetics | ? | Abbruch in der präklinischen Phase | - | |
| HerpV | Agenus | Peptidimpfstoff mit Adjuvans QS-21 | Abbruch nach Phase II[92] | - | |
| VCL-HB01[93] | Vical | DNA-Impfstoff von gD2+UL46 mit Adjuvans Vaxfectin | Abbruch nach Phase II | kein Nutzen[94] | |
Meldepflicht
In Deutschland und der Schweiz besteht keine gesetzliche Meldepflicht für Herpes-simplex-Infektionen. In Österreich sind ausschließlich der Verdacht, die Erkrankung und der Tod an einer HSV-assoziierten Meningoenzephalitis meldepflichtig.
Literatur
- David C. Hutfield: History of herpes genitalis. In: British Journal of Venereal Diseases. Band 42, Nr. 4, 1966, S. 263–268. PMID 5333786. PMC 1047831 (freier Volltext).
- R. Marre, T. Mertens, M. Trautmann, E. Vanek (Hrsg.): Klinische Infektiologie. Urban und Fischer, München/Jena 2000, ISBN 3-437-21740-2, S. 578 ff., 596 ff., 189 f.
- H. Hahn, D. Falke, S. H. E. Kaufmann, U. Ullmann (Hrsg.): Medizinische Mikrobiologie und Infektiologie. 5. Auflage. Springer, Berlin/Heidelberg 2005, ISBN 3-540-21971-4, S. 610 ff.
- C. Mims, H. M. Dockrell u. a. (Hrsg.): Medizinische Mikrobiologie / Infektiologie. Elsevier, München 2006, ISBN 3-437-41272-8.
- Stephan Dreyer: Herpes – Nein danke. Handreichungen für Lippenherpes-Betroffene. Scriptor, Böhl-Iggelheim 2010, ISBN 978-3-9809578-7-8 (eingeschränkte Vorschau in der Google-Buchsuche).
Weblinks
- Herpes-Infektionen – Informationen des Robert Koch-Instituts
- Herpes in der Schwangerschaft, bei Babys und bei Kindern. In: Herpesfree.de. Abgerufen am 22. Juli 2019: „Tabelle: Das Übertragungsrisiko in der Schwangerschaft“
- Susanne Nessler: Freund oder Feind? Herpes-Viren und das Immunsystem. In: br.de. Bayerischer Rundfunk, 27. März 2015, abgerufen am 23. Dezember 2018 (Podcast zur Sendung IQ – Wissenschaft und Forschung).
- Herpes simplex. In: DermIS.net. Abgerufen am 23. Dezember 2018: „28 Bilder für diese Diagnose“
- Dirk Manski: Herpes genitalis: Vireninfektion mit Herpes simplex. In: Urologielehrbuch.de. 22. März 2009, abgerufen am 23. Dezember 2018 (Information und Bilder).
- Katharina Kremser: Lippenherpes: Ursachen, Therapie, Vorbeugen. In: Apotheken-Umschau.de. Abgerufen am 28. November 2019: „Lippenherpes (Herpes labialis) – Symptom einer Infektion mit dem Herpes-simplex-Virus Typ I – bezeichnet der Volksmund auch als Fieberblasen“
Einzelnachweise
- ↑ Corpus Hippocraticum: De mulierum affectibus 1,90.
- ↑ R. H. Kampmeier: Herpes genitalis: a clinical puzzle for two centuries. In: Sex. Trans. Dis. Band 11, 1984, S. 41.
- ↑ Mercutio zu Romeo im 1. Akt, 4. Szene (Text auf Wikisource)
- ↑ Jean Astruc: De morbis venereis. Paris 1736 und A Treatise of Venereal Diseases. London 1754, Band 1, 3. Buch, S. 365.
- ↑ P. G. Unna. In: J. cutan. vener. Dis. Band 1, 1883, S. 321, zugänglich in: J. K. Oates: Venereal disease genital herpes. In: Journal of Hospital Medicine. Band 6, 1983, ISSN 1553-5606, S. 13–19.
- ↑ H. B. Slavin, E. Gavett: Primary herpetic vulvovaginitis. In: Proceedings of the Society for Experimental Biology and Medicine. Band 63, 1946, ISSN 1525-1373, S. 343.
- ↑ L. L. Coriell, G. Rake u. a.: Electron microscopy of herpes simplex. In: Journal of Bacteriology. Band 59, Nr. 1, 1950, S. 61–68. PMID 15400321.
- ↑ Karl Eduard Schneweis: Untersuchungen zur antigenen Analyse und zur Typendifferenzierung beim Herpesvirus hominis. Göttingen 1962.
- ↑ K. E. Schneweis, A. J. Nahmias: Antigens of Herpes simplex virus type 1 and 2-immunodiffusion and inhibition passive hemagglutination studies. In: Z. Immunitätsforsch. Exp. Klin. Immunol. Band 141, Nr. 5, 1971, S. 471–487. PMID 4326538.
- ↑ J. F. Szilágyi, J. Berriman: Herpes simplex virus L particles contain spherical membrane-enclosed inclusion vesicles. In: J. Gen. Virol. Band 75, Nr. 7, 1994, S. 1749–1753. PMID 8021604.
- ↑ W. Hellenbrand, W. Thierfelder u. a.: Seroprevalence of herpes simplex virus type 1 (HSV-1) and type 2 (HSV-2) in former East and West Germany, 1997–1998. In: Eur. J. Clin. Microbiol. Infect. Dis. Band 24, Nr. 2, 2005, S. 131–135. PMID 15692814.
- ↑ Eine Übersicht verschiedener epidemiologischer Studien in B. Halioua, J. E. Malkin: Epidemiology of genital herpes – recent advances. In: Eur J Dermatology. Band 9, Nr. 3, 1999, S. 177–184. PMID 10210781. (Tabelle 2. In: jle.com. Abgerufen am 23. Dezember 2018 (englisch).).
- ↑ C. A. Daniels, S. G. LeGoff: Shedding of infectious virus/antibody complexes from vesicular lesions of patients with recurrent herpes labialis. In: The Lancet. Band 20;2, Nr. 7934, 1975, S. 524–528. PMID 51344.
- ↑ W. W. Liu, J. Goodhouse, N. L. Jeon, L. W. Enquist: A microfluidic chamber for analysis of neuron-to-cell spread and axonal transport of an alpha-herpesvirus. In: PLoS ONE. Band 18;3, Nr. 6, 2008, Artikel e2382. PMID 18560518 PMC 2426917 (freier Volltext).
- ↑ D. Malvy u. a.: Epidemiology of orofacial herpes simplex virus infections in the general population in France: results of the HERPIMAX study. In: J. Eur. Acad. Dermatol. Venereol. Band 21, Nr. 10, 2007, S. 1398–1403. PMID 17958848.
- ↑ Ronald Glaser, Janice Kiecolt-Glaser: Psychological influences on immunity: Implications for AIDS. In: American Psychologist. Band 43, Nr. 11, Nov 1988, S. 892–898. doi:10.1037/0003-066X.43.11.892.
- ↑ H. E. Schmidt u. a.: Stress as a pecipitating factor in subjects with recurrent Herpes labialis. In: Journal of Family Practice. Band 20, Nr. 4, April 1985, S. 359–366. PMID 3981095.
- ↑ M. Ichihashi, H. Nagai, K. Matsunaga: Sunlight is an important causative factor of recurrent herpes simplex. In: Cutis. Band 74, 2004, Supplement 5, S. 14–18. PMID 15603217.
- ↑ Vittorio Mazzarello, Marco Ferrari, Stefano Decandia, Maria Alessandra Sotgiu: Sunlight and Herpes Virus. In: Ronaldo Luis Thomasini (Hrsg.): Human Herpesvirus Infection – Biological Features, Transmission, Symptoms, Diagnosis and Treatment. IntechOpen, 2020, ISBN 978-1-83881-158-7. doi:10.5772/intechopen.82643
- ↑ B. Selling, S. Kibrick: An outbreak of Herpes simplex among wrestlers (Herpes gladiatorum). In: New Engl J Med. Band 7, Nr. 270, 1964, S. 979–982. PMID 14122793.
- ↑ B. J. Anderson: The epidemiology and clinical analysis of several outbreaks of herpes gladiatorum. In: Med. Sci. Sports Exerc. Band 35, Nr. 11, 2003, S. 1809–1814. PMID 14600542.
- ↑ W. B. White, J. M. Grant-Kels: Transmission of herpes simplex virus type 1 infection in rugby players. In: JAMA. Band 27;252, Nr. 4, 1984, S. 533–535. PMID 6737650.
- ↑ I. R. Sanderson u. a.: Eczema herpeticum: a potentially fatal disease. In: Br. Med. J., Band 294, Nr. 6573, 1987, S. 693–694. PMID 3105692, PMC 1245744 (freier Volltext).
- ↑ M. Cordero-Coma u. a.: Herpetic retinitis. (Review) In: Herpes, Band 14, Nr. 1, 2007, S. 4–10; PMID 17848212.
- ↑ J. Maertzdorf u. a.: Herpes simplex virus type 1 (HSV-1)-induced retinitis following herpes simplex encephalitis: indications for brain-to-eye transmission of HSV-1. In: Ann. Neurol. Band 49, Nr. 1, 2001, S. 104–106. PMID 11198277.
- ↑ A. Klein, P. Lefebvre: Three consecutive episodes of acute retinal necrosis due to herpes simplex-1 over twelve years following herpetic encephalitis. (Review) In: Ocul. Immunol. Inflamm. Band 15, Nr. 5, 2007, S. 411–413. PMID 17972228.
- ↑ S. Murakami u. a.: Bell’s palsy and herpes simplex virus: Identification of viral DNA in endoneurial fluid and muscle. In: Ann Intern Med. Band 124, Nr. 1, 1996, S. 27–30. PMID 7503474.
- ↑ H. Wakisaka u. a.: Demyelination associated with HSV-1-induced facial paralysis. In: Exp. Neurol. Band 178, Nr. 1, 2002, S. 68–79. PMID 12460609.
- ↑ Eine Übersicht der HSV-Ösophagitiden in: K. Becker, H. J. Lübke, F. Borchard, D. Häussinger: Entzündliche Speiseröhrenerkrankungen durch Herpes-simplex-Virusinfektionen – Übersicht und Bericht über 15 eigene Fälle. In: Z. Gastroenterol. Band 34, Nr. 5, 1996, S. 286–295. PMID 8686361.
- ↑ J. Ramanathan u. a.: Herpes simplex virus esophagitis in the immunocompetent host: an overview. In: Am. J. Gastroenterol. Band 95, Nr. 9, 2000, S. 2171–2176. PMID 11007213.
- ↑ Übersicht der diagnostischen Problematik in: Th. Mertens, O. Haller, H.-D. Klenk (Hrsg.): Diagnostik und Therapie von Viruskrankheiten – Leitlinien der Gesellschaft für Virologie. 2. Auflage. München 2004, ISBN 3-437-21971-5, S. 126–130.
- ↑ G. Biancofiore u. a.: Liver transplantation due to Herpes Simplex virus-related sepsis causing massive hepatic necrosis after thoracoscopic thymectomy. In: Minerva Anestesiol. Band 73, Nr. 5, 2007, S. 319–322. PMID 17529922.
- ↑ N. J. Schmidt, B. Forghani, E. H. Lennette: Type specificity of complement-requiring and immunoglobulin M neutralizing antibody in initial herpes simplex virus infections of humans. In: Infect Immun. Band 12, Nr. 4, 1975, S. 728–732. PMID 1193713, PMC 415348 (freier Volltext).
- ↑ Marianne Abele-Horn: Antimikrobielle Therapie. Entscheidungshilfen zur Behandlung und Prophylaxe von Infektionskrankheiten. Unter Mitarbeit von Werner Heinz, Hartwig Klinker, Johann Schurz und August Stich, 2., überarbeitete und erweiterte Auflage. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4, S. 306.
- ↑ Cremes gegen Lippenherpes. Mehr Spreu als Weizen. In: Gute Pillen – Schlechte Pillen. 2008. Ausgabe 04, ISSN 1861-6046, S. 03 (auch als PDF; 107 kB (Memento vom 5. Oktober 2021 im Internet Archive)).
- ↑ K. E. Ostheimer u. a.: Randomized double-blind trial of tromantadine versus aciclovir in recurrent herpes orofacialis. In: Arzneimittel-Forschung, Band 39, Nr. 9, 1989, S. 1152–1155. PMID 2686658.
- ↑ M. R. Holdiness: Contact dermatitis from topical antiviral drugs. In: Contact Dermatitis. Band 44, Nr. 5, 2001, S. 265–269. PMID 11298689.
- ↑ I. Maatouk: Contact balanitis to tromantadine. In: Clinical and Experimental Dermatology, Band 41, Nr. 8, 2016, S. 926. PMID 27757977.
- ↑ G. Kleymann u. a.: New helicase-primase inhibitors as drug candidates for the treatment of herpes simplex disease. In: Nat. Med. Band 8, Nr. 4, 2002, S. 392–398, doi:10.1038/nm0402-392, PMID 11927946 (nature.com).
- ↑ Sabine Werner: Cremen, kleben oder Hitze. In: deutsche-apotheker-zeitung.de. 28. Juli 2015, abgerufen am 23. Dezember 2018 (Nr. 16, S. 62).
- ↑ D. J. Freeman u. a.: Treatment of recurrent herpes simplex labialis with topical butylated hydroxytoluene. In: Clin Pharmacol Ther. Band 38, Nr. 1, 1985, S. 56–59. PMID 2988845.
- ↑ M. W. Grogan: Toxicity from BHT ingestion. In: West J Med., Band 145, Nr. 2, 1986, S. 245–246, PMC 1306899 (freier Volltext).
- ↑ V. Mazzarello, M. Ferrari, G. Piu, V. Pomponi, G. Solinas: Do sunscreen prevent recurrent Herpes labialis in summer? In: J Dermatolog Treat. Band 30, Nr. 2, 2019, S. 179–182, doi:10.1080/09546634.2018.1481921.
- ↑ L. Duteil, C. Queille-Roussel, C. Loesche, M. Verschoore: Assessment of the effect of a sunblock stick in the prevention of solar-simulating ultraviolet light-induced herpes labialis. In: Journal of Dermatological Treatment. Band 9, Nr. 1, 1998, S. 11–14, doi:10.3109/09546639809160682.
- ↑ A. A. Chentoufi, E. Kritzer, D. M. Yu, A. B. Nesburn, L. Benmohamed: Towards a rational design of an asymptomatic clinical herpes vaccine: the old, the new, and the unknown. In: Clin. Dev. Immunol. Band 2012, 2012, S. 187585, doi:10.1155/2012/187585, PMID 22548113, PMC 3324142 (freier Volltext).
- ↑ W. P. Halford, R. Püschel, E. Gershburg, A. Wilber, S. Gershburg, B. Rakowski: A live-attenuated HSV-2 ICP0 virus elicits 10 to 100 times greater protection against genital herpes than a glycoprotein D subunit vaccine. In: PLoS ONE. Band 6, Nr. 3, 2011, S. e17748, doi:10.1371/journal.pone.0017748, PMID 21412438, PMC 3055896 (freier Volltext).
- ↑ N. R. Truong, J. B. Smith, K. J. Sandgren, A. L. Cunningham: Mechanisms of Immune Control of Mucosal HSV Infection: A Guide to Rational Vaccine Design. In: Frontiers in immunology. Band 10, 2019, S. 373, doi:10.3389/fimmu.2019.00373. PMID 30894859, PMC 6414784 (freier Volltext).
- ↑ R. Whitley, J. Baines: Clinical management of herpes simplex virus infections: past, present, and future. In: F1000Research. Band 7, 2018, S. …, doi:10.12688/f1000research.16157.1. PMID 30443341, PMC 6213787 (freier Volltext).
- ↑ X. Xu, Y. Zhang, Q. Li: Characteristics of herpes simplex virus infection and pathogenesis suggest a strategy for vaccine development. In: Reviews in Medical Virology. Band 29, Nummer 4, Juli 2019, S. e2054, doi:10.1002/rmv.2054. PMID 31197909, PMC 6771534 (freier Volltext).
- ↑ J. Rajčáni, F. Bánáti, K. Szenthe, S. Szathmary: The potential of currently unavailable herpes virus vaccines. In: Expert review of vaccines. Band 17, Nummer 3, März 2018, S. 239–248, doi:10.1080/14760584.2018.1425620. PMID 29313728.
- ↑ H. S. De Silva Feelixge, D. Stone, P. Roychoudhury, M. Aubert, K. R. Jerome: CRISPR/Cas9 and Genome Editing for Viral Disease-Is Resistance Futile? In: ACS infectious diseases. Band 4, Nummer 6, 06 2018, S. 871–880; doi:10.1021/acsinfecdis.7b00273. PMID 29522311, PMC 5993632 (freier Volltext).
- ↑ Admedus AU Immunotherapies. www.admedus.com, abgerufen am 18. Januar 2017.
- ↑ Admedus US Research & Development - Admedus US. www.admedus.com, abgerufen am 2. August 2016.
- ↑ Hyeon-Cheol Kim: Vaccines against Genital Herpes: Where Are We? 27. Juli 2020, abgerufen am 3. Oktober 2022 (englisch).
- ↑ ADMEDUS ANNOUNCES POSITIVE UNBLINDED HSV-2 PHASE II INTERIM DATA. (PDF) Admedus, 19. Oktober 2016, abgerufen am 30. März 2021.
- ↑ Knipe Lab | Harvard Medical School. knipelab.med.harvard.edu, abgerufen am 2. August 2016.
- ↑ Y. C. Lee: Ventricular fusion beats. In: JAMA. Band 202, Nr. 10, Dezember 2017, S. S415–S416, doi:10.1093/ofid/ofx163.1041, PMC 5630753 (freier Volltext).
- ↑ B. A. Stanfield, J. Stahl, V. N. Chouljenko, R. Subramanian, A. S. Charles, A. A. Saied, J. D. Walker, K. G. Kousoulas: A single intramuscular vaccination of mice with the HSV-1 VC2 virus with mutations in the glycoprotein K and the membrane protein UL20 confers full protection against lethal intravaginal challenge with virulent HSV-1 and HSV-2 strains. In: PLOS ONE. Band 9, Nr. 10, 2014, S. e109890, doi:10.1371/journal.pone.0109890, PMID 25350288, PMC 4211657 (freier Volltext), bibcode:2014PLoSO...9j9890S.
- ↑ B. A. Stanfield, B. Pahar, V. N. Chouljenko, R. Veazey, K. G. Kousoulas: Vaccination of rhesus macaques with the live-attenuated HSV-1 vaccine VC2 stimulates the proliferation of mucosal T cells and germinal center responses resulting in sustained production of highly neutralizing antibodies. In: Vaccine. Band 35, Nr. 4, Januar 2017, S. 536–543, doi:10.1016/j.vaccine.2016.12.018, PMID 28017425.
- ↑ B. A. Stanfield, P. J. Rider, J. Caskey, F. Del Piero, K. G. Kousoulas: Intramuscular vaccination of guinea pigs with the live-attenuated human herpes simplex vaccine VC2 stimulates a transcriptional profile of vaginal Th17 and regulatory Tr1 responses. In: Vaccine. Band 36, Nr. 20, Mai 2018, S. 2842–2849, doi:10.1016/j.vaccine.2018.03.075, PMID 29655629.
- ↑ Herpes Virus Mutant Points Towards New Vaccine Strategy. news.feinberg.northwestern.edu, abgerufen am 13. August 2018 (amerikanisches Englisch).
- ↑ A. L. Richards, P. J. Sollars, J. D. Pitts, A. M. Stults, E. E. Heldwein, G. E. Pickard, G. A. Smith: The pUL37 tegument protein guides alpha-herpesvirus retrograde axonal transport to promote neuroinvasion. In: PLoS Pathogens. Band 13, Nr. 12, Dezember 2017, Artikel e1006741, doi:10.1371/journal.ppat.1006741, PMID 29216315, PMC 5749899 (freier Volltext).
- ↑ C. D. Petro, B. Weinrick, N. Khajoueinejad, C. Burn, R. Sellers, W. R. Jacobs, B. C. Herold: HSV-2 ΔgD elicits FcγR-effector antibodies that protect against clinical isolates. In: JCI Insight. Band 1, Nr. 12, August 2016, doi:10.1172/jci.insight.88529, PMID 27536733, PMC 4985247 (freier Volltext).
- ↑ New Genital Herpes Vaccine Candidate Provides Powerful Protection in Preclinical Tests. In: Penn Medicine News. 19. Januar 2017, abgerufen am 28. Januar 2017.
- ↑ Penn Institute for Immunology – The Friedman laboratory. med.upenn.edu, 3. September 2018, abgerufen am 1. Oktober 2018.
- ↑ S. Awasthi, L. M. Hook, C. E. Shaw, B. Pahar, J. A. Stagray, D. Liu, R. S. Veazey, H. M. Friedman: An HSV-2 Trivalent Vaccine Is Immunogenic in Rhesus Macaques and Highly Efficacious in Guinea Pigs. In: PLoS Pathogens. Band 13, Nr. 1, Januar 2017, Artikel e1006141, doi:10.1371/journal.ppat.1006141, PMID 28103319, PMC 5245903 (freier Volltext).
- ↑ Immune Design Pipeline. Immune Design, archiviert vom (nicht mehr online verfügbar) am 11. Mai 2019; abgerufen am 22. April 2017.
- ↑ J. M. Odegard, P. A. Flynn, D. J. Campbell, S. H. Robbins, L. Dong, K. Wang, J. Ter Meulen, J. I. Cohen, D. M. Koelle: A novel HSV-2 subunit vaccine induces GLA-dependent CD4 and CD8 T cell responses and protective immunity in mice and guinea pigs. In: Vaccine. Band 34, Nr. 1, Januar 2016, S. 101–109, doi:10.1016/j.vaccine.2015.10.137, PMID 26571309, PMC 6322202 (freier Volltext).
- ↑ a b GV2207 – HSV-2 Immunotherapeutic. In: genvec.com. GenVec, Inc. (GNVC), archiviert vom (nicht mehr online verfügbar) am 9. Dezember 2017; abgerufen am 16. August 2016.
- ↑ Nanobio – HSV-2 Vaccine. Abgerufen am 2. August 2016.
- ↑ NanoBio Corporation: NanoBio’s Genital Herpes Vaccine Demonstrates Efficacy In Guinea Pigs As Both A Prophylactic And A Therapeutic Vaccine. Abgerufen am 2. August 2016.
- ↑ PBS Vax™ Therapeutic Vaccines. In: profectusbiosciences.com. Archiviert vom (nicht mehr online verfügbar) am 23. Mai 2019; abgerufen am 15. August 2016.
- ↑ Introducing RVx. 12. März 2016, abgerufen am 2. August 2016 (amerikanisches Englisch).
- ↑ Herpes Vaccine Research. Herpes Vaccine Research, abgerufen am 2. August 2016 (amerikanisches Englisch).
- ↑ FDA Launches Criminal Investigation Into Unauthorized Herpes Vaccine Research. khn.org, abgerufen am 21. Mai 2018.
- ↑ Rational Vaccines: A case study in pharma deregulation - MedCity News. medcitynews.com, März 2017, abgerufen am 26. September 2017.
- ↑ Status of Vaccine Research and Development of Vaccines for Herpes Simplex Virus. (PDF) Abgerufen am 30. August 2016.
- ↑ K. J. Sandgren, K. Bertram, A. L. Cunningham: Understanding natural herpes simplex virus immunity to inform next-generation vaccine design. In: Clinical & Translational Immunology. Band 5, Nr. 7, Juli 2016, S. e94, doi:10.1038/cti.2016.44, PMID 27525067, PMC 4973325 (freier Volltext) – (nature.com).
- ↑ QUESTIONS AND ANSWERS The Herpevac Trial for Women. Abgerufen am 30. August 2016.
- ↑ J. Cohen: Immunology. Painful failure of promising genital herpes vaccine. In: Science. Band 330, Nr. 6002, Oktober 2010, S. 304, doi:10.1126/science.330.6002.304, PMID 20947733, bibcode:2010Sci...330..304C.
- ↑ Better Neutralization of Herpes Simplex Virus Type 1 (HSV-1) Than HSV-2 by Antibody From Recipients of GlaxoSmithKline HSV-2 Glycoprotein D2 Subunit Vaccine. In: The Journal of Infectious Diseases. 15. August 2014, abgerufen am 10. Juli 2019.
- ↑ PaxVax Signs R&D Collaboration with UC San Diego to Develop a Vaccine to Prevent Herpes Simplex Virus Infections. In: paxvax.com. 10. Juni 2014, abgerufen am 15. August 2016.
- ↑ About. Abgerufen am 4. Januar 2017.
- ↑ The PaxVax Platform - Product Pipeline. Abgerufen am 5. September 2016.
- ↑ S. Awasthi, E. E. Zumbrun, H. Si, F. Wang, C. E. Shaw, M. Cai, J. M. Lubinski, S. M. Barrett, J. W. Balliet, J. A. Flynn, D. R. Casimiro, J. T. Bryan, H. M. Friedman: Live attenuated herpes simplex virus 2 glycoprotein E deletion mutant as a vaccine candidate defective in neuronal spread. In: Journal of Virology. Band 86, Nr. 8, April 2012, S. 4586–4598, doi:10.1128/JVI.07203-11, PMID 22318147, PMC 3318599 (freier Volltext).
- ↑ Amgen Pipeline. Abgerufen am 2. August 2016.
- ↑ Genocea Announces Strategic Shift to Immuno-oncology and the Development of Neoantigen Cancer Vaccines. Genocea, 25. September 2017, archiviert vom (nicht mehr online verfügbar) am 26. September 2017; abgerufen am 30. März 2021.
- ↑ AuRx, Inc. AuRx, abgerufen am 4. Januar 2017.
- ↑ AuRx. AuRx, abgerufen am 4. Januar 2017.
- ↑ S. C. McAllister, M. R. Schleiss: Prospects and perspectives for development of a vaccine against herpes simplex virus infections. In: Expert Review of Vaccines. Band 13, Nr. 11, November 2014, S. 1349–60, doi:10.1586/14760584.2014.932694, PMID 25077372, PMC 4385587 (freier Volltext).
- ↑ Mymetics HSV Vaccine Candidate. Mymetics, abgerufen am 22. April 2016.
- ↑ Biological Efficacy Study of HerpV Vaccine With QS-21 to Treat Subjects With Recurrent Genital Herpes. Abgerufen am 31. August 2016.
- ↑ Vical HSV-2 Therapeutic Vaccine VCL-HB01. Abgerufen am 18. Januar 2016.
- ↑ Vical Reports Phase 2 Trial of HSV-2 Therapeutic Vaccine Did Not Meet Primary Endpoint. Vical.com, abgerufen am 16. Juni 2018.