Phosphor
| Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Phosphor, P, 15 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementkategorie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 5, 3, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | weiß-beige (W) dunkelrot (R) Schwarz (S) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 0,09 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 30,97 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 100 (98) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 106 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 180 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Ne] 3s2 3p3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 1011,8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 1907 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 2914,1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 4963,6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 6273,9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modifikationen | 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | monoklin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | W: 1877 R: 2340 S: 2670 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | unmagnetisch | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 317,3 K (44,2 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 550 (277 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | 17,02 · 10−6 m3·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 12,129 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 0,657 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampfdruck | 20,8 Pa bei 294 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spezifische Wärmekapazität | 769 J·kg−1·K−1 bei 298 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | W: 0 R: 0 S: 1,0 · 10−9 S·m−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 0,235 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustände | ±3, 4, 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | 2,19 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
Phosphor (von griechisch φως-φορος „lichttragend“, vom Leuchten des weißen Phosphors bei der Reaktion mit Sauerstoff) ist ein chemisches Element mit dem Symbol P und der Ordnungszahl 15.
Phosphor kommt in mehreren, sich untereinander stark unterscheidenden Modifikationen vor.
Phosphorverbindungen sind für alle Lebewesen essentiell und bei Aufbau und Funktion der Organismen in zentralen Bereichen beteiligt, wie der DNA und der zellulären Energieversorgung (ADP/ATP).
Geschichte
Phosphor wurde 1669 von Hennig Brand, einem deutschen Apotheker und Alchemisten, entdeckt, als dieser – auf der Suche nach dem „Stein der Weisen“ – Urin bis zur Trocknung eindampfte. Als er den Rückstand unter Luftabschluss glühte, entstand durch Reduktion mit organischer Materie weißer Phosphor, der im Dunkeln aufgrund der Phosphoreszenz leuchtete. Obwohl Phosphor zu dieser Zeit noch keine Verwendung außer als Nachtlampe fand, wurde es mit Gold aufgewogen. Hennig Brand wurde durch diese Entdeckung nicht reich und verkaufte das Herstellungsrezept an einen Alchemisten, der hiermit ein Vermögen machte. Johann Daniel Kraft, besagter Alchimist, demonstrierte die Herstellung von Phosphor 1677 vor Robert Boyle.
Weißer Phosphor wurde anfangs auf Grund seiner faszinierenden Eigenschaft der Phosphoreszenz als Heilmittel verwendet. Später spielte er eine wichtige Rolle bei der Streichholzherstellung; da weißer Phosphor hochgiftig ist, kam es jedoch oft zu schweren Vergiftungen bei Arbeitern.
Weißer Phosphor spielte in der Militärgeschichte als Waffe eine Rolle. Dieser wurde als Füllmaterial von Brandbomben, den sogenannten Phosphorbomben verwendet. So setzte die britische Luftwaffe im Zweiten Weltkrieg ein Gemisch aus weißem Phosphor und Kautschuk ein. Durch den Kautschuk klebt die zähflüssige Masse und lässt sich deshalb schlecht abstreifen. Sie verursacht auf der Haut schlecht heilende Wunden.
Vorkommen
In der Natur kommt Phosphor ausschließlich in gebundener Form, das heißt nicht gediegen, meist in Form der Phosphate in der Erdkruste vor (Gehalt in der Erdkruste: ~ 0,09 %>[1]). Typische Mineralien sind etwa die Apatite Ca5(PO4)3(F,Cl,OH). Besonders der Fluorapatit und der mit Calciumcarbonat durchsetzte Phosphorit stellen ökonomisch die wichtigsten Phosphate dar. Darüber hinaus gibt es weitere phosphorhaltige Mineralien, wie beispielsweise den Wavellit Al3(PO4)(F,OH) · 5 H2O, den Vivianit Fe3(PO4)2 · 8 H2O und den Türkis CuAl6[(PO4)(OH2)]4 · 4 H2O.
Die größten Vorkommen an Phosphat-Mineralien findet man in Afrika (Marokko, Westsahara), in China und den USA (Florida). Die kontinentalen Vorkommen reichen nur noch für wenige hundert Jahre. Es existieren allerdings große Vorkommen unter Wasser, die momentan nicht ökonomisch abgebaut werden können.[2]
Außer in Mineralien kommt Phosphor auch in Ablagerungen von Vogelkot von Meeresvögeln, dem sogenannten Guano (Chilesalpeter) vor. Dieser findet sich vorwiegend auf einigen Inseln im Pazifischen Ozean, wie Nauru oder Kiribati und in Südamerika (Peru/Chile).
Von den weltweit jährlich geförderten etwa 100 Millionen Tonnen an Rohphosphaten werden etwa 90 % zur Herstellung von Düngemitteln verwendet. Phosphor kann in Düngemitteln derzeit durch keinen anderen Stoff ersetzt werden.
Phosphor hat auch in der organischen Welt eine wichtige Bedeutung und kommt in verschiedensten Bereichen der Fauna und Flora vor: Etwa als Hydroxylapatit Ca5(PO4)3OH, welcher einer der Hauptbestandteile der Gerüstsubstanz ist, die in Knochen und Zähnen vorkommt. Weiterhin spielen Phosphorverbindungen als Bestandteile der Nukleinsäuren und als Bestandteil des Energieträgers ATP eine wichtige Rolle in lebenden Organismen.
Gewinnung und Darstellung
Dazu wird in elektrischen Lichtbogenöfen Calciumphosphat in Form der Mineralien Phosphorit oder Apatit mit Koks und Quarzsand auf 1400 °C erhitzt und so zu weißem Phosphor umgesetzt. Der im Koks enthaltene Kohlenstoff wirkt dabei als Reduktionsmittel und das Siliciumdioxid des Quarzes dient als Schlackenbildner. Der beim Prozess gasförmig anfallende Phosphor wird kondensiert und unter Wasser gesammelt.
Modifikationen und Eigenschaften

Phosphor tritt in vier allotropen Modifikationen als weißer, roter, schwarzer und violetter Phosphor auf. Jeder dieser Grundtypen bildet verschiedene Kristallstrukturen. Dadurch kommt es zu sehr großen Unterschieden in physikalischen Eigenschaften und Reaktivität.
Da die anderen Modifikationen schwer direkt zu gewinnen sind, wird zunächst immer weißer Phosphor produziert und dieser dann in andere Modifikationen umgewandelt. Diese können durch hohen Druck und hohe Temperatur ineinander überführt werden. Der schwarze Phosphor ist bei Raumtemperatur die eigentlich stabile Modifikation, die anderen sind allerdings auf Grund der geringen Umwandlungsgeschwindigkeit metastabil. Weißen Phosphor kann man im Labor durch Erhitzung von Rotem Phosphor unter Ausschluss von Sauerstoff herstellen. Umgekehrt kann roter Phosphor auch durch mehrstündiges Erhitzen von weißem Phosphor auf etwa 360 °C erzeugt werden. Vorlage:Absatz-L
Gasförmiger Zustand
Im Phosphordampf überwiegen unterhalb von 1200 °C P4-Tetraeder als kleinste molekulare Einheiten. Der Dissoziationsgrad beträgt bei 800 °C ~ 1 %. Zwischen 1200 und 2000 °C überwiegen P2-Moleküle mit stickstoffanaloger Valenzelektronenstruktur, oberhalb von 2000 °C dissoziieren diese mit steigenden Temperaturen schließlich langsam zu atomarem Phosphor. Vorlage:Absatz-L
Weißer Phosphor

Weißer Phosphor ist die flüchtigste und reaktivste Modifikation des Phosphors. Er besitzt eine Dichte von 1,82 g/cm3, einen Schmelzpunkt von 44,1 °C, einen Siedepunkt von 280 °C und ist durchscheinend und wachsartig. Verunreinigt wird der weiße Phosphor auch als gelber Phosphor bezeichnet. Der kubische weiße Phosphor ist in Phosphortrichlorid und Kohlenstoffdisulfid CS2 sehr leicht löslich; 100 g Kohlenstoffdisulfid lösen mehr als 1 kg Phosphor. In Tetrachlorkohlenstoff, Benzol oder Ether ist Phosphor schwach löslich. Da er in Wasser schlecht löslich ist, wird weißer Phosphor unter Wasser aufbewahrt.
Bei –77 °C geht die kubische Form (α-Form) in eine hexagonale Form (β-Form) über. In jeder Form (α-, β-, in Lösung) bildet weißer Phosphor P4-Tetraeder mit einem Bindungswinkel von 60°.
In fein verteiltem Zustand entzündet sich weißer Phosphor an der Luft von selbst, ab etwa 50 °C entzünden sich auch kompakte Stücke und verbrennen zu Phosphor(V)-oxid. Daher muss weißer Phosphor unter Wasser aufbewahrt werden. Brennender Phosphor darf nicht mit Wasser gelöscht werden, da die Gefahr besteht, dass der Phosphorstaub in feine Ritzen gespült wird und sich nach Verdunstung des Wassers wieder selbst entzündet. Brennender Phosphor wird am besten mit Sand gelöscht.
An der Luft kann weißer Phosphor eine hellgrüne Chemolumineszenz zeigen. Diese entsteht aus dem durch den hohen Dampfdruck des weißen Phosphors in der Umgebung vorhandenen gasförmigen P4, das durch Gasphasenoxidation über P4O6 zu P4O10 reagiert. Meist in heftiger exothermer Reaktion verbindet sich Phosphor mit Halogenen, Metallen oder Schwefel. Die hieraus entstehenden Verbindungen sind Phosphorsulfide, Phosphor(III)- oder Phosphor(V)-Verbindungen sowie Phosphide. Unter Einwirkung von starken Laugen bei hoher Temperatur disproportioniert Phosphor zu Phosphin und Hypophosphit. Bedingt durch die hohe Affinität von Phosphor zu Sauerstoff, die durch die starke Phosphor-Sauerstoff-Bindung bewirkt wird, wirkt weißer Phosphor stark reduzierend. So wird Schwefelsäure beim Erwärmen mit weißem Phosphor zu Schwefeldioxid reduziert.
Das bei der Verbrennung von Phosphor entstehenden Phosphorpentoxid ist stark hygroskopisch und bildet mit der Luftfeuchtigkeit dichte Nebel aus Phosphorsäure. Weißer Phosphor wird deshalb in Nebelgranaten verwendet. Während des Irakkrieges wurden von den USA in Falludscha derartige Granaten gegen die Stellungen der Aufständischen eingesetzt. Die in unmittelbarer Nähe explodierten Granaten führten dabei zu teils schwersten Verbrennungen auch bei unbeteiligten Zivilisten, weswegen diese Art des Einsatzes heftig umstritten ist.[3] [4].
Toxizität
Weißer Phosphor ist hochgiftig, bereits 50 mg sind für den Menschen tödlich. Der Tod tritt erst nach fünf bis zehn Tagen ein. Auch wird weißer Phosphor nur langsam ausgeschieden.
Die Toxizität des weißen Phosphors wird vor allem auf sein hohes Reduktionsvermögen zurückgeführt, womit intrazelluläre oxidative Stoffwechselabläufe wie Eiweiß- und Kohlenhydratsynthese gestört werden. Dies betrifft vorwiegend enzymatisch gesteuerte Stoffwechselvorgänge in der Leber. Eine weitere Gefahr bilden die durch Reaktion mit Wasser gebildeten hochgiftigen Phosphane, die als starke Stoffwechselgifte eine besondere Affinität zum Zentralnervensystem besitzen[5].
Schwarzer Phosphor
Die bei Zimmertemperatur stabilste Modifikation existiert in einer amorphen und drei kristallinen Formen. Schwarzer Phosphor ist aufgrund seiner polymeren Form unlöslich, fast unbrennbar, sehr reaktionsträge und besitzt eine Dichte von 2,69 g/cm3. Daher ist der schwarze Phosphor ebenso wie der rote Phosphor ungiftig. Das dem schwarzen Phosphor zugrundeliegende Kristallgitter besteht aus gewellten Doppelschichten, in dem die Phosphoratome pyramidal mit drei weiteren in der Nachbarschaft befindlichen Phosphoratomen in einem Bindungswinkel von 100° verbunden sind. In dieser Konfiguration besitzt Phosphor Halbleitereigenschaften. In feuchter Luft oxidiert schwarzer Phosphor etwas schneller als roter Phosphor, überzieht sich dabei aber mit einer farblosen, viskosen Flüssigkeitshaut aus Phosphorsäuren, so dass der weitere Sauerstoffzutritt verhindert und eine Entzündung erschwert wird.
Schwarzer Phosphor entsteht unter hohem Druck aus weißem oder rotem Phosphor und unterscheidet sich durch seine Farbe stark von den vorgenannten.
Roter Phosphor

Eine Reihe amorpher und kristalliner Formen mit Dichtevariationen zwischen 2,0 und 2,4 g/cm3 und Schmelzpunkten zwischen 585 °C und 610 °C werden unter der Bezeichnung roter Phosphor zusammengefasst. Gemeinhin ist roter Phosphor amorph, lässt sich aber durch Rekristallisation aus geschmolzenem Blei in den monoklinen Hittorfschen (violetten) Phosphor überführen, welcher eine dreidimensional vernetzte polymere Form bildet.
Gewonnen wird roter Phosphor durch mehrstündiges Erhitzen von weißem Phosphor auf etwa 260 °C unter Luftabschluss. Eine langsame Umwandlung geschieht auch bei Lichteinwirkung. Iod katalysiert die Umwandlung von weißen in roten Phosphor
Die Unterschiede zwischen den kristallinen Anteilen im roten Phosphor bedingen die verschiedenen Formen desselben. Einfluss haben hier die Korngröße, die Art des Gitters, Verunreinigungen und die verschiedenen Absättigungen der Randgruppen mit Halogenen, Sauerstoff und Hydroxylgruppen.
Roter Phosphor ist reaktionsträge. Bezogen auf die Reaktivität gleicht der violette Phosphor eher dem schwarzen Phosphor, während sich der Schencksche Phosphor sehr viel reaktionsfreudiger zeigt als „normaler“ roter Phosphor.
Roter Phosphor ist ungiftig, seine Erstbeschreibung wird Anton Schrötter von Kristelli zugeschrieben.
Hellroter Phosphor
Der Hellrote oder auch Schencksche Phosphor (Rudolf Schenck, 1902) entsteht durch Kochen von weißem Phosphor in Phosphortribromid (PBr_3). Das Produkt ist eine Mischverbindung aus Phosphor mit 10 bis 30 % Brom. Die Dichte liegt bei 1,88 g/cm3.
Violetter/Hittorfscher Phosphor


Violetter Phosphor entsteht beim ein- bis zweiwöchigen Erhitzen von weißem Phosphor auf ca. 550 °C. Entdeckt wurde er von Johann Wilhelm Hittorf. Es handelt sich um ein nichtleitendes Polymer, das unlöslich in CS2 ist. Die Strukturaufklärung gelang Ende der 1960er Jahre an der Universität Stuttgart durch Herbert Thurn. Auch der violette Phosphor ist ungiftig.
„Phosphor-Nanostäbchen“
Im August 2004 ist es deutschen Forschern gelungen, zwei weitere Modifikationen des vielgesichtigen Elements zu isolieren und strukturell zu charakterisieren: Phosphor-Nanostäbchen. Bei diesen beiden Modifikationen liegen die Phosphoratome in Form von Kettenmolekülen (Polymeren) vor. Entdecker der neuen Modifikationen sind Arno Pfitzner von der Universität Regensburg und Helmut Eckert von der Universität München. Die rotbraunen Fasern, die sich deutlich von der roten Phosphormodifikation unterscheiden, sind an der Luft in trockenem Zustand über Wochen stabil. Unter dem Elektronenmikroskop zeigte sich diese rotbraune Phosphor-Form als lange, parallel ausgerichtete Nanostäbe mit Querschnitten von ungefähr 0,34 nm (Nanometer) beziehungsweise 0,47 nm.
Isotope
Phosphor hat nur ein stabiles Isotop: 31P, dies ist das einzige in der Natur vorkommende Isotop des Phosphors. Phosphor hat mehrere weitere Isotope, die allerdings alle radioaktiv sind. Das Phosphorisotop 33P hat mit 25,3 Tagen die längste Halbwertszeit. Das Phosphorisotop 32P, welches auch radioaktiv ist, wird in Medizin und Forschung als Tracer benutzt, um Stoffwechselprozesse zu beobachten.
Verwendung
Der größte Teil des hergestellten weißen Phosphors (80 %) wird zu Phosphor(V)-oxid verbrannt, das als Ausgangsmaterial für die Phosphorsäureherstellung sowie für die Darstellung verschiedener Phosphate verwendet wird. Phosphor(V)-oxid hat außerdem noch Bedeutung als eine der wirksamsten wasserentziehenden Substanzen (Trockenmittel).
Ein weiterer Teil wird zu Phosphortrichlorid (PCl3) und Phosphorpentasulfid (P4S10) verarbeitet, die wiederum als Grundstoffe für die Herstellung von Flammschutzmitteln, Additiven, Weichmachern und Pflanzenschutzmitteln dienen.
Roter Phosphor findet Verwendung bei der Streichholzherstellung. Paradoxerweise wird roter Phosphor in fein verteilter Form auch Kunststoffen (z. B. Polyamid) als Flammschutzmittel zugesetzt: Die Reaktionsprodukte von Phosphor, Luftsauerstoff und Wasser (Luftfeuchte, Restfeuchte im Kunststoff) bilden dabei eine verkohlte Schutzschicht gegen die Flammen.
Des Weiteren werden die als Dünger wichtigen Phosphate direkt aus Calciumphosphat gewonnen, indem dieses mit Schwefelsäure aufgeschlossen wird. Es entsteht das so genannte Superphosphat. Hierzu werden etwa 60 % der weltweiten Schwefelsäureerzeugung benötigt.
Phosphor wird auch für militärische Zwecke genutzt. Neben dem Einsatz des Weißen Phosphors in Brandmunitionen spielt der Einsatz des Phosphors in Nebelmunition eine sehr große Rolle. Während früher der sehr giftige und selbstentzündliche Weiße Phosphor auch in militärischen Nebelmitteln eingesetzt wurde, wird heutzutage der ungiftige rote Phosphor in Mischungen mit Oxidationsmitteln und metallischen Brennstoffen verwendet. Bis in die 80er wurde mit weißem Phosphor auch in Schulen experimentiert, bis es aus gesundheitlichen Gründen verboten wurde. Es darf nur noch mit rotem Phosphor experimentiert werden.
Im Boden
Auf natürlichem Wege gelangt Phosphor einerseits über die Apatit-Verwitterung in den Boden oder aber aus zersetzter organischer Materie. Die atmosphärische Deposition spielt bei Phosphor nur ein untergeordnete Rolle. Durch Düngung erhöht der Mensch aktiv den Phosphorgehalt im Boden meist über Phosphate. Als Hauptfaktoren der Verluste kann die Erosion betrachtet werden. Die Auswaschung ist sehr gering und abgesehen von Phosphan-Gas kommt es zu keiner Ausgasung aus dem Boden. Phosphor besitzt eine sehr schlechte Löslichkeit. So führt zum Beispiel eine Adsorption an Fe und Al Hydroxide in sauren Böden zu einer Phosphatfixierung. In basischen Böden kommt es zu einer Ausfällung mit Ca. Generell kann man zwischen drei unterschiedlichen Phosphatfraktionen im Boden unterscheiden:
- In der Bodenlösung verfügbares Phosphat ist direkt pflanzenverfügbar. Jedoch ist diese mit 1–2 kg/ha die kleinste Fraktion.
- Labiles Phosphat ist durch spezifische Sorption an Eisen- und Aluminium-Oxide oder an Tonminerale locker gebunden. 450–900 kg/ha können so im Boden vorliegen. Durch Resorption kann aus dieser Fraktion bodenverfügbares Phosphat gebildet werden.
- Stabiles Phosphat hat praktisch keine Bedeutung für die Pflanzenernährung, obwohl es mit 3000–6000 kg/ha die größte der drei Fraktionen ist. Als wichtigste Vertreter seien hier Apatite und Calciumphosphate genannt.
Biologische Bedeutung
Phosphor ist für alle biologischen Organismen essentiell. Phosphorverbindungen sind Bestandteil der DNA- und RNA-Moleküle, der Trägersubstanz der Erbinformationen aller Lebewesen. Die stark phosphorhaltige Verbindung Adenosintriphosphat spielt eine entscheidende Rolle beim Energiestoffwechsel (aktivierte Zucker) der Zellen. Phosphor ist weiterhin in Zuckerphosphaten, Phospholipiden und Coenzymen enthalten. Die Phosphorylierung ist einer der wichtigsten Regulationsmechanismen in Organismen. Phosphate sind auch ein elemenarer Bestandteil des pH-Puffersystems im Blut.
Terrestrische Pflanzen enthalten ca. 3 % Phosphor, Säugetiere und Menschen ca. 1 %. Die Gerüstsubstanz von Knochen und Zähne besteht hauptsächlich aus Hydroxylapatit (Ca5(PO4)3OH). Der Körper eines Menschen von 70 kg Gewicht enthält etwa 700 Gramm Phosphor, wovon 600 g fest im Knochensystem gebunden sind.
Der Tagesbedarf eines erwachsenen Menschen beträgt ca. 0,75 Gramm Phosphor, vor allem in Milchprodukten, Fleisch, Fisch und Brot ist er reichhaltig vorhanden. Die Phosphatverfügbarkeit wirkt für Pflanzen vielfach als limitierender Wachstumsfaktor, weswegen in der Landwirtschaft große Mengen phosphathaltigen Düngers ausgebracht werden müssen.
Weißer Phosphor und einige Phosphorverbindungen wie Phosphan sind sehr giftig.
Nachweis
Spektroskopisch
Die Methode der Wahl für den Nachweis von Phosphorverbindungen ist die 31P-NMR-Spektroskopie. 31P ist das einzige natürlich vorkommende Phosphor-Isotop und hat eine Kernspin-Quantenzahl von 1/2. Im Vergleich zum Wasserstoff beträgt die relative Empfindlichkeit nur 6,6 %. Der Resonanzbereich beträgt ca. 700 ppm (P4 hat beispielsweise eine Verschiebung von −488 ppm). Als Standard wird im Allgemeinen 85%ige Phosphorsäure verwendet. Da Phosphor ein Spin-1/2-Kern ist, sind die Spektren sehr gut auszuwerten. Wenn zusätzlich der Wasserstoff entkoppelt wird, resultiert meist ein scharfes Signal. Die Phosphorverschiebung ist stark abhängig von seinen Bindungspartner, er ist also sehr gut für die Identifikation von bekannten Verbindungen geeignet. Bei unbekannten Verbindungen ist die Aussagekraft oft beschränkt, weil einem Spektrenbereich nur selten einer Verbindungsklasse exklusiv zuzuordnen ist.
| Derivate mit | Chemische Verschiebung (δ in ppm) |
|---|---|
| 3-bindigem P | −180 bis +200 |
| 4-bindigem P | −120 bis +130 |
| 5-bindigem P | −100 bis −20 |
| 6-bindigem P | −220 bis −130 |
Nasschemisch
Die quantitative und qualitative Bestimmung von Phosphor erfolgt über das Phosphat (genauer Orthophosphat PO43−). Gebundener Phosphor wird hierzu gegebenenfalls durch oxidierenden Aufschluss in Phosphat überführt.
Qualitativer Nachweis
Bei der Nachweisreaktion mit Ammoniummolybdat erhält man in saurer Lösung einen gelben Niederschlag von Ammoniummolybdophosphat:
In alkalischer Ammoniaklösung fällt Phosphat bei Anwesenheit von Magnesium-Ionen als Magnesiumammoniumphosphat aus:
Der Nachweis ist auch in Form von Zirconiumhydrogenphosphat durchführbar:
Nicht korrekt ist, wie in vielen Lehrbüchern angegeben, die Form Zr3(PO4)4, in wässrigen Lösungen bildet sich diese Verbindung nicht!
Historisch ist die Mitscherlich Probe zum Nachweis von weißem Phosphor interessant, die allem voran bei vermuteten Phosphorvergiftungen eingesetzt wurde. Hierbei wird der Mageninhalt mit Wasser erhitzt, wobei der weiße Phosphor, der mit dem Wasserdampf flüchtig ist, anschließend kondensiert und bei Berührung mit Luftsauerstoff durch ein Leuchten (Chemolumineszenz) in Erscheinung tritt.
Bei Strukturuntersuchungen von Verbindungen, in denen Phosphor enthalten ist, eignet sich die 31P-Kernresonanzspektroskopie.
Quantitativer Nachweis
Gravimetrie
Für eine gravimetrische Bestimmung kann aus Phosphat und Molybdationen in stark salzsaurer Lösung ein gelbes Molybdophosphation gebildet werden:
Mit 8-Hydroxychinolin (kurz HOx oder Oxin genannt) bildet sich ein schwer löslicher Niederschlag von Oxin-12-molybdo-1-phosphat, der anschließend bei 160 °C getrocknet und in wasserfreier Form gewogen wird.
- Fällungsform:
- Wägeform:
- (Farbe: dunkelorange)
Der grobkristalline Niederschlag enthält nur 1,37 % Phosphor. Somit sind vor allem kleinere Phosphatmengen gut bestimmbar (siehe Mikromol-Verfahren).
Volumetrie
Volumetrische Phosphatbestimmungen werden durch Fällung mit La3+ oder mit Bi3+-Maßlösungen und anschließender Rücktitration mit EDTA durchgeführt.
Sicherheitshinweise
Weißer Phosphor
Weißer Phosphor kann sich an der Luft entzünden, wenn er fein verteilt vorliegt. Die Selbstentzündungstemperatur liegt bei rund 34 °C, also sehr nahe bei Raumtemperatur. Die Reaktion zu Phosphorpentoxid ist stark exotherm. Mit Wasser und Alkalihydroxiden können giftige Phosphane entstehen. Starke Oxidationsmittel reagieren meist explosionsartig.
Akute Vergiftungen äußern sich durch gastrointestinale Störungen, Leberschädigung mit schweren Stoffwechselstörungen sowie Schädigung von Herz und Nieren. Chronische Vergiftungen führen auch in geringen Mengen zu Störung des Allgemeinbefindens und Schädigung von Blut und der Knochen (Osteoporose), besonders am Kiefer.
Dosen ab 15 mg weißem Phosphor können schwere toxische Wirkungen auslösen. Mengen ab 50 mg (~1 mg/kg Körpergewicht) können bereits letal wirken [6].
Andere Modifikationen
Die anderen bekannten Modifikationen von Phosphor sind wegen ihrer Wasserunlöslichkeit und geringeren Reaktivität in reiner Form ungiftig. Auch entzünden sie sich erst bei höherer Temperatur (Roter Phosphor erst bei 260 °C).
Verbindungen
Phosphor ist sehr reaktiv und bildet mit sehr vielen Nichtmetallen kovalente Verbindungen. Dabei kommt er in allen Oxidationsstufen zwischen –3 und +5 und den Koordinationszahlen 1 bis 6, meist 3 bis 4, vor. Die Oxidationszahlen –3 und +5 sind dabei bevorzugt.
Wasserstoffverbindungen
Phosphane (die alten Bezeichnung Phosphine ist nicht mehr IUPAC-konform, wird aber in der chemischen Literatur, v. a. in der angelsächsischen, fast ausschließlich verwendet) bezeichnen Verbindungen des dreibindigen Phosphors mit Wasserstoff oder Ersatz einer oder mehrere Wasserstoffatome durch organischen Gruppen als Bindungspartner. Die organische Gruppe muss über die Kohlenstoffatome des Grundgerüstes direkt mit dem Phosphoratom verbunden sein. Wird die organische Gruppe durch ein Sauerstoffatom an das Phosphoratom gebunden (also Einheit P-O-C, z. B. im P(OPh)3), spricht man von Phosphiten.
Sauerstoffverbindungen
Vor allem mit Sauerstoff bildet Phosphor sehr viele verschiedene Verbindungen. Dies ist dadurch begründet, dass der Phosphor in vielen verschiedenen Oxidationsstufen vorliegen kann. dabei sind sowohl Phosphor−Sauerstoff–Einfachbindungen als auch Doppelbindungen möglich. auch verbrückende Phosphor−Sauerstoff-Phosphor-Bindungen sind möglich. Besonders umfangreich ist die Zahl der Phosphor-Sauerstoff-Säuren. Phosphor bildet verschiedene Oxide, die dem Adamantan ähnliche Strukturen bilden:
- Phosphortrioxid P4O6ist eine weiße, weiche Verbindung, die sehr giftig und reaktiv ist und schnell zu Phosphorpentoxid weiterreagiert.
- Phosphortetraoxid P2O4 ist ein Mischoxid. Man kann es durch Oxidation von Phosphortrioxid in Tetrachlorkohlenstoff gewinnen.
- Phosphorpentoxid P4O10 ist das wichtigste Phosphoroxid. Es ist sehr hygroskopisch und wird als Trocknungsmittel verwendet.
Von diesen Oxiden können eine große Zahl von Phosphor-Sauerstoff-Säuren und ihre entsprechenden Salze mit einem oder mehreren Phosphoratom abgeleitet werden.
| Oxidationsstufe des Phosphors |
Strukturformel | Name der Säure | Name der Salze | |
|---|---|---|---|---|
| Monophosphorsäuren | ||||
| +I |  |
Phosphinsäure | Phosphinate | |
| +III |  |
Phosphonsäure | Phosphonate | |
| +V | 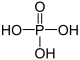 |
Phosphorsäure | Phosphate | |
| +V |  |
Peroxophosphorsäure | Peroxophosphate | |
| Diphosphorsäuren | ||||
| +II |  |
Hypodiphosphonsäure | Hypodiphosphonate | |
| +III |  |
Diphosphonsäure | Diphosphonate | |
| +IV | 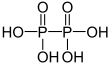 |
Hypodiphosphorsäure | Hypodiphosphate | |
| +V |  |
Diphosphorsäure | Diphosphate | |
| +V |  |
Peroxodiphosphorsäure | Peroxodiphosphate | |
Es gibt eine Reihe von phosphorhaltigen Mineralien, die wichtigsten sind dabei Hydroxylapatit und Fluorapatit. Weitere Phosphormineralien findet man in der Kategorie:Phosphormineral.
Halogenverbindungen
Phosphor bildet eine große Zahl von Verbindungen mit den Halogeniden Fluor, Chlor, Brom und Iod. Die wichtigsten Verbindungentypen sind dabei PX3, P2X4 und PX5. Die Fluorverbindungen sind gasförmig, die Chlorverbindungen meist flüssig, Brom- und Iodverbindungen fest. Viele Phosphorhalogenverbindungen sind giftig. Beipsiele für diese Verbindungsklasse sind Phosphortrichlorid und Phosphorpentachlorid
weitere Phosphorverbindungen
Phosphor bildet mit Schwefel eine Reihe von Verbindungen, die in ihrer Struktur z. T. den Phosphor-Sauerstoff-Verbindungen ähneln. Sie haben allgemein die Struktur P4Sx (x = 3–10)
Stickstoff bildet mit Phosphor Nitride der Zusammensetzung PN und P3N5.
Organische Verbindungen
Organische Phosphorverbindungen und dabei vor allem Triphenylphosphin spielen in vielen organischen Reaktionen, z. B. der Wittig-Reaktion eine wichtige Rolle.
In der Biochemie sind vor allem die Phosphorsäureester relevant. Sie sind lebenswichtiger Teil von vielen Stoffwechselprozessen und Teil der DNA. Wichtige Moleküle sind:
Literatur
- A. F. Holleman, Egon Wiberg, Lehrbuch der Anorganischen Chemie. de Gruyter, Berlin, 1995, ISBN 3-11-012641-9
- Erwin Riedel, Anorganische Chemie. de Gruyter, Berlin, 2002, ISBN 3-11-017439-1
- John Emsley: Phosphor - ein Element auf Leben und Tod. Wiley-VCH, Weinheim 2001, ISBN 3-527-30421-5
Quellen
- ↑ Hollemann, Wiberg:Lehrbuch der Anorganischen Chemie, 91.–100. Auflage,de Gruyter, Berlin, 1985. ISBN 3-11-007511-3 (S.928–931)
- ↑ Phosphat bei USGS Mineral Resources
- ↑ ZDFheute: US-Armee und britische Truppen setzten Phosphor ein, 16. November 2005
- ↑ Stern: USA verteidigen Einsatz von Phosphor, 17. November 2005
- ↑ Medizinische Fakultät der Universität Rostock
- ↑ BGIA Gestis Stoffdatenbank




![{\displaystyle \mathrm {H_{2}PO_{4}^{-}+12\ MoO_{4}^{2-}+22\ H^{+}+3\ NH_{4}^{+}\longrightarrow (NH_{4})_{3}[P(Mo_{3}O_{10})_{4}]} +12\ H_{2}O}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e60443357b8c08a2dd0cf285b83755c0e5b685e3)


![{\displaystyle \mathrm {H_{2}PO_{4}^{-}+12\ [MoO_{2}Cl_{3}(H_{2}O)]^{-}\longrightarrow [P(Mo_{3}O_{10})_{4}]^{3-}+26\ H^{+}+36\ Cl^{-}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/56d476070527b7a9c9659cb8bebfae63420e28a3)
![{\displaystyle \mathrm {[P(Mo_{3}O_{10})_{4}]^{3-}+3\ HOx+3\ H^{+}\longrightarrow (H_{2}Ox)_{3}[P(Mo_{3}O_{10})_{4}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/d0a909a5635b3e3662faca5125cd8212f970ba2b)
![{\displaystyle \mathrm {(H_{2}Ox)_{3}[P(Mo_{3}O_{10})_{4}]\cdot x\ H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b4a4ac6f7c69607fc6cb08462cc8acb0da733f77)
![{\displaystyle \mathrm {(H_{2}Ox)_{3}[P(Mo_{3}O_{10})_{4}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/4015e1b4d1a83dc0b2c857e26fa6cdef99a7a9da)