Titan (Element)
| Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Titan, Ti, 22 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementkategorie | Übergangsmetalle | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 4, 4, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | silbrig metallisch | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-142-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.311 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 47,867(1)[2] u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 140 (176) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 160 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Ar] 3d2 4s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 6.828120(12) eV[3] ≈ 658.81 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 13.5755(25) eV[3] ≈ 1309.84 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 27.49171(25) eV[3] ≈ 2652.55 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 43.26717(19) eV[3] ≈ 4174.65 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 99.299(12) eV[3] ≈ 9580.9 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalisch[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | hexagonal (bis 882 °C, darüber kubisch) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | 4,50 g/cm3 (25 °C)[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohshärte | 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | paramagnetisch (Χm = 1,8 · 10−4)[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 1941 K (1668 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 3533 K[7] (3260 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | 10,64 · 10−6 m3·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 427 kJ/mol[7] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 18,7 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 4140 m·s−1 bei 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spezifische Wärmekapazität | 523[8] J·kg−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Austrittsarbeit | 4,33 eV[9] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 2,5 · 106 S·m−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 22 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mechanisch[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| E-Modul | 105 GPa (= 105 kN/mm2)[10] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poissonzahl | 0,34[10] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemisch[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustände | +2, +3, +4 = stabil | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normalpotential | −0,86 V (TiO2+ + 2 H+ + 4 e− → Ti + H2O) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | 1,54 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Titan ist ein chemisches Element mit dem Elementsymbol Ti und der Ordnungszahl 22. Es gehört zu den Übergangsmetallen und steht im Periodensystem in der 4. Nebengruppe (4. IUPAC-Gruppe) oder Titangruppe. Das Metall ist weiß-metallisch glänzend, hat eine geringe Dichte, ist korrosions- und temperaturbeständig sowie mechanisch fest und duktil.
Titan wird heute üblicherweise zu den Leichtmetallen gezählt. Mit einer Dichte von 4,50 g/cm3 bei Raumtemperatur ist es deren schwerstes, liegt nahe an der heute meist verwendeten Grenze zwischen Leicht- und Schwermetallen von 5 g/cm3.
In der Erdkruste gehört Titan zu den zehn häufigsten Elementen, kommt jedoch fast ausschließlich chemisch gebunden als Bestandteil von Mineralen vor. Nur in wenigen Lagerstätten ist das Auftreten von elementarem Titan nachgewiesen.
Geschichte[Bearbeiten | Quelltext bearbeiten]
Titan wurde 1791 in England von dem Geistlichen und Amateurchemiker William Gregor im Titaneisen entdeckt. Nur zwei Jahre nach der Veröffentlichung von Gregors Entdeckung trennte der deutsche Chemiker Martin Heinrich Klaproth von einer in Boinik (Ungarn) gefundenen Probe roten Schörls das Mineral Rutil (TiO2) ab. Als er seine Ergebnisse 1795 veröffentlichte, verwies er auf Gregors Arbeit und die Ähnlichkeit des von ihm gefundenen Oxids und bezeichnete Gregors Mineral als „Eisenhaltiges Titanit aus Cornwall“. Er gab damit dem Element – angelehnt an das griechische Sagengeschlecht der Titanen – seinen heutigen Namen.[12][13][14]
Es gelang jedoch erst im Jahre 1831 Justus von Liebig, aus dem Erz unreines metallisches Titan in Form eines dunkelvioletblaues Pulvers oder von zusammenhängenden kupferglänzenden Blättern zu gewinnen.[15][16]
Die Herstellung von reinem Titan gelang erstmals 1875 dem russischen Chemiker Dmitri Kirillowitsch Kirillow.[12][17] Seine Veröffentlichung unter dem Namen „Forschungen über Titan“ (russisch Исследования над титаном), in dem er die Ergebnisse seiner Experimente zur Isolierung von reinem Titan behandelte, blieb jedoch unbeachtet. Im Jahr 1887 gelang Lars Fredrik Nilson (Entdecker des Elements Scandium) und Otto Pettersson (Chemieprofessoren an der Universität Uppsala bzw. der Universität Stockholm) die Herstellung von Titan mit einer Reinheit von 95 Prozent, indem sie Titantetrachlorid mit Natrium in einem luftdichten Stahlzylinder reduzierten. Dabei entstanden gelbe Schuppen mit bläulicher Oberfläche. Der französischen Chemiker Henri Moissan veröffentlichte 1895 ein Verfahren, mit dem er Titan mit einer Reinheit von 97 % gewinnen konnte.[12][18] Zu 99,9 % reines Titan stellte 1910 erstmals Matthew A. Hunter (1878–1961) mit dem Hunter-Verfahren her, indem er in einer Stahlbombe Titantetrachlorid (Titan(IV)-chlorid) mit Natrium auf 700 °C bis 800 °C erhitzte. Doch auch seine gewonnene Materialprobe war durch vorhandene Verunreinigungen bei normalen Temperaturen spröde und ließ sich nur bei Rotglut gut formen.[19][12] Erst 1925 konnten Anton Eduard van Arkel und Jan Hendrik de Boer mit Hilfe des Van-Arkel-de-Boer-Verfahrens Titan von hoher Reinheit darstellen, welches sich als auffällig duktil zeigte.[20]
Ende der 1930er Jahre entwickelte William Justin Kroll schließlich ein für die Technik geeignetes Verfahren, den sogenannten Kroll-Prozess, das 1940 patentiert wurde.[21] In der Folge konnte durch Einführung der großtechnischen Reduktion von Titantetrachlorid mit Magnesium das Titan für kommerzielle Anwendungen erschlossen werden. Die erste Pilotanlage welche 100 lb Stücke (je ca. 45 kg) produzieren konnte, wurde 1944 in Boulder City, Nevada, USA, errichtet.[14]
In den Vereinigten Staaten stiegen Ende der 1940er/Anfang der 1950er Jahre mehrere Unternehmen mit starker staatlicher Unterstützung in das Titangeschäft ein. So steigerte eine 1947 von DuPont errichtete Pilotanlage die Produktion bis 1952 auf 800 t Titanschwamm pro Jahr. Im Vereinigten Königreich begann die Imperial Chemical Industries Ltd. 1948 mit der Produktion von Titanschwamm. In Kontinentaleuropa wurde das Schmelzen und die Herstellung von Barren etwa 1955 begonnen und durch Unternehmen in Frankreich, Deutschland und Schweden durchgeführt. Die Geburtsstunde der sowjetischen Titanindustrie war das Jahr 1950 und die Produktion von Titanschwamm nach dem Kroll-Prozess begann im Jahr 1954. Auch in Japan begann ab 1952 die Produktion von Titanschwamm.[22]
In den frühen 1950er Jahren wurden Titanlegierungen mit verbesserten Eigenschaften durch Zusatz von Aluminium, Mangan und Vanadium entdeckt. So die Legierungen Ti-8Mn, Ti-4Al-4Mn (1951) und die viel verwendete Legierung Ti-6Al-4V (1954), die von Crucible Steel patentiert und zuerst im Triebwerk Pratt & Whitney J57 für die Lockheed U-2 eingesetzt wurde. Die erste Beta-Legierung, B120VCA (Ti-13V-11Cr-3Al), wurde ebenfalls von Crucible Steel entwickelt und in großem Umfang für das Aufklärungsflugzeug SR-71 (1955) verwendet. Siliziumzusätze für den Einsatz bei höheren Temperaturen wurden 1956 in Großbritannien eingeführt. Im Rolls-Royce Avon-Triebwerk wurde bereits ab 1954 Ti-2Al-2Mn verwendet. Zur etwa gleichen Zeit fand Titan als Material in korrosiven Umgebungen und für medizinische Implantate Anwendung.[22]
Seit diesen Jahren stieg die Produktion von Titanlegierungen für Flugzeuge stark an und erreichte zwischen 2003 und 2007, mit der Einführung des Airbus A380, des Joint Strike Fighter (JSF, F-35) und der Boeing 787 (sowie den militärischen Konflikten im Irak und in Afghanistan), einen Höchstwert.[22]
Vorkommen und Abbau[Bearbeiten | Quelltext bearbeiten]
Titan kommt in der Erdkruste kaum in elementarer, d. h. metallischer Form, sondern beinahe ausschließlich als Bestandteil von chemischen Verbindungen vor. Es ist keineswegs selten, steht es doch mit einem Gehalt von 0,565 % an 9. Stelle der Elementhäufigkeit in der kontinentalen Erdkruste.[23] Meist ist es nur in geringer Konzentration vorhanden.
Die wichtigsten Minerale, die Titan enthalten, sind aufgrund dessen hoher Sauerstoffaffinität oxidische Verbindungen wie:
- Ilmenit (Titaneisenerz), FeTiO3
- Leukoxen, Gemenge aus eisenarmem Ilmenit und anderen titanhaltigen Mineralen
- Perowskit, CaTiO3
- Titanit (Sphen), CaTi[SiO4]O
- Rutil, TiO2
- Anatas, TiO2
- Brookit, TiO2
Die bekannten Hauptvorkommen liegen in Australien, China, Norwegen, Indien, Russland, Ukraine, Brasilien, Kanada und Südafrika. Im Jahr 2010 wurden auch in Paraguay Lagerstätten entdeckt[24], die aber bisher kaum genutzt werden. 2020 wurden weltweit 8,4[25] bis 8,6[26] Millionen Tonnen Titan (gemessen als TiO2) abgebaut. Hauptabbauland war China, weitere große Abbauländer waren Australien, Mosambik, Südafrika, Kanada und die Ukraine. 90 % der abgebauten Titanminerale waren dabei Ilmenit und der Großteil wurde zur Erzeugung von TiO2-Pigmenten für Farbstoffe, Papier und Kunststoffe verwendet. In den USA betrug dieser Anteil 2021 95 %, aus den restlichen 5 % wurden Überzüge für Schweißstäbe, Carbide, Chemikalien oder metallisches Titan hergestellt.[26] Titan steht auf der Liste kritischer Rohstoffe der USA[27] und wurde 2020 auch von der EU neu in die Liste kritischer Rohstoffe aufgenommen.[28]
Meteoriten können Titan enthalten. In der Sonne und in Sternen der Spektralklasse M wurde ebenfalls Titan nachgewiesen. Auf dem Erdmond sind ebenso Vorkommen vorhanden.[29][30] Gesteinsproben der Mondmission Apollo 17 enthielten bis zu 12,1 % Titan(IV)-oxid. Auch in Kohleaschen und Pflanzen ist es enthalten.
| Land | 2016 | 2017 | 2018 | 2019 | 2020 |
|---|---|---|---|---|---|
| (in Tonnen TiO2) | |||||
| 1.070.000 | 993.000 | 875.250 | 780.465 | 830.800 | |
| 37.660 | 66.930 | 73.090 | 81.650 | 61.940 | |
| 550.000 | 670.000 | 620.000 | 550.000 | 480.000 | |
| 1.196.000 | 1.242.000 | 1.932.000 | 2.306.900 | 2.911.800 | |
| 341.400 | 167.800 | 172.700 | 205.200 | 205.000 | |
| 3.340 | 30.630 | 30.000 | 4.880 | 5.000 | |
| 66.600 | 65.000 | 65.000 | 60.000 | 28.000 | |
| 339.480 | 345.560 | 340.150 | 262.660 | 256.410 | |
| 91.800 | 122.670 | 117.250 | 162.790 | 158.340 | |
| 152.100 | 230.700 | 214.000 | 258.800 | 220.500 | |
| 5.990 | 8.500 | 12.600 | 6.930 | 7.010 | |
| 731.200 | 725.200 | 701.400 | 786.900 | 874.000 | |
| 260.000 | 238.200 | 176.370 | 211.280 | 229.780 | |
| 18.880 | 2.900 | 3.000 | 3.100 | 3.000 | |
| 238.120 | 280.320 | 287.940 | 281.030 | 291.740 | |
| 156.570 | 190.480 | 145.400 | 165.180 | 135.930 | |
| 950.000 | 1.090.000 | 1.000.000 | 970.000 | 950.000 | |
| 16.510 | 30.630 | 35.670 | 25.940 | 11.150 | |
| 0 | 4 | 23 | 64 | 84 | |
| 4.750 | 6.370 | 6.175 | 6.130 | 6.455 | |
| 339.800 | 430.300 | 518.950 | 564.050 | 537.430 | |
| 55.000 | 66.000 | 100.000 | 100.000 | 100.000 | |
| 109.620 | 117.160 | 122.250 | 112.680 | 119.810 | |
| Gesamt | 6.734.820 | 7.120.354 | 7.549.218 | 7.906.629 | 8.424.179 |
Gewinnung[Bearbeiten | Quelltext bearbeiten]
Reines, metallisches Titan kommt in Lagerstätten kaum vor und wird deshalb aus Titaneisenerz (Ilmenit) oder Rutil gewonnen. Der dabei verwendete Herstellungsprozess ist sehr aufwendig, was sich im hohen Preis für Titan niederschlägt. Der Weltmarktpreis ist Schwankungungen unterworfen, insbesondere seit dem Boykott westlicher Staaten gegen Russland. Titan in Barrenform war Ende 2023 für rund 10,5 US$ pro kg aus China erhältlich[31] und damit günstiger als noch im Jahr 2022. Titan als Metall und auch seine Legierungen sind generell teurer als Aluminiumlegierungen oder Stähle.
Seit Entdeckung des Kroll-Prozesses ist die Herstellung fast unverändert. Meist vom Ilmenit oder Rutil ausgehend, wird Titandioxid in der Hitze mit Chlor und Kohle zu Titantetrachlorid und Kohlenstoffmonoxid umgesetzt (siehe chemische Formeln und Abbildung). Anschließend erfolgt mit flüssigem Magnesium die elektrochemische Reduktion des Titantetrachlorids zu Titan-Schwamm. Pro Tonne Titan werden etwa 55.000 kWh[32] elektrische Energie benötigt, was circa 3,7 mal soviel ist wie bei der ebenfalls energieintensiven Aluminiumherstellung mit rund 15.000 kWh/t[33]. Das Verfahren ist nur in Ländern mit geringen Kosten für elektrische Energie rentabel, also nicht in Mitteleuropa. Deshalb ist Recycling wirtschaftlich und ökologisch besonders sinnvoll.

Titan-„Schwamm“, 99,7 %, gewonnen nach dem Kroll-Prozess
Im letzten Reaktionsschritt kann alternativ Natrium statt Magnesium verwendet werden.[34]
Zur Herstellung von kompaktem Metall wird der poröse Titanschwamm im Vakuum-Lichtbogenofen oder seltener mit dem Elektronenstrahl bei über 1700 °C umgeschmolzen. Dieser Prozess ist technologisch sehr anspruchsvoll, da Titan im glühenden Zustand so reaktionsfreudig ist, dass es mit fast allen Materialien, mit denen es in Kontakt kommt, verunreinigt wird. Diese Verunreinigung kann zur Versprödung und zum Verlust der nützlichen Eigenschaften führen. Folglich ist es eine Herausforderung, ein geeignetes Material zu finden, das Titan im geschmolzenen Zustand enthält und Verunreinigungen vermeidet.[22] Schon in den 1950er-Jahren kamen Metallurgen zu der Erkenntnis, dass man Titan nicht in einem üblichen keramischen Tiegel schmelzen kann, weil es der Keramik Sauerstoff entzieht. Auch in Graphit lässt es sich nicht folgenlos schmelzen, weil es mit dem Kohlenstoff reagiert und das Metall dadurch spröde wird.[14] Deshalb werden u. a. wassergekühlte Kupfertiegel verwendet[35].
| Land | 2019 | 2020 |
|---|---|---|
| (in Tonnen) | ||
| 85.000 | 123.000 | |
| 250 | 250 | |
| 49.000 | 49.200 | |
| 16.000 | 15.000 | |
| 44.000 | 31.000 | |
| 100 | 2.800 | |
| 8.000 | 5.000 | |
| Geschäftsgeheimnis | Geschäftsgeheimnis | |
| Gesamt ohne USA (gerundet) | 200.000 | 230.000 |

Ultrareines Titan gewinnt man nach dem Van-Arkel-de-Boer-Verfahren. Da es sich um einen Gasphasenprozess handelt, ist die Produktionsrate relativ gering; es entsteht kein Schwamm als Zwischenprodukt, sondern unmittelbar kompaktes Titan.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Chemische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
| Oxidationszustände von Titan | |
|---|---|
| +2 | TiO, TiCl2 |
| +3 | Ti2O3, TiCl3, TiF3, TiP |
| +4 | TiO2, TiS2, TiCl4, TiF4 |


Titan kann die Oxidationszustände 2, 3 und 4 einnehmen. Nur die Verbindungen mit dem Oxidationszustand 4 sind stabil.
Titan bildet an der Luft spontan eine äußerst beständige oxidische Schutzschicht (Passivierungsschicht) aus, die es gegen viele Medien schützt.
Zu beachten ist die hohe Reaktivität von Titan mit vielen Medien bei erhöhten Temperaturen oder erhöhtem Druck, wenn die Passivierungsschicht diesen Bedingungen nicht standhält. Hier kann die Reaktionsgeschwindigkeit bis zur Explosion anwachsen. In reinem Sauerstoff bei 25 °C und 25 bar verbrennt Titan von einer frischen Schnittkante ausgehend vollständig zum Titandioxid. Trotz Passivierungsschicht reagiert es bei Temperaturen oberhalb von 880 °C mit Sauerstoff, bei Temperaturen ab 550 °C mit Chlor. Titan reagiert („brennt“) auch in reinem Stickstoff.
Gegen verdünnte Schwefelsäure, Salzsäure, chloridhaltige Lösungen, kalte Salpetersäure, Laugen wie Natriumhydroxid und die meisten organischen Säuren ist Titan beständig, löst sich dagegen in konzentrierter Schwefelsäure unter Bildung des violetten Titansulfats langsam auf. Wegen der Explosionsgefahr sind bei Anwendungen in Chlorgas die Sicherheitsvorschriften strikt einzuhalten.
Titan in Pulverform ist pyrophor, also selbstentzündlich. Schon bei Raumtemperatur reagiert es mit der umgebenden Luft, die Reaktionswärme erhitzt das Material bis sich unter Beschleunigung der Reaktion eine rauchende Flamme ausbildet. Die Zündbereitschaft hängt unter anderem sehr stark von der Korngröße und dem Verteilungsgrad ab. Das Metall in kompakter Form ist nicht brennbar. Es nimmt jedoch bei höheren Temperaturen leicht Sauerstoff, Stickstoff und Wasserstoff auf, dies bewirkt Versprödung und Härtesteigerung.[11]

Nachweis[Bearbeiten | Quelltext bearbeiten]
TiO2+ bildet mit Wasserstoffperoxid einen charakteristischen gelb-orangen Komplex (Triaquohydroxooxotitan(IV)-Komplex), der auch zum photospektrometrischen Nachweis geeignet ist. Die Probe wird mit einem Überschuss konzentrierter Schwefelsäure gekocht und in ein Eisbad mit Wasserstoffperoxid gegossen. Bei lautem Zischen färbt sich das Eisbad gelb-orange[38][39].
Aufgrund der großen farblichen Ähnlichkeit wird dieser Nachweis umgangssprachlich auch als „Tequila Sunrise-Nachweis“ bezeichnet.
Kristallstruktur[Bearbeiten | Quelltext bearbeiten]
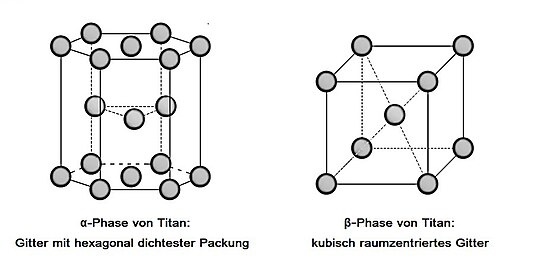
Titan kristallisiert im Magnesium-Typ mit der Raumgruppe P63/mmc (Raumgruppen-Nr. 194) in einer hexagonal dichtesten Kugelpackung mit a = 295,04 pm sowie c = 468,33 pm[40] und bildet dann die sogenannte α-Phase (siehe links in der Abbildung). Das Achsenverhältnis c/a beträgt 1,587 und weicht leicht vom Idealwert 1,633[41] der hexagonal dichtesten Kugelpackung ab. Bei Erhitzung auf über 882 °C bildet sich die β-Phase, die ein raumzentriertes Gitter darstellt (siehe rechts in der Abbildung). Die β-Phase kann in Titanlegierungen schon bei Raumtemperatur auftreten, wenn sie Vanadium, Niobium oder Tantal als Legierungselement enthalten.
Elektrische Leitfähigkeit[Bearbeiten | Quelltext bearbeiten]
Die elektrische Leitfähigkeit von Titan beträgt nur S/m und damit erheblich weniger als bei Kupfer und Aluminium, die in der Elektrotechnik als Leiterwerkstoffe verwendet werden. Unterhalb einer Temperatur von 0,4 K[42] wird Titan supraleitend.
(Hinweis: Weitere physikalische Kennwerte sind in der großen Tabelle zu Beginn des Artikels zu finden)
Farbgebung[Bearbeiten | Quelltext bearbeiten]
Titan kann durch gezieltes Erzeugen einer Oxidschicht mittels Anodisieren farblich gestaltet werden. Dabei wird die Farbe durch Lichtbrechung an unterschiedlich dicken Schichten und nicht durch Farbpigmente erzielt, vgl. Dünnschichtinterferenz. Bei 10–25 nm Schichtdicke ergibt sich eine Goldfarbe, bei 25–40 nm Lila, bei 40–50 nm Dunkelblau, bei 50–80 nm Hellblau, bei 80–120 nm Gelb, bei 120–150 nm Orange, bei 150–180 nm Lila, bei 180–210 nm Grün.
Reintitan als Werkstoff[Bearbeiten | Quelltext bearbeiten]
Für Anwendungen steht reines, d. h. unlegiertes Titan in vier unterschiedlichen Reinheitsgraden zur Verfügung[43]:
- Titan Grade 1 (DIN Werkstoffnummer 3.7025)
- Titan Grade 2 (DIN Werkstoffnummer 3.7035)
- Titan Grade 3 (DIN Werkstoffnummer 3.7055)
- Titan Grade 4 (DIN Werkstoffnummer 3.7065)
Der Reinheitsgrad (englisch „grade“) nimmt von Titan Grade 1 bis Titan Grade 4 ab. Die wichtigsten Begleitelemente sind Eisen, Kohlenstoff, Stickstoff, Sauerstoff und Wasserstoff, deren Konzentration jedoch immer deutlich unter 1 % liegt. Die Festigkeit nimmt von Titan Grade 1 in Richtung Titan Grade 4 zu, während die Duktilität in derselben Richtung abnimmt.
Obwohl Reintitan keine metallischen Legierungselemente enthält, hat es für eine Reihe von Anwendungen eine ausreichende Festigkeit. (Hierin unterscheidet sich Titan von dem Metallen Eisen und Aluminium, die nur durch zusätzliche Legierungselemente eine hohe Festigkeit erreichen). Der Elastizitätsmodul beträgt 105 000 - 110 000 N/mm² und ist damit etwa halb so groß wie der von Stahl. Die Zugfestigkeit hängt außer vom Reinheitsgrad auch von der Wärmebehandlung ab und liegt zwischen 290 und 740 N/mm²[43], also im Bereich von vielen Stählen, jedoch bei geringerer Dichte (4,5 g/cm³ statt rund 7,9 g/cm³).
Die Duktilität von Reintitan reicht aus, um es kalt oder warm zu verformen. Hierbei tritt Kaltverfestigung auf. Bei höheren Temperaturen versprödet es an Luft durch Aufnahme von Sauerstoff, Stickstoff und Wasserstoff.
Titanlegierungen[Bearbeiten | Quelltext bearbeiten]
Die mechanischen Eigenschaften und das Korrosionsverhalten lassen sich durch meist geringfügige Legierungszusätze von Aluminium, Vanadium, Mangan, Molybdän, Palladium, Kupfer, Zirconium und Zinn erheblich verbessern. Dadurch sind Titanlegierungen besonders für Anwendungen geeignet, bei denen es auf hohe Korrosionsbeständigkeit, Festigkeit und geringes Gewicht ankommt. Oberhalb einer Temperatur von 400 °C gehen die Festigkeitseigenschaften aber zurück.

Abhängig davon, welche Phasen in den Titan-Legierungen vorkommen, unterscheidet man zwischen:
- α-Titanlegierungen
- β-Titanlegierungen
- α+β-Titanlegerungen (beide Phasen enthaltend, siehe Abbildung)
Die folgende Tabelle erläutert, welche Legierungselemente die Bildung der α-Phase oder der β-Phase bewirken und fasst die wesentlichen Eigenschaften der Legierungstypen zusammen.
| α-Ti-Legierung | β-Ti-Legierung | α+β-Ti-Legierung | |
|---|---|---|---|
| Kristallstruktur | Gitter mit hexa-gonal dichtester Packung | kubisch raum-zentriertes Gitter | zweiphasig: Gitter von α-Ti und von β-Ti |
| phasenbestimende
Legierungselemente |
Aluminium | Vanadium, Niobium, Tantal | entsprechend α und β |
| Umformbarkeit | nur bei erhöhter Temperatur | bei Raumtem-peratur möglich | schwierig bei Raumtemperatur, Warmumformung bevorzugt |
| mechanische Eigenschaften | mittlere Festigkeit; gute Tempera-turbeständigkeit | hohe Festigkeit; geringere Temperaturbes-tändigkeit als α-Ti; geringerer Elasti-
zitätsmodul als α-Ti |
hohe Festigkeit und hohe Schwingfestigkeit; gute Temperatur-beständigkeit |
Titan-Legierungen werden häufig nach dem US-amerikanischen Standard ASTM mit Grade 5 bis 39 charakterisiert.[44][45]
Ti-6Al-4V[Bearbeiten | Quelltext bearbeiten]
Der wirtschaftlich bedeutendste (auch für Turbolader-Schaufeln) eingesetzte[46] Werkstoff Ti-6Al-4V („Ti64“; 6 % Aluminium, 4 % Vanadium, ASTM: Grade 5) hat die Nummer 3.7165 für industrielle Anwendungen und 3.7164 für Luftfahrtanwendungen.[47] Er gehört zum Typ der α+β-Ti-Legierungen.
Weitere wichtige Titanlegierungen, die hauptsächlich in der Luftfahrtindustrie eingesetzt werden:
| Bezeichnung | Legierungs-Zusammensetzung (in %) | Elastizitätsmodul in GPa | Dichte in g·cm−3 |
|---|---|---|---|
| Ti6246 | Ti-6Al-2Sn-4Zr-6Mo | 125,4 | 4,51 |
| Ti6242 | Ti-6Al-2Sn-4Zr-2Mo | bis 114 | 4,50 |
Die Zugfestigkeit von Titanlegierungen liegt mit 290 bis 1200 N/mm²[48] im Bereich von Baustahl mit 310 bis 690 N/mm²[49] und legierten Stählen mit 1100 bis 1300 N/mm²[50].
Ti-6Al-4V wird wie die meistens anderen Titanlegierungen bei erhöhter Temperatur umgeformt, d. h. heiß geschmiedet oder warm gewalzt. Bei der Herstellung von Blechen aus Blöcken macht z. B. Walzen ca. 50 % der gesamten Kosten des Produktes aus. Beim Verformen von Titanlegierungen tritt ähnlich wie bei rostfreiem Stahl Verfestigung auf.
Bei spanender Bearbeitung tritt Hitzeentwicklung auf, wobei reines Argon als Schutzgas eingesetzt wird. Um die Werkzeugschneiden zu schonen, kann der Einsatz eines flüssigen Kühlmittels zweckmäßig sein.[51]
Verwendung[Bearbeiten | Quelltext bearbeiten]

Konstruktionsteile:


- Verschleißteile in Lötanlagen, direkter Kontakt mit Elektrolot bis 500 °C
- Federn in Fahrgestellen von Kraftfahrzeugen
- In Flugzeugen und Raumschiffen für besonders beanspruchte Teile, die trotzdem leicht sein müssen (beispielsweise Außenhaut bei Überschallgeschwindigkeit, Verdichterschaufeln und andere Triebwerksteile, Fahrwerk[52])
- In Dampfturbinen für die am stärksten belasteten Schaufeln des Niederdruckteiles
- In der Rüstung: Einige U-Boot-Typen der Sowjetunion hatten Druckkörper aus einer Titanlegierung (z. B. Mike-Klasse, Alfa-Klasse, Projekt 661 oder Sierra-Klasse). Daneben kommt Titan, stärker als bei der zivilen Luftfahrt, in der militärischen Luftfahrt zum Einsatz. Dies führte dazu, dass zu Hochzeiten der sowjetischen Rüstungsproduktion ein Großteil der weltweiten Titanherstellung und -verwendung in der Sowjetunion erfolgte.
- Wegen seiner geringen Dichte bei der Herstellung von Niveauanzeigen und Schwimmern
- Liner für carbonfaserumwickelte Druckbehälter (Typ III). Um beim Wiedereintritt von Weltraumsatelliten ein vollständiges Verglühen/Zerstäuben zu gewährleisten ist jedoch das niedrigerschmelzende Aluminium vorteilhaft.[53]
Anwendungen in Seewasser und chloridhaltigen Medien:
- Schiffspropellerteile wie Wellen sowie Verspannungen für maritime Anwendungen (z. B. stehendes Gut bei Rennsegelyachten)
- Einbauteile in Meerwasserentsalzungsanlagen
- Bauteile für die Eindampfung von Kaliumchlorid-Lösungen
- Anoden von HGÜ-Seekabeln
- Apparate in Anlagen der Chlorchemie
Schutzausrüstung Militär und Polizei:
- Titanhelm und Titanschutzweste
Medizin:
- Als Biomaterial für Implantate in der Medizintechnik und Zahnheilkunde (Zahnimplantate, jährlich ca. 200.000 Stück allein in Deutschland) wegen seiner sehr guten Korrosionsbeständigkeit im Gegensatz zu anderen Metallen. Eine immunologische Abstoßungsreaktion (Implantatallergie) gibt es nicht. Auch bei Zahnkronen und Zahnbrücken wird es wegen der erheblich niedrigeren Kosten im Vergleich zu Goldlegierungen verwendet. In der Unfallchirurgie und chirurgischen Orthopädie ist es heute das Standardmaterial für Endoprothesen (Hüftgelenksersatz, Schultergelenksersatz) und Osteosynthesen (Platten, Nägel, Schrauben). Die Titan-Oxidschicht ermöglicht das feste Anwachsen von Knochen an das Implantat (Osseointegration) und ermöglicht damit den festen Einbau des künstlichen Implantates in den menschlichen Körper.
- In der Mittelohrchirurgie findet Titan als Material für Gehörknöchelchenersatz-Prothesen und für Paukenröhrchen bevorzugte Verwendung.
- In der Neurochirurgie haben Titan-Clips für Aneurysma-Operationen wegen ihrer günstigeren NMR-Eigenschaften solche aus Edelstahl weitgehend verdrängt.
Outdoor- und Sportartikel:
- Bei hochwertigen Fahrrädern legiert mit Aluminium und Vanadium als Rahmenmaterial und für Schrauben
- (Taucher-)Messer mit Titan- oder Titanlegierungsklingen, ebenso Essbestecke
- Als Zeltheringe (hohe Festigkeit trotz geringen Gewichts)
- Bei Golfschlägern als Schlägerkopf. Etwa 25 % des Titans wird hierfür verwendet.[54]
- Beim Stockschießen als äußerst stabiler Stab beim Eisstockstiel
- Als besonders leichte Eisschraube beim Bergsteigen
- Als Lacrosse-Schaft für höhere Festigkeit bei geringerem Gewicht
- Als bissfestes Vorfach beim Angeln auf Raubfische mit scharfen Zähnen
Elektronik:
- Im Jahr 2002 brachte Nokia das Handy-Modell 8910 und ein Jahr später das Handy 8910i auf den Markt, die ein Gehäuse aus Titan haben.
- Im April 2002 brachte Apple das Notebook PowerBook G4 Titanium auf den Markt. Große Anteile des Gehäuses waren aus Titan gefertigt, und das Notebook besaß in der 15,2-Zoll-Bildschirm-Ausführung bei einer Dicke von einem Zoll (2,54 cm) ein Gewicht von nur 2,4 kg.
- Im September 2019 brachte Apple die Apple Watch in 5. Generation Apple Watch in einer Titan-Edition auf den Markt. Die im September 2022 eingeführte Apple Watch Ultra besitzt ein 49-Millimeter Titangehäuse und wiegt 61,3 g.
- Die im September 2023 von Apple veröffentlichen iPhone-Modelle iPhone 15 Pro und iPhone 15 Pro Max verwenden eine Titanlegierung im Rahmen der Geräte.
- Einige Notebooks der ThinkPad-Serie von Lenovo (früher IBM) besitzen ein titanverstärktes Kunststoffgehäuse oder einen Gehäuserahmen aus einem Titan-Magnesium-Verbundstoff.
- Membranen der Lautsprecher von HiFi-Lautsprecherboxen, insbesondere für den Hochtonbereich
Elektrische Zigaretten:
- Titandraht wird hier als Heizspirale verwendet, da sich der elektrische Widerstand von Titan abhängig von der Temperatur messbar verändert. Auf dieser Grundlage bilden die neuesten elektrischen Akkuträger eine Temperaturregelung der Wicklung (Heizspirale) nach, um Temperaturschäden am Dochtmaterial (organische Watte) zu verhindern. Neben Nickel-200-Drähten und V2A-Stahldrähten gewinnt Titan in der Szene für diesen Zweck an Beliebtheit.
Sonstige Anwendungsgebiete:


- Schmuck, Armbanduhren und Brillengestelle aus Titan
- Münzen mit Titankern (z. B. österreichische 200-Schilling-Münzen)
- Titan-Sublimationspumpe zur Erzeugung von Ultrahochvakuum
- in der Galvanotechnik als Trägergestell bei der anodischen Oxidation von Aluminium (ELOXAL)
- als Bestandteil der nach CRISAT standardisierten beschusshemmenden Westen
- als Musikinstrument: Gongs aus Titan, wegen ihrer besonderen Klangeigenschaften
Verwendung als Legierungselement:
- Titan wird unter anderem als Mikrolegierungselement für Stahl (und andere Metalle) verwendet. Es verleiht Stahl bereits in Konzentrationen von 0,01–0,1 Prozent Massenanteil eine hohe Zähigkeit, Festigkeit und Duktilität. In rostfreien Stählen verhindert Titan die interkristalline Korrosion.
- Titanzink (Zink mit Titanzusatz) dient als witterungsbeständiger Werkstoff für Bleche z. B. für Dächer, Dachrinnen oder Wetterverkleidungen.
- Nitinol (Nickel-Legierung mit hohem Titangehalt) ist eine Formgedächtnis-Legierung und hoch pseudo-elastisch, weshalb es für Brillengestelle und Exstirpationsnadeln eingesetzt wird.
Verwendung als Bestandteil von Verbindungen:
- Herstellung weicher künstlicher Edelsteine
- Titandotierte Saphir-Einkristalle dienen als aktives Medium im Titan-Saphir-Laser für ultrakurze Pulse im Femtosekunden-Bereich
- Als Titantetrachlorid zur Herstellung von Glasspiegeln und künstlichem Nebel
- Bildung von intermetallischen Phasen (Ni3Ti) in hochwarmfesten Nickellegierungen
- Supraleitende Niob-Titan-Legierungen (z. B. als supraleitende Kabel in Elektromagneten von HERA bei DESY)
- In der Pyrotechnik
- Als Titannitrid für Beschichtungen von Wendeschneidplatten, Bohrern und Fräsern in der Fertigungstechnik
- Verbindungen des Titans mit Bor, Kohlenstoff oder Stickstoff finden Verwendung als Hartstoffe. Auch zur Herstellung von Cermets, speziellen Hartmetallsorten, werden Titanverbindungen eingesetzt.
- Titandioxid kann außerdem Bestandteil der Färbung von Arznei- und Nahrungsergänzungsmitteln in Tablettenform sein.
Normen[Bearbeiten | Quelltext bearbeiten]
Titan und Titanlegierungen sind unter anderem genormt in:
- DIN 17850, Ausgabe:1990-11 Titan; chemische Zusammensetzung
- ASTM B 348: Standard Specification for Titanium and Titanium Alloy, Bars and Billets
- ASTM B 265: Standard Specification for Titanium and Titanium Alloy, Sheets and Plates
- ASTM F 67: Standard Specification for Unalloyed Titanium, for Surgical Implant Applications
- ASTM F 136: Standard Specification for Wrought Titanium-6Aluminum-4Vanadium ELI (Extra Low Interstitial) Alloy for Surgical Implant Applications
- ASTM B 338: Standard Specification for Seamless and Welded Titanium and Titanium Alloy Tubes for Condensers and Heat Exchangers
- ASTM B 337: Specification for Seamless and Welded Titanium and Titanium Alloy Pipe
- ASTM F2885-11: Standard Specification for Metal Injection Molded Titanium-6Aluminum-4Vanadium Components for Surgical Implant Applications
Sicherheitshinweise[Bearbeiten | Quelltext bearbeiten]
Titan ist als Pulver feuergefährlich, kompakt ungefährlich. Die meisten Titansalze gelten als harmlos. Unbeständige Verbindungen wie Titantrichlorid sind stark korrosiv, da sie schon mit Spuren von Wasser Salzsäure bilden.
Titantetrachlorid wird in Rauchgranaten eingesetzt; es reagiert mit der Luftfeuchte und bildet einen weißen Rauch aus Titandioxid, außerdem Salzsäurenebel.
Biologische Nachteile des Titans im menschlichen Körper sind zurzeit unbekannt. So lösten die bisher aus Titan hergestellten Hüftgelenke oder Kieferimplantate, im Gegensatz zu Edelstahl, welcher Nickel enthält, keinerlei Allergien aus.[15]
Verbindungen[Bearbeiten | Quelltext bearbeiten]
Während metallisches Titan wegen der hohen Herstellungskosten nur anspruchsvollen technischen Anwendungen vorbehalten bleibt, ist das relativ preiswerte und ungiftige Farbpigment Titandioxid ein Begleiter des alltäglichen Lebens geworden. Praktisch alle heutigen weißen Kunststoffe und Farben und auch Lebensmittelfarben enthalten Titandioxid (es ist in Lebensmitteln als E 171 zu finden). Aber auch in der Elektro- und Werkstofftechnik und neuerdings auch in der Herstellung von Hochleistungsakkumulatoren für den Fahrzeugantrieb (Lithium-Titanat-Akku) werden Titanverbindungen eingesetzt.
Oxide[Bearbeiten | Quelltext bearbeiten]


Das wichtigste Titanoxid ist Titan(IV)-oxid (TiO2), das in drei wichtigen Polymorphen vorliegt: Anatas, Brookit und Rutil. Sie nehmen polymere Strukturen an, in denen Titan von sechs Oxidliganden umgeben ist. Es ist eine Vielzahl von reduzierten Oxiden (Suboxiden) von Titan bekannt, hauptsächlich reduzierten Stöchiometrien von Titan(IV)-oxid, die durch atmosphärisches Plasmaspritzen erhalten werden. Ti3O5 ist ein purpurroter Halbleiter, der durch Reduktion von Titan(IV)-oxid hergestellt wird mit Wasserstoff bei hohen Temperaturen und wird industriell eingesetzt, wenn Oberflächen mit Titan(IV)-oxid bedampft werden müssen: Es verdampft als reines Titan(II)-oxid, während Titan(IV)-oxid als Gemisch aus Oxiden verdampft und Beschichtungen mit variablem Brechungsindex abscheidet.[55] Bekannt ist auch Titan(III)-oxid mit der Korund-Struktur und Titan(II)-oxid mit der Natriumchlorid-Struktur.
Sulfide[Bearbeiten | Quelltext bearbeiten]
Titan(IV)-sulfid bildet Kristalle, die eine Schichtstruktur aufweisen, nämlich die Cadmiumiodid-Struktur.[56] Es kann als Elektrodenmaterial in Lithiumbatterien oder Lithium-Ionen-Akkumulatoren verwendet werden, wobei das niedrige Atomgewicht von Titan von Vorteil ist.
Titanate[Bearbeiten | Quelltext bearbeiten]
Titanate werden als Keramikmaterial verwendet. Viele, zum Beispiel Bleititanat, Blei-Zirkonat-Titanat, Bariumtitanat und Strontiumtitanat, bilden Ionenkristalle mit Perowskit-Struktur der Raumgruppe Pm3m (Raumgruppen-Nr. 221) mit ferroelektrischen Eigenschaften aus.[57] Bariumtitanat weist piezoelektrische Eigenschaften auf und wird als Wandler bei der Umwandlung von Schall und Elektrizität verwendet. Tetraisopropylorthotitanat ist als Lewis-Säure ein wichtiger Katalysator für Veresterungs- und Umesterungsreaktionen und für Sharpless-Epoxidierungen und ist Ausgangsmaterial für ultradünne Titan(IV)-oxid-Schichten und -Nanopartikel.
Halogenide[Bearbeiten | Quelltext bearbeiten]

Titan bildet je nach Oxidationszustand verschiedenartige Halogenide. Titan(IV)-chlorid ist eine farblose flüchtige Flüssigkeit, die an der Luft unter spektakulärer Emission weißer Wolken hydrolysiert. Beim Kroll-Prozess wird es bei der Umwandlung von Titanerzen zu Titan(IV)-oxid erzeugt.[58] In der organischen Chemie wird es als Lewis-Säure verwendet, beispielsweise bei der Mukaiyama-Aldolreaktion.[59] Beim Van-Arkel-de-Boer-Verfahren wird Titan(IV)-iodid zur Herstellung von hochreinem Titanmetall erzeugt.
Titan(III)-fluorid, Titan(III)-chlorid, Titan(III)-bromid und Titan(III)-iodid bilden verschiedene Kristallstrukturen aus. Titan(III)-chlorid kommt in vier verschiedenen Strukturen vor, die unterschiedliche chemische Eigenschaften haben.
Titan(II)-chlorid, Titan(II)-bromid und Titan(II)-iodid sind kristalline Feststoffe und haben eine trigonale Kristallstruktur vom Cadmium(II)-iodid-Typ (Polytyp 2H) mit der Raumgruppe P3m1 (Raumgruppen-Nr. 164).[60]
Weitere anorganische Verbindungen[Bearbeiten | Quelltext bearbeiten]
Titannitrid bildet goldgelbe Kristalle. Titancarbid ist ein graues Pulver. Beide haben ähnliche Eigenschaften: Sie bilden ein kubisches Gitter, sind extrem hart, haben eine hohe thermodynamische Stabilität, eine hohe Wärmeleitfähigkeit und elektrische Leitfähigkeit sowie einen sehr hohen Schmelzpunkt und Siedepunkt.[61] Titanborid wird zusammen mit Bornitrid als Material für Verdampferschiffchen verwendet. In kleinerem Umfang wird es als Versuchsmaterial für Kathoden von Aluminium-Schmelzflusselektrolysezellen und als Panzermaterial sowie als Ersatz für Diamantstaub und für Beschichtungen verwendet. Durch Einlagerung von Titanborid-Partikeln in Aluminium lassen sich die Eigenschaften des Aluminiums verbessern.
Titanylsulfat wird als Nachweisreagenz für Wasserstoffperoxid und Titan verwendet, da sich bei dessen Anwesenheit das intensiv orangegelb gefärbte Peroxotitanyl-Ion (TiO2)2+ bildet. Dieser Nachweis ist sehr empfindlich und es lassen sich schon Spuren von Wasserstoffperoxid nachweisen. Es entsteht auch als Zwischenprodukt beim Sulfatverfahren zur Herstellung von Titan(IV)-oxid.
Titandihydrid ist ein in Reinform metallisch glänzendes Pulver. Sonst ist es hellgrau und kann eine durch Sauerstoff- oder Stickstoffspuren blau oder gelb getönte Oberfläche aufweisen. Es wird als Treibmittel zur Herstellung von Metallschäumen verwendet. Es wird mit Metallpulver vermischt und das Gemisch dann bis fast zum Schmelzpunkt des Metalls erhitzt, das Titandihydrid setzt dabei Wasserstoffblasen frei, wodurch Metallschaum entsteht.
Metallorganische Komplexe[Bearbeiten | Quelltext bearbeiten]

Titanocendichlorid mit der Halbstrukturformel [Ti(Cp)2Cl2] oder auch [Ti(C5H5)2Cl2], ist ein Metallocen des Titans, das heißt eine metallorganische Verbindung mit aromatischen Ringsystemen. Es kann aus Titan(IV)-chlorid und Cyclopentadien gewonnen werden.[62]
Literatur[Bearbeiten | Quelltext bearbeiten]
- Gerd Lütjering, James C. Williams: Titanium. Springer, Berlin 2007, ISBN 978-3-540-71397-5.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Mineralienatlas:Titan (Wiki)
- Kristallines Titan als Abbildung in der Elementesammlung von Heinrich Pniok
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus webelements.com (titanium) entnommen.
- ↑ CIAAW, Standard Atomic Weights Revised 2013.
- ↑ a b c d e Eintrag zu titanium in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- ↑ a b c d e Eintrag zu titanium bei WebElements, www.webelements.com, abgerufen am 11. Juni 2020.
- ↑ N. N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. 1988, ISBN 3-527-26169-9, S. 1231.
- ↑ Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- ↑ a b Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- ↑ Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- ↑ David R. Lide: CRC Handbook of Chemistry and Physics. CRC Press, 1998, ISBN 0-8493-0479-2.
- ↑ a b der-wirtschaftsingenieur.de: Elastizitäts-Modul (E-Modul), abgerufen am 29. Mai 2013.
- ↑ a b c Eintrag zu Titan, Pulver in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. April 2017. (JavaScript erforderlich)
- ↑ a b c d C. Leyens, M. Peters.: Titanium and Titanium Alloys. Wiley, 2003, ISBN 3-527-60520-7 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Carl Hintze: Elemente, Sulfide, Oxyde, Haloide, Carbonate, Sulfate, Borate, Phaosphate, … Walter de Gruyter GmbH, 2021, S. 1590 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Kathleen L. Housley: Black Sand: The History of Titanium. Metal Management, Inc, 2007, ISBN 978-0-935297-43-0, S. 5.
- ↑ a b Alexander Stirn: Vom Triebwerk bis zum Campanile. In: Süddeutsche Zeitung. 25. April 2009, S. 22.
- ↑ Justus Liebig: Darstellung des metallischen Titans. In: Annalen der Physik und Chemie. Band 97, Nr. 1, 1831, S. 159–160, doi:10.1002/andp.18310970113.
- ↑ MetalSpace: Металлургия титана - Реферат | Металлургический портал MetalSpace.ru, abgerufen am 19. August 2023
- ↑ Henri Moissan, Titanium, 6. April 1895, Scientific American volume 39 issue 1005supp S. 16061, doi:10.1038/scientificamerican04061895-16061bsupp
- ↑ Matthew A. Hunter: Metallic Titanium. In: Journal of the American Chemical Society. 32. Jahrgang, Nr. 3, März 1910, S. 330–336, doi:10.1021/ja01921a006 (englisch).
- ↑ A. E. van Arkel, J. H. de Boer: Darstellung von reinem Titanium-, Zirkonium-, Hafnium- und Thoriummetall. In: Zeitschrift für anorganische und allgemeine Chemie. Band 148, Nr. 1, 1925, S. 345–350, doi:10.1002/zaac.19251480133.
- ↑ Patent US2205854: Method for manufacturing titanium. Angemeldet am 6. Juli 1938, Erfinder: Wilhelm Kroll.
- ↑ a b c d F. H. Froes: Titanium. ASM International, 2015, ISBN 978-1-62708-080-4, S. 16 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Geophysics, Astronomy, and Acoustics; Abundance of Elements in the Earth’s Crust and in the Sea, S. 14-18.
- ↑ latina-press.com: Riesige Titan-Vorkommen in Paraguay entdeckt, 8. November 2010.
- ↑ a b Titan. (PDF) Bundesministerium für Landwirtschaft, Regionen und Tourismus Seite 116, abgerufen am 25. August 2022.
- ↑ a b U.S. Geological Survey, Mineral Commodity Summaries 2022: TITANIUM MINERALS.
- ↑ Federal Register der US-Bundesregierung, 2022 Final List of Critical Minerals
- ↑ Europäische Kommission Critical Raw Materials.
- ↑ NASA-Daten weisen auf reiche Titan-Vorkommen auf dem Mond hin derstandard.at
- ↑ Forscher preisen den Mond als Rohstofflieferanten welt.de, abgerufen am 10. Oktober 2011.
- ↑ Base Metals Price Chart,China Shfe Price Today - Shanghai Metals Market. Abgerufen am 6. Dezember 2023.
- ↑ Carsten Siemers: Titan und Titanlegierungen. Hrsg.: Technische Universität Braunschweig. Vorlesung, 2015.
- ↑ Jürgen Vasters, Gudrun Franken: Aluminium - Informationen zur Nachhaltigkeit. Bundesanstalt für Geowissenschaften und Rohstoffe, Hannover 2020.
- ↑ Titanium, Titanium Alloys, and Titanium Compounds. Ullmann’s Encyclopedia of Industrial Chemistry, 15. Juni 2000, doi:10.1002/14356007.a27_095.
- ↑ INTECO melting and casting technologies GmbH, Titan-Produktion, 2023
- ↑ U.S. Geological Survey, Mineral Commodity Summaries 2022: TITANIUM.
- ↑ U.S. Geological Survey, Mineral Commodity Summaries 2021: TITANIUM.
- ↑ Jander, Blasius: Anorganische Chemie I. Hrsg.: Eberhard Schweda. 17., völlig neu bearbeitete Auflage. S. Hirzel Verlag, Stuttgart 2011, ISBN 978-3-7776-2134-0, S. 369.
- ↑ Eberhard Gerdes: Qualitative Anorganische Analyse. 2., korrigierte und überarbeitete Auflage. Springer-Verlag, Berlin/Heidelberg, S. 255.
- ↑ The lattice parameters of high purity alpha titanium; and the effects of oxygen and nitrogen on them. doi:10.1007/BF03398899 (springer.com [abgerufen am 21. November 2022]).
- ↑ Lexikon der Physik – hexagonal-dichteste Packung. Spektrum.de, abgerufen am 14. Februar 2024.
- ↑ Physikalische Eigenschaften von Titan bei webelements.com.
- ↑ a b Zapp Precision Metals GmbH: Titan Grade 1-4 l 3.7025/ 3.7035/ 3.7055/ 3.7065 l High Performance Alloys Datenblatt. Abgerufen am 4. Januar 2024.
- ↑ Specification for Titanium and Titanium Alloy Strip, Sheet, and Plate. ASTM International, doi:10.1520/b0265-15 (astm.org [abgerufen am 17. August 2018]).
- ↑ Titan-Schweisstechnik: Schweisstechnische Verarbeitung von Titan-Werkstoffen. (Memento vom 2. September 2016 im Internet Archive) (PDF; 595 kB).
- ↑ Firmenangaben Keller & Kalmbach.
- ↑ Werkstoffdatenblatt Ti-6Al-4V (PDF; 20 kB).
- ↑ Bargel: Werkstoffkunde, 11. Auflage, S. 343.
- ↑ Haberhauer: Maschinenelelemente. 17. Auflage, S. 625.
- ↑ Holzmann: Festigkeitslehre. 10. Auflage, S. 69.
- ↑ Verarbeitung von Titanwerkstoffen, Teil 1 form-technik.biz, Juli 2014, abgerufen am 5. Dezember 2019.
- ↑ Leibniz-Institut für Werkstofforientierte Technologien: Vorlesung „Werkstoffe des Leichtbaus II, Teil 3“ (Memento vom 20. August 2018 im Internet Archive), abgerufen am 20. August 2018
- ↑ Abgespact: Peak Technology entwickelt Satellitentanks für die ESA. In: factorynet.at. 22. November 2019, abgerufen am 11. Dezember 2023.
- ↑ Bernhard Ilschner, Robert F. Singer: Werkstoffwissenschaften und Fertigungstechnik. 5., neu bearbeitete Auflage, 2010, Springer, S. 456.
- ↑ Antonio Bonardi, Gerd Pühlhofer, Stephan Hermanutz, Andrea Santangelo: A new solution for mirror coating in $γ$-ray Cherenkov Astronomy. In: Experimental Astronomy. 38. Jahrgang, 2014, S. 1–9, doi:10.1007/s10686-014-9398-x, arxiv:1406.0622, bibcode:2014ExA....38....1B (englisch, arxiv.org [SUBMITTED MANUSCRIPT]).
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verbesserte und stark erweiterte Auflage. Walter de Gruyter, Berlin 1985, ISBN 3-11-007511-3, S. 1065.
- ↑ Ferroelektrikum, auf infos-aus-germanien.info
- ↑ Richard W. Johnson: The Handbook of Fluid Dynamics. Springer, 1998, ISBN 978-3-540-64612-9, S. 38–21 (englisch, google.com).
- ↑ Robert M. Coates, Leo A. Paquette: Handbook of Reagents for Organic Synthesis. John Wiley and Sons, 2000, ISBN 978-0-470-85625-3, S. 93 (englisch).
- ↑ J. D. Fast: The preparation of pure titanium iodides. In: Recueil des Travaux Chimiques des Pays-Bas. 58, 1939, S. 174–180, doi:10.1002/recl.19390580209.
- ↑ Naresh Saha: Titanium nitride oxidation chemistry: An x-ray photoelectron spectroscopy study. In: Journal of Applied Physics. no. 7. Jahrgang, Nr. 7, 1992, S. 3072–3079, doi:10.1063/1.351465, bibcode:1992JAP....72.3072S (englisch, scitation.org [PDF]).
- ↑ Datenblatt Bis(cyclopentadienyl)titanium(IV) dichloride bei Sigma-Aldrich, abgerufen am 24. April 2011 (PDF).
- Feuergefährlicher Stoff
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 40
- Gruppe-4-Element
- Übergangsmetall
- Leichtmetall
- Periode-4-Element
- Chemisches Element
- Elemente (Mineralklasse)
- Hexagonales Kristallsystem
- Kubisches Kristallsystem
- Metallischer Werkstoff
- Anerkanntes Mineral
- Werkstoff der Halbleiterelektronik
- Titan






![{\displaystyle \mathrm {[Ti(O_{2})\cdot aq]^{2+}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9f3a434e4ce744367884114975e0ec855aaf26f1)
![{\displaystyle [\mathrm {Ti} (\mathrm {OH} )_{2}(\mathrm {H} _{2}\mathrm {O} )_{4}]^{2+}+\mathrm {H} _{2}\mathrm {O} _{2}\rightarrow \underbrace {[\mathrm {Ti} (\mathrm {O} _{2})\cdot \mathrm {aq} ]^{2+}} _{\mathrm {orange} }+6\,\mathrm {H} _{2}\mathrm {O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/a27e37c01e1ae6844bd86dd91a5849cf14f4f5a4)
