Kristallviolett
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Kristallviolett | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C25H30ClN3 | |||||||||||||||||||||
| Kurzbeschreibung |
grüner, geruchloser Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 407,99 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Dichte |
1,19 g·cm−3 (20 °C)[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
wenig in Wasser (10 g·l−1 bei 20 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Kristallviolett (nach dem botanischen Namen des Enzians auch Gentianaviolett beziehungsweise Enzianviolett genannt, nach dem Colour Index C.I. Basic Violet 3) ist ein violetter kationischer Triphenylmethanfarbstoff mit der Summenformel C25H30N3Cl. Der Name bezieht sich auf die Farbe, die den Blütenblättern bestimmter Enzianarten ähnelt, es wird jedoch nicht aus Enzian oder Veilchen gewonnen. In festem Zustand hat es einen goldgrünen, metallischen Glanz, in Wasser gelöst erscheint es dunkelviolett. Kristallviolett wurde erstmals 1883 hergestellt.
Es wird unter anderem für das Färben von Textilien, in Druckfarben, zur Herstellung von dokumentenechten Stiften, Stempel- und hektografischen Farben sowie das Färben von Papier verwendet. Als histologisches Färbemittel und in der Gram-Färbung wird es zur Klassifizierung von Bakterien verwendet.
Kristallviolett besitzt antibakterielle, antimykotische und anthelmintische, wurmtötende Eigenschaften und war früher als topisches Antiseptikum von Bedeutung. Die medizinische Verwendung des Farbstoffs wurde durch modernere Arzneimittel weitgehend verdrängt.
Geschichte[Bearbeiten | Quelltext bearbeiten]

Kristallviolett fiel zunächst als einer der Bestandteile von Methylviolett an, einem Farbstoff, der erstmals 1861 von Charles Lauth synthetisiert wurde.[3] Dabei handelte es sich um ein Gemisch aus tetra-, penta- und hexamethylierten Pararosanilinen.[4] Ab 1866 wurde Methylviolett von der Firma Poirrier et Chappat in Saint-Denis hergestellt und unter dem Namen „Violet de Paris“ vermarktet.
Reines Kristallviolett wurde erstmals 1883 von Alfred Kern synthetisiert, der in Basel bei der Firma Bindschedler & Busch arbeitete.[5] Um die schwierige Synthese mit Phosgen zu optimieren, arbeitete Kern mit dem deutschen Chemiker Heinrich Caro bei der BASF zusammen.[6] Kern entdeckte zudem, dass er den eng verwandten violetten Farbstoff, der heute als C.I. 42600 oder C.I. Basic Violet 4 bekannt ist, synthetisieren konnte, wenn er mit N,N-Diethylanilin statt mit N,N-Dimethylanilin begann.
Der Name „Enzianviolett“ wurde wahrscheinlich von dem deutschen Apotheker Georg Grübler eingeführt, der 1880 in Leipzig eine Firma gründete, die sich auf den Vertrieb von Färbereagenzien für die Histologie spezialisierte.[7] Die von Grübler vertriebene Enzianviolettfärbung enthielt wahrscheinlich eine Mischung aus methylierten Pararosanilinfarbstoffen.[8] Die Färbung erwies sich als populär und wurde 1884 von Hans Christian Gram zum Färben von Bakterien verwendet. Er schrieb die Anilin-Enzianviolett-Mischung Paul Ehrlich zu. Die selektive Anfärbung von Mikroorganismen in einem Wirtsorganismus mit verschiedenen Farbstoffen führte Paul Ehrlich zu der Annahme, dass es möglich sein müsste, Mikroorganismen abzutöten, ohne den Wirtsorganismus zu schädigen. Aus den Arbeiten mit Farbstoffen entwickelte Ehrlich die Begriffe „selektive Toxizität“ und „Chemotherapie“.[9] Grüblers Enzianviolett war wahrscheinlich sehr ähnlich, wenn nicht identisch, mit dem Methylviolett von Lauth, das 1875 von Victor André Cornil als Färbemittel verwendet wurde.
Obwohl der Name Enzianviolett weiterhin für histologische Färbungen verwendet wurde, fand er in der Farbstoff- und Textilindustrie keine Verwendung. Die Zusammensetzung des Farbstoffes war nicht definiert und verschiedene Lieferanten verwendeten unterschiedliche Mischungen. 1922 setzte die Biological Stain Commission ein Komitee unter dem Vorsitz von Harold Conn ein, um die Eignung der verschiedenen kommerziellen Produkte zu untersuchen.[10] In seinem Buch „Biological Stains“ beschreibt Conn Enzianviolett als „eine schlecht definierte Mischung violetter Rosaniline“.
Die Entdeckung der antiseptischen Eigenschaften von Enzianviolett wird dem deutschen Augenarzt Jakob Stilling zugeschrieben. Er veröffentlichte 1890 eine Monographie über die bakterizide Wirkung einer Lösung, die er „Pyoktanin“ nannte und bei der es sich wahrscheinlich um eine dem Enzianviolett ähnliche Mischung von Anilinfarbstoffen handelte.[11] Er ging eine Partnerschaft mit E. Merck & Co. ein, um „Pyoktanin caeruleum“ als Antiseptikum zu vermarkten.[12]
Carl Benda wies 1898 durch Färbung mit Kristallviolett Hunderte von Körnchen im Cytoplasma eukaryotischer Zellen nach und nannte sie Mitochondrien, von griechisch mitos, Faden, und khondrion, Körnchen.[13]
Im Jahr 1902 stellten Wilhelm von Drigalski und Heinrich Conradi fest, dass Kristallviolett zwar das Wachstum vieler Bakterien hemmt, jedoch nur eine geringe Wirkung auf Bacillus coli (Escherichia coli) und Bacillus typhi (Salmonella typhi), beides gramnegative Bakterien, hat.[14] Eine sehr viel detailliertere Studie über die Wirkung von Grüblers Enzianviolett auf verschiedene Bakterienstämme wurde 1912 von John Churchman veröffentlicht. Er stellte fest, dass die meisten grampositiven (angefärbten) Bakterien empfindlich auf den Farbstoff reagierten, während die meisten gramnegativen (nicht angefärbten) Bakterien unempfindlich waren, und beobachtete, dass der Farbstoff eher bakteriostatisch als bakterizid wirkt.[15]
In der ersten Hälfte des 20. Jahrhunderts wurde Kristallviolett zur Behandlung einer Vielzahl von Krankheiten eingesetzt, nach der Entdeckung und großtechnischen Herstellung von Sulfonamiden und Penicillin in den 1940er Jahren jedoch kaum noch verwendet. Die Forschung konzentrierte sich stattdessen auf die Entwicklung neuer Klassen von Antibiotika. Mit dem Auftreten von Antibiotikaresistenzen gewann jedoch die Anwendung von Kristallviolett in der Dermatologie und zur Bekämpfung von Sepsis wieder an Bedeutung.[16]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Kristallviolett wird durch Kondensation von Michlers Keton (4,4′-Bis-dimethylamino-benzophenon) (1) mit N,N-Dimethylanilin (2) in Gegenwart von Phosphorylchlorid erhalten. Dabei findet eine elektrophile Substitution am N,N-Dimethylanilin in para-Stellung durch den Kohlenstoff der Carbonylgruppe von Michlers Keton statt. Phosphorylchlorid dient als Elektronenpaarakzeptor für den Sauerstoff der Carbonylgruppe des Ketons. Das Kohlenstoffatom ist dadurch positiv geladen und damit in der Lage, den Aromaten elektrophil anzugreifen. Aus der entstehenden Carbinolbase (3) wird anschließend Wasser eliminiert.[6]

Michlers Keton lässt sich durch die Umsetzung von N,N-Dimethylanilin mit Phosgen unter Lewis-Katalyse beispielsweise mit Zinkchlorid darstellen. Mit einem Überschuss N,N-Dimethylanilin wird unter diesen Bedingungen direkt, ohne Isolierung von Michlers Keton, Kristallviolett gebildet.[17]
Eine weitere Darstellung erfolgt über die Reaktion von N,N-Dimethylanilin (1) mit Formaldehyd (2). Es entsteht zunächst die Michlers Base (3) die mit Blei(IV)-oxid zu dem Benzhydrol-Derivat (4) oxidiert wird. Dieses kondensiert mit N,N-Dimethylanilin zum Leuko-Kristallviolett (5). Durch die Oxidation mit einem Oxidationsmittel wie Mangandioxid in Gegenwart von Salzsäure entsteht Kristallviolett (6).[17]

Kristallviolett wird in Indien, China und in gewissem Umfang in den USA hergestellt. Die Produktionsmengen in China und Indien sind nicht bekannt, in den USA wurden 1986 und 1990 Produktionsmengen von Kristallviolett zwischen 227 und 454 Tonnen pro Jahr angegeben. Kristallviolett wird in der Europäischen Union nicht hergestellt, jedoch importierte die EU zwischen 210 und 230 Tonnen Kristallviolett im Jahr 2012.[18]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Physikalische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
- Kristallviolett als Feststoff und in wässriger Lösung
-
Kristallviolett-Nadeln mit gold-grünlichem, metallischem Glanz
-
Wässrige Lösung von Kristallviolett
Kristallviolett liegt meist in Form feiner, metallisch-gold glänzender Nadeln vor. Es löst sich in Wasser und anderen polaren Lösungsmitteln mit intensiv violetter Farbe mit einem Absorptionsmaximum bei 590 Nanometern.[19] Das Absorptionsspektrum zeigt neben den Absorptionsmaxima eine Schulterbande. Diese Besonderheit des Absorptionsspektrums wird durch die Existenz zweier in wässriger Lösung im Gleichgewicht vorliegenden Grundzustandsisomere erklärt, die planare und die pyramidale Form.[20]
Aus der Kristallstrukturanalyse geht hervor, dass Kristallviolett im festen Zustand eine propellerartige Struktur aufweist, bei der die aromatischen Ringe um 32 ° gegenüber der zentralen horizontalen Ebene gedreht sind.[21]
Das Kristallviolettkation wird als Resonanzhybrid betrachtet, bei dem die positive Ladung auf die drei Stickstoffatome sowie das zentrale Kohlenstoffatom delokalisiert ist. Der Einfachheit halber wird meist nur eine Grenzstruktur angegeben.[17]
Chemische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Bei Zugabe von starken Säuren zur wässrigen Lösung durchläuft Kristallviolett eine Reihe von Farbumwandlungen. Dieses halochrome Verhalten erlaubt seinen Einsatz als pH-Indikator bei der wasserfreien Gehaltsbestimmung von schwachen Basen. Wird eine Lösung von Kristallviolett leicht angesäuert, erfolgt ein Farbumschlag von Violett nach Grün, weil das Auxochrom des dritten Kernes seine elektronenliefernde Fähigkeit und damit seine Farbrelevanz durch Addition eines Protons verliert. Ein stärkeres Ansäuern führt zu einer gelben Verbindung, bei der ein weiteres Auxochrom durch Protonierung deaktiviert wird. Die verschiedenen Farben ergeben sich aus den unterschiedlichen Ladungszuständen des Farbstoffmoleküls.[22]
In der gelben Form tragen alle drei Stickstoffatome eine positive Ladung, von denen zwei protoniert sind, während die grüne Farbe einer Form des Farbstoffs entspricht, in der zwei der Stickstoffatome positiv geladen sind. Bei neutralem pH-Wert gehen die beiden zusätzlichen Protonen an die Lösung verloren, so dass nur noch eines der Stickstoffatome positiv geladen ist. Die pKa für den Verlust der beiden Protonen betragen etwa 1,15 und 1,8.[19]
Bei Zugabe von Natronlauge zu einer stark verdünnten Kristallviolettlösung entfärbt sich die Lösung langsam. Hierbei lagert sich ein Hydroxidion an das in einer mesomeren Grenzform im Zentrum des Moleküls gebildete Carbeniumion, die sogenannte Pseudobase des Kristallvioletts, Kristallviolettcarbinol. Diese Reaktion lässt sich reaktionskinetisch mit einem Photometer untersuchen. Wenn die Konzentration des Kristallvioletts viel kleiner ist als die Konzentration der Natronlauge läuft die Reaktion pseudo-erster Ordnung ab.[23]

Bei der Färbermethode nach Gram werden Bakterien mit Kristallviolett angefärbt und anschließend mit Iod-Kaliumiodid-Lösung versetzt, wodurch ein Iod-Kaliumiodid-Farbstoff-Charge-Transfer-Komplex entsteht.[24] Durch die Umsetzung von Natriumtetraphenylborat mit Kristallviolett in Methanol bei Raumtemperatur entsteht unter Salzmetathese Kristallvioletttetraphenylborat, eine kristalline, grün-violette Substanz mit einem Schmelzbereich von 196 bis 198 °C.[25] Durch die Fällung von Kristallviolett mit Molybdatophosphorsäure wird das Druckfarbenpigment C.I. Pigment Violet 39 erhalten.[26]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Kristallviolett färbt Naturfasern leuchtend violett, ist jedoch verhältnismäßig leicht auswaschbar. Bei Triphenylmethanfarbstoffe wie Kristallviolett entfielen im Jahr 2001 weltweit 55 bis 60 % der Nachfrage auf Druckfarben, etwa 20 % auf Beschichtungen, etwa 15 % auf Kunststoffe und der Rest auf Branchen wie die Textilindustrie.[17] Kristallviolett findet Verwendung als Farbstoff in Farbbändern, Lacken, Druckfarben und in Kopierstiften. Weiterhin wird es beim Plaque-Assay eingesetzt. Es wird als Purpurfarbstoff für Textilien wie Baumwolle, Seide und Nylon verwendet. Kristallviolett wird unter anderem zum Färben von mit Polyacrylnitril modifiziertem Nylon und Wolle sowie zum Färben von Kunststoffen, Fetten, Ölen und Wachsen verwendet.[27]
Farbloses Kristallviolettcarbinol setzt bei Bestrahlung mit ionisierender und Ultraviolettstrahlung das farbige Kristallviolettkation frei. Es kann daher in Filmen zur Messung der Strahlendosis verwendet werden, da die optische Dichte des bestrahlten Films proportional zur absorbierten Strahlung ist.[28]
Kristallviolett eignet sich zur elektrolytischen Einfärbung von anodisierten Oberflächen aus eloxiertem Aluminium oder Aluminiumlegierungen. Aufgrund seiner positiven Ladung lagert sich das Kristallviolettkation dabei während der negativen Halbwelle des Wechselstroms in den Porenöffnungen der Oberflächenoxidschicht ab.[29]
Matrizendruck[Bearbeiten | Quelltext bearbeiten]

Aufgrund seiner hohen Farbstärke eignete sich Kristallviolett für den Einsatz im Matrizendruck oder Ormigverfahren, einem bis Ende der 1970er Jahre verbreiteten Vervielfältigungsverfahren für Dokumente. Dazu wurde Kristallviolett in einem Wachs auf die Rückseite eines Schreibmaschinen-Kopierblattes, der sogenannten Matrize, aufgetragen. Die beschriftete Matrize wurde auf eine Trommel gespannt und das leicht mit Alkohol befeuchtete zu bedruckende Papier löste daraus winzige Farbwachspartikel ab und nahm diese auf. Mit dem alkoholbenetzten Papier konnten mehr als 200 gute Kopien der Vorlage hergestellt werden.[30]
Spurensicherung[Bearbeiten | Quelltext bearbeiten]
Mit einem Spurensicherungspulver, zum Beispiel auf der Basis von Zinkcarbonat/Zinkhydroxid-Monohydrat oder Molybdänsulfid und Kristallviolett, können Fingerabdrücke auf nicht-porösen Gegenständen selbst nach dem Eintauchen in Wasser nachgewiesen werden. Die Anwendung erfolgt als Mischung aus Ethanol, Wasser, Phenol und Kristallviolett.[31] Beim Cyanacrylat-Verfahren, bei dem farblose Cyanacrylatdämpfe auf einem in den Dampfraum eingebrachten Gegenstand mit der Restfeuchte einer daktyloskopischen Spur polymerisieren, wird das entstehende Polymer zur Kontrastverstärkung mit Kristallviolett eingefärbt. Die Spurensicherung erfolgt fotografisch.[32]
Gelelektrophorese[Bearbeiten | Quelltext bearbeiten]
Gelgestützte DNA-Sequenzierungsverfahren basieren auf der Erzeugung von Populationen basenspezifisch terminierter DNA, die in einer anschließenden denaturierenden Polyacrylamid-Gelelektrophorese nach Größe aufgetrennt werden. Häufig verwendete Fluoreszenzreagenzien wie Ethidiumbromid erfordern eine UV-Bestrahlung zur Erzeugung einer Fluoreszenzbande im Agarosegel. Wird Kristallviolett als Alternative zu Fluoreszenzfarbstoffen verwendet, ist keine UV-Beleuchtung erforderlich und die UV-induzierte DNA-Zerstörung bei der in vitro-DNA-Klonierung wird vermieden. Die Empfindlichkeit kann durch die Verwendung einer Methylorange-Gegenfärbung und einer komplexeren Färbemethode weiter verbessert werden.[33]
Histologische Färbung[Bearbeiten | Quelltext bearbeiten]
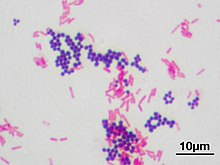
Die Gram-Färbung ist eine Färbemethode zur Einteilung der Bakterienarten in zwei Gruppen, die grampositiven und die gramnegativen Bakterien. Im ersten Schritt wird dazu ein dünner Ausstrich einer Bakterienkultur zum Beispiel durch Hitze auf einem Objektträger fixiert. Im zweiten Schritt wird Kristallviolett in wässriger Lösung aufgetragen, wobei die Ionen die Zellwand und die Membran sowohl grampositiver als auch gramnegativer Bakterienzellen durchdringen. Grampositive Bakterien besitzen eine dicke Peptidoglycanschicht in der Zellwand, während gramnegative Bakterien eine dünnere Schicht haben. Im dritten Schritt bilden sich durch Zugabe von Iod im Cytoplasma und in den äußeren Zellschichten dunkelblaue Farbstoff-Charge-Transfer-Komplexe.[34] In einem weiteren Schritt werden durch Zugabe von dehydratisierend wirkendem Ethanol oder Aceton der Abstand zwischen den Peptidoglycanen verringert, so dass die Kristallviolett-Komplexe bei grampositiven Bakterien nicht von Ethanol oder Aceton ausgewaschen werden können und die dunkelblaue Färbung erhalten bleibt. Bei gramnegativen Bakterien wird dagegen der Farbstoffkomplex ausgewaschen. Im letzten Schritt werden die gramnegativen Bakterien mit Safranin T rosa gegengefärbt.[35]
Bei der Färbung nach Neisser handelt es sich um einen Test auf das Vorhandensein von in den Zellen gespeicherten Polyphosphaten mit einer Mischung aus Kristallviolett, Methylenblau und Chrysoidin-Y. Zudem können damit die für die biologische Phosphorelimination verantwortlichen Bakterien sichtbar gemacht werden.[36]
Bei oralen epithelialen Dysplasien und oralen Plattenepithelkarzinomen ist die Mitosezahl, das heißt die Anzahl der Mitosen pro 2 Quadratmillimeter, im Vergleich zur normalen Mundschleimhaut signifikant erhöht. Die Kristallviolettfärbung eignet sich als selektive Färbung für die Bestimmung der Mitosezahl besser als eine Hämatoxylin-Eosin-Färbung, wobei mit Kristallviolett die Metaphase die dabei am häufigsten beobachtete Phase der Mitose ist.[37]
Medizinische Verwendung[Bearbeiten | Quelltext bearbeiten]

Medizinisch wurde Kristallviolett lange Zeit, bis zur Entdeckung anderer wirksamer Antimykotika, zur Behandlung von Hautpilzerkrankungen (Mykosen), insbesondere Fußpilzen, sowie von Mundsoor und Mundwinkelentzündung verwendet.[38] Dazu wird es als Pyoktaninlösung (0,5–2 %) aufgepinselt. In der westlichen Welt wird es heute wegen der Einfärbung der Haut fast nur noch in der Naturheilkunde verwendet. In der pädiatrischen Dermatologie findet es noch Anwendung bei Herden des atopischen Ekzems, wenn dieses durch grampositive Bakterien oder Dermatophyten ausgelöst wird. Bei HIV-positiven Kindern und Heranwachsenden können Pilze der Gattung Candida orale Candidose verursachen und innere Organe befallen und schwere Erkrankungen auslösen. Kristallviolett war in mehreren Studien Nystatin, ein Polyen-Makrolacton, das als Antimykotikum zur Behandlung von Pilzinfektionen eingesetzt wird, in der klinischen Heilung überlegen.[39] Als diagnostischer Test bei Pityriasis versicolor wird Kristallviolett auf den infizierten Bereich aufgetragen, wodurch die infizierten Bereiche im Vergleich zur nicht infizierten Haut hervorgehoben werden. Mit diesem Test kann Pityriasis versicolor von anderen Erkrankungen wie atopisches Ekzem, Vitiligo und Röschenflechte unterschieden werden.[40]
Intravenös wird es eingesetzt zur Therapie von sekundären Lungenmykosen. Die fungistatische Wirkung von Kristallviolett ist, je nach Mykosenart, um den Faktor 10 bis 100 stärker als die des stark verbreiteten Clotrimazol. Übertroffen wird es von Amphotericin B, das jedoch im Vergleich stark toxisch ist. Daher wird Kristallviolett häufig bei immungeschwächten Patienten eingesetzt.
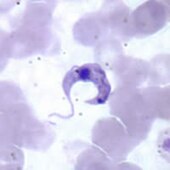
Im Jahr 1953 entdeckten Ruth und Victor Nussenzweig, dass Kristallviolett den einzelligen Parasiten Trypanosoma cruzi in Blutkonserven abtötet. Trypanosoma cruzi, der Erreger der Chagas-Krankheit, wird von blutsaugenden Raubwanzen übertragen. Daher wird Kristallviolett in Blutbanken in endemischen Gebieten verwendet, um den Parasiten aus dem Blut zu entfernen, das für Bluttransfusionen verwendet wird.[41]
Kristallviolett wurde zur Behandlung von Fadenwürmern wie dem Zwergfadenwurm verwendet, der sich im Darm des Menschen ansiedelt.[42] Es wurde ebenfalls zur Behandlung von Madenwürmern bei Kindern eingesetzt, selbst bei schwerem Befall.[43]
Nach Empfehlungen der WHO war Kristallviolett bis ins Jahr 2011 als essenzielles Medikament einzustufen.[44] Kristallviolett ist in Europa frei verkäuflich und auch die FDA, die US-Behörde für Lebens- und Arzneimittel, erlaubt den rezeptfreien Verkauf von Kristallviolett.[16]
Tiermedizinische Verwendung[Bearbeiten | Quelltext bearbeiten]
In den 1930er Jahren wurde ein Schweinepest-Impfstoff aus dem von Fibrinogen befreitem Blut von mit Schweinepest infizierten Tieren und Kristallviolett hergestellt. Obwohl die Sicherheit und Wirksamkeit dieses Impfstoffs gering war, wurde er bis in die 1970er Jahre benutzt.[45][46]
Kristallviolett wird als Fungizid und als Bakterizid gegen grampositive Bakterien in Futtermitteln für Geflügel eingesetzt. Es hemmt die Aktivität und Infektiosität verschiedener Virusstämme, einschließlich der Newcastle-Krankheit und des Geflügelpestvirus. Bei Konzentrationen im Bereich von 0,05 bis 0,1 % im Endfutter konnte es nicht im Geflügelfleisch nachgewiesen werden. In hohen Konzentrationen von 2,5 bis 5,0 Gramm pro Kilogramm Körpergewicht wirkt Kristallviolett auf Geflügel toxisch.[47]
Kristallviolett ist für die Verwendung in der Aquakultur für die Zucht von Fischen, Muscheln, Krebsen und Algen in vielen Ländern nicht zugelassen. Für die Behandlung von Zierfischen ist es jedoch erhältlich.[48] Die Behandlung von für den menschlichen Verzehr bestimmten Tieren mit Kristallviolett ist aufgrund seiner toxikologischen Eigenschaften weltweit verboten.[49]
Toxikologie[Bearbeiten | Quelltext bearbeiten]
Kristallviolett darf nicht ins Auge gelangen, da es dort schwere Schäden verursachen kann.[50] Ferner ist bei äußerlicher Anwendung eine Überdosierung zu vermeiden, da Kristallviolett, ebenso wie die verwandten und ähnlich verwendeten Triphenylmethanfarbstoffe Malachitgrün und Brilliantgrün, zelltoxisch auf die Haut wirkt.
Im Anhang IV der Verordnung (EG) Nr. 1272/2008 (CLP) wurde Kristallviolett mit der Einstufung Carc. 2-H351, „kann vermutlich Krebs erzeugen“, aufgenommen. Liegt Michlers Keton in Konzentrationen größer als 0,1 % vor, ändert sich die Einstufung zu Carc. 1B-H350, „kann Krebs erzeugen“.[49] Seit November 2020 ist Kristallviolett in der Europäischen Union wegen seines krebserregenden Potentials über REACH Anhang XVII auf eine Konzentration von 50 mg/kg in einem homogenen Material begrenzt.[51] Kristallviolett erfüllt nur dann die Kriterien des REACH-Artikels 57 (a), wenn es Michlers Keton oder Michlers Base in einer Konzentration von größer oder gleich 0,1 % enthält. Reines Kristallviolett selbst gilt nicht als besonders besorgniserregender Stoff.[52]
Im Juni 2019 warnte die kanadische Gesundheitsbehörde Health Canada vor einer möglichen Krebsgefährdung durch Kristallviolett und empfahl, Anwendungen in der Tiermedizin zu stoppen.[53] Über den Safe Drinking Water and Toxic Enforcement Act of 1986 besteht in Kalifornien seit 23. November 2018 eine Kennzeichnungspflicht, wenn Kristallviolett in einem Produkt enthalten ist.[54]
Umweltrelevanz[Bearbeiten | Quelltext bearbeiten]
Während der Herstellung und Verarbeitung gehen etwa 12 % der synthetischen Farbstoffe verloren. Wasser wird in jeder Phase der Textilverarbeitung verwendet, beispielsweise bei der Nassveredelung, beim Übertragen von Chemikalien auf Textilien und beim Waschen. Dies hat zur Folge, dass große Mengen gefärbten Abwassers anfallen. Wenn Kristallviolett ungeklärt in aquatischen Ökosysteme gelangt, beeinträchtigt es die photosynthetische Aktivität der Wasserpflanzen, was zu einer Verringerung des Gehalts an gelöstem Sauerstoff führt und somit letztlich den normalen Lebensprozess der Wasserflora und -fauna stört.[27] Für die Entfernung von Kristallviolett aus Abwasser wurden daher verschiedene physikalische, chemische und biologische Methoden vorgeschlagen. Zu den physikalischen Methoden zählen die Adsorption an modifizierten Chitosanen, Lignin und Nanocellulose.[55][56][57]
Als chemische Behandlungsmethoden wurden Systeme auf Basis der Fenton-Reaktion getestet.[58] Daneben wurden photochemische Methoden sowie die Ozonierung eingesetzt.[27] Kristallviolett wurde mit Hilfe eines Systems von manganoxidierenden Bakterien aus Bacillus sp. und Sphingobacterium sp. vollständig entfärbt.[59] Neben Bakterien wurden Abbaumechanismen über Hefen und Pilze getestet.[27]
Literatur[Bearbeiten | Quelltext bearbeiten]
- S. Mani, R.N. Bharagava: Exposure to Crystal Violet, Its Toxic, Genotoxic and Carcinogenic Effects on Environment and Its Degradation and Detoxification for Environmental Safety. In: P. de Voogt (Hrsg.): Reviews of Environmental Contamination and Toxicology. Springer International Publishing, Schweiz, 2016, Bd. 237, doi:10.1007/978-3-319-23573-8_4.
- Dean Thetford: Triphenylmethane and related Dyes. In: Kirk-Othmer Encyclopedia of Chemical Technology, Wiley, 2001, doi:10.1002/0471238961.2018091620080520.a01.pub2, S. 1–21.
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Eintrag zu Kristallviolett in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Eintrag zu [4-[4,4′-bis(dimethylamino)benzhydrylidene]cyclohexa-2,5-dien-1-ylidene]dimethylammonium chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ C. Lauth: On the new aniline dye, Violet de Paris. In: Laboratory. 1, 1867, S. 138–139.
- ↑ W. M. Gardner: The British coal-tar industry: its origin, development, and decline. Lippincott, Philadelphia, (Online).
- ↑ Patent US290856A: Manufacture of dye-stuff. Veröffentlicht am 25. Dezember 1883, Erfinder: H. Caro, A. Kern.
- ↑ a b C. Reinhardt, A. S. Travis: Heinrich Caro and the creation of modern chemical industry. Kluwer Academic, Dordrecht, 2000, ISBN 0-7923-6602-6,s.&nbp;208–209.
- ↑ M. Titford: George Grubler and Karl Hollborn: Two Founders of the Biological Stain Industry. In: Journal of Histotechnology. 16.2, 1993, S. 155–158, doi:10.1179/his.1993.16.2.155.
- ↑ M. Titford: Comparison of historic Grübler dyes with modern counterparts using thin layer chromatography. In: Biotechnic and Histochemistry. 82.4–5, 2007, S. 227–234, doi:10.1080/10520290701714005.
- ↑ Ernst Mutschler: Arzneimittel – Erfolge, Mißerfolge, Hoffnungen. In: Reimar Lüst u. a. (Hrsg.): Beobachtung, Experiment und Theorie in Naturwissenschaft und Medizin. Wissenschaftliche Verlagsgesellschaft, Stuttgart, 1987, ISBN 3-8047-0912-5, S. 287–307.
- ↑ H. J. Conn: An Investigation of American Gentian Violets Report of Committee on Bacteriological Technic. In: Journal of Bacteriology. 7.5, 1922, S. 529–536, doi:10.1128/jb.7.5.529-536.1922.
- ↑ J. Stilling: Anilin Farbstoffe als Antiseptica und ihre Anwendung in der Praxis. 1890.
- ↑ R. L. Berrios, J. L. Arbiser: Novel antiangiogenic agents in dermatology. In: Archives of Biochemistry and Biophysics. 508.2, 2011, S. 222–226, doi:10.1016/j.abb.2010.12.016.
- ↑ Paulo N. Correa, Alexandra N. Correa: Wilhelm Reich's Claim of the Heterogenesis of Eukaryotic Amoebae. In: Journal of Biophysics, Hematology and Oncology. 1.1, 2010, S. 1–17, (online).
- ↑ W. von Drigalski, H. Conradi: Ueber ein Verfahren zum Nachweis der Typhusbacillen. In: Zeitschrift für Hygiene und Infektionskrankheiten. 39.1, 1902, S. 283–300, doi:10.1007/bf02140310.
- ↑ J. W. Churchman: The selective bactericidal action of Gentian Violett. In: Journal of Experimental Medicine. 16.2, 1912, S. 221–247, doi:10.1084/jem.16.2.221.
- ↑ a b A. M. Maley, J. L. Arbiser: Gentian Violet: a 19th century drug re‐emerges in the 21st century. In: Experimental Dermatology. 22.12, 2013, S. 775–780, doi:10.1111/exd.12257.
- ↑ a b c d Dean Thetford: Triphenylmethane and related Dyes. In: Kirk-Othmer Encyclopedia of Chemical Technology. 1. Auflage. Wiley, 2001, S. 1–21, doi:10.1002/0471238961.2018091620080520.a01.pub2.
- ↑ IARC Working Group on the Identification of Carcinogenic Hazards to Humans: Gentian Violet, Leucogentian Violet, Malachite Green, Leucomalachite Green, and CI Direct Blue 218. IARC Monographs on the Identification of Carcinogenic Hazards to Humans, No. 129, 2022, ISBN 978-92-832-0169-4 (online).
- ↑ a b E. Q. Adams, Ludwig Rosenstein: The Color and Ionization of Crystal Violet. In: Journal of the American Chemical Society. 36.7, 1914, S. 1452–1473, doi:10.1021/ja02184a014.
- ↑ G. N. Lewis, T. T. Magel, D. Lipkin: Isomers of Crystal Violet Ion. Their Absorption and Re-emission of Light. In: Journal of the American Chemical Society. 64.8, 1942, S. 1774–1782, doi:10.1021/ja01260a009.
- ↑ P. Sharma, N. Sohal, B. Maity: Encapsulation and release of non-fluorescent crystal violet confined in bile-salt aggregates. In: RSC Advances. 11.18, 2021, S. 10912–10921, doi:10.1039/d0ra06599d.
- ↑ Ralf Martens-Menzel, Lena Harwardt, Hanns-Jürgen Krauss (Hrsg.): Gerhart Jander, Karl-Friedrich Jahr: Maßanalyse. De Gruyter, Berlin, Boston, 2022, ISBN 978-3-11-071074-8, S. 120–122.
- ↑ L. Dayo Felix: Kinetic Study of the Discoloration of Crystal Violet Dye in Sodium Hydroxide Medium. In: Journal of Chemistry and Applied Chemical Engineering. 02.01, 2018, doi:10.4172/2576-3954.1000115.
- ↑ G. J. Hucker, H. J. Conn: Methods of Gram Staining. New York Agricultural Experiment Station. Technical Bulletin No. 93. The Station, Geneva, N.Y., 1923. (online).
- ↑ B. D. Spangler, P. Vanysek, I. C. Hernandez, R. D. Rogers: Structure of crystal violet tetraphenylborate. In: Journal of Crystallographic and Spectroscopic Research. 19.3, 1989, S. 589–596, doi:10.1007/bf01185394.
- ↑ Pigment Violet 39. In: dyestuffintermediates.com. Abgerufen am 23. April 2024.
- ↑ a b c d S. Mani, R.N. Bharagava: Exposure to Crystal Violet, Its Toxic, Genotoxic and Carcinogenic Effects on Environment and Its Degradation and Detoxification for Environmental Safety. In: P. de Voogt (Hrsg.): Reviews of Environmental Contamination and Toxicology. Band 237, Springer International Publishing, Schweiz, 2016, doi:10.1007/978-3-319-23573-8_4.
- ↑ Patent US3609093A: Photochromic radiation dosimeter. Veröffentlicht am 28. September 1971, Erfinder: Larry A Harrah.
- ↑ Patent US4877495: Electrolytic Coloring of anodized Aluminum. Veröffentlicht am 31. Oktober 1989, Erfinder: Willi Buchmeier, Dieter Brodalia.
- ↑ James A. Kent: Riegel’s Handbook of Industrial Chemistry. Van Nostrand Reinhold, New York, Cincinnati, Toronto, London, Melbourne, 1974, ISBN 0-442-24347-2, S. 671.
- ↑ R. Rohatgi, G. S. Sodhi, A. K. Kapoor: Small particle reagent based on crystal violet dye for developing latent fingerprints on non-porous wet surfaces. In: Egyptian Journal of Forensic Sciences. 5.4, 2015, S. 162–165, doi:10.1016/j.ejfs.2014.08.005.
- ↑ Ingo Wirth (Hrsg.): Kriminalistik-Lexikon. Hüthig Jehle Rehm, 2011, Heidelberg, München, Landsberg, Frechen, Hamburg, ISBN 978-3-7832-0804-7, S. 245–246.
- ↑ Y. I. Yang U. a.: Counterion-dye staining method for DNA in agarose gels using crystal violet and methyl orange. In: Electrophoresis. 22.5, 2001, S. 855–859, PMID 11332752.
- ↑ A. A. Paray, M. Singh, M. Mir: Gram Staining: A Brief Review. In: International Journal of Research and Review. 10.9, 2023, S. 336–341, doi:10.52403/ijrr.20230934.
- ↑ Nishant Tripathi, Amit Sapra: Gram staining. In: StatPearls [Internet]. Treasure Island, StatPearls Publishing, 2024, PMID 32965827, (online).
- ↑ Dick H. Eikelboom: Process Control of Activated Sludge Plants by Microscopic Investigation. IWA Publishing, 2000, ISBN 978-1-900222-29-7, S. 15–18.
- ↑ K. Jadhav, B. Ahmed Mujib, N. Gupta: Crystal violet stain as a selective stain for the assessment of mitotic figures in oral epithelial dysplasia and oral squamous cell carcinoma. In: Indian Journal of Pathology and Microbiology. 55.3, 2012, S. 283–287, doi:10.4103/0377-4929.101731.
- ↑ Gentian Violet (Topical Route) Proper Use - Mayo Clinic. In: mayoclinic.org. 1. Februar 2024, abgerufen am 10. April 2024 (englisch).
- ↑ E. D. Pienaar, T. Young, H. Holmes: Interventions for the prevention and management of oropharyngeal candidiasis associated with HIV infection in adults and children. In: Cochrane Database of Systematic Reviews. 3, 2006, doi:10.1002/14651858.CD003940.pub2.
- ↑ N. Prabha, R. Arora, S. Ganguly, N. Chhabra: Gentian violet: Revisited. In: Indian Journal of Dermatology, Venereology and Leprology. 86.5, 2020, S. 600–603, doi:10.4103/ijdvl.ijdvl_579_19.
- ↑ D. Steverding: The history of Chagas disease. In: Parasites and Vectors. 7.1, 2014, S. 317, doi:10.1186/1756-3305-7-317.
- ↑ S. Denman, S. Jameel, J. Hay, J. K. Sugden: Photostability of Crystal Violet (CI 42555). In: Dyes and Pigments. 30.1, 1996, S. 67–72, doi:10.1016/0143-7208(95)00067-4.
- ↑ Rodney C. Jung, Paul C. Beaver: Treatment of enterobiasis (pinworm infestation) with diphenanR, egressinR and gentian violet. In: Pediatrics. 11.6, 1953, S. 611–616, PMID 13073294.
- ↑ WHO Model Lists of Essential Medicines, März 2010, Rubrik 13.2 (Anti-infective medicines) (englisch: PDF; 424 kB)
- ↑ S. Blome, C. Moß, I. Reimann, P. König, M. Beer: Classical swine fever vaccines—State-of-the-art. In: Veterinary Microbiology. 206, 2017, S. 10–20, doi:10.1016/j.vetmic.2017.01.001.
- ↑ A. J. de Smit: Laboratory diagnosis, epizootiology, and efficacy of marker vaccines in classical swine fever: A review. In: Veterinary Quarterly. 22.4, 2000, S. 182–188, doi:10.1080/01652176.2000.9695054.
- ↑ A. Kamyab, E. Mcgill, J. D. Firman: The use of hexamethyl-p-rosaniline chloride as an ingredient in poultry feed. In: World’s Poultry Science Journal. 65.3, 2009, S. 475–480, doi:10.1017/s0043933909000336.
- ↑ Center for Food Safety, Applied Nutrition: Laboratory Information Bulletin (LIB) 4395: Analyses of Crystal Violet & Brilliant Green | FDA. In: fda.gov. 21. September 2018, abgerufen am 10. April 2024 (englisch).
- ↑ a b BfR-Kommission für pharmakologisch wirksame Stoffe und Tierarzneimittel: Toxikologische Einschätzung von Kristallviolett. In: Empfehlung des Bundesinstituts für Risikobewertung. 16. Mai 2019, abgerufen am 11. April 2024.
- ↑ B. Ballantyne, M. F. Gazzard, D. W. Swanston: Proceedings: Eye damage caused by crystal violet. In: British Journal of Pharmacology. 49.1, 1973, S. 181P–182P, PMID 4787555.
- ↑ Verordnung (EU) 2018/1513 (PDF)
- ↑ Liste der für eine Zulassung in Frage kommenden besonders besorgniserregenden Stoffe - ECHA. In: echa.europa.eu. Abgerufen am 23. April 2024.
- ↑ Health Canada warns Canadians of potential cancer risk associated with gentian violet - Canada.ca. In: recalls-rappels.canada.ca. 12. Juni 2019, abgerufen am 2. April 2024 (englisch).
- ↑ Gentian Violet. OEHHA, 23. November 2018, abgerufen am 1. Juni 2022 (englisch).
- ↑ Asitha T. Cooray, Kavindya Weerasinghe, Samantha Ranaweera: Applications of Chitosan-and Chitin-Based Biomaterials in Cationic Dye Removal. In: Subramanian Senthilkannan Muthu, Ali Khadir (Hrsg.): Textile Wastewater Treatment. Sustainable Bio-nano Materials and Macromolecules. Band 1, Springer Nature, Singapore, 2022, ISBN 978-981-19-2831-4, S. 36.
- ↑ Md. Din Islam, M. K. Mohammad Ziaul Hyder, Md. Masudur Rhaman, Sajjad Husain Mir: Application of Lignin-Based Biomaterials in Textile Wastewater. In: Subramanian Senthilkannan Muthu, Ali Khadir (Hrsg.): Textile Wastewater Treatment. Sustainable Bio-nano Materials and Macromolecules. Band 1, Springer Nature, Singapore, 2022, ISBN 978-981-19-2831-4, S, 82–87.
- ↑ Swarnalatha Venkatanarasimhan, D. Gangadharan, Thilagavathy Palanisamy: Cellulose Nanocrystal as a New Promising Candidate in Textile Wastewater Treatment. In: Subramanian Senthilkannan Muthu, Ali Khadir (Hrsg.): Textile Wastewater Treatment. Sustainable Bio-nano Materials and Macromolecules. Band 1, Springer Nature, Singapore, 2022, ISBN 978-981-19-2831-4, S, 125.
- ↑ F. Rehman u. a.: Degradation of Crystal Violet Dye by Fenton and Photo-Fenton Oxidation Processes. In: Zeitschrift für Physikalische Chemie. 232.12, 2018, S. 1771–1786, doi:10.1515/zpch-2017-1099.
- ↑ D. Bharathi u. a.: Microbial approaches for sustainable remediation of dye-contaminated wastewater: a review. In: Archives of Microbiology. 204.3, 2022, S. 1–11, doi:10.1007/s00203-022-02767-3.
- Gesundheitsschädlicher Stoff bei Verschlucken
- Ätzender Stoff
- Stoff mit Verdacht auf krebserzeugende Wirkung
- Umweltgefährlicher Stoff (chronisch wassergefährdend)
- Diphenylethen
- Iminocyclohexadien
- Dimethylaminobenzol
- Quartäre Ammoniumverbindung
- Chlorid
- Antimykotikum
- Triphenylmethanfarbstoff
- Beschränkter Stoff nach REACH-Anhang XVII
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 72






