„Superkondensator“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
doi aktiviert |
Korrektur diverser Quellenangaben; dabei auch redundante Informationen entfernt |
||
| Zeile 32: | Zeile 32: | ||
=== Entwicklung elektrochemischer Kondensatoren === |
=== Entwicklung elektrochemischer Kondensatoren === |
||
[[Datei:Bockris Group At Imperical College, London 1947.png|mini|Brian Evans Conway in der John Bockris Gruppe am [[Imperial College]], London 1947]] |
[[Datei:Bockris Group At Imperical College, London 1947.png|mini|Brian Evans Conway in der John Bockris Gruppe am [[Imperial College]], London 1947]] |
||
In den frühen 1950er Jahren experimentierten Ingenieure bei [[General Electric]] (GE) mit Geräten für [[Brennstoffzelle]]n und neuartigen [[Akkumulator]]en, die mit hoch-porösen Kohlenstoffelektroden versehen waren. Aktivkohle ist einerseits ein elektrischer Leiter, besitzt andererseits aber auch mit seiner schwammartigen Struktur eine äußerst große Oberfläche und ist deswegen ideal für Elektroden aller Art verwendbar. Mit solchen Elektroden entwickelte H. I. Becker bei GE in Unkenntnis des wirklichen kapazitiven Prinzips einen „Niederspannungs-Elektrolytkondensator mit porösen Kohlenstoffelektroden“, der 1957 patentiert wurde<ref>{{Patent|Erfinder=H. I. Becker|Titel=Low voltage electrolytic capacitor|Land=US|V-Nr=2800616|V-Datum=1957-07-23}}</ref>. Becker glaubte, dass die elektrische Ladung seines neuen hochkapazitiven Kondensators in den Poren des Kohlenstoffs gespeichert wird, ähnlich wie in den Poren aufgerauter Aluminium-Anodenfolien von [[Elektrolytkondensator]]en. In dem Patent wurde daher sinngemäß zum Speicherprinzip geschrieben: „Es ist nicht genau bekannt, was im Bauelement stattfindet, wenn es als Energiespeicher benutzt wird, aber es führt zu einer außerordentlich hohen Kapazität.“<ref name="Boggs">J. Ho, T. R. Jow, S. Boggs: [http://www.ifre.re.kr/board/filedown.php?seq=179 ''Historical Introduction to Capacitor Technology''.] (PDF) (abgerufen am 5. Januar 2014)</ref><ref>[http://www.cantecsystems.com/ccrdocs/brief-history-of-supercapacitors.pdf ''A brief history of supercapacitors''.] (PDF; 1,5 MB) AUTUMN 2007 |
In den frühen 1950er Jahren experimentierten Ingenieure bei [[General Electric]] (GE) mit Geräten für [[Brennstoffzelle]]n und neuartigen [[Akkumulator]]en, die mit hoch-porösen Kohlenstoffelektroden versehen waren. Aktivkohle ist einerseits ein elektrischer Leiter, besitzt andererseits aber auch mit seiner schwammartigen Struktur eine äußerst große Oberfläche und ist deswegen ideal für Elektroden aller Art verwendbar. Mit solchen Elektroden entwickelte H. I. Becker bei GE in Unkenntnis des wirklichen kapazitiven Prinzips einen „Niederspannungs-Elektrolytkondensator mit porösen Kohlenstoffelektroden“, der 1957 patentiert wurde<ref>{{Patent|Erfinder=H. I. Becker|Titel=Low voltage electrolytic capacitor|Land=US|V-Nr=2800616|V-Datum=1957-07-23}}</ref>. Becker glaubte, dass die elektrische Ladung seines neuen hochkapazitiven Kondensators in den Poren des Kohlenstoffs gespeichert wird, ähnlich wie in den Poren aufgerauter Aluminium-Anodenfolien von [[Elektrolytkondensator]]en. In dem Patent wurde daher sinngemäß zum Speicherprinzip geschrieben: „Es ist nicht genau bekannt, was im Bauelement stattfindet, wenn es als Energiespeicher benutzt wird, aber es führt zu einer außerordentlich hohen Kapazität.“<ref name="Boggs">J. Ho, T. R. Jow, S. Boggs: [http://www.ifre.re.kr/board/filedown.php?seq=179 ''Historical Introduction to Capacitor Technology''.] (PDF) (abgerufen am 5. Januar 2014)</ref><ref>[http://www.cantecsystems.com/ccrdocs/brief-history-of-supercapacitors.pdf ''A brief history of supercapacitors''.] (PDF; 1,5 MB) AUTUMN 2007 – Batteries & Energy Storage Technology, abgerufen am 5. Januar 2014.</ref> |
||
Auch in dem neun Jahre später eingereichten Patent von 1966, eines „Energiespeicher-Apparates“ von R. A. Rightmire<ref>{{Patent|Erfinder=R. A. Rightmire|Titel=Electrical energy storage apparatus|Land=US|V-Nr=3288641|V-Datum=1966-11-29}}</ref> angemeldet für [[Standard Oil of Ohio]] (SOHIO), wo an experimentellen Brennstoffzellen geforscht wurde, wurde die wahre Natur der elektrochemischen Energiespeicherung nicht benannt. Noch 1970 wurde im Patent von Donald L. Boos ein elektrochemischer Kondensator als Elektrolytkondensator mit Aktivkohle-Elektroden<ref>{{Patent|Erfinder=D. L. Boos|Titel=Electrolytic capacitor having carbon paste electrodes|Land=US|V-Nr=3536963|V-Datum=1970-10-27}}</ref> angemeldet. |
Auch in dem neun Jahre später eingereichten Patent von 1966, eines „Energiespeicher-Apparates“ von R. A. Rightmire<ref>{{Patent|Erfinder=R. A. Rightmire|Titel=Electrical energy storage apparatus|Land=US|V-Nr=3288641|V-Datum=1966-11-29}}</ref> angemeldet für [[Standard Oil of Ohio]] (SOHIO), wo an experimentellen Brennstoffzellen geforscht wurde, wurde die wahre Natur der elektrochemischen Energiespeicherung nicht benannt. Noch 1970 wurde im Patent von Donald L. Boos ein elektrochemischer Kondensator als Elektrolytkondensator mit Aktivkohle-Elektroden<ref>{{Patent|Erfinder=D. L. Boos|Titel=Electrolytic capacitor having carbon paste electrodes|Land=US|V-Nr=3536963|V-Datum=1970-10-27}}</ref> angemeldet. |
||
| Zeile 57: | Zeile 57: | ||
<math>C_\text{gesamt} = \frac{C_1 \cdot C_2}{C_1 + C_2}</math> |
<math>C_\text{gesamt} = \frac{C_1 \cdot C_2}{C_1 + C_2}</math> |
||
Superkondensatoren können entweder mit symmetrischen oder mit asymmetrischen Elektroden aufgebaut sein. Bei symmetrischen Elektroden haben beide Elektroden den gleich großen Kapazitätswert. Das bedeutet, wenn '''C<sub>1</sub> = C<sub>2</sub>''' dann ist '''C<sub>gesamt</sub> = 0 |
Superkondensatoren können entweder mit symmetrischen oder mit asymmetrischen Elektroden aufgebaut sein. Bei symmetrischen Elektroden haben beide Elektroden den gleich großen Kapazitätswert. Das bedeutet, wenn '''C<sub>1</sub> = C<sub>2</sub>''' dann ist '''C<sub>gesamt</sub> = 0,5·C<sub>1</sub>'''. Bei symmetrischen Elektroden hat der Kondensator deshalb einen Kapazitätswert, der dem halben Wert einer Elektrode entspricht. |
||
Bei asymmetrischen Elektroden hat eine Elektrode einen meist sehr viel höheren Kapazitätswert als die andere. Das bedeutet, wenn '''C<sub>1</sub> <nowiki>>></nowiki> C<sub>2</sub>''' dann ist '''C<sub>gesamt</sub> ≈ C<sub>2</sub>'''. Bei asymmetrischen Elektroden kann der Superkondensator einen Kapazitätswert erreichen, der dem Wert einer Elektrode entspricht. |
Bei asymmetrischen Elektroden hat eine Elektrode einen meist sehr viel höheren Kapazitätswert als die andere. Das bedeutet, wenn '''C<sub>1</sub> <nowiki>>></nowiki> C<sub>2</sub>''' dann ist '''C<sub>gesamt</sub> ≈ C<sub>2</sub>'''. Bei asymmetrischen Elektroden kann der Superkondensator einen Kapazitätswert erreichen, der dem Wert einer Elektrode entspricht. |
||
| Zeile 97: | Zeile 97: | ||
[[Datei:Voltagramm.png|mini|In einem [[Cyclovoltammetrie|Cyclovoltammogramm]] zeigt sich die Pseudokapazität durch einen geschwungenen Kurvenverlauf]] |
[[Datei:Voltagramm.png|mini|In einem [[Cyclovoltammetrie|Cyclovoltammogramm]] zeigt sich die Pseudokapazität durch einen geschwungenen Kurvenverlauf]] |
||
Die Fähigkeit von Kondensatorelektroden, Redoxreaktionen für eine Pseudokapazität zu bewerkstelligen, hängt sehr stark von der Beschaffenheit und der Struktur des Elektrodenmaterials ab. Elektrodenmaterialien, die pseudokapazitive Eigenschaften aufweisen sind z. B. [[Metalloxid]]e von [[Übergangsmetall]]en, die die zum Teil durch [[Dotierung]] in das Elektrodenmaterial eingebracht oder mit Hilfe einer [[Interkalation (Chemie)|Interkalation]] eingefügt werden. Auch leitfähige [[Polymer]]e wie [[Polyanilin]] oder Derivate von [[Polythiophen]], die auf die Strukturen von [[Kohlenstoff]]elektroden aufgebracht sind, eignen sich für Pseudokondensatoren. Aber auch Kohlenstoffelektroden können eine Pseudokapazität aufweisen.<ref>Roy Peter Richner, Entwicklung neuartig gebundener Kohlenstoffmaterialien für elektrische Doppelschichtkondensatorelektroden, DISS.ETH Nr. 14413, 2001 [http://e-collection.library.ethz.ch/eserv/eth:25657/eth-25657-02.pdf e-collection.library.ethz.ch] (abgerufen am 5. Januar 2014)</ref> Der Anteil an pseudokapazitiven Reaktionen an Kohlenstoffelektroden kann auch durch maßgeschneiderte Porengrößen deutlich gesteigert werden.<ref name="Bakhmatyuk2003">{{Literatur|Autor=B. P. Bakhmatyuk, B. Y. Venhryn, I. I. Grygorchak, M. M. Micov, S. I. Mudry|Titel=Intercalation Pseudo-Capacitance In Carbon Systems Of Energy Storage|Sammelwerk=Rev. Adv. Mater. Sci|Band=14|Jahr=2007|Seiten=151–156|Online=[http://www.ipme.ru/e-journals/RAMS/no_21407/bakhmatyuk.pdf PDF]| |
Die Fähigkeit von Kondensatorelektroden, Redoxreaktionen für eine Pseudokapazität zu bewerkstelligen, hängt sehr stark von der Beschaffenheit und der Struktur des Elektrodenmaterials ab. Elektrodenmaterialien, die pseudokapazitive Eigenschaften aufweisen sind z. B. [[Metalloxid]]e von [[Übergangsmetall]]en, die die zum Teil durch [[Dotierung]] in das Elektrodenmaterial eingebracht oder mit Hilfe einer [[Interkalation (Chemie)|Interkalation]] eingefügt werden. Auch leitfähige [[Polymer]]e wie [[Polyanilin]] oder Derivate von [[Polythiophen]], die auf die Strukturen von [[Kohlenstoff]]elektroden aufgebracht sind, eignen sich für Pseudokondensatoren. Aber auch Kohlenstoffelektroden können eine Pseudokapazität aufweisen.<ref>Roy Peter Richner, Entwicklung neuartig gebundener Kohlenstoffmaterialien für elektrische Doppelschichtkondensatorelektroden, DISS.ETH Nr. 14413, 2001 [http://e-collection.library.ethz.ch/eserv/eth:25657/eth-25657-02.pdf e-collection.library.ethz.ch] (abgerufen am 5. Januar 2014)</ref> Der Anteil an pseudokapazitiven Reaktionen an Kohlenstoffelektroden kann auch durch maßgeschneiderte Porengrößen deutlich gesteigert werden.<ref name="Bakhmatyuk2003">{{Literatur|Autor=B. P. Bakhmatyuk, B. Y. Venhryn, I. I. Grygorchak, M. M. Micov, S. I. Mudry|Titel=Intercalation Pseudo-Capacitance In Carbon Systems Of Energy Storage|Sammelwerk=Rev. Adv. Mater. Sci|Band=14|Jahr=2007|Seiten=151–156|Online=[http://www.ipme.ru/e-journals/RAMS/no_21407/bakhmatyuk.pdf PDF]| Zugriff= 2014-01-05}}</ref> |
||
Wie bei Doppelschichtelektroden ergibt sich das Speichervermögen von Pseudokondensatorelektroden aus dem [[Elektrisches Potential|potentialabhängigen]] Bedeckungsgrad der Elektrodenoberfläche mit adsorbierten Ionen. Da bei allen pseudokapazitiv wirksamen Reaktionen die Ionen desolvatisiert sind, d. h. keine die kugelförmig umhüllende Schicht von Lösungsmittelmolekülen aufweisen, sind sie deutlich kleiner als die solvatisierten Ionen, die zur Doppelschichtkapazität beitragen. Deshalb benötigen sie entsprechend weniger Elektrodenoberfläche. Die Pseudokapazität einer dafür geeigneten Elektrode kann beispielsweise bei gleicher Oberfläche der Elektrode um den Faktor 100 größer sein als die Doppelschichtkapazität.<ref name="conway1" /><ref name="Frackowiak" /><ref name="Pandolfo">A.G. Pandolfo, A.F. Hollenkamp |
Wie bei Doppelschichtelektroden ergibt sich das Speichervermögen von Pseudokondensatorelektroden aus dem [[Elektrisches Potential|potentialabhängigen]] Bedeckungsgrad der Elektrodenoberfläche mit adsorbierten Ionen. Da bei allen pseudokapazitiv wirksamen Reaktionen die Ionen desolvatisiert sind, d. h. keine die kugelförmig umhüllende Schicht von Lösungsmittelmolekülen aufweisen, sind sie deutlich kleiner als die solvatisierten Ionen, die zur Doppelschichtkapazität beitragen. Deshalb benötigen sie entsprechend weniger Elektrodenoberfläche. Die Pseudokapazität einer dafür geeigneten Elektrode kann beispielsweise bei gleicher Oberfläche der Elektrode um den Faktor 100 größer sein als die Doppelschichtkapazität.<ref name="conway1" /><ref name="Frackowiak" /><ref name="Pandolfo">{{Literatur | Autor = A. G. Pandolfo, A. F. Hollenkamp | Titel = Carbon properties and their role in supercapacitors | Sammelwerk = Journal of Power Sources | Band = 157 | Jahr = 2006 | Datum = 2006-06-19| Nummer = 1| Seiten = 11–27| DOI= 10.1016/j.jpowsour.2006.02.065}}</ref><ref name="Bakhmatyuk2003" /><ref name="Simon-Burke">{{Literatur | Autor = Patrice Simon, A. F. Burke | Titel = Nanostructured carbons: double-layer capacitance and more | Sammelwerk = The electrochemical society interface | Band = 17 | Jahr = 2008 | Datum = 2008| Nummer = 1| Seiten = 38|Online=[http://www.electrochem.org/dl/interface/spr/spr08/spr08_p38-43.pdf PDF; 633 kB]|Zugriff=2015-02-01}}</ref> |
||
Die [[Elektrische Ladung|Ladungsmenge]] der in einer Pseudokapazität gespeicherten Energie verhält sich linear zur anliegenden [[Elektrische Spannung|Spannung]]. Die Einheit der Pseudokapazität ist [[Farad]]. |
Die [[Elektrische Ladung|Ladungsmenge]] der in einer Pseudokapazität gespeicherten Energie verhält sich linear zur anliegenden [[Elektrische Spannung|Spannung]]. Die Einheit der Pseudokapazität ist [[Farad]]. |
||
| Zeile 157: | Zeile 157: | ||
Elektroden aus Kohlenstoff weisen eine sehr hohe statische Doppelschichtkapazität auf. Der Anteil an Pseudokapazität an solchen Elektroden ist meist recht gering. Der faradaysche Ladungstausch findet nur an den kantigen Strukturbereichen oder in zufällig vorhandenen Nanoporen mit entsprechender Größe statt. Allerdings kann bei neuen Kohlenstoffmaterialien mit maßgeschneiderten Porengrößen der Anteil an Pseudokapazität stark ansteigen, so dass dann eine eindeutige Zuordnung zu einer Doppelschicht- oder Pseudokapazität nicht mehr gegeben werden kann. |
Elektroden aus Kohlenstoff weisen eine sehr hohe statische Doppelschichtkapazität auf. Der Anteil an Pseudokapazität an solchen Elektroden ist meist recht gering. Der faradaysche Ladungstausch findet nur an den kantigen Strukturbereichen oder in zufällig vorhandenen Nanoporen mit entsprechender Größe statt. Allerdings kann bei neuen Kohlenstoffmaterialien mit maßgeschneiderten Porengrößen der Anteil an Pseudokapazität stark ansteigen, so dass dann eine eindeutige Zuordnung zu einer Doppelschicht- oder Pseudokapazität nicht mehr gegeben werden kann. |
||
Das am häufigsten verwendete Elektrodenmaterial für Superkondensatoren ist Kohlenstoff in seinen verschiedenen Erscheinungsformen, wie Aktivkohle (AC), Aktivkohlefaser (AFC), Carbid-abgeleiteter Kohlenstoff (CDC), Kohlenstoff-Aerogel, Graphit ([[Graphen]]) und Kohlenstoffnanoröhren (CNTs ).<ref name="Frackowiak" /><ref name="Pandolfo">A.G. Pandolfo, A.F. Hollenkamp |
Das am häufigsten verwendete Elektrodenmaterial für Superkondensatoren ist Kohlenstoff in seinen verschiedenen Erscheinungsformen, wie Aktivkohle (AC), Aktivkohlefaser (AFC), Carbid-abgeleiteter Kohlenstoff (CDC), Kohlenstoff-Aerogel, Graphit ([[Graphen]]) und Kohlenstoffnanoröhren (CNTs ).<ref name="Frackowiak" /><ref name="Pandolfo">{{Literatur | Autor = A. G. Pandolfo, A. F. Hollenkamp | Titel = Carbon properties and their role in supercapacitors | Sammelwerk = Journal of Power Sources | Band = 157 | Jahr = 2006 | Datum = 2006-06-19| Nummer = 1| Seiten = 11–27| DOI= 10.1016/j.jpowsour.2006.02.065}}</ref><ref name="Simon-Burke">{{Literatur|Autor=P. Simon, A. F. Burke| Titel=Nanostructured carbons: double-layer capacitance and more| Sammelwerk=The Electrochemical Society Interface| Band=17| Nummer=1| Jahr=2008| Seiten=38| Datum=2008-00-00|Online=[http://www.electrochem.org/dl/interface/spr/spr08/spr08_p38-43.pdf PDF]|Zugriff=2013-01-08}}</ref><ref>K. Kinoshita: ''Carbon, Electrochemical and Physicochemical Properties.'' John Wiley & Sons, New York 1988, ISBN 0-471-84802-6.</ref> |
||
===== Aktivkohle ===== |
===== Aktivkohle ===== |
||
[[Datei:ActivatedCharcoalPowder BrightField.jpg|mini|[[Hellfeldmikroskopie]] von granulierter Aktivkohle. Die brüchige Struktur der Kohlepartikel deutet auf die enorme Größe der Oberfläche hin. Jeder Partikel im Bild hat einen Durchmesser von etwa 0,1 mm und eine Oberfläche von mehreren Quadratmetern.]] |
[[Datei:ActivatedCharcoalPowder BrightField.jpg|mini|[[Hellfeldmikroskopie]] von granulierter Aktivkohle. Die brüchige Struktur der Kohlepartikel deutet auf die enorme Größe der Oberfläche hin. Jeder Partikel im Bild hat einen Durchmesser von etwa 0,1 mm und eine Oberfläche von mehreren Quadratmetern.]] |
||
Das Elektrodenmaterial in den ersten Doppelschichtkondensatoren bestand aus industriell hergestellter [[Aktivkohle]] ({{enS|''activated carbon (AC)''}}). Aktivkohle hat entlang der Kristallebenen des Kohlenstoffs eine elektrische [[Leitfähigkeit]] von 1.250 bis 3.000 [[Siemens ( |
Das Elektrodenmaterial in den ersten Doppelschichtkondensatoren bestand aus industriell hergestellter [[Aktivkohle]] ({{enS|''activated carbon (AC)''}}). Aktivkohle hat entlang der Kristallebenen des Kohlenstoffs eine elektrische [[Leitfähigkeit]] von 1.250 bis 3.000 [[Siemens (Einheit)|S]]/m, das ist nur etwa 0,003 % einer metallischen Leitfähigkeit, aber das ist gut genug für die Verwendung als Elektrodenmaterial von Superkondensatoren.<ref name="Halper" /><ref name="Namisnyk" /> |
||
Aktivkohle bildet eine extrem poröse, offenporige Elektrode mit schwammartiger Struktur, die, bezogen auf das Volumen eine extrem große spezifische Oberfläche von etwa 1000 bis 3000 m² pro Gramm hat.<ref name="Pandolfo" /> Das ist in etwa die Fläche von 4 bis 12 Tennisplätzen oder mit einem anderen Vergleich, 2,5 g Aktivkohle hat eine Oberfläche von ungefähr der Fläche eines Fußballfeldes. Die Dicke der Elektrode beträgt oft nur wenige 100 µm. Eine Elektrode aus Aktivkohle mit einer Oberfläche von etwa 1000 m<sup>2</sup>/g ergibt eine typische Doppelschichtkapazität von etwa 10 μF/cm² beziehungsweise eine spezifischen Kapazität von 100 F/g. |
Aktivkohle bildet eine extrem poröse, offenporige Elektrode mit schwammartiger Struktur, die, bezogen auf das Volumen eine extrem große spezifische Oberfläche von etwa 1000 bis 3000 m² pro Gramm hat.<ref name="Pandolfo" /> Das ist in etwa die Fläche von 4 bis 12 Tennisplätzen oder mit einem anderen Vergleich, 2,5 g Aktivkohle hat eine Oberfläche von ungefähr der Fläche eines Fußballfeldes. Die Dicke der Elektrode beträgt oft nur wenige 100 µm. Eine Elektrode aus Aktivkohle mit einer Oberfläche von etwa 1000 m<sup>2</sup>/g ergibt eine typische Doppelschichtkapazität von etwa 10 μF/cm² beziehungsweise eine spezifischen Kapazität von 100 F/g. |
||
Aktivkohle ist sehr preiswert herzustellen, ist ungiftig, chemisch [[Inerte Substanz|inert]] und [[Korrosion|korrosionsbeständig]]. Sie enthält keine die Umwelt schädigenden Stoffe und kann außerdem aus preisgünstigen natürlichen Ausgangsstoffen hergestellt werden.<ref name="Oertel">Dagmar Oertel: ''Sachstandsbericht zum Monitoring »Nachhaltige Energieversorgung« Energiespeicher – Stand und Perspektiven.'' In: ''Arbeitsbericht Nr. 123.'' S. 86ff (Abschnitt: Elektrochemische Kondensatoren; [http://www.tab-beim-bundestag.de/de/pdf/publikationen/berichte/TAB-Arbeitsbericht-ab123.pdf#page=88 PDF]).</ref> Ab 2010 verwenden praktisch alle kommerziellen Superkondensatoren Aktivkohle in Pulverform, die umweltfreundlich aus Kokosnussschalen hergestellt wird.<ref>{{cite journal| last=Laine| first=Jorge| coauthors=Simon Yunes| title=Effect of the preparation method on the pore size distribution of activated carbon from coconut shell| journal=Carbon| year=1992| volume=30| issue=4| pages=601–604| doi=10.1016/0008-6223(92)90178-Y |
Aktivkohle ist sehr preiswert herzustellen, ist ungiftig, chemisch [[Inerte Substanz|inert]] und [[Korrosion|korrosionsbeständig]]. Sie enthält keine die Umwelt schädigenden Stoffe und kann außerdem aus preisgünstigen natürlichen Ausgangsstoffen hergestellt werden.<ref name="Oertel">Dagmar Oertel: ''Sachstandsbericht zum Monitoring »Nachhaltige Energieversorgung« Energiespeicher – Stand und Perspektiven.'' In: ''Arbeitsbericht Nr. 123.'' S. 86ff (Abschnitt: Elektrochemische Kondensatoren; [http://www.tab-beim-bundestag.de/de/pdf/publikationen/berichte/TAB-Arbeitsbericht-ab123.pdf#page=88 PDF]).</ref> Ab 2010 verwenden praktisch alle kommerziellen Superkondensatoren Aktivkohle in Pulverform, die umweltfreundlich aus Kokosnussschalen hergestellt wird.<ref>{{cite journal| last=Laine| first=Jorge| coauthors=Simon Yunes| title=Effect of the preparation method on the pore size distribution of activated carbon from coconut shell| journal=Carbon| year=1992| volume=30| issue=4| pages=601–604| doi=10.1016/0008-6223(92)90178-Y}}</ref> |
||
Nachteil von Elektroden aus Aktivkohle ist, dass im Gegensatz zu Elektroden aus Nanoröhren nur weniger als 1/3 der Fläche für die Bildung einer Doppelschichtkapazität zur Verfügung steht.<ref name="Du">CHUNSHENG DU, NING PAN, Carbon Nanotube-Based Supercapacitors, NANOTECHNOLOGY LAW &BUSINESS , MARCH 2007, [http://ningpan.net/Publications/101-150/125.pdf PDF]</ref> Höhere Oberflächenausnutzung mit anderen Kohlenstoffmaterialien sind möglich, allerdings sind diese mit höheren Kosten verbunden. |
Nachteil von Elektroden aus Aktivkohle ist, dass im Gegensatz zu Elektroden aus Nanoröhren nur weniger als 1/3 der Fläche für die Bildung einer Doppelschichtkapazität zur Verfügung steht.<ref name="Du">CHUNSHENG DU, NING PAN, Carbon Nanotube-Based Supercapacitors, NANOTECHNOLOGY LAW &BUSINESS , MARCH 2007, [http://ningpan.net/Publications/101-150/125.pdf PDF]</ref> Höhere Oberflächenausnutzung mit anderen Kohlenstoffmaterialien sind möglich, allerdings sind diese mit höheren Kosten verbunden. |
||
| Zeile 183: | Zeile 183: | ||
[[Kohlenstoff]]-[[Aerogel]] ist ein [[Synthese|synthetisches]], sehr hoch poröses und ultraleichtes Material aus einem organischen [[Gel]], in dem die flüssige Komponente des Gels durch [[Pyrolyse]] mit einem [[Gas]] ersetzt wurde. Aerogele werden auch „gefrorener Rauch“ genannt. |
[[Kohlenstoff]]-[[Aerogel]] ist ein [[Synthese|synthetisches]], sehr hoch poröses und ultraleichtes Material aus einem organischen [[Gel]], in dem die flüssige Komponente des Gels durch [[Pyrolyse]] mit einem [[Gas]] ersetzt wurde. Aerogele werden auch „gefrorener Rauch“ genannt. |
||
Kohlenstoff-Aerogel-Elektroden werden mit der [[Pyrolyse]] von [[Resorcin]]-[[Formaldehyd]] hergestellt.<ref>{{cite journal| first1=U. | last1=Fischer | first2=R. | last2=Saliger | first3=V. | last3=Bock | first4=R. | last4=Petricevic | first5=J. | last5=Fricke | title=Carbon Aerogels as Electrode Material in Supercapacitors | journal=Journal of Porous Materials | volume=4| issue=4 | year=1997 | pages=281–285 | doi=10.1023/A:1009629423578 |
Kohlenstoff-Aerogel-Elektroden werden mit der [[Pyrolyse]] von [[Resorcin]]-[[Formaldehyd]] hergestellt.<ref>{{cite journal| first1=U. | last1=Fischer | first2=R. | last2=Saliger | first3=V. | last3=Bock | first4=R. | last4=Petricevic | first5=J. | last5=Fricke | title=Carbon Aerogels as Electrode Material in Supercapacitors | journal=Journal of Porous Materials | volume=4| issue=4 | year=1997 | pages=281–285 | doi=10.1023/A:1009629423578}}</ref><ref>{{Literatur|Autor=M. LaClair|Titel=Replacing Energy Storage with Carbon Aerogel Supercapacitors|Sammelwerk=Power Electronics, Feb 1, 2003, Cooper Electronic Technologies, Boynton Beach FL |Online=[http://powerelectronics.com/mag/power_replacing_energy_storage/ powerelectronics.com]|Zugriff=2013-01-29}}</ref> |
||
Kohlenstoff-Aerogel hat eine bessere elektrische Leitfähigkeit als Aktivkohle. Es ermöglicht dünne und mechanische stabile Elektroden mit einer Höhe im Bereich von mehreren hundert Mikrometern mit einheitlicher Porengröße. Durch die hohe mechanische Stabilität kann Kohlenstoff-Aerogel als Elektrodenmaterial für Superkondensatoren mit hoher Vibrationsfestigkeit verwendet werden. |
Kohlenstoff-Aerogel hat eine bessere elektrische Leitfähigkeit als Aktivkohle. Es ermöglicht dünne und mechanische stabile Elektroden mit einer Höhe im Bereich von mehreren hundert Mikrometern mit einheitlicher Porengröße. Durch die hohe mechanische Stabilität kann Kohlenstoff-Aerogel als Elektrodenmaterial für Superkondensatoren mit hoher Vibrationsfestigkeit verwendet werden. |
||
| Zeile 196: | Zeile 196: | ||
[[Datei:Figure4CDC.jpg|mini|Verteilung der Porengrößen verschiedener Carbid-abgeleiteter Kohlenstoffe]] |
[[Datei:Figure4CDC.jpg|mini|Verteilung der Porengrößen verschiedener Carbid-abgeleiteter Kohlenstoffe]] |
||
[[Carbid]]-abgeleitete Kohlenstoffe, ({{enS|''carbide-derived carbons (CDC)''}}), auch „abstimmbare nanoporöse Kohlenstoffe“ ({{enS|''tunable nanoporous carbons''}}) genannt, bestehen aus einer Anzahl von Stoffen, die aus Carbiden wie z. B. [[Siliciumcarbid]] und [[Titancarbid]] durch [[Thermolyse|thermische Zersetzung]] oder durch chemische [[Halogenierung]] in reinen Kohlenstoff umgewandelt wurden.<ref name="Presser"> |
[[Carbid]]-abgeleitete Kohlenstoffe, ({{enS|''carbide-derived carbons (CDC)''}}), auch „abstimmbare nanoporöse Kohlenstoffe“ ({{enS|''tunable nanoporous carbons''}}) genannt, bestehen aus einer Anzahl von Stoffen, die aus Carbiden wie z. B. [[Siliciumcarbid]] und [[Titancarbid]] durch [[Thermolyse|thermische Zersetzung]] oder durch chemische [[Halogenierung]] in reinen Kohlenstoff umgewandelt wurden.<ref name="Presser">{{Literatur | Autor = Volker Presser, Min Heon, Yury Gogotsi | Titel = Carbide-Derived Carbons – From Porous Networks to Nanotubes and Graphene | Sammelwerk = Advanced Functional Materials | Band = 21 | Jahr = 2011 | Datum = 2011| Nummer = 5| Seiten = 810–833| DOI= 10.1002/adfm.201002094}}</ref><ref name="Korenblit">Y. Korenblit, M. Rose, E. Kockrick, L. Borchardt, A. Kvit, St. Kaskel, G. Yushin, [http://www.nano-tech.gatech.edu/ACS_NANO_preprint.pdf High-Rate Electrochemical Capacitors Based on Ordered Mesoporous Silicon Carbide-Derived Carbon] (PDF; 472 kB)</ref> |
||
Elektroden aus CDC besitzen große Oberflächen mit maßgeschneiderten Porengrößen. Sie können mit Porengrößen im Bereich von [[Mesoporöse Festkörper|Mikroporen]] bis Mesoporen hergestellt werden. Poren mit Porendurchmessern von <2 nm erhöhen die Pseudokapazität der Elektrode deutlich, weil de-solvatisierte Ionen, die in die kleinen Poren der CDC-Elektrode eindringen können, sehr viel kleiner als Ionen mit ihrer Solvatisationshülle sind, wodurch die Packungsdichte interkalierten Ionen ansteigt, die durch faradayschen Ladungstausch die Pseudokapazität generieren. Diese CDC-Elektroden haben eine um 75 % höhere Energiedichte als herkömmliche Elektroden aus Aktivkohle. |
Elektroden aus CDC besitzen große Oberflächen mit maßgeschneiderten Porengrößen. Sie können mit Porengrößen im Bereich von [[Mesoporöse Festkörper|Mikroporen]] bis Mesoporen hergestellt werden. Poren mit Porendurchmessern von <2 nm erhöhen die Pseudokapazität der Elektrode deutlich, weil de-solvatisierte Ionen, die in die kleinen Poren der CDC-Elektrode eindringen können, sehr viel kleiner als Ionen mit ihrer Solvatisationshülle sind, wodurch die Packungsdichte interkalierten Ionen ansteigt, die durch faradayschen Ladungstausch die Pseudokapazität generieren. Diese CDC-Elektroden haben eine um 75 % höhere Energiedichte als herkömmliche Elektroden aus Aktivkohle. |
||
| Zeile 222: | Zeile 222: | ||
[[Kohlenstoffnanoröhre]]n ({{enS|''carbon nanotubes, (CNT)''}}) sind zu zylindrischen Nanoröhren umgeformte Graphenschichten. Es gibt einwandige Nanoröhren ({{enS|''single wall nano tubes, (SWNT)''}}) und mehrwandige Nanoröhren ({{enS|''carbon nanotubes, (CNT)''}}), bei denen mehrere einwandige Nanoröhren koaxial ineinander verschachtelt angeordnet sind. Die Durchmesser der SWNTs können variieren und liegen im Bereich der Mikroporen bis Mesoporen mit Werten zwischen 1 bis 3 nm. Die Nanoröhren können direkt auf ein Substrat aufwachsen, das als Kollektor dienen kann, z. B. auf einem Siliziumwafer, wodurch die gute elektrische Leitfähigkeit des Kohlenstoffs in Achsrichtung zur Erhöhung der Leistungsdichte führt. |
[[Kohlenstoffnanoröhre]]n ({{enS|''carbon nanotubes, (CNT)''}}) sind zu zylindrischen Nanoröhren umgeformte Graphenschichten. Es gibt einwandige Nanoröhren ({{enS|''single wall nano tubes, (SWNT)''}}) und mehrwandige Nanoröhren ({{enS|''carbon nanotubes, (CNT)''}}), bei denen mehrere einwandige Nanoröhren koaxial ineinander verschachtelt angeordnet sind. Die Durchmesser der SWNTs können variieren und liegen im Bereich der Mikroporen bis Mesoporen mit Werten zwischen 1 bis 3 nm. Die Nanoröhren können direkt auf ein Substrat aufwachsen, das als Kollektor dienen kann, z. B. auf einem Siliziumwafer, wodurch die gute elektrische Leitfähigkeit des Kohlenstoffs in Achsrichtung zur Erhöhung der Leistungsdichte führt. |
||
Im Vergleich zu der theoretisch maximalen Elektrodenoberfläche von Aktivkohle (3000 m<sup>2</sup>/g) besitzen CNT-Elektroden nur eine moderate Oberfläche von etwa 1315 m<sup>2</sup>/g. Wegen der besseren Benetzbarkeit haben CNT-Elektroden dennoch eine höhere Kapazität als Aktivkohle-Elektroden, z. B. 102 F/g für MWNT- und 180 F/g für SWNT-Elektroden.<ref name="Wen-Lu">Wen Lu: [http://cdn.intechopen.com/pdfs/10024/InTech-Carbon_nanotube_supercapacitors.pdf ''Carbon Nanotube Supercapacitors''.] (PDF; 1,9 MB) ADA Technologies Inc.</ref> Es wird erwartet, dass Superkondensatoren mit CNT-Elektroden eine Energiedichte von 21 Wh/kg bei der Nennspannung von 2,7 V erreichen werden.<ref name="Signorelli">{{Literatur|Autor=R. Signorelli, D. C. Ku, J. G. Kassakian, J. E. Schindall| Titel=Electrochemical Double-Layer Capacitors Using Carbon Nanotube Electrode Structures| Sammelwerk=Proceedings of the IEEE| Band=97| Nummer=11| Jahr=2009| Seiten=1837–1847| Datum=2009-11| DOI=10.1109/JPROC.2009.2030240|Online=[http://dspace.mit.edu/handle/1721.1/54729 Volltext]|Zugriff=2013-01-29}}</ref><ref>{{Literatur|Autor=B. Zhang, J. Liang, C. L. Xu, B. Q. Wei, D. B. Ruan, D. H. Wu| Titel=Electric double-layer capacitors using carbon nanotube electrodes and organic electrolyte| Sammelwerk=Materials Letters| Band=51| Nummer=6| Jahr=2001| Seiten=539–542| Datum=2001-12| DOI=10.1016/S0167-577X(01)00352-4|Online=[http://www.sciencedirect.com/science/article/pii/S0167577X01003524 PDF]|Zugriff=2013-07-28}}</ref><ref>{{Literatur|Autor=Qiao-Ling Chen, Kuan-Hong Xue, Wei Shen, Fei-Fei Tao, Shou-Yin Yin, Wen Xu| Titel=Fabrication and electrochemical properties of carbon nanotube array electrode for supercapacitors| Sammelwerk=Electrochimica Acta| Band=49| Nummer=24| Jahr=2004| Seiten=4157–4161| Datum=2004-09-30| DOI=10.1016/j.electacta.2004.04.010 |
Im Vergleich zu der theoretisch maximalen Elektrodenoberfläche von Aktivkohle (3000 m<sup>2</sup>/g) besitzen CNT-Elektroden nur eine moderate Oberfläche von etwa 1315 m<sup>2</sup>/g. Wegen der besseren Benetzbarkeit haben CNT-Elektroden dennoch eine höhere Kapazität als Aktivkohle-Elektroden, z. B. 102 F/g für MWNT- und 180 F/g für SWNT-Elektroden.<ref name="Wen-Lu">Wen Lu: [http://cdn.intechopen.com/pdfs/10024/InTech-Carbon_nanotube_supercapacitors.pdf ''Carbon Nanotube Supercapacitors''.] (PDF; 1,9 MB) ADA Technologies Inc.</ref> Es wird erwartet, dass Superkondensatoren mit CNT-Elektroden eine Energiedichte von 21 Wh/kg bei der Nennspannung von 2,7 V erreichen werden.<ref name="Signorelli">{{Literatur|Autor=R. Signorelli, D. C. Ku, J. G. Kassakian, J. E. Schindall| Titel=Electrochemical Double-Layer Capacitors Using Carbon Nanotube Electrode Structures| Sammelwerk=Proceedings of the IEEE| Band=97| Nummer=11| Jahr=2009| Seiten=1837–1847| Datum=2009-11| DOI=10.1109/JPROC.2009.2030240|Online=[http://dspace.mit.edu/handle/1721.1/54729 Volltext]|Zugriff=2013-01-29}}</ref><ref>{{Literatur|Autor=B. Zhang, J. Liang, C. L. Xu, B. Q. Wei, D. B. Ruan, D. H. Wu| Titel=Electric double-layer capacitors using carbon nanotube electrodes and organic electrolyte| Sammelwerk=Materials Letters| Band=51| Nummer=6| Jahr=2001| Seiten=539–542| Datum=2001-12| DOI=10.1016/S0167-577X(01)00352-4|Online=[http://www.sciencedirect.com/science/article/pii/S0167577X01003524 PDF]|Zugriff=2013-07-28}}</ref><ref>{{Literatur|Autor=Qiao-Ling Chen, Kuan-Hong Xue, Wei Shen, Fei-Fei Tao, Shou-Yin Yin, Wen Xu| Titel=Fabrication and electrochemical properties of carbon nanotube array electrode for supercapacitors| Sammelwerk=Electrochimica Acta| Band=49| Nummer=24| Jahr=2004| Seiten=4157–4161| Datum=2004-09-30| DOI=10.1016/j.electacta.2004.04.010}}</ref><ref>{{Literatur|Autor=Chunsheng Du, Ning Pan| Titel=Carbon Nanotube-Based Supercapacitors| Sammelwerk=Nanotechnology Law & Business| Band=4| Jahr=2007| Seiten=569–576| Datum=2007}}</ref>. |
||
Ähnlich wie bei CDC-Elektroden kann die Porengröße von Matten aus einwandigen oder mehrwandigen Nanoröhren präzise an die Ionendurchmesser aus dem Elektrolyten angepasst werden, um den Anteil an Pseudokapazität zu erhöhen.<ref name="Arepalli">{{cite journal| last=Arepalli| first=S.| coauthors=H. Fireman, C. Huffman, P. Moloney, P. Nikolaev, L. Yowell, C.D. Higgins, K. Kim, P.A. Kohl, S.P. Turano, and W.J. Ready| title=Carbon-Nanotube-Based Electrochemical Double-Layer Capacitor Technologies for Spaceflight Applications| journal=JOM| year=2005| pages=24–31 | url=http://eosl.gtri.gatech.edu/Portals/2/4.pdf}}</ref> Allerdings verursacht die wiederholte Interkalation während der Lade- und Entladevorgänge eine Volumenänderung, die die mechanische Stabilität der Poren verringert, so dass die Zyklusfestigkeit von Superkondensatoren mit CNT-Elektroden noch begrenzt ist. Die Forschung ist dabei, dieses Verhalten zu verbessern.<ref name="Conway-Birss">{{cite journal| last=Dillon| first=A.C.| title=Carbon Nanotubes for Photoconversion and Electrical Energy Storage| journal=Chem. Rev.| year=2010| volume=110| pages=6856–6872| doi=10.1021/cr9003314| pmid=20839769| issue=11}}</ref><ref name="Jian Li">Jian Li, Xiaoqian Cheng, Alexey Shashurin, Michael Keidar: |
Ähnlich wie bei CDC-Elektroden kann die Porengröße von Matten aus einwandigen oder mehrwandigen Nanoröhren präzise an die Ionendurchmesser aus dem Elektrolyten angepasst werden, um den Anteil an Pseudokapazität zu erhöhen.<ref name="Arepalli">{{cite journal| last=Arepalli| first=S.| coauthors=H. Fireman, C. Huffman, P. Moloney, P. Nikolaev, L. Yowell, C.D. Higgins, K. Kim, P.A. Kohl, S.P. Turano, and W.J. Ready| title=Carbon-Nanotube-Based Electrochemical Double-Layer Capacitor Technologies for Spaceflight Applications| journal=JOM| year=2005| pages=24–31 | url=http://eosl.gtri.gatech.edu/Portals/2/4.pdf}}</ref> Allerdings verursacht die wiederholte Interkalation während der Lade- und Entladevorgänge eine Volumenänderung, die die mechanische Stabilität der Poren verringert, so dass die Zyklusfestigkeit von Superkondensatoren mit CNT-Elektroden noch begrenzt ist. Die Forschung ist dabei, dieses Verhalten zu verbessern.<ref name="Conway-Birss">{{cite journal| last=Dillon| first=A.C.| title=Carbon Nanotubes for Photoconversion and Electrical Energy Storage| journal=Chem. Rev.| year=2010| volume=110| pages=6856–6872| doi=10.1021/cr9003314| pmid=20839769| issue=11}}</ref><ref name="Jian Li">Jian Li, Xiaoqian Cheng, Alexey Shashurin, Michael Keidar: ''Review of Electrochemical Capacitors Based on Carbon Nanotubes and Graphene''. In: ''Graphene''. 2012, 1, 1–13, [[doi:10.4236/graphene.2012.11001]].</ref> |
||
Elektroden mit Kohlenstoffnanoröhren eignen sich gut für besonders flache Bauformen, die typische mechanische Höhe einer Nanoröhrenelektrode ist ca. 20 bis 100 µm.<ref>S. Akbulut: [http://etd.library.vanderbilt.edu/available/etd-07262011-155004/unrestricted/serkanakbulut.pdf ''Optimization of Carbon Nanotube Supercapacitor Electrode''.] (PDF; 5 MB) Graduate School of Vanderbilt University, Nashville TN August 2011.</ref> |
Elektroden mit Kohlenstoffnanoröhren eignen sich gut für besonders flache Bauformen, die typische mechanische Höhe einer Nanoröhrenelektrode ist ca. 20 bis 100 µm.<ref>S. Akbulut: [http://etd.library.vanderbilt.edu/available/etd-07262011-155004/unrestricted/serkanakbulut.pdf ''Optimization of Carbon Nanotube Supercapacitor Electrode''.] (PDF; 5 MB) Graduate School of Vanderbilt University, Nashville TN August 2011.</ref> |
||
| Zeile 237: | Zeile 237: | ||
Viele Oxide von Übergangsmetallen sind In der Lage, Redox-Reaktionen mit faradayschem Ladungstransfer zu bewerkstelligen. Dazu gehören die Oxide von [[Ruthenium]] (RuO<sub>2</sub>), [[Iridium]] (chem|IrO<sub>2</sub>), [[Eisen]] (Fe<sub>3</sub>O<sub>4</sub>), [[Mangan]] (MnO<sub>2</sub>). Aber auch Schwefelverbindungen wie z. B. [[Titansulfide]] (TiS<sub>2</sub>) oder deren Kombinationen sind in der Lage Pseudokapazitäten zu bilden.<ref>M. Jayalakshmi, K. Balasubramanian: [http://www.electrochemsci.org/papers/vol3/3111196.pdf ''Simple Capacitors to Supercapacitors – An Overview''.] (PDF; 901 kB) In: ''Int. J. Electrochem. Sci.'', 3, 2008, S. 1196–1217</ref> |
Viele Oxide von Übergangsmetallen sind In der Lage, Redox-Reaktionen mit faradayschem Ladungstransfer zu bewerkstelligen. Dazu gehören die Oxide von [[Ruthenium]] (RuO<sub>2</sub>), [[Iridium]] (chem|IrO<sub>2</sub>), [[Eisen]] (Fe<sub>3</sub>O<sub>4</sub>), [[Mangan]] (MnO<sub>2</sub>). Aber auch Schwefelverbindungen wie z. B. [[Titansulfide]] (TiS<sub>2</sub>) oder deren Kombinationen sind in der Lage Pseudokapazitäten zu bilden.<ref>M. Jayalakshmi, K. Balasubramanian: [http://www.electrochemsci.org/papers/vol3/3111196.pdf ''Simple Capacitors to Supercapacitors – An Overview''.] (PDF; 901 kB) In: ''Int. J. Electrochem. Sci.'', 3, 2008, S. 1196–1217</ref> |
||
[[Ruthenium(IV)-oxid]] in Kombination mit [[Schwefelsäure]] H<sub>2</sub>SO<sub>4</sub> als Elektrolyt bietet eines der besten Beispiele für die Pseudokapazität. Diese Kombination hat eine etwa 10fach höhere spezifische Kapazität von 720 F/g, eine etwa 5fach höhere gravimetrische Energiedichte von 26.7 Wh/kg verglichen mit Elektroden aus Aktivkohle.<ref>J. P. Zheng, P. J. Cygan, T. R. Jow |
[[Ruthenium(IV)-oxid]] in Kombination mit [[Schwefelsäure]] H<sub>2</sub>SO<sub>4</sub> als Elektrolyt bietet eines der besten Beispiele für die Pseudokapazität. Diese Kombination hat eine etwa 10fach höhere spezifische Kapazität von 720 F/g, eine etwa 5fach höhere gravimetrische Energiedichte von 26.7 Wh/kg verglichen mit Elektroden aus Aktivkohle.<ref>{{Literatur | Autor = J. P. Zheng, P. J. Cygan, T. R. Jow | Titel = Hydrous Ruthenium Oxide as an Electrode Material for Electrochemical Capacitors | Sammelwerk = Journal of The Electrochemical Society | Band = 142 | Jahr = 1995 | Datum = 1995-01-08| Nummer = 8| Seiten = 2699–2703| DOI= 10.1149/1.2050077}}</ref> |
||
Weitere Vorteile dieser Elektroden sind die gute elektrische Leitfähigkeit sowie die hohe Zyklusfestigkeit von mehr als einer Million Zyklen. |
Weitere Vorteile dieser Elektroden sind die gute elektrische Leitfähigkeit sowie die hohe Zyklusfestigkeit von mehr als einer Million Zyklen. |
||
| Zeile 265: | Zeile 265: | ||
Kompositelektroden bestehen aus dem Basismaterial Kohlenstoff, das mit pseudokapazitiv aktivem Material beschichtet ist,<ref>M. Morita, M. Araki, N. Yoshimoto: ''Pseudo-capacitance of Activated Carbon Fiber Coated by Polythiophenes.'' In: ''2004 Joint International Meeting, E1 – Electrochemical Capacitor and Hybrid Power Sources.'' Electrochemical Society, 3.–8. Okt. 2004 (Abs# 676, [http://www.electrochem.org/dl/ma/206/pdfs/0676.pdf PDF])</ref> oder in deren atomares Gefüge pseudokapazitiv aktives Material eingefügt ist. Diese Kombination verleiht der Elektrode sowohl eine hohe Doppelschichtkapazität als auch eine hohe Pseudokapazität. Die sich daraus ergebende Gesamtkapazität ist deutlich höher als bei einem reinen Doppelschichtkondensator. |
Kompositelektroden bestehen aus dem Basismaterial Kohlenstoff, das mit pseudokapazitiv aktivem Material beschichtet ist,<ref>M. Morita, M. Araki, N. Yoshimoto: ''Pseudo-capacitance of Activated Carbon Fiber Coated by Polythiophenes.'' In: ''2004 Joint International Meeting, E1 – Electrochemical Capacitor and Hybrid Power Sources.'' Electrochemical Society, 3.–8. Okt. 2004 (Abs# 676, [http://www.electrochem.org/dl/ma/206/pdfs/0676.pdf PDF])</ref> oder in deren atomares Gefüge pseudokapazitiv aktives Material eingefügt ist. Diese Kombination verleiht der Elektrode sowohl eine hohe Doppelschichtkapazität als auch eine hohe Pseudokapazität. Die sich daraus ergebende Gesamtkapazität ist deutlich höher als bei einem reinen Doppelschichtkondensator. |
||
Der Anteil an Pseudokapazität bei Kompositelektroden kann durch maßgeschneiderte Porengröße und die damit verbundene Interkalation desolvatisierter Ionen noch erhöht werden. Besonders vielversprechend sind Neuentwicklungen mit Kohlenstoffnanoröhren. CNTs mit [[Polypyrrol]]-Einlagerungen oder Beschichtungen erreichen eine sehr gute Benetzbarkeit mit dem Elektrolyten und eine gleichmäßige dreidimensionale Verteilung der elektrischen Ladung. Darüber hinaus hat die Struktur beschichteter Kohlenstoffnanoröhren gezeigt, dass die mechanischen Beanspruchungen durch die faradayschen Lade- und Entladevorgänge geringer als bei reinen redoxaktiven Polymer-Elektroden ausfallen, wodurch eine größere Zyklenstabilität erreicht wird.<ref name="Frackowiak2">E. Frackowiak, V. Khomenko, K. Jurewicz, K. Lota, F. Béguin |
Der Anteil an Pseudokapazität bei Kompositelektroden kann durch maßgeschneiderte Porengröße und die damit verbundene Interkalation desolvatisierter Ionen noch erhöht werden. Besonders vielversprechend sind Neuentwicklungen mit Kohlenstoffnanoröhren. CNTs mit [[Polypyrrol]]-Einlagerungen oder Beschichtungen erreichen eine sehr gute Benetzbarkeit mit dem Elektrolyten und eine gleichmäßige dreidimensionale Verteilung der elektrischen Ladung. Darüber hinaus hat die Struktur beschichteter Kohlenstoffnanoröhren gezeigt, dass die mechanischen Beanspruchungen durch die faradayschen Lade- und Entladevorgänge geringer als bei reinen redoxaktiven Polymer-Elektroden ausfallen, wodurch eine größere Zyklenstabilität erreicht wird.<ref name="Frackowiak2">{{Literatur | Autor = E. Frackowiak, V. Khomenko, K. Jurewicz, K. Lota, F. Béguin | Titel = Supercapacitors based on conducting polymers/nanotubes composites | Sammelwerk = Journal of Power Sources | Band = 153 | Jahr = 2006 | Datum = 2006-02-28| Nummer = 2| Seiten = 413–418| DOI= 10.1016/j.jpowsour.2005.05.030}}</ref> |
||
Kompositelektroden können jedoch auch mit einem pseudokapazitiv aktiven Material [[Dotierung|dotiert]] werden. Das erfolgt in Entwicklungen von CNT-Kompositelektroden, die beispielsweise Übergangsmetalloxide wie RuO<sub>2</sub>, IrO<sub>2</sub>, MnO<sub>2</sub> oder [[Nitride]] von [[Molybdän]], [[Titan (Element)|Titan]] und [[Eisen]] als pseudokapazitiv aktives Material verwenden. Solche Kompositelektroden erreichen spezifische Kapazitätswerte im Bereich von 150 bis 250 μF/cm².<ref name="Naoi-Simon">K. Naoi, P. Simon: ''New Materials and New Configurations for Advanced Electrochemical Capacitors.'' ECS, Vol. 17, No. 1, Spring 2008, [http://www.electrochem.org/dl/interface/spr/spr08/spr08_p34-37.pdf PDF].</ref> |
Kompositelektroden können jedoch auch mit einem pseudokapazitiv aktiven Material [[Dotierung|dotiert]] werden. Das erfolgt in Entwicklungen von CNT-Kompositelektroden, die beispielsweise Übergangsmetalloxide wie RuO<sub>2</sub>, IrO<sub>2</sub>, MnO<sub>2</sub> oder [[Nitride]] von [[Molybdän]], [[Titan (Element)|Titan]] und [[Eisen]] als pseudokapazitiv aktives Material verwenden. Solche Kompositelektroden erreichen spezifische Kapazitätswerte im Bereich von 150 bis 250 μF/cm².<ref name="Naoi-Simon">K. Naoi, P. Simon: ''New Materials and New Configurations for Advanced Electrochemical Capacitors.'' ECS, Vol. 17, No. 1, Spring 2008, [http://www.electrochem.org/dl/interface/spr/spr08/spr08_p34-37.pdf PDF].</ref> |
||
| Zeile 318: | Zeile 318: | ||
Der Wert des Entladestromes richtet sich nach der Applikation, für die die Superkondensatoren vorgesehen werden. Die Norm IEC 62391-1 definiert hier vier Klassen: |
Der Wert des Entladestromes richtet sich nach der Applikation, für die die Superkondensatoren vorgesehen werden. Die Norm IEC 62391-1 definiert hier vier Klassen: |
||
* Klasse 1, Erhalt von Speichern, Entladestrom in mA = 1 |
* Klasse 1, Erhalt von Speichern, Entladestrom in mA = 1·C (F) |
||
* Klasse 2, Energiespeicherung, Entladestrom in mA = 0,4 |
* Klasse 2, Energiespeicherung, Entladestrom in mA = 0,4·C (F)·U (V) |
||
* Klasse 3, Leistungsanwendungen, Entladestrom in mA = 4 |
* Klasse 3, Leistungsanwendungen, Entladestrom in mA = 4·C (F)·U (V) |
||
* Klasse 4, Momentanleistung, Entladestrom in mA = 40 |
* Klasse 4, Momentanleistung, Entladestrom in mA = 40·C (F)·U (V) |
||
Die Kapazität ''C'' ergibt sich dann aus der Formel: |
Die Kapazität ''C'' ergibt sich dann aus der Formel: |
||
| Zeile 364: | Zeile 364: | ||
Der Innenwiderstand ''R<sub>i</sub>'' bestimmt mehrere Eigenschaften von Superkondensatoren. Er begrenzt zum einen die Lade- bzw. Entladegeschwindigkeit des Kondensators. Zusammen mit der Kapazität ''C'' des Kondensators ergibt sich die [[Zeitkonstante]] ''τ'' mit |
Der Innenwiderstand ''R<sub>i</sub>'' bestimmt mehrere Eigenschaften von Superkondensatoren. Er begrenzt zum einen die Lade- bzw. Entladegeschwindigkeit des Kondensators. Zusammen mit der Kapazität ''C'' des Kondensators ergibt sich die [[Zeitkonstante]] ''τ'' mit |
||
:<math>\tau = R_\text{i} \cdot C</math> |
:<math>\tau = R_\text{i} \cdot C</math> |
||
Diese Zeitkonstante bestimmt die zeitliche Grenze, mit der ein Kondensator ge- bzw. entladen werden kann. Ein 100-F-Kondensator mit dem Innenwiderstand von 30 mΩ hat z. B. eine Zeitkonstante von 0,03 |
Diese Zeitkonstante bestimmt die zeitliche Grenze, mit der ein Kondensator ge- bzw. entladen werden kann. Ein 100-F-Kondensator mit dem Innenwiderstand von 30 mΩ hat z. B. eine Zeitkonstante von 0,03 · 100 = 3 s, d. h., nach 3 s Laden mit einem nur durch den Innenwiderstand begrenzten Strom hat der Kondensator 62,3 % der Ladespannung erreicht. Da bis zum vollständigen Laden des Kondensators eine Zeitdauer von etwa 5 <math>\tau</math> benötigt wird, hat die Spannung dann nach etwa 15 s die Ladespannung erreicht. |
||
Der [[Widerstand (Bauelement)|Innenwiderstand]] ''R<sub>i</sub>'' ist aber auch der begrenzende Faktor, wenn mit Superkondensatoren der Vorteil der schnellen Lade-/Entladefähigkeit gegenüber Akkumulatoren ausgenutzt werden soll. Denn bei den sehr hohen Lade- und Entladeströmen ''I'', die bei Leistungsanwendungen von Superkondensatoren auftreten, treten interne Verluste ''P<sub>v</sub>'' auf, |
Der [[Widerstand (Bauelement)|Innenwiderstand]] ''R<sub>i</sub>'' ist aber auch der begrenzende Faktor, wenn mit Superkondensatoren der Vorteil der schnellen Lade-/Entladefähigkeit gegenüber Akkumulatoren ausgenutzt werden soll. Denn bei den sehr hohen Lade- und Entladeströmen ''I'', die bei Leistungsanwendungen von Superkondensatoren auftreten, treten interne Verluste ''P<sub>v</sub>'' auf, |
||
| Zeile 467: | Zeile 467: | ||
|- class="hintergrundfarbe6" |
|- class="hintergrundfarbe6" |
||
! Hersteller |
! Hersteller |
||
! Kondensator |
! Kondensator­name |
||
! Kapazitäts |
! Kapazitäts­bereich (F) |
||
! Zellen |
! Zellen­spannung (V) |
||
! Innen |
! Innen­widerstand bei C<sub>max</sub> (mΩ) |
||
! Volumetrische |
! Volumetrische Energie­dichte (Wh/dm³) |
||
! Gravimetrische |
! Gravimetrische Energie­dichte (Wh/kg) |
||
! Hinweise |
! Hinweise |
||
|- |
|- |
||
| APowerCap<ref>[http://www.apowercap.com/?pg=18&lang=eng&rand=95679520 APowerCap]</ref> ||APowerCap||4…550||2,7|| |
| APowerCap<ref>[http://www.apowercap.com/?pg=18&lang=eng&rand=95679520 APowerCap]</ref> ||APowerCap||4…550||2,7|| – || – ||4,5|| – |
||
|- |
|- |
||
| AVX<ref>[http://www.avx.com/docs/catalogs/bestcap.pdf AVX Kyocera, BestCap®] (PDF; 869 kB)</ref> ||BestCap®||0,068…0,56||3,6|| |
| AVX<ref>[http://www.avx.com/docs/catalogs/bestcap.pdf AVX Kyocera, BestCap®] (PDF; 869 kB)</ref> ||BestCap®||0,068…0,56||3,6|| – ||0,13|| – ||Module bis 16 V |
||
|- |
|- |
||
| Cap-XX<ref>[http://www.cap-xx.com/products/products.php Cap-XX]</ref>||Cap-XX||0,16…2,4||2,75…2,75||14||1,45||1,36|| |
| Cap-XX<ref>[http://www.cap-xx.com/products/products.php Cap-XX]</ref>||Cap-XX||0,16…2,4||2,75…2,75||14||1,45||1,36|| – |
||
|- |
|- |
||
| CDE<ref>[http://www.cde.com/catalog/Ultracap/ CDE Cornell Dubilier Supercapacitor]</ref>||Ultracapacitor||0,1…3000||2,7||0,29||7,7||6,0|| |
| CDE<ref>[http://www.cde.com/catalog/Ultracap/ CDE Cornell Dubilier Supercapacitor]</ref>||Ultracapacitor||0,1…3000||2,7||0,29||7,7||6,0|| – |
||
|- |
|- |
||
| Cooper<ref>[http://www.cooperindustries.com/content/public/en/bussmann/electronics/products/powerstor_supercapacitors.html Cooper Bussmann, PowerStor]</ref>||PowerStor||0,1…400||2,5…2,7||4,5||5,7|| |
| Cooper<ref>[http://www.cooperindustries.com/content/public/en/bussmann/electronics/products/powerstor_supercapacitors.html Cooper Bussmann, PowerStor]</ref>||PowerStor||0,1…400||2,5…2,7||4,5||5,7|| – || – |
||
|- |
|- |
||
| Elna<ref>[http://www.elna.co.jp/en/capacitor/pdf/catalog_10_11_e.pdf Elna, DYNACAP] (PDF; 7,1 MB)</ref>||DYNACAP<br />POWERCAP||0,047…300<br />||2,5...3,6<br />2,5||8,0<br />3,0||5,4<br />5,3||-<br /> |
| Elna<ref>[http://www.elna.co.jp/en/capacitor/pdf/catalog_10_11_e.pdf Elna, DYNACAP] (PDF; 7,1 MB)</ref>||DYNACAP<br />POWERCAP||0,047…300<br />||2,5...3,6<br />2,5||8,0<br />3,0||5,4<br />5,3||-<br /> – || – <br /> – |
||
|- |
|- |
||
| Elton<ref>[http://www.elton-cap.com/products/capacitor-cells/ Elton]</ref> ||Supercapacitor||1800…12000||1,5||0,5||6,8||4,2|| Module bis 29 V |
| Elton<ref>[http://www.elton-cap.com/products/capacitor-cells/ Elton]</ref> ||Supercapacitor||1800…12000||1,5||0,5||6,8||4,2|| Module bis 29 V |
||
|- |
|- |
||
| Evans<ref>[http://www.evanscap.com/capattery.htm Evans Capacitor Company, Capattery]</ref> ||Capattery||0,001…10||125||200|| |
| Evans<ref>[http://www.evanscap.com/capattery.htm Evans Capacitor Company, Capattery]</ref> ||Capattery||0,001…10||125||200|| – || – ||Hybridkondensatoren |
||
|- |
|- |
||
| HCC<ref>[http://www.hccenergy.com/en/products.asp Beijing HCC Energy Technology Co., HCAP]</ref> ||HCAP||0,22…5000||2,7||15||10,6|| |
| HCC<ref>[http://www.hccenergy.com/en/products.asp Beijing HCC Energy Technology Co., HCAP]</ref> ||HCAP||0,22…5000||2,7||15||10,6|| – ||Module bis 45 V |
||
|- |
|- |
||
| FDK<ref>''FDK To Begin Mass Production of High-Capacity Li-Ion Capacitors''. FDK, AFEC Asahi Kasei FDK Energy Device Co., Ltd., |
| FDK<ref>''FDK To Begin Mass Production of High-Capacity Li-Ion Capacitors''. FDK, AFEC Asahi Kasei FDK Energy Device Co., Ltd., |
||
| Zeile 497: | Zeile 497: | ||
||EneCapTen||2000||4,0||-||25||14||Li-Ion-Kondensatoren |
||EneCapTen||2000||4,0||-||25||14||Li-Ion-Kondensatoren |
||
|- |
|- |
||
| Illinois<ref>[http://www.illinoiscapacitor.com/products/super-capacitors.aspx Illinois Capacitor Inc., Supercapacitor]</ref> ||Supercapacitor||1…3500||2,3…2,7||0,24||7,6||5,9|| |
| Illinois<ref>[http://www.illinoiscapacitor.com/products/super-capacitors.aspx Illinois Capacitor Inc., Supercapacitor]</ref> ||Supercapacitor||1…3500||2,3…2,7||0,24||7,6||5,9|| – |
||
|- |
|- |
||
| Ioxus<ref>[http://www.ioxus.com/products/ ioxus Inc., Supercapacitor]</ref>||Ultracapacitor||100…3000<br />220…1000||2,7<br />2,3||0,25<br />14||7,8<br />8,7||6,0<br />6,4||Superkondensatoren<br />Hybridkondensatoren |
| Ioxus<ref>[http://www.ioxus.com/products/ ioxus Inc., Supercapacitor]</ref>||Ultracapacitor||100…3000<br />220…1000||2,7<br />2,3||0,25<br />14||7,8<br />8,7||6,0<br />6,4||Superkondensatoren<br />Hybridkondensatoren |
||
| Zeile 505: | Zeile 505: | ||
| Korchip<ref>[http://www.korchip.com/html/eng/starcap_product.asp Korchip, STARCAP]</ref>||STARCAP||0,01…400||2,7||12||7,0||6,1||Module bis 50 V |
| Korchip<ref>[http://www.korchip.com/html/eng/starcap_product.asp Korchip, STARCAP]</ref>||STARCAP||0,01…400||2,7||12||7,0||6,1||Module bis 50 V |
||
|- |
|- |
||
| Liyuan<ref>[http://www.cyliyuan.com/en/product1.asp Chaoyang Liyuan New Energy Co., Supercapacitor]</ref>||Supercapacitor||1…400||2,5||10||4,4||4,6|| |
| Liyuan<ref>[http://www.cyliyuan.com/en/product1.asp Chaoyang Liyuan New Energy Co., Supercapacitor]</ref>||Supercapacitor||1…400||2,5||10||4,4||4,6|| – |
||
|- |
|- |
||
| LS Mtron<ref>[http://www.lsmtron.com/product/product_view.asp?cate_code=74&kItem=3 LSMtron, Ultracapacitor]</ref>||Ultracapacitor||100…3000||2,8||0,25||6,0||5,9||Module bis 84 V |
| LS Mtron<ref>[http://www.lsmtron.com/product/product_view.asp?cate_code=74&kItem=3 LSMtron, Ultracapacitor]</ref>||Ultracapacitor||100…3000||2,8||0,25||6,0||5,9||Module bis 84 V |
||
| Zeile 511: | Zeile 511: | ||
| Maxwell<ref>[http://www.maxwell.com/ultracapacitors/ Maxwell Technologies, Ultracapacitor]</ref>||Boostcap®||10…3000||2,2…2,7||0,29||7,8||6,0||Module bis 125 V |
| Maxwell<ref>[http://www.maxwell.com/ultracapacitors/ Maxwell Technologies, Ultracapacitor]</ref>||Boostcap®||10…3000||2,2…2,7||0,29||7,8||6,0||Module bis 125 V |
||
|- |
|- |
||
| Murata<ref>[http://www.murata.com/products/edlc/index.html Murata Manufactoring Co., EDLC]</ref>||EDLC||0,35…0,7||2,1||30||0,8|| |
| Murata<ref>[http://www.murata.com/products/edlc/index.html Murata Manufactoring Co., EDLC]</ref>||EDLC||0,35…0,7||2,1||30||0,8|| – || – |
||
|- |
|- |
||
| NEC<ref>[http://www.nec-tokin.com/english/product/dl_capacitor.html NEC Tokin, Supercapacitor]</ref> ||Supercapacitor<br />LIC Capacitor||0,01…100<br />1100…1200||2,7<br />3,8||30.000<br />1,0||5,3 |
| NEC<ref>[http://www.nec-tokin.com/english/product/dl_capacitor.html NEC Tokin, Supercapacitor]</ref> ||Supercapacitor<br />LIC Capacitor||0,01…100<br />1100…1200||2,7<br />3,8||30.000<br />1,0||5,3<br /> – ||4,2<br /> – || – <br />Li-Ion-Kondensatoren |
||
|- |
|- |
||
| Nesscap<ref>[http://www.nesscap.com/product/overview.jsp Nesscap Energy Inc., Ultracapacitor, Pseudocapacitor]</ref>||EDLC,<br />Pseudocapacitor||3…60<br />50…300||2,3<br />2,3||35<br />18||4,3<br />12,9||3,3<br />8,7||Module bis 125 V |
| Nesscap<ref>[http://www.nesscap.com/product/overview.jsp Nesscap Energy Inc., Ultracapacitor, Pseudocapacitor]</ref>||EDLC,<br />Pseudocapacitor||3…60<br />50…300||2,3<br />2,3||35<br />18||4,3<br />12,9||3,3<br />8,7||Module bis 125 V |
||
| Zeile 525: | Zeile 525: | ||
| Samwha<ref>[http://www.samwha.com/goodsProduct.html?f_search_type=all&f_com=SWEI&f_cate=SWEI_001&f_sub_cate= Samwha Electric Co., GreenCap]</ref>||Green-Cap®||3…3000||2,7||0,28||7,7||5,6||Module bis 125 V |
| Samwha<ref>[http://www.samwha.com/goodsProduct.html?f_search_type=all&f_com=SWEI&f_cate=SWEI_001&f_sub_cate= Samwha Electric Co., GreenCap]</ref>||Green-Cap®||3…3000||2,7||0,28||7,7||5,6||Module bis 125 V |
||
|- |
|- |
||
| Skeleton<ref>[http://skeletontech.com/Skeleton-Technologies-SkelCap-Datasheet-121224.pdf Skeleton, SkelCap] (PDF; 9,1 MB)</ref> ||SkelCap||900…3500||2,85||0,2||14,1||10,1|| |
| Skeleton<ref>[http://skeletontech.com/Skeleton-Technologies-SkelCap-Datasheet-121224.pdf Skeleton, SkelCap] (PDF; 9,1 MB)</ref> ||SkelCap||900…3500||2,85||0,2||14,1||10,1|| – |
||
|- |
|- |
||
| Taiyo Yuden<ref>[http://www.yuden.co.jp/eu/product/category/energy_device/ Taiyo Yuden, PAS Capacitor, LIC Capacitor]</ref>|| PAS Capacitor<br /> LIC Capacitor||0,03…50<br />0,25…200||2,5…3,0<br /> 3,8||70<br />50 || 6,1<br /> |
| Taiyo Yuden<ref>[http://www.yuden.co.jp/eu/product/category/energy_device/ Taiyo Yuden, PAS Capacitor, LIC Capacitor]</ref>|| PAS Capacitor<br /> LIC Capacitor||0,03…50<br />0,25…200||2,5…3,0<br /> 3,8||70<br />50 || 6,1<br /> – || – <br /> – ||Pseudokondensatoren<br />Li-Ion-Kondensatoren |
||
|- |
|- |
||
| VinaTech<ref>[http://www.vina.co.kr/new_html/eng/product/info.asp?cate1=10 Vina Technology Co., Hy-Cap]</ref>||Hy-Cap||1,5…350||2,3…3,0||10||7,6||8,1|| |
| VinaTech<ref>[http://www.vina.co.kr/new_html/eng/product/info.asp?cate1=10 Vina Technology Co., Hy-Cap]</ref>||Hy-Cap||1,5…350||2,3…3,0||10||7,6||8,1|| – |
||
|- |
|- |
||
| WIMA<ref>[http://www.wima.com/DE/products_super.htm Wima Spezialvertrieb Elektronischer Bauelemente, SuperCaps]</ref>||SuperCap||12…6500||2,5…2,7||0,18||5,2||4,3|| Module bis 112 V |
| WIMA<ref>[http://www.wima.com/DE/products_super.htm Wima Spezialvertrieb Elektronischer Bauelemente, SuperCaps]</ref>||SuperCap||12…6500||2,5…2,7||0,18||5,2||4,3|| Module bis 112 V |
||
|- |
|- |
||
| YEC<ref>[http://www.yec.com.tw/dir-energy/energys-product-factory-list/energys-product-factory-list-1/ YEC Yeon Long Technologies, Kapton capacitor]</ref>||Kapton capacitor||0,5…400||2,7||12||7,0||5,5|| |
| YEC<ref>[http://www.yec.com.tw/dir-energy/energys-product-factory-list/energys-product-factory-list-1/ YEC Yeon Long Technologies, Kapton capacitor]</ref>||Kapton capacitor||0,5…400||2,7||12||7,0||5,5|| – |
||
|- |
|- |
||
| Yunasko<ref>[http://www.yunasko.com/index.php?option=com_content&view=article&id=83&Itemid=105&lang=en Yunasco]</ref>|| Ultracapacitor||480…1700||2,7||0,17||6,1||5,8||- |
| Yunasko<ref>[http://www.yunasko.com/index.php?option=com_content&view=article&id=83&Itemid=105&lang=en Yunasco]</ref>|| Ultracapacitor||480…1700||2,7||0,17||6,1||5,8||- |
||
| Zeile 560: | Zeile 560: | ||
|Nennspannung<br />pro Zelle (V)||4...550||1,2…3,3||2,5…3,3||2,2…3,8||2,5…4,2 |
|Nennspannung<br />pro Zelle (V)||4...550||1,2…3,3||2,5…3,3||2,2…3,8||2,5…4,2 |
||
|- |
|- |
||
|Lade-/Entlade-Zyklen||unbegrenzt||10<sup>5</sup>…10<sup>6</sup>||10<sup>5</sup>…10<sup>6</sup>||2 |
|Lade-/Entlade-Zyklen||unbegrenzt||10<sup>5</sup>…10<sup>6</sup>||10<sup>5</sup>…10<sup>6</sup>||2·10<sup>4</sup>…10<sup>5</sup>||500…10<sup>4</sup> |
||
|- |
|- |
||
|Kapazitätsbereich (F)||≤ 1||0,1…470||100…12000||300…2200||— |
|Kapazitätsbereich (F)||≤ 1||0,1…470||100…12000||300…2200||— |
||
| Zeile 736: | Zeile 736: | ||
Unter den Regeln für Prototypen des 24-Stunden-Rennens von [[Le Mans]] wurde von [[Toyota]] ein Rennwagen, der [[Toyota TS030 Hybrid]] LMP1, entwickelt, der einen Hybrid-Antriebsstrang besitzt und einen Energiespeicher zur Rückgewinnung der Bremsenergie nutzt, der mit Superkondensatoren bestückt ist<ref>{{cite web|url=http://www.racecar-engineering.com/news/toyota-ts030-lmp1-hybrid-revealed/ |title=Toyota TS030 LMP1 hybrid revealed |publisher=Racecar Engineering |date=2012-01-24 |accessdate=2013-05-30}}</ref><ref>[http://www.sportauto.de/motorsport/die-hybridtechnik-im-toyota-ts030-mit-superkondensatoren-zum-lemans-erfolg-4419021.html ''Die Hybridtechnik im Toyota TS030: Mit Superkondensatoren zum LeMans-Erfolg''.] sportauto.de</ref>. |
Unter den Regeln für Prototypen des 24-Stunden-Rennens von [[Le Mans]] wurde von [[Toyota]] ein Rennwagen, der [[Toyota TS030 Hybrid]] LMP1, entwickelt, der einen Hybrid-Antriebsstrang besitzt und einen Energiespeicher zur Rückgewinnung der Bremsenergie nutzt, der mit Superkondensatoren bestückt ist<ref>{{cite web|url=http://www.racecar-engineering.com/news/toyota-ts030-lmp1-hybrid-revealed/ |title=Toyota TS030 LMP1 hybrid revealed |publisher=Racecar Engineering |date=2012-01-24 |accessdate=2013-05-30}}</ref><ref>[http://www.sportauto.de/motorsport/die-hybridtechnik-im-toyota-ts030-mit-superkondensatoren-zum-lemans-erfolg-4419021.html ''Die Hybridtechnik im Toyota TS030: Mit Superkondensatoren zum LeMans-Erfolg''.] sportauto.de</ref>. |
||
Im Rennen 2012 fuhr dieser Sport-Prototyp seine schnellste Runde nur 1,055 Sekunden langsamer (3:24.842 gegenüber 3:23.787)<ref>{{cite web|author=Fred Jaillet |url=http://www.toyotahybridracing.com/toyota-racing-impresses-in-le-mans-qualifying/?myvar=News |title=Post TOYOTA Racing Impresses In Le Mans Qualifying |
Im Rennen 2012 fuhr dieser Sport-Prototyp seine schnellste Runde nur 1,055 Sekunden langsamer (3:24.842 gegenüber 3:23.787)<ref>{{cite web|author=Fred Jaillet |url=http://www.toyotahybridracing.com/toyota-racing-impresses-in-le-mans-qualifying/?myvar=News |title=Post TOYOTA Racing Impresses In Le Mans Qualifying – TOYOTA Racing – FIA World Endurance Championship Team |publisher=Toyotahybridracing.com |date=2012-06-15 |accessdate=2013-05-30}}</ref> als das schnellste Auto, ein [[Audi R18 e-tron quattro]] mit Schwungradspeicher. Diese beiden Fahrzeuge, die auf unterschiedliche Art und Weise die Bremsenergie zurückgewannen, waren die schnellsten Autos im Rennen. |
||
==== Kraftfahrzeuge ==== |
==== Kraftfahrzeuge ==== |
||
| Zeile 762: | Zeile 762: | ||
! Titel der<br />Neuentwicklung !! Datum !! Energiedichte<br />(Fußnote) !! Leistungsdichte !! Zyklen !! Spez. Kapazität !!Hinweise |
! Titel der<br />Neuentwicklung !! Datum !! Energiedichte<br />(Fußnote) !! Leistungsdichte !! Zyklen !! Spez. Kapazität !!Hinweise |
||
|- |
|- |
||
| Graphen-Elektroden in Subnanometer Konfiguration mit hoher Ionendichte<ref>Xiaowei Yang, Chi Cheng, Yufei Wang, Ling Qiu, Dan Li |
| Graphen-Elektroden in Subnanometer Konfiguration mit hoher Ionendichte<ref>{{Literatur | Autor = Xiaowei Yang, Chi Cheng, Yufei Wang, Ling Qiu, Dan Li | Titel = Liquid-Mediated Dense Integration of Graphene Materials for Compact Capacitive Energy Storage | Sammelwerk = Science | Band = 341 | Jahr = 2013 | Datum = 2013-02-08| Nummer = 6145| Seiten = 534–537| DOI= 10.1126/science.1239089| PMID = 23908233}}</ref> ||2013 || 60 Wh/l|| || || || Poröse, dicht gepackten Graphenelektroden mit großer Oberfläche, die mit Kapillarkräften eine hohe Ionendichte bewirken |
||
|- |
|- |
||
| Elektrode mit vertikal angeordneten Kohlenstoffnanoröhren<ref name="Schindall" /><ref name="Signorelli" /> || 2007<br />2009<br />2013 || 13,50 Wh/kg || 37,12 W/g || 300.000|| || Erste Anwendung siehe:<ref>{{cite web|author=Fastcap|url=http://www.fastcapsystems.com/technology |title=Paradigm shift |publisher=FastCap Systems |date=|accessdate=2013-05-30}}</ref> |
| Elektrode mit vertikal angeordneten Kohlenstoffnanoröhren<ref name="Schindall" /><ref name="Signorelli" /> || 2007<br />2009<br />2013 || 13,50 Wh/kg || 37,12 W/g || 300.000|| || Erste Anwendung siehe:<ref>{{cite web|author=Fastcap|url=http://www.fastcapsystems.com/technology |title=Paradigm shift |publisher=FastCap Systems |date=|accessdate=2013-05-30}}</ref> |
||
| Zeile 769: | Zeile 769: | ||
|| 2010 || 85,6 Wh/kg || || ||550 F/g || Die Elektroden mit zweidimensionaler Struktur formen Mesoporen mit großer Pseudokapazität. |
|| 2010 || 85,6 Wh/kg || || ||550 F/g || Die Elektroden mit zweidimensionaler Struktur formen Mesoporen mit großer Pseudokapazität. |
||
|- |
|- |
||
| Maßgeschneiderte dreidimensionale kristalline Graphitelektrode<ref>{{cite web|url=http://www.rsc.org/chemistryworld/News/2011/May/13051102.asp |title=New carbon material boosts supercapacitors |publisher=Rsc.org |date=2011-05-13 |accessdate=2013-05-30}}</ref><ref>{{ |
| Maßgeschneiderte dreidimensionale kristalline Graphitelektrode<ref>{{cite web|url=http://www.rsc.org/chemistryworld/News/2011/May/13051102.asp |title=New carbon material boosts supercapacitors |publisher=Rsc.org |date=2011-05-13 |accessdate=2013-05-30}}</ref><ref>{{Literatur | Autor = Yanwu Zhu u. a. | Titel = Carbon-Based Supercapacitors Produced by Activation of Graphene | Sammelwerk = Science | Band = 332 | Jahr = 2011 | Datum = 2011-06-24| Nummer = 6037| Seiten = 1537–1541| DOI= 10.1126/science.1200770| PMID = 21566159}}</ref> || 2011 || 85 Wh/kg || ||>10.000 ||550 F/g || Chemisch aktiviertes [[Graphit]] mit dreidimensionaler kristalliner Elektrodenstruktur mit Meso/Makroporen |
||
|- |
|- |
||
| Aktivierter Graphen-basierter Kohlenstoff mit Makro- und Mesoporen<ref>TaeYoung Kim, Gyujin Jung, Seonmi Yoo, Kwang S. Suh, Rodney S. Ruoff , Activated Graphene-Based Carbons as Supercapacitor Electrodes with Macro- and Mesopores [[doi:10.1021/nn402077v]]</ref>|| 2013 || 74 Wh/kg || || || || Dreidimensionale Porenstruktur in graphenabgeleitetem Kohlenstoff mit Mesoporen, die in Makroporen integriert sind und eine Oberfläche von 3290 m<sup>2</sup>/g besitzen |
| Aktivierter Graphen-basierter Kohlenstoff mit Makro- und Mesoporen<ref>TaeYoung Kim, Gyujin Jung, Seonmi Yoo, Kwang S. Suh, Rodney S. Ruoff , Activated Graphene-Based Carbons as Supercapacitor Electrodes with Macro- and Mesopores [[doi:10.1021/nn402077v]]</ref>|| 2013 || 74 Wh/kg || || || || Dreidimensionale Porenstruktur in graphenabgeleitetem Kohlenstoff mit Mesoporen, die in Makroporen integriert sind und eine Oberfläche von 3290 m<sup>2</sup>/g besitzen |
||
|- |
|- |
||
| Dreidimensionale poröse Graphen-Elektrode<ref> |
| Dreidimensionale poröse Graphen-Elektrode<ref>{{Literatur | Autor = Long Zhang u. a. | Titel = Porous 3D graphene-based bulk materials with exceptional high surface area and excellent conductivity for supercapacitors | Sammelwerk = Scientific Reports | Band = 3 | Jahr = 2013 | Datum = 2013-03-11| DOI= 10.1038/srep01408|PMID=23474952}}</ref> || 2013 || 98 Wh/kg || || || 231 F/g || Dreidimensionales Graphen-basierter Elektrodenmaterial aus einlagigen gefalteten Graphenschichten mit kovalenten Bindungen |
||
|- |
|- |
||
| SWNT Komposit-Elektrode<ref>K. Hata u. a.: ''High-power supercapacitor electrodes from single-walled carbon nanohorn/nanotube composite.'' In: ''[[ACS Nano]]'', 5, Nr. 2, 2011, pp 811–819, [[doi:10.1021/nn1017457]]</ref> ||2011 || ||990 kW/kg || || || Komposit-Elektrode mit einwandigen Kohlenstoffnanoröhren mit einer maßgeschneiderten Porenstruktur in der Größenordnung der Meso- und Makroporen |
| SWNT Komposit-Elektrode<ref>K. Hata u. a.: ''High-power supercapacitor electrodes from single-walled carbon nanohorn/nanotube composite.'' In: ''[[ACS Nano]]'', 5, Nr. 2, 2011, pp 811–819, [[doi:10.1021/nn1017457]]</ref> ||2011 || ||990 kW/kg || || || Komposit-Elektrode mit einwandigen Kohlenstoffnanoröhren mit einer maßgeschneiderten Porenstruktur in der Größenordnung der Meso- und Makroporen |
||
| Zeile 780: | Zeile 780: | ||
|| 2011 || 53 Wh/kg|| || 10,000|| || Das “Aza-Fused π-Conjugated Microporous Framework” ist ein mikroporöses Polymer (CMP), in dem sich in seinen Doppelbindungen einige Elektronen als „Elektronenwolke“ frei bewegen können, und ist geeignet für eine große Pseudokapazität. |
|| 2011 || 53 Wh/kg|| || 10,000|| || Das “Aza-Fused π-Conjugated Microporous Framework” ist ein mikroporöses Polymer (CMP), in dem sich in seinen Doppelbindungen einige Elektronen als „Elektronenwolke“ frei bewegen können, und ist geeignet für eine große Pseudokapazität. |
||
|- |
|- |
||
| [[Nickel(II)-hydroxid|Nickelhydroxid]] Komposit-Elektrode<ref>Zhe Tang, Chun-hua Tang, Hao Gong |
| [[Nickel(II)-hydroxid|Nickelhydroxid]] Komposit-Elektrode<ref>{{Literatur | Autor = Zhe Tang, Chun-hua Tang, Hao Gong | Titel = A High Energy Density Asymmetric Supercapacitor from Nano-architectured Ni(OH)2/Carbon Nanotube Electrodes | Sammelwerk = Advanced Functional Materials | Band = 22 | Jahr = 2012 | Datum = 2012| Nummer = 6| Seiten = 1272–1278| DOI= 10.1002/adfm.201102796}}</ref> |
||
|| 2012 || 50,6 Wh/kg || || ||3300 F/g || Asymmetrische Komposit-Elektrode, auf der Nickelhydroxid als Nanoflocken auf Kohlenstoffnanoröhren eingelagert sind, gekoppelt mit einer Kohlenstoff-Elektrode für einen Hybridkondensator mit 1,8 V Zellenspannung |
|| 2012 || 50,6 Wh/kg || || ||3300 F/g || Asymmetrische Komposit-Elektrode, auf der Nickelhydroxid als Nanoflocken auf Kohlenstoffnanoröhren eingelagert sind, gekoppelt mit einer Kohlenstoff-Elektrode für einen Hybridkondensator mit 1,8 V Zellenspannung |
||
|- |
|- |
||
| Zeile 807: | Zeile 807: | ||
== Literatur == |
== Literatur == |
||
<!--alphabetische Sortierung nach dem Nachnamen des ersten Autors--> |
|||
*{{Literatur|Autor=Héctor D. Abruña, Yasuyuki Kiya, Jay C. Henderson|Titel=Batteries and electrochemical capacitors|Sammelwerk=[[Physics Today]]|Nummer=12|Jahr=2008|Seiten=43–47|Online=[https://ecee.colorado.edu/~ecen4555/SourceMaterial/ElectricalEnerStor1208.pdf PDF]}} |
*{{Literatur|Autor=Héctor D. Abruña, Yasuyuki Kiya, Jay C. Henderson|Titel=Batteries and electrochemical capacitors|Sammelwerk=[[Physics Today]]|Nummer=12|Jahr=2008|Seiten=43–47|Online=[https://ecee.colorado.edu/~ecen4555/SourceMaterial/ElectricalEnerStor1208.pdf PDF]}} |
||
* F. Béguin, E. Raymundo-Piñero, E. Frackowiak: ''Carbons for Electrochemical Energy Storage and Conversion Systems.'' Chapter 8: ''Electrical Double-Layer Capacitors and Pseudocapacitors.'' CRC Press, 2009, ISBN 978-1-4200-5307-4, S. 329–375. (eBook, ISBN 978-1-4200-5540-5, [[doi:10.1201/9781420055405-c8]]) |
* F. Béguin, E. Raymundo-Piñero, E. Frackowiak: ''Carbons for Electrochemical Energy Storage and Conversion Systems.'' Chapter 8: ''Electrical Double-Layer Capacitors and Pseudocapacitors.'' CRC Press, 2009, ISBN 978-1-4200-5307-4, S. 329–375. (eBook, ISBN 978-1-4200-5540-5, [[doi:10.1201/9781420055405-c8]]) |
||
*{{Literatur|Autor=J. O’M. Bockris, M. A. V. Devanathan, K. Muller|Titel=On the Structure of Charged Interfaces| Sammelwerk=Proceedings of the Royal Society|Band=274|Nummer=1356|Jahr=1963|Seiten=55–79|DOI=10.1098/rspa.1963.0114}} |
*{{Literatur|Autor=J. O’M. Bockris, M. A. V. Devanathan, K. Muller|Titel=On the Structure of Charged Interfaces| Sammelwerk=Proceedings of the Royal Society|Band=274|Nummer=1356|Jahr=1963|Seiten=55–79|DOI=10.1098/rspa.1963.0114}} |
||
*{{Literatur|Autor=B. E. Conway|Titel=Electrochemical Supercapacitors: Scientific Fundamentals and Technological Applications|Verlag=Springer|Ort=Berlin|Jahr=1999|ISBN=0-306-45736-9|Online={{Google Buch|BuchID=8yvzlr9TqI0C|Seite=1}}}} |
*{{Literatur|Autor=B. E. Conway|Titel=Electrochemical Supercapacitors: Scientific Fundamentals and Technological Applications|Verlag=Springer|Ort=Berlin|Jahr=1999|ISBN=0-306-45736-9|Online={{Google Buch|BuchID=8yvzlr9TqI0C|Seite=1}}}} |
||
* |
* {{Literatur | Herausgeber = Farzad Ebrahimi(Herausgeber) | Titel = Nanocomposites - New Trends and Developments | Verlag = InTech | Jahr = 2012 | ISBN = 978-953-51-0762-0|DOI=10.5772/3389|Kommentar= Open-Access-Buch}} |
||
* Kim Kinoshita |
* {{Literatur | Autor = Kim Kinoshita | Titel = Carbon: Electrochemical and Physicochemical Properties | Auflage = 1 edition | Ort = New York | Verlag = Wiley-Interscience | Jahr = 1988 | ISBN = 0-471-84802-6}} |
||
* K. W. Leitner, M. Winter, J. O. Besenhard |
* {{Literatur | Autor = K. W. Leitner, M. Winter, J. O. Besenhard | Titel = Composite supercapacitor electrodes | Sammelwerk = Journal of Solid State Electrochemistry | Band = 8 | Jahr = 2003 | Datum = 2003-08-05| Nummer = 1| Seiten = 15–16| DOI= 10.1007/s10008-003-0412-x|ISSN=1433-0768}} |
||
*{{Literatur|Autor=Dagmar Oertel|Titel=Energiespeicher – Stand und Perspektiven|Sammelwerk=[[Büro für Technikfolgen-Abschätzung beim Deutschen Bundestag|TAB]] Arbeitsbericht|Nummer=123|Jahr=2008|Seiten=86–92|Online=[http://www.tab-beim-bundestag.de/de/pdf/publikationen/berichte/TAB-Arbeitsbericht-ab123.pdf PDF]|Kommentar=Abschnitt: Elektrochemische Kondensatoren}} |
*{{Literatur|Autor=Dagmar Oertel|Titel=Energiespeicher – Stand und Perspektiven|Sammelwerk=[[Büro für Technikfolgen-Abschätzung beim Deutschen Bundestag|TAB]] Arbeitsbericht|Nummer=123|Jahr=2008|Seiten=86–92|Online=[http://www.tab-beim-bundestag.de/de/pdf/publikationen/berichte/TAB-Arbeitsbericht-ab123.pdf PDF]|Kommentar=Abschnitt: Elektrochemische Kondensatoren}} |
||
*{{Literatur|Autor=Volkmar M. Schmidt|Titel=Elektrochemische Verfahrenstechnik. Grundlagen, Reaktionstechnik, Prozessoptimierung|Verlag=Wiley-VCH|Ort=Weinheim|Jahr=2003|ISBN=3-527-29958-0|Seiten=539–639|Online={{Google Buch|BuchID=Uu_4SJWQ0mIC|Seite=539}}|Kommentar=Kapitel 7: ''Elektrochemische Energietechnik''}} |
*{{Literatur|Autor=Volkmar M. Schmidt|Titel=Elektrochemische Verfahrenstechnik. Grundlagen, Reaktionstechnik, Prozessoptimierung|Verlag=Wiley-VCH|Ort=Weinheim|Jahr=2003|ISBN=3-527-29958-0|Seiten=539–639|Online={{Google Buch|BuchID=Uu_4SJWQ0mIC|Seite=539}}|Kommentar=Kapitel 7: ''Elektrochemische Energietechnik''}} |
||
* Yu |
* {{Literatur | Autor = Yu M. Vol’fkovich, T. M. Serdyuk | Titel = Electrochemical Capacitors | Sammelwerk = Russian Journal of Electrochemistry | Band = 38 | Jahr = 2002 | Datum = 2002-09-01| Nummer = 9| Seiten = 935–959| DOI= 10.1023/A:1020220425954|ISSN=1023-1935}} |
||
*{{Literatur|Autor=Jiujun Zhang, Lei Zhang, Hansan Liu, Andy Sun, Ru-Shi Liu|Titel=Electrochemical Technologies for Energy Storage and Conversion|Band=Band 1|Verlag=Wiley-VCH|Ort=Weinheim|Jahr=2011|ISBN=978-3-527-32869-7|Seiten=317–376|Online={{Google Buch|BuchID=AN3B3L5RtqUC|Seite=317}}|Kommentar=Kapitel 8: ''Electrochemical Supercapacitors''}} |
*{{Literatur|Autor=Jiujun Zhang, Lei Zhang, Hansan Liu, Andy Sun, Ru-Shi Liu|Titel=Electrochemical Technologies for Energy Storage and Conversion|Band=Band 1|Verlag=Wiley-VCH|Ort=Weinheim|Jahr=2011|ISBN=978-3-527-32869-7|Seiten=317–376|Online={{Google Buch|BuchID=AN3B3L5RtqUC|Seite=317}}|Kommentar=Kapitel 8: ''Electrochemical Supercapacitors''}} |
||
Version vom 1. Februar 2015, 20:34 Uhr
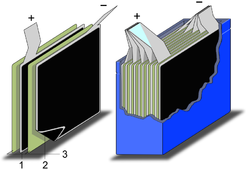
Superkondensatoren (englisch Supercapacitors, SC[1][2][3]), auch Ultrakondensatoren genannt, sind elektrochemische Kondensatoren (englisch electrochemical capacitors) und als solche eine Weiterentwicklung der Doppelschichtkondensatoren (englisch electric double-layer capacitor, EDLC). Sie besitzen im Gegensatz zu Keramik-, Folien- und Elektrolytkondensatoren kein Dielektrikum im herkömmlichen Sinne. Die Kapazitätswerte dieser Kondensatoren ergeben sich aus der Summe zweier hochkapazitiver Speicherprinzipien:
- aus der statischen Speicherung elektrischer Energie durch Ladungstrennung in Helmholtz-Doppelschichten[4] in einer Doppelschichtkapazität.
- aus der elektrochemischen Speicherung elektrischer Energie durch faradayschen Ladungstausch mit Hilfe von Redoxreaktionen[5] in einer Pseudokapazität.
Doppelschicht- und Pseudokapazität summieren sich in allen elektrochemischen Kondensatoren zu einer Gesamtkapazität. Sie haben jedoch, je nach Ausführung der Elektroden, einen stark unterschiedlichen Anteil an der Gesamtkapazität. Die Pseudokapazität einer dafür geeigneten Elektrode kann beispielsweise bei gleicher Oberfläche um den Faktor 100 größer sein als die Doppelschichtkapazität.[1]
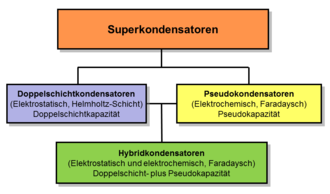
Superkondensatoren gliedern sich, bedingt durch die Ausführung ihrer Elektroden, in drei unterschiedliche Kondensatorfamilien:
- Doppelschichtkondensatoren besitzen Kohlenstoffelektroden oder deren Derivate mit einer sehr hohen statischen Doppelschichtkapazität. Der Anteil der faradayschen Pseudokapazität an der Gesamtkapazität ist nur gering.
- Pseudokondensatoren besitzen Elektroden aus Metalloxiden oder aus leitfähigen Polymeren und haben einen sehr hohen Anteil an faradayscher Pseudokapazität.
- Hybridkondensatoren besitzen asymmetrische Elektroden, eine mit einer hohen Doppelschicht-, die zweite mit einer hohen Pseudokapazität. Zu den Hybridkondensatoren gehören die Lithium-Ionen-Kondensatoren.[6][2][3]
In Superkondensatoren ist der Elektrolyt die leitfähige Verbindung zwischen zwei Elektroden. Das unterscheidet sie von Elektrolytkondensatoren, bei denen der Elektrolyt die Kathode ist und somit die zweite Elektrode bildet.
Superkondensatoren gehören als Industrieprodukte zu den passiven elektronischen Bauelementen und überbrücken die Lücke zwischen Kondensatoren und Akkumulatoren. Sie haben unter den Kondensatoren die höchsten Kapazitätswerte pro Bauelement, die mit bis zu 10.000 F/1,2 V etwa 10.000-fach größer sind als die von Elektrolytkondensatoren.[7]
Im Vergleich zu Akkumulatoren gleichen Gewichts weisen Superkondensatoren nur etwa 10 % von deren Energiedichte auf, allerdings ist ihre Leistungsdichte etwa 10 bis 100-fach größer. Superkondensatoren können deshalb sehr viel schneller ge- und entladen werden. Sie überstehen außerdem sehr viel mehr Schaltzyklen als Akkus und eignen sich deshalb als deren Ersatz oder Ergänzung, wenn eine große Schaltbeanspruchung gefordert wird.
Das Einsatzgebiet von Superkondensatoren reicht von der Bereitstellung kleinster Ströme zum Datenerhalt von statischen Speichern (SRAM) in elektronischen Geräten bis in den Bereich der Leistungselektronik, so zum Beispiel als Speicher elektrischer Energie im KERS-System von Formel-1-Rennwagen oder bei der Rückgewinnung von Bremsenergie (Rekuperation) in Fahrzeugen wie Bussen und Bahnen.
Superkondensatoren sind gepolte Bauelemente, die nur mit korrekter Polarität betrieben werden dürfen. Die Polarität ist bei asymmetrischen Elektroden konstruktiv bedingt, bei symmetrischen Elektroden entsteht sie durch eine Spannnungsbeaufschlagung während der Fertigung.
Außergewöhnlich und kennzeichnend für Superkondensatoren sind die vielen unterschiedlichen Handelsnamen der unterschiedlichen Hersteller, wie z. B.: APowerCap, BestCap, BoostCap, CAP-XX, DLCAP, EneCapTen, EVerCAP, DynaCap, Faradcap, GreenCap, Goldcap, HY-CAP, Kapton capacitor, Super capacitor, SuperCap, PAS Capacitor, PowerStor, PseudoCap, Ultracapacitor.
Geschichte
Entwicklung der wissenschaftlichen Grundlagen
Zur Entwicklung der wissenschaftlichen Grundlagen siehe Elektrochemische Doppelschicht
Entwicklung elektrochemischer Kondensatoren
In den frühen 1950er Jahren experimentierten Ingenieure bei General Electric (GE) mit Geräten für Brennstoffzellen und neuartigen Akkumulatoren, die mit hoch-porösen Kohlenstoffelektroden versehen waren. Aktivkohle ist einerseits ein elektrischer Leiter, besitzt andererseits aber auch mit seiner schwammartigen Struktur eine äußerst große Oberfläche und ist deswegen ideal für Elektroden aller Art verwendbar. Mit solchen Elektroden entwickelte H. I. Becker bei GE in Unkenntnis des wirklichen kapazitiven Prinzips einen „Niederspannungs-Elektrolytkondensator mit porösen Kohlenstoffelektroden“, der 1957 patentiert wurde[8]. Becker glaubte, dass die elektrische Ladung seines neuen hochkapazitiven Kondensators in den Poren des Kohlenstoffs gespeichert wird, ähnlich wie in den Poren aufgerauter Aluminium-Anodenfolien von Elektrolytkondensatoren. In dem Patent wurde daher sinngemäß zum Speicherprinzip geschrieben: „Es ist nicht genau bekannt, was im Bauelement stattfindet, wenn es als Energiespeicher benutzt wird, aber es führt zu einer außerordentlich hohen Kapazität.“[9][10]
Auch in dem neun Jahre später eingereichten Patent von 1966, eines „Energiespeicher-Apparates“ von R. A. Rightmire[11] angemeldet für Standard Oil of Ohio (SOHIO), wo an experimentellen Brennstoffzellen geforscht wurde, wurde die wahre Natur der elektrochemischen Energiespeicherung nicht benannt. Noch 1970 wurde im Patent von Donald L. Boos ein elektrochemischer Kondensator als Elektrolytkondensator mit Aktivkohle-Elektroden[12] angemeldet.
Aufgrund geringer Verkaufszahlen gab SOHIO 1971 das Produkt auf und lizenzierte die Technik an NEC. Inzwischen hatte sich in der Literatur für diese Kondensatoren der Begriff „Doppelschichtkondensator“ etabliert. NEC erkannte die großen kommerziellen Möglichkeiten, die sich durch hohe spezifische Kapazität dieser Kondensatoren ergaben, und vermarkte sie unter dem Begriff „Supercapacitor“. Weitere Hersteller folgten ab dem Ende der 1970er Jahre; aus Gründen des Marketings jeweils mit ihren eigenen Handelsnamen. 1978 brachte Panasonic seine "Goldcaps“[13] und 1987 ELNA seine „DynaCap“[14] genannten EDLCs auf den Markt. Diesen Produkten gemeinsam war ein relativ hoher Innenwiderstand, der zwar den Entladestrom begrenzte, der jedoch für den Strombedarf in Pufferbatterien für SRAM zum Datenerhalt o. ä. hinreichend groß genug war. Damit erzielten diese Doppelschichtkondensatoren ihre ersten größeren Erfolge.[15] In den 1980er Jahren wurden an den Materialien der Kondensatoren deutliche Verbesserungen durchgeführt. Mit neuen Elektrodenmaterialien konnten höheren Kapazitätswerte pro Bauvolumen erreicht werden, und durch leitfähigere Elektrolyte wurde der interne Widerstand verringert, so dass die Lade-Entlade-Ströme erhöht werden konnten. Zusammen mit einer Reduzierung der Kosten entwickelten sich daraus die Superkondensatoren für Leistungsanwendungen. Der erste Superkondensator mit niedrigem Innenwiderstand für Leistungsanwendungen wurde 1982 für militärische Anwendungen durch das Pinnacle Research Institute (PRI) entwickelt und unter dem Namen „PRI Ultracapacitor“ am Markt etabliert. Im Jahre 1992 übernahmen die Maxwell Laboratories diese Entwicklung, ein 1965 als Auftragnehmer der US-Regierung gegründetes Unternehmen, das heute (2012) unter dem Namen Maxwell Technologies bekannt ist. Die aus der Entwicklung von PRI hervorgegangenen „BoostCaps“[3] wurden als „Ultrakondensatoren“ vermarktet und waren die ersten elektrochemischen Kondensatoren für Leistungsanwendungen.
Zwischen 1975 und 1980 betrieb Brian Evans Conway Grundlagenforschung über Redox-Prozesse mit pseudokapazitivem Verhalten an dotierten Ruthenium(IV)-oxid-Elektroden. Er beschrieb 1991 den elektrochemischen Unterschied zwischen Kondensatoren und Akkumulatoren (From Supercapacitor to „Battery“) und prägte 1999 den Begriff „Superkondensator“ (englisch Supercapacitor).[16][1] Conway war damit maßgeblich an der Entwicklung von Pseudokondensatoren beteiligt.
Da der Energieinhalt eines Kondensators mit dem Quadrat der Spannung ansteigt, wurde nach einer Möglichkeit gesucht, die Spannungsfestigkeit elektrochemische Kondensatoren zu erhöhen. Dies gelang 1994 David A. Evans mit seinen „Elektrolytischen-Elektrochemischen Hybrid-Kondensatoren“.[17][18] In diesen für 200 V ausgelegten Kondensatoren wurde eine Anode aus einem Tantal-Elektrolytkondensator verwendet. Die Oxidschicht auf der Tantal-Anode ergab die hohe Spannungsfestigkeit, mit der der Energieinhalt dieses Superkondensators bei gleicher Baugröße etwa um den Faktor 5 höher wurde als ein vergleichbarer Tantal-Elektrolytkondensator. Diese Hybridkondensatoren von Evans,[19] die später auch unter dem Begriff „Capattery“ bekannt wurden, zeichnen sich aus durch eine Kombination einer pseudokapazitiven Metalloxidelektrode (Ruthenium(IV)-oxid) mit einer formierten Anode eines herkömmlichen Elektrolytkondensators, deren jeweilige Oxidschicht (Tantalpentoxid, Aluminiumoxid) die hohe Spannungsfestigkeit ergibt.[20] Diese Kondensatoren sind allerdings recht teuer, sodass sie bislang nur in sehr speziellen militärischen Anwendungen eingesetzt werden.
Die Kopplung einer Elektrode mit hoher Pseudokapazität mit einer weiteren Elektrode mit hoher Doppelschichtkapazität, die „Hybridkondensatoren“ genannt werden, brachte Mitte der 2000er Jahre die weitere Verbesserung bei den Superkondensatoren, sowohl bei der spezifischen Kapazität und Energiedichte als auch bei der Strombelastbarkeit und Leistungsdichte. Es sind dies die Lithium-Ionen-Kondensatoren, die durch den Betrieb bei einem höheren Spannungspegel ihre erhöhte Energiedichte erreichen. Sie wurden 2007 durch FDK erstmals auf den Markt gebracht.[21]
Grundlagen
Prinzipieller Aufbau

Elektrochemische Kondensatoren (Superkondensatoren) bestehen im Prinzip aus zwei Elektroden, die durch einen elektrisch durchlässigen Separator mechanisch voneinander getrennt sind aber durch einen Elektrolyten elektrisch miteinander verbunden sind.[22] Durch Anlegen einer Spannung an den Kondensator bildet sich an beiden Elektroden je eine Helmholtz-Doppelschicht aus, in denen sich je eine Lage positiver und negativer Ionen in spiegelbildlicher Anordnung bildet.
Kapazitätsverteilung
Die beiden Elektroden eines Superkondensators bilden eine Serienschaltung zweier Einzelkondensatoren C1 und C2. Die Gesamtkapazität Cgesamt ergibt sich dann aus der Formel:
Superkondensatoren können entweder mit symmetrischen oder mit asymmetrischen Elektroden aufgebaut sein. Bei symmetrischen Elektroden haben beide Elektroden den gleich großen Kapazitätswert. Das bedeutet, wenn C1 = C2 dann ist Cgesamt = 0,5·C1. Bei symmetrischen Elektroden hat der Kondensator deshalb einen Kapazitätswert, der dem halben Wert einer Elektrode entspricht.
Bei asymmetrischen Elektroden hat eine Elektrode einen meist sehr viel höheren Kapazitätswert als die andere. Das bedeutet, wenn C1 >> C2 dann ist Cgesamt ≈ C2. Bei asymmetrischen Elektroden kann der Superkondensator einen Kapazitätswert erreichen, der dem Wert einer Elektrode entspricht.
Speicherarten
Elektrochemische Kondensatoren besitzen im Gegensatz zu den o.g. konventionellen statischen Kondensatoren kein Dielektrikum im herkömmlichen Sinne. Die elektrische Energie wird auf zwei Elektroden in den jeweiligen Doppelschichten gespeichert. Die Kapazitätswerte dieser Kondensatoren ergeben sich aus der Summe zweier neuer hochkapazitiver Speicherprinzipien, die sich aus dem chemisch-physikalischen Verhalten der Doppelschichten ergeben. Es sind dies die Speicherprinzipien der
- statischen Speicherung elektrischer Energie in einer Doppelschichtkapazität durch Ladungstrennung in den Doppelschichten.[4]
- elektrochemischen Speicherung elektrischer Energie in einer Pseudokapazität durch faradayschen Ladungstausch mit Hilfe von Redoxreaktionen[5]
Doppelschicht- und Pseudokapazität summieren sich in allen elektrochemischen Kondensatoren untrennbar zu einer Gesamtkapazität. Beide Speicherarten sind nur messtechnisch voneinander zu unterscheiden. Sie haben jedoch, je nach Ausführung der Elektroden, einen stark unterschiedlichen Anteil an der Gesamtkapazität.
Statische Doppelschichtkapazität

Jeder elektrochemische Kondensator hat zwei Elektroden, mechanisch getrennt durch einen Separator, die elektrisch über den Elektrolyten miteinander verbunden sind. Der Elektrolyt ist eine Mischung aus positiven und negativen Ionen in einem Lösungsmittel, z. B. Wasser. An jeder der beiden Elektroden gibt es einen Bereich, in dem die Flüssigkeit (Elektrolyt) die metallisch leitende Oberfläche der Elektrode berührt. In dieser Grenzschicht (Phasengrenze) tritt ein ganz besonderes Phänomen auf, der Doppelschichteffekt.
An dieser Phasengrenze entstehen nach dem Anlegen einer Spannung, zwei ionisierte Schichten. Eine Schicht Ionen befindet sich im atomaren Oberflächenbereich der metallisch leitenden Elektrode. Die zweite Schicht aus dissoziierten und solvatisierten Ionen entgegengesetzter Polarität befindet sich im anliegenden Bereich des flüssigen Elektrolyten. Diese beiden Schichten, die „Doppelschicht“,[4] ionisierter elektrischer Ladungen werden getrennt durch eine molekulare Lage aus polaren Molekülen des Elektrolyt-Lösungsmittels, d. h. bei wässrigen Elektrolyten aus Wassermolekülen. Sie haften durch Adsorption fest an der Oberfläche der Elektrode und wirken elektrisch trennend, ähnlich wie das Dielektrikum in einem konventionellen Kondensator. Diese Ladungstrennung in der Doppelschicht durch die molekulare Lage der Lösungsmittelmoleküle bewirkt eine statische Speicherung elektrische Energie in einem elektrischen Feld.

Die Ladungsverteilung an der einen Elektrode findet sich spiegelbildlich an der zweiten Elektrode des Kondensators wieder.
Die Ladungsmenge, d. h. die Anzahl der Ionen, die aus dem Elektrolyten kommend sich durch Anreicherung in einer Doppelschicht ansammeln kann, ist abhängig von der Konzentration der Ionen im Elektrolyten und der Oberfläche der Elektrode. Sie ist bis zu einem Grenzwert, der sog. Zersetzungsspannung des Elektrolyten, linear abhängig von der angelegten Spannung. Steigt die Spannung über die Zersetzungsspannung des Elektrolyten hinaus (siehe auch Elektrolyse), dann bricht die trennende Wirkung der Helmholtz-Doppelschicht zusammen und es entsteht ein Kurzschluss.
Die Helmholtz-Doppelschicht wirkt wie ein Plattenkondensator mit dem Abstand der Dicke eines Lösungsmittelmoleküls. Die Kapazität berechnet sich nach der Formel des Plattenkondensators.
Das bedeutet, die Kapazität „C“ eines Kondensators ist umso größer, je größer die Elektrodenfläche „A“ und die Permittivität „ε“ ist und je dünner das Dielektrikum „d“ ist. Die hoch-aufgeraute sehr große Oberfläche der Elektroden dieser Kondensatoren und die äußerst dünne innere Helmholtz-Schicht in der Größenordnung von einigen Nanometern bewirken zusammen die sehr große Doppelschichtkapazität.[2][3]
Elektrochemische Pseudokapazität
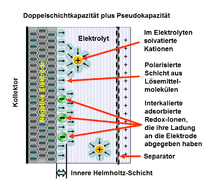
In einer Helmholtz-Doppelschicht können bei bestimmten Strukturen oder Materialien einige Ionen aus dem Elektrolyten die trennende Schicht aus Lösungsmittelmolekülen überwinden und direkt mit der Oberfläche der Elektrode in Kontakt kommen. Bei der damit verbundenen chemischen Reaktion geben sie ein Elektron an die Elektrode ab, es entsteht eine Pseudokapazität, ohne dass dabei eine chemische Verbindung entsteht.
Eine Pseudokapazität speichert elektrischer Energie mit Hilfe von reversiblen Redoxreaktionen an dafür geeigneten Elektroden einem elektrochemischen Kondensator mit einer Helmholtz-Doppelschicht[4] Die Redoxreaktionen sind verbunden mit einem faradayschen Ladungstausch aus den Ionen im Elektrolyten an die metallisch leitenden Ionen in der Elektrode. Dabei ist jeweils nur ein Elektron aus einem desolvatierten und adsorbierten Ion beteiligt. Das adsorbierte Ion geht keine chemische Bindung mit der Elektrode ein. Es findet nur ein Elektronentransfer statt.[1][2][23]
Eine Pseudokapazität tritt immer nur zusammen mit einer Doppelschichtkapazität auf. Sie summieren sich in allen elektrochemischen Kondensatoren untrennbar zu einer Gesamtkapazität.[23]

Die Fähigkeit von Kondensatorelektroden, Redoxreaktionen für eine Pseudokapazität zu bewerkstelligen, hängt sehr stark von der Beschaffenheit und der Struktur des Elektrodenmaterials ab. Elektrodenmaterialien, die pseudokapazitive Eigenschaften aufweisen sind z. B. Metalloxide von Übergangsmetallen, die die zum Teil durch Dotierung in das Elektrodenmaterial eingebracht oder mit Hilfe einer Interkalation eingefügt werden. Auch leitfähige Polymere wie Polyanilin oder Derivate von Polythiophen, die auf die Strukturen von Kohlenstoffelektroden aufgebracht sind, eignen sich für Pseudokondensatoren. Aber auch Kohlenstoffelektroden können eine Pseudokapazität aufweisen.[24] Der Anteil an pseudokapazitiven Reaktionen an Kohlenstoffelektroden kann auch durch maßgeschneiderte Porengrößen deutlich gesteigert werden.[25]
Wie bei Doppelschichtelektroden ergibt sich das Speichervermögen von Pseudokondensatorelektroden aus dem potentialabhängigen Bedeckungsgrad der Elektrodenoberfläche mit adsorbierten Ionen. Da bei allen pseudokapazitiv wirksamen Reaktionen die Ionen desolvatisiert sind, d. h. keine die kugelförmig umhüllende Schicht von Lösungsmittelmolekülen aufweisen, sind sie deutlich kleiner als die solvatisierten Ionen, die zur Doppelschichtkapazität beitragen. Deshalb benötigen sie entsprechend weniger Elektrodenoberfläche. Die Pseudokapazität einer dafür geeigneten Elektrode kann beispielsweise bei gleicher Oberfläche der Elektrode um den Faktor 100 größer sein als die Doppelschichtkapazität.[1][23][26][25][27]
Die Ladungsmenge der in einer Pseudokapazität gespeicherten Energie verhält sich linear zur anliegenden Spannung. Die Einheit der Pseudokapazität ist Farad.
Potentialverlauf


In Keramikkondensatoren und Kunststoff-Folienkondensatoren wird die elektrische Energie in einem Dielektrikum zwischen den Elektroden statisch im elektrischen Feld gespeichert. Das Potential eines aufgeladenen Kondensators fällt intern über das Dielektrikum linear zwischen den Elektroden ab. Dies gilt auch für Elektrolytkondensatoren mit der dünnen Anoden-Oxidschicht als Dielektrikum. Da jedoch der Elektrolyt als Kathode des Kondensators mit einem Widerstand behaftet sein kann, wird sich bei Elkos mit flüssigem Elektrolyten noch ein kleiner Spannungsabfall über diesen internen Widerstand (ESR) bis zur Kathodenfolie ergeben. Bei „Elkos“ mit Polymer-Elektrolyten ist dieser Spannungsabfall jedoch vernachlässigbar.

Das Potential am Superkondensator verteilt sich auf beide Elektroden, der interne Spannungsabfall verläuft symmetrisch über die beiden Doppelschichten, sofern die Elektroden symmetrisch sind. Der Widerstand des Elektrolyten, der leitfähigen Verbindung zwischen den Elektroden, bewirkt im internen Potentialverlauf jedoch noch einen kleinen Spannungsabfall zwischen den Elektroden.
Der Spannungsverlauf an den Anschlüssen beim Laden und Entladen von konventionellen Kondensatoren mit herkömmlichen Dielektrika und auch von Superkondensatoren, verhält sich linear proportional zur gespeicherten elektrischen Ladung. Dieser lineare Spannungsverlauf unterscheidet Kondensatoren grundsätzlich von Akkumulatoren, deren Spannung an den Anschlüssen, unabhängig vom Ladezustand, weitgehend konstant bleibt.
Familienzuordnung

Die Kapazität von Superkondensatoren ergibt sich aus der Summe ihrer Doppelschicht- und Pseudokapazität. Der jeweilige Anteil der jeweiligen Speicherart an der Gesamtkapazität der Kondensatoren ist unterschiedlich und ergibt sich aus dem Material und der Struktur der Elektroden. Daraus ergeben sich drei unterschiedliche Kondensatorfamilien:
- Doppelschichtkondensatoren mit Elektroden aus Aktivkohle oder deren Derivaten, bei denen der Anteil der statischen Doppelschichtkapazität deutlich überwiegt und der Anteil an faradayscher Pseudokapazität sehr gering ist.
- Pseudokondensatoren mit Elektroden aus speziellen Materialien mit überwiegender Pseudokapazität und sehr viel geringerem Anteil an Doppelschichtkapazität.
- Hybridkondensatoren sind überwiegend asymmetrisch aufgebaut und besitzen eine Elektrode mit einer hohen Doppelschicht- und eine zweite mit einer hohen Pseudokapazität. Zu den Hybridkondensatoren gehören die Lithium-Ionen-Kondensatoren.
In einem herkömmlichen Doppelschichtkondensator wird angenommen, dass der Anteil an Pseudokapazität nur etwa 1 bis 5 % beträgt. Bei einem Pseudokondensator und einem Hybridkondensator ist der Anteil an elektrochemischer Pseudokapazität deutlich größer als 5 %.
In den Datenblättern der Hersteller von Superkondensatoren werden Konstruktionsmerkmale von Elektroden oder die Zuordnung des jeweiligen Produktes zu einer dieser genannten Familie nur selten erwähnt.
Aufbau von Superkondensatoren
Konstruktionsmerkmale
- Konstruktionsmerkmale von Superkondensatoren
-
Schematischer Aufbau eines gewickelten Superkondensators
1. Anschlüsse, 2. Sicherheitsventil,
3. Abdichtscheibe, 4. Becher, 5. Positive Elektrode mit: 6. Separator, 7., 8., 9. doppelseitige Elektrode mit zentralem Kollektor, 10. Negative Elektrode -
Schematischer Aufbau eines Superkondensators mit gestapelten Elektroden
1. positive Elektrode, 2. negative Elektrode,
3. Separator
Superkondensatoren besitzen zunächst zwei Metallfolien, den Kollektoren, die die Verbindungen für den elektrischen Strom von den Anschlüssen des Kondensators zu den Elektroden schaffen. Die Kollektoren sind jeweils mit der Elektrode beschichtet. Für Doppelschichtkondensatoren ist die eine etwa 100 bis 500 µm dicke Schicht aus Aktivkohle, die elektrochemisch zu einer schwammartigen Struktur geätzt wird, so dass sich die Oberfläche gegenüber einer glatten Oberfläche etwa um den Faktor 100.000 vergrößert. Die beiden jetzt großflächigen Elektroden werden durch einen porösen, elektrisch durchlässigen Separator mechanisch voneinander getrennt, um sie gegen eine direkte Berührung, die einen Kurzschluss verursachen könnte, zu schützen. Dieser Aufbau, gewickelt oder in mehreren Lagen geschichtet, wird in ein Gehäuse eingebaut und mit einem flüssigen Elektrolyten imprägniert. Der Elektrolyt, ein Ionenleiter, dringt in die Poren der Elektroden ein und bildet über den Separator hinweg eine leitfähige Verbindung zwischen den Elektroden. Das Gehäuse wird anschließend mehr oder weniger hermetisch verschlossen und mit den äußeren Anschlüssen versehen. Es entsteht ein Kondensator mit einer Kapazität im Farad-Bereich.
Bauformen
- Unterschiedliche Bauformen von Superkondensatoren
-
Flache Bauform eines Superkondensators für mobile Geräte
-
Typische Leiterplatten-bestückbare 5 V-„Knopf“-Kondensatoren für den Datenerhalt mit zwei seriellen Zellen in einem Gehäuse
-
Radiale Bauformen (Lithium-Ionen-Kondensatoren) für Leiterplattenmontage
Materialien von Superkondensatoren
Die Eigenschaften von Superkondensatoren werden durch das Zusammenspiel der verwendeten Materialien bestimmt. Die Kombination von Elektrodenmaterial und der Art des Elektrolyten bestimmt die Funktionalität sowie die thermischen und elektrischen Eigenschaften der Kondensatoren. Darüber hinaus wird die Unterscheidung der drei Familien der Superkondensatoren durch die Art der verwendeten Elektroden bestimmt.
Elektroden
Elektroden für Superkondensatoren müssen elektrisch leitfähig sein und sich sowohl elektrisch als auch mechanisch gut mit dem Kollektor kontaktieren lassen. Generell sollten sie zur Erzielung einer möglichst großen Kapazität eine möglichst große Oberfläche bei kleinstem Volumen oder Gewicht haben, denn Elektrodenoberfläche bestimmt in erster Line die Größe des Kapazitätswertes. Außerdem sollten die Elektroden gegenüber dem Elektrolyten chemisch inert und korrosionsbeständig sein sowie eine hohe Temperaturstabilität besitzen. Weitere geforderte Eigenschaften für Elektroden sind Umweltverträglichkeit und geringer Preis.
Elektroden dieser Art werden typischerweise aus speziell behandelten Kohlenstoffen in seinen unterschiedlichen Erscheinungsformen wie z. B. Aktivkohle hergestellt. Dieses poröse Material hat eine schwammartige Struktur, deren innere Oberfläche sich zu einer großen Gesamtoberfläche summiert. Elektroden für eine hohe Pseudokapazität bestehen aus speziell dafür geeigneten Materialien wie Übergangsmetalloxide oder leitfähige Polymere. Auch „maßgeschneiderte“ Porengrößen im Elektrodenmaterial führen zu pseudokapazitiven Reaktionen.
Die Porengröße von Elektroden bestimmt außerdem die Strombelastbarkeit der Superkondensatoren. Sehr kleine Poren haben einen höheren Innenwiderstand mit geringerer Strombelastbarkeit zur Folge, führen aber zu einem höheren Kapazitätswert. Größere Poren gewährleisten einen kleineren Innenwiderstand und somit eine höhere Strombelastbarkeit, haben jedoch einen kleineren Kapazitätswert zur Folge.
Elektroden mit großer Doppelschichtkapazität
Elektroden aus Kohlenstoff weisen eine sehr hohe statische Doppelschichtkapazität auf. Der Anteil an Pseudokapazität an solchen Elektroden ist meist recht gering. Der faradaysche Ladungstausch findet nur an den kantigen Strukturbereichen oder in zufällig vorhandenen Nanoporen mit entsprechender Größe statt. Allerdings kann bei neuen Kohlenstoffmaterialien mit maßgeschneiderten Porengrößen der Anteil an Pseudokapazität stark ansteigen, so dass dann eine eindeutige Zuordnung zu einer Doppelschicht- oder Pseudokapazität nicht mehr gegeben werden kann.
Das am häufigsten verwendete Elektrodenmaterial für Superkondensatoren ist Kohlenstoff in seinen verschiedenen Erscheinungsformen, wie Aktivkohle (AC), Aktivkohlefaser (AFC), Carbid-abgeleiteter Kohlenstoff (CDC), Kohlenstoff-Aerogel, Graphit (Graphen) und Kohlenstoffnanoröhren (CNTs ).[23][26][27][28]
Aktivkohle

Das Elektrodenmaterial in den ersten Doppelschichtkondensatoren bestand aus industriell hergestellter Aktivkohle (englisch activated carbon (AC)). Aktivkohle hat entlang der Kristallebenen des Kohlenstoffs eine elektrische Leitfähigkeit von 1.250 bis 3.000 S/m, das ist nur etwa 0,003 % einer metallischen Leitfähigkeit, aber das ist gut genug für die Verwendung als Elektrodenmaterial von Superkondensatoren.[2][3]
Aktivkohle bildet eine extrem poröse, offenporige Elektrode mit schwammartiger Struktur, die, bezogen auf das Volumen eine extrem große spezifische Oberfläche von etwa 1000 bis 3000 m² pro Gramm hat.[26] Das ist in etwa die Fläche von 4 bis 12 Tennisplätzen oder mit einem anderen Vergleich, 2,5 g Aktivkohle hat eine Oberfläche von ungefähr der Fläche eines Fußballfeldes. Die Dicke der Elektrode beträgt oft nur wenige 100 µm. Eine Elektrode aus Aktivkohle mit einer Oberfläche von etwa 1000 m2/g ergibt eine typische Doppelschichtkapazität von etwa 10 μF/cm² beziehungsweise eine spezifischen Kapazität von 100 F/g.
Aktivkohle ist sehr preiswert herzustellen, ist ungiftig, chemisch inert und korrosionsbeständig. Sie enthält keine die Umwelt schädigenden Stoffe und kann außerdem aus preisgünstigen natürlichen Ausgangsstoffen hergestellt werden.[29] Ab 2010 verwenden praktisch alle kommerziellen Superkondensatoren Aktivkohle in Pulverform, die umweltfreundlich aus Kokosnussschalen hergestellt wird.[30]
Nachteil von Elektroden aus Aktivkohle ist, dass im Gegensatz zu Elektroden aus Nanoröhren nur weniger als 1/3 der Fläche für die Bildung einer Doppelschichtkapazität zur Verfügung steht.[31] Höhere Oberflächenausnutzung mit anderen Kohlenstoffmaterialien sind möglich, allerdings sind diese mit höheren Kosten verbunden.
Elektroden aus Aktivkohle weisen überwiegend eine statische Doppelschichtkapazität auf. Allerdings sind spezielle Kohlen mit Porendurchmessern im Bereich von <2 nm nur zugänglich für de-solvatisierte Ionen und sind deshalb auch pseudokapazitiv wirksam.[23]
Aktivkohlefaser

Aktivkohle kann zu Kohlenstofffasern (englisch activated fiber carbon(AFC)) verarbeitet werden, die einen typischen Durchmesser von etwa 10 µm haben. Die Fasern können für flexible Elektroden zu einem Gewebe versponnen werden. Ein spezielles Gewebe kann kontrolliert mit Mikroporen mit einem Durchmesser von <2 nm hergestellt werden. Mit solch einem Gewebe entstehen Elektrodenoberflächen von etwa 2500 m2/g. Vorteile der Elektroden aus Aktivkohlefasergewebe sind neben der hohen spezifischen Kapazität die gute Leitfähigkeit entlang der Faserachse und der gute elektrische Kontakt zum Kollektor.[26]
Nachteilig der kleinen Porengröße ist die Erhöhung des Leitungswiderstandes im Elektrolyten wodurch die Leistungsdichte geringer wird.[27][22]
AFC-Elektroden weisen zwar überwiegend eine hohe Doppelschichtkapazität auf, können aber wegen der maßgeschneiderten Porengröße auch einen signifikanten Anteil an Pseudokapazität haben.
Kohlenstoff-Aerogel

Kohlenstoff-Aerogel ist ein synthetisches, sehr hoch poröses und ultraleichtes Material aus einem organischen Gel, in dem die flüssige Komponente des Gels durch Pyrolyse mit einem Gas ersetzt wurde. Aerogele werden auch „gefrorener Rauch“ genannt.
Kohlenstoff-Aerogel-Elektroden werden mit der Pyrolyse von Resorcin-Formaldehyd hergestellt.[32][33]
Kohlenstoff-Aerogel hat eine bessere elektrische Leitfähigkeit als Aktivkohle. Es ermöglicht dünne und mechanische stabile Elektroden mit einer Höhe im Bereich von mehreren hundert Mikrometern mit einheitlicher Porengröße. Durch die hohe mechanische Stabilität kann Kohlenstoff-Aerogel als Elektrodenmaterial für Superkondensatoren mit hoher Vibrationsfestigkeit verwendet werden.
In Forschungslaboren sind Elektroden aus Kohlenstoff-Aerogelen entwickelt worden, die eine große Oberfläche von 400 bis 1200 m2/g mit einer spezifischen Kapazität von 104 F/cm³ aufweisen. Diese Elektroden haben sowohl eine sehr hohe Energiedichte von 90 Wh/kg als auch eine große Leistungsdichte mit 20 W/g.[34][35]
2013 wurde ein Graphen-Aerogel mit einer Dichte von nur 0,16 mg/cm³ entwickelt. Es ist das bisher leichteste Material das jemals hergestellt wurde.[36]
Aerogel-Elektroden für Superkondensatoren können auch beschichtet oder dotiert werden, sind dann also dem Bereich der Kompositelektroden zuzuordnen.[37]
Carbid-abgeleitete Kohlenstoffe

Carbid-abgeleitete Kohlenstoffe, (englisch carbide-derived carbons (CDC)), auch „abstimmbare nanoporöse Kohlenstoffe“ (englisch tunable nanoporous carbons) genannt, bestehen aus einer Anzahl von Stoffen, die aus Carbiden wie z. B. Siliciumcarbid und Titancarbid durch thermische Zersetzung oder durch chemische Halogenierung in reinen Kohlenstoff umgewandelt wurden.[38][39]
Elektroden aus CDC besitzen große Oberflächen mit maßgeschneiderten Porengrößen. Sie können mit Porengrößen im Bereich von Mikroporen bis Mesoporen hergestellt werden. Poren mit Porendurchmessern von <2 nm erhöhen die Pseudokapazität der Elektrode deutlich, weil de-solvatisierte Ionen, die in die kleinen Poren der CDC-Elektrode eindringen können, sehr viel kleiner als Ionen mit ihrer Solvatisationshülle sind, wodurch die Packungsdichte interkalierten Ionen ansteigt, die durch faradayschen Ladungstausch die Pseudokapazität generieren. Diese CDC-Elektroden haben eine um 75 % höhere Energiedichte als herkömmliche Elektroden aus Aktivkohle.
2013 wurden diese Elektroden in Superkondensatoren mit der Kapazität von 4.000 F und einer Energiedichte von 8.3 Wh/kg verwendet. Sie erreichten eine Zyklusfestigkeit von 1 Million Lade-Entlade-Zyklen.[40]
Graphen

Graphen besteht aus einem zweidimensionalen hexagonalen (honigwabenförmigen) Gitter aus Kohlenstoffatomen. Mehrere Lagen Graphen übereinander ergeben Graphit. Graphen kann als ultradünne Schicht ähnlich Papier hergestellt werden.[41][42]
Graphen hat eine hohe Leitfähigkeit von >1700 S/m und besitzt eine sehr große gravimetrische Oberfläche von 2630 m2/g, mit der theoretisch Superkondensatoren mit einer Kapazität von 550 F/g hergestellt werden können.[43]
Eine Entwicklung im Jahre 2012 nutzt die gute Leitfähigkeit der flächigen Graphenschicht direkt als Elektrode ohne Kollektor eines extrem flachen Superkondensators für portable Anwendungen.[44]
Graphenschichten können gekrümmt werden und so zerknüllt gepackt werden, dass zwischen den Schichten Mesoporen gebildet werden und sie nicht, ähnlich wie Graphit, flächig übereinanderliegen. Die Poren sind relativ groß und somit für die Ladungsträger leicht zugänglich, wodurch ein sehr schnelles Laden/Entladen möglich ist. Damit könnten Superkondensatoren mit Graphenelektroden für 100/120 Hz-Filter-Anwendungen geeignet sein. Eine Anwendung, die bisher nicht für Superkondensatoren erreichbar war.[45]
Superkondensatoren mit Graphen-Elektroden erreichten in einer Entwicklung die recht hohe spezifische Energiedichte von 85,6 Wh/kg bei Raumtemperatur.[46][47] [48]
Graphen kann im Jahre 2013 als Labormuster in verschiedenen Laboren hergestellt werden, ist aber noch nicht in großen Mengen verfügbar.
Kohlenstoffnanoröhren

Kohlenstoffnanoröhren (englisch carbon nanotubes, (CNT)) sind zu zylindrischen Nanoröhren umgeformte Graphenschichten. Es gibt einwandige Nanoröhren (englisch single wall nano tubes, (SWNT)) und mehrwandige Nanoröhren (englisch carbon nanotubes, (CNT)), bei denen mehrere einwandige Nanoröhren koaxial ineinander verschachtelt angeordnet sind. Die Durchmesser der SWNTs können variieren und liegen im Bereich der Mikroporen bis Mesoporen mit Werten zwischen 1 bis 3 nm. Die Nanoröhren können direkt auf ein Substrat aufwachsen, das als Kollektor dienen kann, z. B. auf einem Siliziumwafer, wodurch die gute elektrische Leitfähigkeit des Kohlenstoffs in Achsrichtung zur Erhöhung der Leistungsdichte führt.
Im Vergleich zu der theoretisch maximalen Elektrodenoberfläche von Aktivkohle (3000 m2/g) besitzen CNT-Elektroden nur eine moderate Oberfläche von etwa 1315 m2/g. Wegen der besseren Benetzbarkeit haben CNT-Elektroden dennoch eine höhere Kapazität als Aktivkohle-Elektroden, z. B. 102 F/g für MWNT- und 180 F/g für SWNT-Elektroden.[49] Es wird erwartet, dass Superkondensatoren mit CNT-Elektroden eine Energiedichte von 21 Wh/kg bei der Nennspannung von 2,7 V erreichen werden.[50][51][52][53].
Ähnlich wie bei CDC-Elektroden kann die Porengröße von Matten aus einwandigen oder mehrwandigen Nanoröhren präzise an die Ionendurchmesser aus dem Elektrolyten angepasst werden, um den Anteil an Pseudokapazität zu erhöhen.[54] Allerdings verursacht die wiederholte Interkalation während der Lade- und Entladevorgänge eine Volumenänderung, die die mechanische Stabilität der Poren verringert, so dass die Zyklusfestigkeit von Superkondensatoren mit CNT-Elektroden noch begrenzt ist. Die Forschung ist dabei, dieses Verhalten zu verbessern.[55][56]
Elektroden mit Kohlenstoffnanoröhren eignen sich gut für besonders flache Bauformen, die typische mechanische Höhe einer Nanoröhrenelektrode ist ca. 20 bis 100 µm.[57]
Zurzeit (2013) ist die Herstellung von SWNTs noch deutlich kostenintensiver als diejenige vom MWNTs. Auch findet eine Massenfertigung von Superkondensatoren mit CNT-Elektroden noch nicht statt.
Elektroden mit großer Pseudokapazität
Elektroden aus Oxiden von Übergangsmetallen oder aus leitfähigen Polymeren haben die Eigenschaft, neben einer Doppelschichtkapazität auch vermehrt Redoxreaktionen verbunden mit faradayschem Ladungstausch hervorrufen zu können. Sie sind die Voraussetzung für Pseudokondensatoren, das sind Superkondensatoren mit überwiegender Pseudokapazität.
Übergangsmetalloxide
Am besten erforscht und verstanden durch die Untersuchungen von B. E. Conway sind die Übergangsmetalloxide, die als Elektroden eine hohe Pseudokapazität bewirken können. Viele Oxide von Übergangsmetallen sind In der Lage, Redox-Reaktionen mit faradayschem Ladungstransfer zu bewerkstelligen. Dazu gehören die Oxide von Ruthenium (RuO2), Iridium (chem|IrO2), Eisen (Fe3O4), Mangan (MnO2). Aber auch Schwefelverbindungen wie z. B. Titansulfide (TiS2) oder deren Kombinationen sind in der Lage Pseudokapazitäten zu bilden.[58]
Ruthenium(IV)-oxid in Kombination mit Schwefelsäure H2SO4 als Elektrolyt bietet eines der besten Beispiele für die Pseudokapazität. Diese Kombination hat eine etwa 10fach höhere spezifische Kapazität von 720 F/g, eine etwa 5fach höhere gravimetrische Energiedichte von 26.7 Wh/kg verglichen mit Elektroden aus Aktivkohle.[59]
Weitere Vorteile dieser Elektroden sind die gute elektrische Leitfähigkeit sowie die hohe Zyklusfestigkeit von mehr als einer Million Zyklen. Wegen des recht hohen Preises werden solche Pseudokondensatoren jedoch nur für militärische Anwendungen hergestellt.[60]
Elektroden aus weniger teuren Oxiden wurden vielfältig untersucht, am meisten Elektroden aus Mangandioxid (MnO2). Bisher (2013) wurde jedoch keine dieser untersuchten Elektroden kommerziell in Superkondensatoren eingesetzt.[61]
Leitfähige Polymere
Ein anderes Elektrodenmaterial mit hoher Pseudokapazität sind leitfähige Polymere wie beispielsweise Polypyrrol, Polyanilin, Pentacen oder Polythiophen. Diese Elektroden sind preiswert und führen aufgrund der zusätzlichen Pseudokapazität zu der deutlich höheren spezifischen Kapazität von etwa 450 F/g.[62]
Die mit leitfähigem Polymer hergestellten Elektroden sind allerdings empfindlich gegen Überspannungen. Bei zu hohen Spannungen oxidieren diese Materialien und werden dadurch dauerhaft zerstört.[63]
Pseudokondensatoren weisen außerdem aufgrund chemischer Instabilitäten bei ihren elektrochemischen Reaktionen eine verringerte Zyklusfestigkeit von etwa 104 bis 105 Zyklen gegenüber Doppelschichtkondensatoren von etwa 106 Zyklen auf.[64] Jedoch sind sie damit immer noch deutlich zyklusfester als Akkumulatoren.
Elektroden für Hybridkondensatoren
Alle am Markt erfolgreichen Hybrid-Superkondensatoren sind asymmetrisch aufgebaut. Sie verbinden die statische elektrische Energiespeicherung in einer Doppelschichtkapazität mit einer faradayschen Energiespeicherung durch Ladungstausch durch Kopplung einer Doppelschicht-Elektrode mit einer Elektrode mit hoher Pseudokapazität. In Hybridkondensatoren gibt die Elektrode für die Pseudokapazität eine hohe Energiedichte während die Doppelschichtelektrode eine hohe Leistungsdichte erbringt.
Der asymmetrische Aufbau von Hybridkondensatoren kombiniert zwei Elektroden mit unterschiedlicher Kapazität. Deshalb verteilt sich die Gesamtkapazität des Kondensators entsprechend der jeweiligen Einzelkapazität seiner Elektroden nach der Formel der Serienschaltung zweier Kondensatoren, siehe #Kapazitätsverteilung. Damit kann sich die Kapazität des asymmetrischen Hybridkondensators gegenüber einem symmetrischen Doppelschichtkondensator verdoppeln.
Die pseudokapazitiven Elektroden haben zwar generell eine höhere Kapazität und kleinere interne Widerstande, jedoch ist ihre Spannungsfestigkeit und vor allen bei Elektroden aus leitfähigen Polymeren ihre Zyklusfestigkeit geringer als die von Doppelschichtelektroden. Der asymmetrische Aufbau der Hybridkondensatoren lindert diese Nachteile und schafft die Voraussetzung für höhere Energie- und Leistungsdichte sowie für eine bessere Zyklusfestigkeit.
In Hybridkondensatoren werden überwiegend Kompositelektoden oder Elektroden aus dem Bereich der Akkumulatoren eingesetzt, die asymmetrische Kopplung einer Doppelschicht- und einer reinen Pseudoelektrode gehört mehr in den Bereich der Forschung.
Kompositelektroden
Kompositelektroden bestehen aus dem Basismaterial Kohlenstoff, das mit pseudokapazitiv aktivem Material beschichtet ist,[65] oder in deren atomares Gefüge pseudokapazitiv aktives Material eingefügt ist. Diese Kombination verleiht der Elektrode sowohl eine hohe Doppelschichtkapazität als auch eine hohe Pseudokapazität. Die sich daraus ergebende Gesamtkapazität ist deutlich höher als bei einem reinen Doppelschichtkondensator.
Der Anteil an Pseudokapazität bei Kompositelektroden kann durch maßgeschneiderte Porengröße und die damit verbundene Interkalation desolvatisierter Ionen noch erhöht werden. Besonders vielversprechend sind Neuentwicklungen mit Kohlenstoffnanoröhren. CNTs mit Polypyrrol-Einlagerungen oder Beschichtungen erreichen eine sehr gute Benetzbarkeit mit dem Elektrolyten und eine gleichmäßige dreidimensionale Verteilung der elektrischen Ladung. Darüber hinaus hat die Struktur beschichteter Kohlenstoffnanoröhren gezeigt, dass die mechanischen Beanspruchungen durch die faradayschen Lade- und Entladevorgänge geringer als bei reinen redoxaktiven Polymer-Elektroden ausfallen, wodurch eine größere Zyklenstabilität erreicht wird.[66]
Kompositelektroden können jedoch auch mit einem pseudokapazitiv aktiven Material dotiert werden. Das erfolgt in Entwicklungen von CNT-Kompositelektroden, die beispielsweise Übergangsmetalloxide wie RuO2, IrO2, MnO2 oder Nitride von Molybdän, Titan und Eisen als pseudokapazitiv aktives Material verwenden. Solche Kompositelektroden erreichen spezifische Kapazitätswerte im Bereich von 150 bis 250 μF/cm².[67]
Bereits im Handel sind Hybridkondensatoren mit Kompositelektroden, die mit Lithium-Ionen dotiert sind. In diesen Elektroden werden die relativ kleinen Lithium-Atome im Kohlenstoff zwischen den Ebenen „eingelagert“, es entsteht eine Interkalationsverbindung (z. B. LixnC).[68] die zu einer großen Pseudokapazität führt. Mit dieser Dotierung wird bei diesen Lithium-Ionen-Kondensatoren eine Vorspannung der Elektrode erzeugt, die die Nennspannung des Kondensators auf 3,8 bis 4 V anhebt. Die höhere Spannung bewirkt die deutlich höhere Energiedichte der Li-Ionen-Kondensatoren gegenüber Standard-Superkondensatoren.[15]
Batterie-Elektroden
Die Entwicklung von Elektroden neuartiger Akkumulatoren, hier aufgrund einer umgangssprachlichen Verallgemeinerung „Batterie-Elektroden“ genannt, hat einen großen Einfluss auf die Elektroden von Superkondensatoren.
Die Entwicklung des Lithium-Ionen-Akkus mit Kohlenstoffelektroden 1985 durch Akira Yoshino beispielsweise hatte zur Folge, dass im Bereich der Superkondensatoren ebenfalls Elektroden entwickelt wurden, die mit Lithium-Ionen dotiert waren. Daraus entstanden dann die Lithium-Ionen-Kondensatoren. Aus den einstmaligen Batterie-Elektroden wurden Elektroden für Superkondensatoren, die dann aber in die Definition der Kompositelektroden fallen.
Elektrolyt
Der Elektrolyt in Superkondensatoren, die elektrisch leitfähige Verbindung beider Elektroden, bestimmt das Spannungsfenster, in dem der Kondensator betrieben werden kann, seinen Temperaturbereich, den Innenwiderstand (ESR) und über seine Stabilität auch das Langzeitverhalten des Kondensators.
Ein Elektrolyt besteht immer aus einem Lösungsmittel mit gelösten Chemikalien, die in positive Kationen und negative Anionen dissoziieren und dadurch seine Leitfähigkeit bewirken. Je mehr Ionen der Elektrolyt enthält, desto besser ist seine Leitfähigkeit. Der Elektrolyt muss in die porige, schwammartige oder vernetzte Struktur der Elektroden eindringen können, seine Viskosität muss klein genug sein, um die Elektrodenoberfläche voll benetzen zu können. Er muss außerdem chemisch inert sein und darf die Materialien des Kondensators chemisch nicht angreifen. Aus dem Bereich der Anwendungen kommen dann die anderen Anforderungen an den Elektrolyten, der gewünschte Temperaturbereich und die geforderte Spannungsfestigkeit. Einen idealen Elektrolyten gibt es nicht, die Eigenschaften eines Elektrolyten sind immer ein Kompromiss aus Leistungsvermögen und Anforderungsprofil.
Der Elektrolyt hat außerdem Einfluss auf die Kapazität einer Elektrode. Bei gleichem Elektrodenmaterial aus Aktivkohle wird beispielsweise mit einem wasserhaltigen Elektrolyten eine Kapazität von 160 F/g erreicht. Mit einem Elektrolyten, der auf einem organischen Lösungsmittel beruht, wird jedoch nur eine Kapazität von 100 F/g erreicht.[27]
Wasser ist ein relativ gutes Lösungsmittel für anorganische Chemikalien. Mit Säuren wie Schwefelsäure (H2SO4), Alkalien wie Kaliumhydroxid (KOH) oder Salzen, wie quartäre Phosphoniumsalze, Natriumperchlorat (NaClO4), Lithiumperchlorat (LiClO4) oder Lithiumhexafluoridoarsenat (LiAsF6) versetzt, können relativ hohe Leitfähigkeitswerte von etwa 100 bis 1000 mS/cm erreicht werden. Preiswerte wasserhaltige Elektrolyte haben aber eine Spannungsfestigkeit von nur 1,15 V pro Elektrode (2,3 V per Kondensator) und einen relativ kleinen Betriebstemperaturbereich. Wasserhaltige Elektrolytsysteme werden überwiegend in Superkondensatoren mit geringer Energiedichte, aber hoher Leistungsdichte eingesetzt.
Elektrolyte mit organischen Lösungsmitteln wie Acetonitril, Propylencarbonat, Tetrahydrofuran, Diethylcarbonat, γ-Butyrolacton und Lösungen mit quaternären Ammoniumsalzen oder Alkylammoniumsalzen wie z. B. Tetraethylammoniumtetrafluoroborat (N(Et)4BF4,[69]) oder Triethyl(metyl)ammoniumtetrafluoroborat (NMe(Et)3BF4) sind teurer als wässrige Elektrolyte, haben aber eine höhere Spannungsfestigkeit von typisch 1,35 V pro Elektrode (2,7 V pro Kondensator) und einen höheren Temperaturbereich. Ihre Leitfähigkeit von etwa 10 bis 60 mS/cm führt zwar zu einer geringeren Leistungsdichte, da jedoch die Energiedichte mit dem Quadrat der Spannung ansteigt, haben Superkondensatoren mit organischen Lösungsmittelelektrolyten eine etwas höhere Energiedichte als EDLCs mit wässrigen Elektrolyten.[70]
Separatoren
Separatoren sollen die beiden Elektroden mechanisch voneinander trennen um einen Kurzschluss zu verhindern. Sie können sehr dünn sein (wenige hundertstel Millimeter)[71] und müssen sehr porös sein um möglichst wenig zum Innenwiderstand (ESR) des Kondensators beizutragen. Außerdem müssen sie chemisch inert sein, um den Einfluss auf die Langzeitstabilität und die Leitfähigkeit des Elektrolyten gering zu halten. Preiswerte Lösungen verwenden offene Kondensatorpapiere als Separatoren, professionelle Superkondensatoren verwenden poröse Kunststofffolien, Glasfasergewebe oder poröse Keramikgewebe als Separatoren.[6]
Kollektoren und Gehäuse
Die Kollektoren (Stromsammler) dienen dem elektrischen Kontaktieren des Elektrodenmaterials und verbinden diese mit den Anschlüssen des Kondensators. Sie müssen eine gute Leitfähigkeit besitzen, immerhin sollen Spitzenströme von bis zu 100 A problemlos auf die Kondensatorzelle verteilt bzw. von ihr abgenommen werden. Sofern das Gehäuse wie üblich aus einem Metall besteht, sollten Kollektoren und Gehäuse aus demselben Material bestehen, meist Aluminium, weil sich sonst in Anwesenheit eines Elektrolyten eine galvanische Zelle bilden würde, die zu Korrosion führen könnte. Die Kollektoren werden entweder in einem Sprühverfahren auf die Elektroden aufgesprüht oder bestehen aus einer Metallfolie, auf der die Elektrode angebracht ist.
Elektrische Eigenschaften
Kapazität
Die Kapazität von Superkondensatoren ergibt sich aus der Reihenschaltung der beiden Elektroden C1 und C2, siehe #Kapazitätsverteilung.
Einfluss der Porenstruktur auf die Kapazität


Die Beweglichkeit der Ladungsträger im Elektrolyten ist begrenzt. In der porigen Struktur der Elektroden müssen sie unterschiedlich lange Wege durchlaufen. Im ersten Bereich der Pore sind sie schneller am Ort ihrer Bestimmung als am Ende einer Pore. Die in die Poren eindringenden Ionen erhöhen nach und nach die Kapazität, dabei muss der fließende Strom einen immer größer werdenden Leitungswiderstand überwinden. Beim Ausschalten des Kondensators erfolgt der gleiche zeitliche Verlauf in entgegengesetzter Richtung.
Die kapazitiven Eigenschaften, die sich daraus ergeben, lassen sich elektrisch recht gut mit einer Reihenschaltung hintereinandergeschalteter RC-Glieder beschreiben. Um also die gesamte Kapazität des Kondensators messen zu können, müssen alle Einzelkapazitäten über die seriellen RC-Zeitkonstanten zusammengefasst werden. Somit wird der Gesamtwert der Kapazität eines Superkondensators nur mit einer Messung erfassbar, die das zeitliche Verhalten der Ionenbeladung mit erfasst und somit sehr zeitaufwendig ist. Zum Vergleich der Messergebnisse muss solch eine Messung genormt sein.
Nennkapazitäts-Messbedingungen

Die Kapazität handelsüblicher Superkondensatoren wird in den Datenblättern als Nennkapazität CN (englisch Rated capacitance CR) spezifiziert. Das ist der Kapazitätswert, für den der Kondensator gefertigt ist. Der Nennkapazitätswert ist mit einer Toleranz, meist 20 %, versehen und muss innerhalb dieses Toleranzbereiches liegen. Die typischen Kapazitätswerte von Superkondensatoren liegen im Farad (F) Bereich.
Die Kapazität von Superkondensatoren kann wegen des stark zeitabhängigen Ladeverhaltens nicht mit einer Wechselspannung, so wie es bei konventionellen Kondensatoren der Fall ist, gemessen werden. Sie wird deshalb aus dem Energieinhalt W eines mit der Ladespannung ULade geladenen Kondensators ermittelt:
Dazu wird der Kondensator zunächst mit einer Konstantstromquelle auf seine Nennspannung geladen. Danach wird der Kondensator 30 Minuten auf diesem Spannungswert gehalten und dann mit einem definierten Entladestrom IEntlade entladen, wobei dann die Zeit ermittelt wird, die vergeht, in der die Spannung von 80 % auf 40 % der Nennspannung abfällt, siehe Bild rechts.
Der Wert des Entladestromes richtet sich nach der Applikation, für die die Superkondensatoren vorgesehen werden. Die Norm IEC 62391-1 definiert hier vier Klassen:
- Klasse 1, Erhalt von Speichern, Entladestrom in mA = 1·C (F)
- Klasse 2, Energiespeicherung, Entladestrom in mA = 0,4·C (F)·U (V)
- Klasse 3, Leistungsanwendungen, Entladestrom in mA = 4·C (F)·U (V)
- Klasse 4, Momentanleistung, Entladestrom in mA = 40·C (F)·U (V)
Die Kapazität C ergibt sich dann aus der Formel:
Die so ermittelte Kapazität wird auch „Gleichspannungskapazität“ genannt.
Die Messverfahren, die von den einzelnen Herstellern spezifiziert werden, stimmen weitgehend mit dem nach den IEC Normen 62391-1 und -2 überein.[72][73].
Frequenzabhängigkeit der Kapazität

Das genormte Messverfahren zur Messung der Kapazität ist sehr zeitaufwendig. In der industriellen Produktion können Superkondensatoren mit diesen Verfahren nicht überprüft werden. Die spezifizierte Nennkapazität wird deshalb mit einem sehr viel schnelleren Messverfahren mit einer kleinen Messfrequenz als Wechselspannungskapazität gemessen und mit Hilfe eines Korrelationsfaktors berechnet. Allerdings ist die Kapazität eines Superkondensators sehr stark frequenzabhängig. Schon bei einer Messfrequenz von 10 Hz fällt der Messwert auf nur etwa 20 % des Gleichspannungswertes ab. Der Korrelationsfaktor kann deshalb nur mit sehr viel Erfahrungen und Vergleichen festgelegt werden.
Die starke Zeitabhängigkeit der Kapazität bedingt durch die begrenzte Ladungsträgerbeweglichkeit hat in der Praxis zur Folge, dass in vielen Anwendungen, besonders bei hohen Spitzenstrombelastungen, der Nennkapazitätswert des Kondensators der Schaltung nicht zur Verfügung steht. Um den in der Anwendung benötigten Kapazitätswert zu berechnen hat sich für Anwendungen mit hoher Strombelastung als sinnvoll herausgestellt, von der benötigten Energie WAnwendung auszugehen und dann den Spannungsabfall ΔU am Kondensator praxisgerecht abzuschätzen, beispielsweise als Spannungsabfall von 0,9 UR auf 0,4 UR. Dann errechnet sich die benötigte Kapazität mit:
Spannungsfestigkeit

Superkondensatoren arbeiten mit sehr niedrigen Betriebsspannungen im Spannungsbereich von nur einigen Volt. Weil schon geringe Überspannungen den Kondensator irreparabel schädigen können, ist die Einhaltung der in den Datenblättern spezifizierten Spannung von großer Bedeutung. Diese Spannung ist die Nennspannung UN (englisch Rated voltage UR). Sie ist die maximale Gleichspannung oder Spitzenwert der Impulsspannung, die dauernd innerhalb des spezifizierten Temperaturbereiches am Kondensator anliegen darf.
Die Nennspannung ist so spezifiziert, dass sie einen Sicherheitsabstand gegenüber der chemisch bedingten Zersetzungsspannung des Elektrolyten aufweist. Die Zersetzungsspannung ist die Spannung, bei der die Moleküle des Elektrolyt-Lösungsmittels zerbrechen. Wasser zersetzt sich dann in Wasserstoff und Sauerstoff. Das Überschreiten der Zersetzungsspannung führt zur Gasbildung und kann zur Zerstörung des Kondensators führen.
Standard Superkondensatoren mit wasserhaltigen Elektrolyten werden üblicherweise mit Nennspannungswerten von 2,1 bis 2,3 V spezifiziert, Kondensatoren mit Lösungsmittelelektrolyten mit Nennspannungen von 2,5 bis 2,7 V. Bei einigen Hybridkondensatoren wie z. B. Lithium-Ionen-Kondensatoren mit dotierter Anode wird eine Spannungsfestigkeit von 3,8 bis 4 V erreicht, wobei jedoch, bedingt durch die Dotierung, eine untere Spannungsgrenze von etwa 2,2 V nicht unterschritten werden darf.
Die Nennspannung von Superkondensatoren ist der Regel kleiner als die erforderliche Betriebsspannung in der Anwendung. Um die erforderliche Betriebsspannung zu erzielen, ist es notwendig, Superkondensatoren in einer Reihenschaltung miteinander zu verbinden. Da jeder Kondensator kleine Unterschiede in seinen Eigenschaften gegenüber den anderen Exemplaren aufweist, z. B. beim ESR-Wert, ist es notwendig, die Kondensatoren mit einer aktiven oder einer passiven Symmetrierung auszubalancieren. Passive Symmetrierung kann mit Widerständen erfolgen, bei aktiver Symmetrierung sorgt eine elektronische Steuerschaltung für die gleichmäßige Verteilung der Kondensatorspannungen.
Innenwiderstand

Das Laden oder Entladen eines Superkondensators ist verbunden mit einer Polarisierung der Ionen im Elektrolyten und einer Bewegung der Ladungsträger durch den Separator hindurch bis tief in die Poren der Elektroden hinein. Bei dieser Bewegung der Ionen im Elektrolyten treten Verluste auf, die als Innenwiderstand des Kondensators gemessen werden können. Der Innenwiderstand hängt stark von der Zusammensetzung des Elektrolyten ab und ist Baureihen und Hersteller spezifisch.
Mit dem elektrischen Modell seriell geschalteter RC-Glieder, siehe #Kapazität, lässt sich dabei leicht erklären, dass der Innenwiderstand von Superkondensatoren mit zunehmender Eindringtiefe der Ladungsträger in die Poren der Elektroden zeitverzögert zunimmt. Da die Ladungsträgerbeweglichkeit begrenzt ist, ist nicht nur die Kapazität sondern auch der Innenwiderstand zeitabhängig und damit auch stark frequenzabhängig.
Der wirksame Innenwiderstand eines Superkondensators, der Innenwiderstand Ri, mitunter auch ESRDC genannt, wird über den Spannungsabfall ΔU2, der sich aus dem Schnittpunkt der Verlängerung des graden Abschnitts der Entladespannung mit der Entladekurve zum Zeitpunkt des Entladebeginns ergibt, nach folgender Formel berechnet:
Als Entladestrom für die Messung des Innenwiderstandes gilt der Strom nach der Klasseneinteilung gemäß IEC 62391-1, siehe #Kapazität. Der so ermittelte Wert ist ein Gleichstromwiderstand.
Der Gleichstromwiderstand darf nicht verwechselt werden mit dem ESR oder auch ESRAC (englisch Equivalent Series Resistance, ESR). Der ESR ist ein Wechselstromwiderstand, der mit 1 kHz, vereinzelt auch mit 100 Hz, gemessen wird und einen deutlich kleineren Widerstandswert aufweisen kann. Da die Messung mit einem kleinen Wechselstrom deutlich schneller durchgeführt werden kann, dient sie in den Endmessungen nach der Fertigung der Kondensatoren als Referenz, die mit Hilfe von Korrelationsfaktoren auf den Gleichstrom-Innenwiderstand umgerechnet wird.
Der Innenwiderstand Ri bestimmt mehrere Eigenschaften von Superkondensatoren. Er begrenzt zum einen die Lade- bzw. Entladegeschwindigkeit des Kondensators. Zusammen mit der Kapazität C des Kondensators ergibt sich die Zeitkonstante τ mit
Diese Zeitkonstante bestimmt die zeitliche Grenze, mit der ein Kondensator ge- bzw. entladen werden kann. Ein 100-F-Kondensator mit dem Innenwiderstand von 30 mΩ hat z. B. eine Zeitkonstante von 0,03 · 100 = 3 s, d. h., nach 3 s Laden mit einem nur durch den Innenwiderstand begrenzten Strom hat der Kondensator 62,3 % der Ladespannung erreicht. Da bis zum vollständigen Laden des Kondensators eine Zeitdauer von etwa 5 benötigt wird, hat die Spannung dann nach etwa 15 s die Ladespannung erreicht.
Der Innenwiderstand Ri ist aber auch der begrenzende Faktor, wenn mit Superkondensatoren der Vorteil der schnellen Lade-/Entladefähigkeit gegenüber Akkumulatoren ausgenutzt werden soll. Denn bei den sehr hohen Lade- und Entladeströmen I, die bei Leistungsanwendungen von Superkondensatoren auftreten, treten interne Verluste Pv auf,
die über den Innenwiderstand Ri zu einer Erwärmung des Kondensators führen. Diese Erwärmung ist die Hauptursache für die größenmäßige Begrenzung der Lade- und Entladeströme bei den Superkondensatoren, insbesondere bei häufig auftretenden Lade- und Entladevorgängen.
Da bei Superkondensatoren keine Reaktionen, die zu chemischen Bindungen führen, auftreten, ist der Innenwiderstand Ri deutlich kleiner als der von Akkumulatoren.
Energie- und Leistungsdichte


Die maximale Energie Wmax, die von einem Superkondensator mit der Kapazität Cmax und der anliegenden Spannung Umax gespeichert werden kann, errechnet sich nach der Formel:
Die Energiedichte ist davon abgeleitet das Maß der speicherbaren elektrischen Energie. Sie wird entweder auf die Masse des Kondensators bezogen und als gravimetrische Energiedichte in Wh/kg oder bezogen auf das Volumen als volumetrische Energiedichte in Wh/cm³ oder Wh/l angegeben.
Die Energiedichte von Superkondensatoren ist ein wichtiger Kennwert zum Vergleich mit Akkumulatoren. In der Realität erreichen bislang (2013) die in Datenblättern der Hersteller publizierten Werte der Energiedichte von Superkondensatoren mit Werten zwischen 0,5 bis etwa 15 Wh/kg bei weitem noch nicht die Werte von Akkumulatoren. Zum Vergleich: Eine herkömmliche Blei-Säure-Batterie speichert typischerweise 30 bis 40 Wh/kg und moderne Lithium-Ionen-Batterien etwa 100 bis 265 Wh/kg. Das bedeutet, Superkondensatoren speichern nur etwa ein Zehntel der Batterien.
Mit einem Ragone-Diagramm werden die Angaben der Leistungsdichte und der Energiedichte von Bauelementen visualisiert, um einen schnellen Vergleich der Werte auch mit anderen Technologien zu ermöglichen.
In der Praxis ist die maximale Energie, die in einem Kondensator laut Datenblatt gespeichert ist, nicht verfügbar, Sie reduziert sich noch um den Spannungsabfall über den Innenwiderstand und um den verbleibenden Rest an Energie, der auch nach längerer Entladung noch im Kondensator verbleibt. Die sich damit ergebende nutzbare (effektive) Energie Weff errechnet sich dann mit:[49]
Obwohl bei den Superkondensatoren die Energiedichte geringer als bei Akkus ist, haben die Kondensatoren einen wichtigen Vorteil, ihre Leistungsdichte ist deutlich größer. Mit der Angabe der Leistungsdichte wird die Geschwindigkeit, mit der die Energie an eine Last geliefert oder von einer Energiequelle aufgenommen werden kann, definiert.
Die Leistungsdichte ist durch die Wärmeentwicklung bei der Strombelastung über den Innenwiderstand bestimmt. Hohe Leistungsdichten ermöglichen Energiespeicher-Anwendungen zur Pufferung von Verbrauchern, die kurzzeitig einen hohen Strom benötigen oder abgeben, beispielsweise bei der Nutzbremsung oder in USV-Anlagen.
Die maximale Leistung Pmax eines Kondensators errechnet sich mit der anliegenden Spannung U und dem Innenwiderstand Ri nach der Formel:
Auch die Leistung eines Superkondensators wird entweder auf die Masse bezogen als gravimetrische Leistungsdichte in kW/kg oder auf das Volumen bezogen als Volumenleistungsdichte in kW/cm³ oder in kW/l angegeben.
Die mit obiger Formel berechnete maximale Leistung Pmax entspricht der Leistung eines einzelnen Rechteckimpulses des maximalen Spitzenstromes bei einer gegebenen Spannung. In der Realität ist der Stromimpuls jedoch nicht rechteckig, er wird verzögert verursacht durch die interne Zeitkonstante und reduziert durch den Spannungsabfall über den Innenwiderstand. Die Norm IEC 62391-2 schlägt deshalb vor, die Formel für die erreichbare Leistung der Realität anzupassen. Daraus resultiert die Formel für eine „effektive“ Leistung für Superkondensatoren in Power-Anwendungen:
Zyklusfestigkeit und Strombelastung
Weil die elektrostatische und die pseudokapazitive Speicherung elektrischer Energie in Superkondensatoren normalerweise ohne die Erzeugung chemischer Bindungen erfolgt, wird die Strombelastung der Kondensatoren, damit sind zyklische Lade-und Entladeströme und auch Impulsströme gemeint, nicht durch langsame chemische Reaktionen begrenzt. Das Be- und Entladen des Kondensators sowohl in der Doppelschicht als auch mit dem faradayschen Ladungstausch erfolgt sehr schnell. Der elektrische Strom wird dabei nur durch den Innenwiderstand des Kondensators, der deutlich kleiner als der von Akkumulatoren ist, begrenzt. Dadurch zeichnen sich Superkondensatoren gegenüber Akkumulatoren durch eine sehr viel größere Strombelastbarkeit aus.
Die Strombelastung von Superkondensatoren mit dem Strom I erzeugt über den internen Gleichstrom-Innenwiderstand Ri einen internen Wärmeverlust PVerlust
Diese Verlustwärme erwärmt den Kondensator und wird an die Umgebung weitergeleitet, wobei eine Temperaturdifferenz gegenüber der Umgebungstemperatur im Kondensator verbleibt. Die so entstandene Kondensatortemperatur darf den spezifizierten Maximalwert nicht überschreiten und ist über die Diffusionsrate gasförmiger Bestandteile des Elektrolyten aus dem Kondensatorgehäuse hinaus für die Lebensdauer der Bauelemente bestimmend.
Die gegenüber der Umgebungstemperatur zulässige Temperaturdifferenz, die durch die Strombelastung entsteht, sollte kleiner als 5 bis 10 K betragen, damit sie nur einen geringen Einfluss auf die zu erwartende Lebensdauer hat.
Die in Datenblättern spezifizierte maximale Strombelastbarkeit umfasst Lade-und Entladestrom, Frequenz und Pulsdauer und gilt innerhalb des spezifizierten Temperatur- und Spannungsbereiches für eine definierte Lebensdauer. Allgemein gilt, dass eine geringere Strombelastung, die entweder durch eine niedrigere Betriebsspannung oder durch langsameres Laden und Entladen erreicht werden kann, sowie durch eine möglichst niedrige Umgebungstemperatur die Lebensdauer der Kondensator verlängert werden kann.[73]
Der für eine Dauerbelastung spezifizierte zulässige Lade- und Entladestrom kann für Anwendungsfälle, in denen ein hoher Impulsstrom gefordert wird, deutlich überschritten werden. Bei impulsförmiger Strombelastung muss dann aber die kurzzeitig entstehende Wärme über längere Pausen zwischen den Impulsen thermisch verteilt werden. Solch ein „Spitzenstrom“ kann für große Superkondensatoren für Leistungsanwendungen mit einer Kapazität von mehr als 1000 F gemäß Datenblattspezifikation kurzzeitig einen maximalen Strom von über 1000 A betragen.[74] Solche Ströme dürfen allerdings nicht als Dauerwert betrachtet werden. Denn bei solch hohen Strömen tritt nicht nur eine starke interne Erwärmung der Kondensatoren auf, bei der die Wärmeausdehnung einen zusätzlichen Stressfaktor bildet, sondern es entstehen auch noch starke elektromagnetische Kräfte mit Auswirkung auf die Festigkeit der Elektroden-Kollektor-Verbindung. Eine große Impulsfestigkeit von Superkondensatoren ist also nicht nur eine Frage der Temperaturbelastung, sondern auch noch Ergebnis einer mechanisch robusten und stabilen Konstruktion
Superkondensatoren zeichnen sich gegenüber Akkumulatoren jedoch nicht nur durch eine sehr viel höhere Strombelastbarkeit aus, sondern sie besitzen auch noch eine sehr viel größere Zyklusfestigkeit. Das bedeutet, dass Superkondensatoren eine sehr viel größere Anzahl von Lade-Entladezyklen überstehen, ohne dass durch chemische Prozesse eine Verkürzung der Lebensdauer eintritt. Die chemische Stabilität, insbesondere bei der Pseudokapazität mit faradayschem Ladungstransfer, ist schon bei Superkondensatoren mit Elektroden aus pseudokapazitiven Polymeren so groß, dass damit hergestellte Kondensatoren mehr als 10.000 Zyklen überstehen. Das ist rund das Zehnfache dessen, was Lithium-Ionen-Akkumulatoren für Leistungsanwendungen überstehen. Superkondensatoren mit sehr hohem Anteil an Doppelschichtkapazität und auch Pseudokondensatoren mit Elektroden aus Übergangsmetalloxiden erreichen eine Zyklusfestigkeit von mehr als einer Million Zyklen, ohne dass die Kapazität nennenswert abfällt oder der Innenwiderstand deutlich ansteigt.
Lebensdauer

Superkondensatoren unterscheiden sich von Akkumulatoren nicht nur durch die höhere Strombelastbarkeit und die höhere Zyklusfestigkeit sondern auch durch eine höhere Lebensdauer. Weil die elektrostatische und die pseudokapazitive Speicherung elektrischer Energie in Superkondensatoren normalerweise ohne die Erzeugung chemischer Bindungen erfolgt, wird die Lebensdauer dieser Kondensatoren überwiegend von der Kondensatortemperatur und der damit verbundenen Diffusionsrate gasförmiger Bestandteile des flüssigen Elektrolyten aus dem Kondensatorgehäuse hinaus bestimmt. Darüber hinaus hat aber auch noch die Betriebsspannung einen gewissen Einfluss auf die Lebensdauer.
Die Lebensdauer von Superkondensatoren wird an einem Kollektiv in zeitraffenden Prüfungen bei der oberen Grenztemperatur und bei voller Nennspannung ermittelt. Bedingt durch das temperaturabhängige langsame Verdunsten des Elektrolyten durch die Abdichtung hindurch ändern sich elektrische Parameter; die Kapazität sinkt ab, der Innenwiderstand steigt an. Durch diese Änderungen der Kennwerte werden die Kondensatoren irgendwann ihre Funktion nur noch vermindert erfüllen können. Deshalb werden Änderungsgrenzen festgelegt, deren Überschreitungen als sogenannte „Änderungsausfälle“ gewertet werden. Wird in den zeitraffenden Lebensdauerprüfungen auch nur eine dieser Grenzen unter- bzw. überschritten, ist das Ende der Lebensdauer des Kondensators erreicht. Die Kondensatoren sind zwar auch dann noch weiter betriebsfähig, nur eben mit verminderten elektrischen Eigenschaften.
Für die Kapazität ist die Grenze zum Änderungsausfall nach IEC 62391-2 erreicht, wenn der Kapazitätswert sich um 30 % gegenüber seinem Anfangswert vermindert hat. Für den Innenwiderstand gilt nach der Norm als Änderungsausfall, wenn er den vierfachen Wert seiner Spezifikation überschritten hat.
Diese nach der Norm zulässigen Änderungen sind jedoch Leistungsanwendungen mit hohen Ein- und Ausschaltströmen meist zu hoch. Viele Hersteller, deren Superkondensatoren für hohe Ströme vorgesehen sind, legen deshalb deutlich engere Änderungsgrenzen fest, beispielsweise mit nur 20 % Änderung der Kapazität kombiniert mit der maximalen Änderung des Innenwiderstandes auf den doppelten Datenblattwert.[75] Insbesondere für den Innenwiderstand ist diese engere Definition bei hoher Strombelastung wichtig, da die Wärmeentwicklung im Kondensator linear mit dem Innenwiderstand ansteigt und bei einem vierfach höheren Innenwiderstand die Verlustwärme ebenfalls vierfach höher wäre und es möglicherweise dadurch zu einer unzulässigen Gasdruckentwicklung im Kondensator kommen könnte.
Die bis zum ersten Änderungsausfall gemessene Zeit, gerundet, wird von den Herstellern meist als „Lebensdauer“ (englisch life time, load life, endurance) spezifiziert. Die Schreibweise dieser Lebensdauerspezifikation, z. B. „5000 h/65 °C“ beinhaltet die Zeit in Stunden (h) und die obere Grenztemperatur in Grad Celsius (°C). Sie ist stark von der jeweiligen Baureihe abhängig.
Die in den Datenblättern spezifizierte Lebensdauer bei der oberen Grenztemperatur kann von Anwendern in Lebensdauerzeiten für abweichende Betriebsbedingungen umgerechnet werden. Dies erfolgt allgemein bei herkömmlichen Superkondensatoren, die nicht für Leistungsanwendungen vorgesehen sind, ähnlich wie bei Aluminium-Elektrolytkondensatoren mit flüssigem Elektrolyten, nach dem „10-Grad-Gesetz“, auch Arrhenius-Gesetz genannt. Danach verdoppelt sich die abschätzbare Lebensdauer pro 10 °C niedrigere Betriebstemperatur, weil die Änderungen der elektrischen Parameter entsprechend langsamer verlaufen.
- Lx = zu berechnende Lebensdauer
- L0 = im jeweiligen Datenblatt spezifizierte Lebensdauer
- T0 = obere Grenztemperatur
- Tx = aktuelle Betriebstemperatur der Kondensatorzelle
Ist eine Baureihe wie im nebenstehenden Bild mit 5000 h bei 65 °C spezifiziert, dann werden die Kondensatoren mit etwa 10.000 h bei 55 °C gleiche Änderungen der elektrischen Parameter aufweisen wie nach 20.000 h bei 45 °C, jedoch eine doppelt so lange Betriebszeit bei der kleineren Temperatur haben.
Die Lebensdauer von Superkondensatoren ist aber auch noch abhängig von der Betriebsspannung. Für diese Spannungsabhängigkeit der Lebensdauer kann keine allgemein geltende Formel angegeben werden. Der Kurvenverlauf, der aus dem nebenstehenden Bild hervorgeht, ist deshalb nur als ein Erfahrungswert eines Herstellers zusehen.
Obwohl die Lebensdauer nach der obigen Formel berechnet werden kann, ist das Ergebnis dieser Berechnung immer nur eine Abschätzung der Lebensdauer als statistischen Mittelwert eines Kollektivs eingesetzter Kondensatoren unter gleichartigen Bedingungen.
Reststrom und Selbstentladung
Die Speicherung elektrischer Energie statisch in den Helmholtzschen Doppelschichten erfolgt in einem Abstand der Ladungsträger zueinander, der im molekularen Bereich liegt. Bei diesem geringen Abstand können Effekte auftreten, die zum Austausch von Ladungsträgern führen. Diese Selbstentladung ist als Reststrom, auch Leckstrom genannt, messbar. Dieser Reststrom hängt von der Spannung und von der Temperatur am Kondensator ab. Er ist bei Raumtemperatur, bezogen auf die gespeicherte Ladungsmenge, so gering, dass üblicherweise die Selbstentladung des Kondensators als Ladungsverlust oder als Spannungsverlust für eine bestimmte Zeit spezifiziert wird. Als Beispiel sei hier ein „5-V/1-F-Goldcapacitor“ von Panasonic angeführt, dessen Spannungsverlust bei 20 °C in 600 Stunden (25 Tage) etwa 3 V beträgt, für die Einzelzelle also 1,5 V.[76] Die Selbstentladungsrate ist also höher als die von Akkumulatoren und schränkt im Vergleich damit die Anwendungsgebiete ein.
Polarität

Obwohl bei Superkondensatoren mit symmetrisch aufgebauten Elektroden theoretisch keine wirkliche Polarität existiert, sind sie in der Praxis doch gepolte Kondensatoren. Die Polarität entsteht bei Superkondensatoren mit symmetrischen Elektroden durch eine Spannungsbeaufschlagung während der Fertigung, bei asymmetrischen Elektroden ist sie außerdem noch konstruktiv bedingt. Superkondensatoren sind deshalb gepolte Kondensatoren. Sie dürfen nicht in „falscher“ Polarität entgegen der Polaritätskennung betrieben werden. Das schließt auch einen Betrieb mit Wechselspannungen aus. Ein Betrieb mit falscher Polarität führt zur Gasentwicklung und Zerstörung des Kondensators.
Die Polarität von Superkondensatoren ist wie bei anderen polarisierten Kondensatoren mit einem Minusbalken in der Isolierumhüllung (−) zur Kennzeichnung der Kathode markiert.
Bei der Bezeichnung der Polarität von Bauelementen durch die Begriffe Anode und Kathode kann es, je nachdem, ob ein Bauelement als Erzeuger oder als Verbraucher betrachtet wird, zu Verwechslungen kommen. Denn bei einem elektrischen Erzeuger für Gleichspannung (Akkumulator) hat die Kathode positive Polarität (+) und die Anode negative Polarität (−). Dahingegen hat bei einem elektrischen Verbraucher (Kondensatoren sind Verbraucher) die Kathode negative Polarität (−) und die Anode positive Polarität (+). Bei der Substitution von Akkumulatoren durch Superkondensatoren oder bei der Parallelschaltung mit Akkumulatoren muss deshalb die Polaritätskennzeichnung mit dem negativen Balken (−) besonders beachtet werden.
Technische Daten im Vergleich
Vergleich technischer Daten verschiedener Superkondensatoren
Bei Superkondensatoren führt, ähnlich wie bei Elektrolytkondensatoren, die Kombination maßgeschneiderter Elektroden mit einem der Anwendung angepassten Elektrolyten zu einer großen Anzahl von unterschiedlichen technischen Lösungen mit unterschiedlichen technischen Werten. Besonders mit der Entwicklung niederohmiger Elektrolytsysteme in Kombination mit Elektroden mit hoher Pseudokapazität lassen eine große Variationsbreite von technischen Lösungen zu. Entsprechend vielfältig ist das Angebot an Superkondensatoren auf dem Markt. Wie aus der folgenden Tabelle entnommen werden kann, unterscheiden sich deshalb die Kondensatoren der verschiedenen Hersteller deutlich bei den Werten für den Kapazitätsbereich, der Zellenspannung, beim Innenwiderstand sowie bei der Energiedichte.
In der Tabelle bezieht sich der Innenwiderstand jeweils auf den größten Kapazitätswert des jeweiligen Herstellers. In ganz grober Abschätzung können dabei die Superkondensatoren in zwei Gruppen aufgeteilt werden. Die erste Gruppe mit Innenwiderständen größer etwa 20 mΩ weist Kapazitätswerte von 0,1 bis 470 F auf. Dies sind die typischen „Doppelschichtkondensatoren“ für den Datenerhalt oder ähnliche Applikationen. Die zweite Gruppe mit Kapazitätswerten von etwa 100 bis 12.000 F hat deutlich kleinere Innenwiderstände, die zum Teil bis auf etwa 0,2 mΩ hinuntergehen. Diese Superkondensatoren sind für Leistungsanwendungen geeignet.
Aus dieser Tabelle geht der prozentuale Anteil von Doppelschicht- und Pseudokapazität an der Gesamtkapazität eines angebotenen Kondensators nicht hervor. Die Hersteller selbst sind nur in seltenen Fällen bereit, hierzu etwas zu veröffentlichen. Selbst diesen wenigen Angaben, im Artikel von Pandolfo und Hollenkamp zusammengetragen, ist eine prozentuale Verteilung des Anteils an Doppelschicht- und Pseudokapazität nicht zu entnehmen.[26]
| Hersteller | Kondensatorname | Kapazitätsbereich (F) | Zellenspannung (V) | Innenwiderstand bei Cmax (mΩ) | Volumetrische Energiedichte (Wh/dm³) | Gravimetrische Energiedichte (Wh/kg) | Hinweise |
|---|---|---|---|---|---|---|---|
| APowerCap[77] | APowerCap | 4…550 | 2,7 | – | – | 4,5 | – |
| AVX[78] | BestCap® | 0,068…0,56 | 3,6 | – | 0,13 | – | Module bis 16 V |
| Cap-XX[79] | Cap-XX | 0,16…2,4 | 2,75…2,75 | 14 | 1,45 | 1,36 | – |
| CDE[80] | Ultracapacitor | 0,1…3000 | 2,7 | 0,29 | 7,7 | 6,0 | – |
| Cooper[81] | PowerStor | 0,1…400 | 2,5…2,7 | 4,5 | 5,7 | – | – |
| Elna[82] | DYNACAP POWERCAP |
0,047…300 |
2,5...3,6 2,5 |
8,0 3,0 |
5,4 5,3 |
- – |
– – |
| Elton[83] | Supercapacitor | 1800…12000 | 1,5 | 0,5 | 6,8 | 4,2 | Module bis 29 V |
| Evans[84] | Capattery | 0,001…10 | 125 | 200 | – | – | Hybridkondensatoren |
| HCC[85] | HCAP | 0,22…5000 | 2,7 | 15 | 10,6 | – | Module bis 45 V |
| FDK[86] | EneCapTen | 2000 | 4,0 | - | 25 | 14 | Li-Ion-Kondensatoren |
| Illinois[87] | Supercapacitor | 1…3500 | 2,3…2,7 | 0,24 | 7,6 | 5,9 | – |
| Ioxus[88] | Ultracapacitor | 100…3000 220…1000 |
2,7 2,3 |
0,25 14 |
7,8 8,7 |
6,0 6,4 |
Superkondensatoren Hybridkondensatoren |
| JSR Micro[89] | Ultimo | 1100…3300 | 3,8 | 1,2 | 12 | 20 | Li-Ion-Kondensatoren |
| Korchip[90] | STARCAP | 0,01…400 | 2,7 | 12 | 7,0 | 6,1 | Module bis 50 V |
| Liyuan[91] | Supercapacitor | 1…400 | 2,5 | 10 | 4,4 | 4,6 | – |
| LS Mtron[92] | Ultracapacitor | 100…3000 | 2,8 | 0,25 | 6,0 | 5,9 | Module bis 84 V |
| Maxwell[93] | Boostcap® | 10…3000 | 2,2…2,7 | 0,29 | 7,8 | 6,0 | Module bis 125 V |
| Murata[94] | EDLC | 0,35…0,7 | 2,1 | 30 | 0,8 | – | – |
| NEC[95] | Supercapacitor LIC Capacitor |
0,01…100 1100…1200 |
2,7 3,8 |
30.000 1,0 |
5,3 – |
4,2 – |
– Li-Ion-Kondensatoren |
| Nesscap[96] | EDLC, Pseudocapacitor |
3…60 50…300 |
2,3 2,3 |
35 18 |
4,3 12,9 |
3,3 8,7 |
Module bis 125 V |
| Nichicon[97] | EVerCAP® | 0,47…6000 | 2,5…2,7 | 2,2 | 6,9 | 4,0 | - |
| NCC, ECC[98] | DLCCAP | 350…2300 | 2,5 | 1,2 | 5,9 | 4,1 | Module bis 15 V |
| Panasonic[99] | Goldcap | 0,015…70 | 2,1…2,3 | 100 | 3,4 | - | - |
| Samwha[100] | Green-Cap® | 3…3000 | 2,7 | 0,28 | 7,7 | 5,6 | Module bis 125 V |
| Skeleton[101] | SkelCap | 900…3500 | 2,85 | 0,2 | 14,1 | 10,1 | – |
| Taiyo Yuden[102] | PAS Capacitor LIC Capacitor |
0,03…50 0,25…200 |
2,5…3,0 3,8 |
70 50 |
6,1 – |
– – |
Pseudokondensatoren Li-Ion-Kondensatoren |
| VinaTech[103] | Hy-Cap | 1,5…350 | 2,3…3,0 | 10 | 7,6 | 8,1 | – |
| WIMA[104] | SuperCap | 12…6500 | 2,5…2,7 | 0,18 | 5,2 | 4,3 | Module bis 112 V |
| YEC[105] | Kapton capacitor | 0,5…400 | 2,7 | 12 | 7,0 | 5,5 | – |
| Yunasko[106] | Ultracapacitor | 480…1700 | 2,7 | 0,17 | 6,1 | 5,8 | - |
| Fußnote: Volumetrische und gravimetrische Energiedichte berechnet mit dem maximalen Kapazitätswert, der zugehörenden Spannung und den Abmessungen, sofern nicht im jeweiligen Datenblatt spezifiziert | |||||||
Tabelle, Stand Juli 2013
Vergleich technische Daten von Superkondensatoren mit anderen Technologien
Superkondensatoren stehen im Wettbewerb einerseits mit Elektrolytkondensatoren und andererseits mit Akkumulatoren, insbesondere mit Lithium-Ionen-Akkumulatoren. Die folgende Tabelle vergleicht die wichtigsten technischen Daten der drei unterschiedlichen Familien innerhalb der Superkondensatoren mit Elkos und Akkus.
| Kennwerte | Elektrolyt- kondensatoren |
Superkondensatoren | Lithium- Ionen- Akkumulatoren | ||
|---|---|---|---|---|---|
| Super- kondensatoren für den Datenerhalt |
Super- kondensatoren für Leistungs- anwendungen |
Hybrid kondensatoren (Li-Ionen- Kondensatoren) | |||
| Betriebs- temperaturbereich (°C) |
−40…+125 | −20…+70 | −20…+70 | −20…+70 | −20…+60 |
| Nennspannung pro Zelle (V) |
4...550 | 1,2…3,3 | 2,5…3,3 | 2,2…3,8 | 2,5…4,2 |
| Lade-/Entlade-Zyklen | unbegrenzt | 105…106 | 105…106 | 2·104…105 | 500…104 |
| Kapazitätsbereich (F) | ≤ 1 | 0,1…470 | 100…12000 | 300…2200 | — |
| Energiedichte (Wh/kg) | 0,01…0.3 | 1,5…3,9 | 4…9 | 10…25 | 100…265 |
| Effektive Leistungsdichte (kW/kg) | > 100 | 2…10 | 3…10 | 3…6 | 0,3…1,5 |
| Selbstentladezeit bei Raumtemperatur | kurz (Tage) |
mittel (Wochen) |
mittel (Wochen) |
mittel (Wochen) |
lang (Monate) |
| Wirkungsgrad (%) | 99 | 95 | 95 | 90 | 90 |
| Lebensdauer bei Raumtemperatur (Jahre) | > 20 | 5…10 | 5…10 | 5…10 | 3…5 |
Elektrolytkondensatoren haben Vorteile wegen ihrer Eignung zur Entkopplung niederfrequenter Frequenzen bis etwa 500 kHz und ihrer hohen Spannungsfestigkeit bis 550 V. Ihre Speicherfähigkeit ist dagegen deutlich geringer.
Superkondensatoren sind wie auch Akkumulatoren nur für reine Gleichspannungsanwendungen geeignet. Die Vorteile von Superkondensatoren gegenüber Akkumulatoren sind die längere Lebensdauer, die deutlich höhere Leistungsdichte mit hoher Spitzenstrombelastbarkeit, die deutlich größere Zyklusfestigkeit und der wartungsfreie Betrieb. Die Nachteile sind der höhere Preis, die geringere Energiedichte und die schnellere Selbstentladung.
Normung

Die technischen Eigenschaften von Superkondensatoren unterscheiden sich beträchtlich voneinander. Besonders bei Anwendungen mit hohen Spitzenströmen sind die elektrischen Werte oft von den Messbedingungen abhängig, so dass standardisierte Prüfungen und Messvorschriften unabdingbar sind, um eine Vergleichbarkeit der Bauelemente zu erreichen.[107]
Diese Prüfungen und Messvorschriften sowie die Anforderungen an die geprüften Kondensatoren sind in einer international harmonisierten (IEC) Norm festgelegt, die im deutschen Sprachraum von den jeweiligen Länderorganisationen (DIN, OEVE/OENORM, SN) als europäische Norm EN, übernommen wurden.[108] Es ist dies die:
- Fachgrundspezifikation IEC 62391-1,Elektrische Doppelschichtkondensatoren zur Verwendung in Geräten der Elektronik
- Klasse 1, Datenerhalt' von Speichern,
- Klasse 2, Energiespeicherung, z. B. für den Betrieb von Antriebsmotoren,
- Klasse 3, Leistungsanwendungen, höherer Leistungsbedarf für längeren Betrieb
- Klasse 4, Momentanleistung, höhere Spitzenströme für Kurzzeitbetrieb
Für die Superkondensatoren für Leistungsanwendungen nach Klasse 4 werden die besonderen Anforderungen in einer ebenfalls international harmonisierten Rahmenspezifikation festgelegt:
- Rahmenspezifikation EN 62391-2, Elektrische Doppelschichtkondensatoren für Leistungsanwendungen
Darüber hinaus werden in der beiden folgenden Normen die speziellen Anforderungen an Superkondensatoren für definierte Einsatzbereiche spezifiziert:
- IEC 62576, Anforderungen für den Einsatz im Bereich der Automobilelektronik
- IEC 61881-3, Anforderungen für den Einsatz im Bereich der Bahnen
Anwendungen
Allgemeine Anwendungen
Superkondensatoren haben Vorteile in Anwendungen, in denen eine große Energiemenge für eine relativ kurze Zeit oder für eine sehr hohe Zahl von Lade-/ Entladezyklen benötigt wird. Typische Beispiele umfassen Ströme im Bereich von Milliampere oder Milliwatt für einige Minuten bis zu Strömen im Bereich mehrerer Hundert Ampere oder mehreren hundert Kilowatt während kurzer Lastspitzen.
Die Zeit t, während der ein Superkondensator einen konstanten Strom I liefern kann, wird berechnet mit:
wobei die Spannung auf absinkt.
Wenn die Anwendung eine konstante Leistung für eine gewisse Zeit benötigt, kann dies berechnet werden mit:
wobei die Spannung ebenfalls bis auf absinkt.
Superkondensatoren sind nicht für Wechselspannungsanwendungen geeignet.
Konsumerelektronik
Superkondensatoren stabilisieren in Anwendungen mit schwankender Belastung die Stromversorgung. Beispiele sind: Laptops, PDAs, GPS, tragbare DVD-Player und Smartphones.[109]
Superkondensatoren liefern in kurzer Zeit große Stromspitzen und werden deshalb parallel zu Akkumulatoren in Digitalkameras zum Schreiben der Bilddateien und als Energielieferant für Blitzlichtgeräte eingesetzt.[110]
Für Notfall-LED-Blitzlichttaschenlampe wird ihre schnelle Ladefähigkeit genutzt.[111][112]
Für Heimwerker wird ein elektrischer Schraubendreher mit Superkondensatoren angeboten, der zwar nur halb so lange wie ein Akku-Modell läuft, jedoch in 90 s aufgeladen ist.[113]
Superkondensatoren liefern die Energie in Netz-unabhängigen Lautsprechern.[114]
Industrielle Elektronik
Superkondensatoren liefern die benötigte Energie für elektrische Verbraucher, deren Funktion bei kurzzeitigem Stromausfall weiter gewährleistet werden sollte, beispielsweise zum Datenerhalt bei elektronischen Datenspeichern (RAM, SRAM) in der industriellen Elektronik.
Superkondensatoren sind als zusätzliche Energiequelle in intelligenten Stromzählern (Smart Meter) zu finden.[110]
Im Zusammenwirken mit parallel geschalteten Akkumulatoren puffern Superkondensatoren bei stark schwankenden Belastungen in Funk- und Telekommunikationsgeräten die ein- und ausfließenden Ströme des Akkus und dämpfen somit Belastungsspitzen. Damit kann die Lebensdauer der Akkus verlängert werden.
Ein typischer industrieller Anwendungsfall für Superkondensatoren sind unterbrechungsfreie Stromversorgungen (USV) zur Überbrückung kurzzeitiger Netzausfälle. Mit ihnen kann eine deutliche Platzersparnis gegenüber Elektrolytkondensatoren erreicht werden.[115][116][117]
Superkondensatoren werden als Energielieferant zum Antrieb elektrischer Lokomotiven in einigen Kohlebergwerken in China verwendet. Der Vorteil dieses Antriebs ist die schnelle Ladezeit der Kondensatoren gegenüber Akkus. In weniger als 30 Minuten ist der Zug wieder fahrbereit. Mit dieser Lösung wird die Explosionsgefahr gegenüber elektrischen Antrieben mit Fahrdraht deutlich verringert.[118]
Auch Zugmaschinen auf Flughafen-Terminals mit einem elektrischen Antrieb gespeist aus Superkondensatoren sind bereits im Einsatz. Sie bieten eine kostengünstige, ruhige und verschmutzungsfreie Alternative zu Diesel-Zugmaschinen.[118]
Erneuerbare Energien

Superkondensatoren liefern den Strom für die Flügelsteuerung (Drehzahlregelung, Notabschaltung) von Windkraftanlagen. So ist es z. B. bei Sturm möglich, die Rotorblätter aus dem Wind zu drehen, selbst wenn die Verbindung zum elektrischen Netz unterbrochen ist.[110][119]
Superkondensatoren können die Spannung, die von photovoltaischen Anlagen erzeugt wird, stabilisieren. Diese Spannung ist Schwankungen unterworfen, die von vorbeiziehenden Wolken oder durch Abschattung begründet ist. Die Stabilisierung reduziert den Aufwand des Netzbetreibers, die Netzspannung und die Netzfrequenz stabilisieren zu müssen.[120][121]
Bei genügender Auslegung eignen sich Superkondensatoren ebenfalls zur Kurzzeitspeicherung der elektrischen Energie bei der photovoltaischen Einspeisung ins Niedrigspannungsnetz.[110][122]
Straßenbeleuchtung

Die Anwendung von Superkondensatoren in der Straßenbeleuchtung von Sado City in der japanische Präfektur Niigata kann völlig ohne Netzanschluss betrieben werden. In dieser Anwendung werden tagsüber die Superkondensatoren über Solarzellen geladen und liefern ab Einbruch der Dunkelheit den Strom für LED-Leuchten. Wegen der besseren Tieftemperatureigenschaften und der längeren Lebensdauer von über 10 Jahren bekamen Superkondensatoren den Vorzug gegenüber Akkus.[123]
Luftseilbahn
In manchen Luftseilbahnen besitzen die Fahrzeuge eine Stromversorgung während der Fahrt für Beleuchtung, Sprechanlagen und auch für Infotainmentsysteme.[124] Da Akkumulatoren für das Aufladen während der Stationsdurchfahrten und -aufenthalte eine zu lange Ladezeit aufweisen, können stattdessen Superkondensatoren, die bei jeder Stationsdurchfahrt über eine Stromschiene geladen werden, zum Einsatz kommen. Gondeln mit Superkondensatoren in der Stromversorgung sind beispielsweise in Zell am See und bei der Emirates Air Line, der Seilbahn über die Themse in London, zu finden.[125]
Medizinische Elektronik
Superkondensatoren werden in Defibrillatoren eingesetzt, in denen sie die benötigte Energie für die lebensrettenden Impulse zur Verfügung stellen können.[126]
Luftfahrtelektronik

Seit dem Jahre 2005 verwendet Diehl Luftfahrt Elektronik GmbH Superkondensatoren als Energiequellen für die Notöffnung der Türen und die Aktivierung der Notrutschen in Geräten für Flugzeuge einschließlich des Airbus 380.[119][110]

Hinter dem Projektil entsteht durch den großen Druckunterschied eine Plasmawolke.
Militärelektronik
Der Kaltstart von Dieselmotoren stellt eine besondere Herausforderung an die Bereitstellung kurzzeitiger Stromspitzen dar. Superkondensatoren mit niedrigen Innenwiderständen werden schon seit längerer Zeit zum Start von Dieselmotoren in Panzern und U-Booten zur Unterstützung der Batterien beim Kaltstart eingesetzt.[127]
Weitere militärische Anwendungen, in denen Superkondensatoren wegen ihrer hohen Leistungsdichte eingesetzt werden, sind phasengesteuerte Gruppenantennen, Stromversorgungen für Impulslaser, Avionik-Anzeigen und –Instrumente, Airbag-Zünderschaltungen und GPS-Lenkwaffenraketen und Projektile.[128][129]
Zudem könnten Superkondensatoren in Zukunft zur Deckung des kurzzeitig sehr hohen Energiebedarfs von sogenannten Railguns oder Gaußgewehren zum Einsatz kommen.
Energierückgewinnung

Eine primäre Herausforderung für öffentliche und private Verkehrsmittel ist die Senkung des Energieverbrauchs und die Verringerung der CO2-Emissionen. Rückgewinnung der Bremsenergie (Rekuperation) erfüllt beide Herausforderungen. Sie sind wegen ihrer hohen Strombelastbarkeit und der Zyklusfestigkeit, des hohen Wirkungsgrades und der langen Lebensdauer ideal geeignet für die Rückgewinnung von kinetischer Energie.[131][22][132]
Eisenbahnen

Superkondensatoren kommen als Ergänzung zu den Akkus als Starterbatterie in Dieselloks mit diesel-elektrischem Antrieb und zum Vorheizen des Katalysators zum Einsatz. Die Kondensatoren nehmen wegen ihrer hohen Strombelastbarkeit gleichzeitig auch die Energie auf, die beim Bremsen des Zuges generiert wird, und liefern außerdem den Spitzenstrom, der beim Starten des Zuges auftritt. In einer Untersuchung wurde festgestellt, dass damit 25 bis 30 % Energieeinsparung möglich ist.[133][134] Da die Akkumulatoren wegen der reduzierten Spitzenbelastung entsprechend kleiner ausgelegt werden können, wird durch Gewichts- und Bauraum-Reduzierung mit dieser Lösung ein höherer Treibstoffvorrat in den Loks möglich. Wartungsfreiheit und umweltfreundliche Materialien waren bei der Entscheidung, diesen Versuch durchzuführen, weitere entscheidende Vorteile für den Einsatz von Superkondensatoren.
Kräne und Gabelstapler

Mobile Hybrid-Diesel- Elektro-Containerbrücken bewegen und stapeln Container innerhalb eines Containerterminals. Das Heben der Container erfordert eine große Menge an Energie. Ein Teil der Energie wird im Containerterminal von Kuantan (China) mit Hilfe von Superkondensatoren während des Absenkens der Last zurückgewonnen. Dadurch ist eine erhebliche Energieeinsparung möglich. Ein weiterer Vorteil dieses Aufbaus ist die Verkleinerung der primären Dieselmaschine, da die Spitzenbelastung beim Heben der Last durch die in den Kondensatoren gespeicherte Energie und die angesteuerten Elektromotoren übernommen werden kann.[132]
In einer speziellen Version eines „Triple-Hybrid-Gabelstaplers“ wird eine Brennstoffzelle als primäre Energiequelle verwendet, die zum Aufladen einer parallel geschalteten Kombination von Akkumulatoren und Superkondensatoren genutzt wird. Die Superkondensatoren liefern den Strom für die Spitzenbelastung beim Heben der Last und nehmen die beim Absenken der Last freiwerdende Energie wieder auf. Dieses Triple-Hybrid-System bietet mehr als 50 % Energieeinsparung im Vergleich zu einem reinen Diesel- oder Brennstoffzellen-System.[135]
Stadtbahnen und Trams

Superkondensatoren können nicht nur elektrische Energie aus der Nutzbremsung von Stadtbahnen und Trams “on-board” zwischenspeichern, sondern bieten auch noch die Möglichkeit, kurze Strecken ohne Oberleitung fahren zu können. Die zum Fahren benötigte Energie kann in kurzer Zeit an den Haltestellen während eines Stopps über eine nur hier installierte Oberleitung aufgenommen werden. Hierbei können erhebliche Einsparungen bei der Einrichtung der Infrastruktur durch Wegfall der Oberleitung über die Strecke erreicht werden. Außerdem können in historischen Städten die optisch störenden Oberleitungen entfallen.
Seit dem Jahre 2003 fährt in Mannheim ein Prototyp einer Stadtbahn des Herstellers Bombardier Transportation mit einem System zur Rückgewinnung der Bremsenergie (Nutzbremsung). Dieses MITRAC-Energy-Saver[136] genannte System arbeitet mit Superkondensatoren und ist im Dach des Triebwagens untergebracht. Es enthält mehrere Speicherblöcke, die aus 192 Einzelkondensatoren mit je 2700 F/2,7 V in drei parallel geschalteten Strängen zusammengeschaltet sind. Damit ergibt sich ein 518-V-System mit einem Energieinhalt von 1,5 kWh. Zur Beschleunigung beim Anfahren können aus diesem „On-Board-System“ kurzzeitig 600 kW bereitgestellt werden. Damit kann außerdem bis zu 1 km ohne Oberleitung gefahren werden. Der spanische Hersteller Construcciones y Auxiliar de Ferrocarriles (CAF) bietet für seine Urbos-3-Straßenbahnen das System „Acumulador de Carga Rápida“ (ACR) an, es wird seit 2011 in Sevilla eingesetzt und soll an verschiedenen Standorten getestet werden, z. B. in Freiburg im Breisgau[137]
Mit solchen Systemen wird der Spitzenstrombedarf vom Netz um etwa 50 % reduziert, und es können etwa 30 % der zum Betrieb benötigten Energie eingespart werden.[29][138] Obwohl die Einrichtung mit dem Superkondensatoren als Energiespeicher zusätzliche Kosten von etwa €270.000 pro Bahn verursacht, erwartet der Betreiber, dass sich die Mehrkosten in 15 Jahren amortisiert haben.
Im März 2008 wurde der Test erfolgreich abgeschlossen[139] Aus diesem Grunde bestellte der Verkehrsverbund Rhein-Neckar, auch zuständig für Heidelberg, wo die Stadtbahn seit 2009 ohne durchgehende Oberleitung fährt, im April 2011 weitere 11 Stadtbahnen.[140]
Siemens bietet seit 2007 ein System zur Ernergierückgewinnung bei Stadtbahnen an[141].

In Paris fuhr von Mai 2009 bis September 2010 eine Stadtbahn der Straßenbahnlinie 3 mit einem „STEEM“ genannten Energie-Rückgewinnungssystem des Herstellers Alstom. Es sollte gezeigt werden, dass in oberleitungsfreien Teilstrecken Straßenbahnen mit der in den Superkondensatoren gespeicherten Energie fahren können[142] Ein Erlass der zuständigen Behörde erlaubte allerdings nur Leerfahrten ohne Fahrgäste.[143]
In Genf wird seit 2012 ein Prototyp einer Stadtbahn mit Superkondensatoren im Gesamtgewicht von einer Tonne für die Rückgewinnung der Bremsenergie eingesetzt. Das Speichersystem wurde von ABB entwickelt und kann das elektrische Äquivalent der kinetischen Energie des leeren Zuges, der mit 55 km/h fährt, aufnehmen[144].
Im August 2012 präsentierte die CSR Zhouzhou Electric Locomotive corporation of China einen Prototyp einer Stadtbahn mit einem Anhänger, der mit einem Energie-Rückgewinnungssystem ausgestattet ist. Die Kapazität der Superkondensatoren ist dafür ausgelegt, dass die Bahn ohne Oberleitung fährt und der Kondensator an den Stationen die zusätzliche, zum Fahren benötigte Energie aufnimmt[145].

Eine andere Lösung zur Rückgewinnung der Bremsenergie wurde 2012 in Hongkong angewendet. Die Bahnen speisen die bei der Nutzbremsung gewonnene Energie nicht in eine „on-board“-Einheit ein, sondern ins Netz zurück. Dazu wurde die Hong Kong’s South Island Metro Line mit zwei Speichereinheiten ausgestattet, die mit Superkondensatoren bestückt sind, die beide jeweils eine Leistung von 2 MW aufnehmen können. Die Gesellschaft verspricht sich dadurch eine Energieersparnis von etwa 10 %[146].
Stadtbusse

Schon 2001 wurde der sog. „Ultracapbus“ von MAN der Öffentlichkeit vorgestellt, der erste Hybridbus in Europa, der in der Lage war, seine Bremsenergie zurückzugewinnen. Er wurde in den Jahren 2001/2002 im realen Linienbetrieb in Nürnberg erprobt. Jeder Bus enthielt acht Superkondensator-Module, die mit 640 V betrieben wurden. Der Energieinhalt der Module betrug 0,4 kWh bei einem Gewicht von 400 kg und lieferte einen maximalen Strom von 400 A. Die Vorteile des Systems waren eine deutliche Reduzierung des Kraftstoffverbrauchs (derzeit 10 bis 15 % im Vergleich zum konventionellen Dieselfahrzeug), eine Reduktion der CO2-Emissionen, das Verlassen der Haltestelle ohne störende Geräusch- und Abgasbelastung, die Erhöhung des Fahrkomforts (ruckfreies, vibrationsarmes Fahren) und eine Reduktion der Wartungskosten[147][148].
Ein weiterer Betriebsversuch mit Superkondensatoren zur Energierückgewinnung wurde 2002 mit der TOHYCO-Rider-Kleinbusflotte in Luzern, Schweiz, erfolgreich durchgeführt. Die Busse können an jeder Haltestelle in wenigen Minuten berührungslos induktiv aufgeladen werden. Alle Versuche fielen erfolgreich aus, sodass der Flottenversuch 2004 weiter fortgesetzt wurde[149][150].

Im Frühjahr 2005 wurde in Shanghai ein „Capabus“ genannter elektrischer Bus in den Probebetrieb geschickt. Dieser Bus ist mit Superkondensatoren für die Rekuperation und den Fahrbetrieb ausgerüstet. Sie werden an den Haltestellen, wie unter einem „elektrischen Schirm“, mit Hilfe der nur dort installierten Oberleitung für den Fahrbetrieb aufgeladen. 2013 sind in Shanghai bereits drei solcher Buslinien mit insgesamt 17 Bussen in Betrieb. Die Betreiber gehen davon aus, dass der Betrieb wegen der höheren Zyklusfestigkeit und der längeren Lebensdauer der Kondensatoren kostengünstiger als mit Li-Ionen-Akkumulatoren sein wird und über seine Betriebsdauer mehr als $200.000 Einsparungen gegenüber einem Dieselbetrieb erwirtschaften wird[151][152].
Ein anderes Konzept eines elektrischen Busses, das völlig ohne Oberleitung auskommt, wurde von der University of Glamorgan (Wales) vorgestellt. Als Energiequelle wird sowohl Wasserstoff in Kombination mit einer Brennstoffzelle als auch Strom aus Solarzellen verwendet. Die Zwischenspeicherung erfolgt über parallel geschaltete Akkus und Superkondensatoren. Dieser „Tribrid“ genannte Bus dient dem Transport der Studenten auf dem Campus[153][154].
Motorsport

Die FIA, der internationale Dachverband des Automobilsports, hat im Jahre 2007 im Regelwerk für die Formel-1-Rennwagen erlaubt, dass im Antriebsstrang ein 200-kW-Hybrid-Antrieb verwendet werden darf, der Superkondensatoren und Akkumulatoren in Parallelschaltung enthält.
Durch Einspeisen der Bremsenergie und Rücklieferung beim Beschleunigen lassen sich mit diesem „Kinetic Energy Recovery System“ (KERS) etwa 20 % Treibstoff einsparen.[155][156][157]
Unter den Regeln für Prototypen des 24-Stunden-Rennens von Le Mans wurde von Toyota ein Rennwagen, der Toyota TS030 Hybrid LMP1, entwickelt, der einen Hybrid-Antriebsstrang besitzt und einen Energiespeicher zur Rückgewinnung der Bremsenergie nutzt, der mit Superkondensatoren bestückt ist[158][159].
Im Rennen 2012 fuhr dieser Sport-Prototyp seine schnellste Runde nur 1,055 Sekunden langsamer (3:24.842 gegenüber 3:23.787)[160] als das schnellste Auto, ein Audi R18 e-tron quattro mit Schwungradspeicher. Diese beiden Fahrzeuge, die auf unterschiedliche Art und Weise die Bremsenergie zurückgewannen, waren die schnellsten Autos im Rennen.
Kraftfahrzeuge

Siehe auch: Elektroauto, Hybridelektrokraftfahrzeug, Nutzbremse und Elektromotorische Bremse
In den bislang ausgelieferten Elektroautos und Hybridfahrzeugen (HEV) sind bislang, soweit bekannt, keine Superkondensatoren enthalten, weder im Antriebsstrang noch in der Rekuperation (siehe Liste der Hybridautomobile in Serienfertigung), obwohl die Kondensatorindustrie große Anstrengungen unternommen hat, die Vorzüge der Kondensatoren deutlich herauszustellen.[152][107][161][162][163] Eine Rückgewinnung der Bremsenergie erfolgt zur Zeit (2014) beispielsweise mit Hilfe von Hochleistungs-Akkus im Toyota Prius im HSD-Antriebstranges, die für eine hohe Zyklusfestigkeit ausgelegt wurden. Die Differenz der zurückgewonnenen Rekuperationsenergie zwischen der Akku-Lösung und einer Lösung mit Superkondensatoren von schätzungsweise 10 % rechtfertigt den Einsatz von Superkondensatoren nicht, da die eigentliche Zielsetzung dieser Fahrzeuge eine längere Fahrleistung ist.
Jedoch haben alle bedeutenden Hersteller entsprechende Entwicklungen und Versuchsaufbauten auch mit Superkondensatoren bestückt bzw. haben Prototypen, die seit Jahren vorgestellt werden[164] Aber aufgrund des unterschiedlichen Spannungsverhalten von Kondensator und Akku wird das Batterie-Management-System[165] mit DC/DC-Wandler und eine für den unterschiedlichen Spannungsverlauf ausgelegte Ansteuerelektronik deutlich schwieriger, was gleichbedeutend mit mehr Gewicht und höherem Preis ist.

Allerdings stellte Ende 2012 der Hersteller Mazda für den Mazda 2 Demio ein regeneratives Bremssystem mit Superkondensator zur Energiespeicherung vor,[166][167][168][169] in dem die Vorteile der Superkondensatoren wie sehr hohe Spitzenstrombelastbarkeit und sehr große Zyklusfestigkeit verbunden mit langer Lebensdauer und guten Tieftemperatureigenschaften sowie eine große Zuverlässigkeit[170] zur Geltung kommen. In diesem i-ELOOP genannten System werden Superkondensatoren des Herstellers NCC[171], die speziell für die Verwendung in Fahrzeugen temperatur- und vibrationsfester konzipiert wurden, parallel zu Li-Ionen-Akkus als Speichereinheit genutzt. Mazda erwartet mit diesem System eine Energieersparnis von etwa 10 %.
Eine weitere Hybridfahrzeug-Modellreihe mit Superkondensatoren zur Bremsenergierückgewinnung, die russischen Yo-Autos der ё-mobil Reihe, befindet sich noch in der Entwicklungsphase. Der Unternehmer Michail Prochorow stellte 2010 Prototypen des russischen ë-Concept und ë-Crossover vor, die einen Wankelmotor und Generator im Dauerbetrieb für die Versorgung von zwei Elektromotoren nutzen, während ein Superkondensator vergleichsweise geringer Kapazität beim Beschleunigen den Motor unterstützt und dann beim Abbremsen sich wieder auflädt.[172][173]
Neuentwicklungen
Handelsübliche Superkondensatoren für professionelle Anwendungen standen 2013 mit einer Energiedichte von etwa 6 Wh/kg, Lithium-Ionen-Kondensatoren mit etwa 15 Wh/kg zur Verfügung. Mit diesen Werten haben Superkondensatoren eine deutlich geringere Energiespeicherfähigkeit als moderne Akkumulatoren. Um speziell den sich abzeichnenden Massenmarkt für Elektro-und Hybridfahrzeuge noch erreichen zu können, sind eine große Anzahl von Forschungs-und Entwicklungsabteilungen in vielen Unternehmen und Hochschulen dabei, Fortschritte bei diesen speziellen Kondensatoren zu entwickeln.[174][67] Zielsetzungen der Forschungsprojekte sind Erhöhung der spezifischen Kapazität durch Entwicklung neuer nanostrukturierter Elektroden[56], Maßgeschneiderte Porenstrukturen zur Erhöhung der Pseudokapazität, Verringerung des Innenwiderstandes und somit Erhöhung der Leistungsdichte, Erhöhung der Spannungs- und Temperaturfestigkeit, Verbesserung der chemischen Stabilität der Elektroden sowie Kostenreduzierung durch Automatisierung in der Produktion und preiswertere Basismaterialien. Hier einige Beispiele von Neuentwicklungen der letzten Jahre:
| Titel der Neuentwicklung |
Datum | Energiedichte (Fußnote) |
Leistungsdichte | Zyklen | Spez. Kapazität | Hinweise |
|---|---|---|---|---|---|---|
| Graphen-Elektroden in Subnanometer Konfiguration mit hoher Ionendichte[175] | 2013 | 60 Wh/l | Poröse, dicht gepackten Graphenelektroden mit großer Oberfläche, die mit Kapillarkräften eine hohe Ionendichte bewirken | |||
| Elektrode mit vertikal angeordneten Kohlenstoffnanoröhren[15][50] | 2007 2009 2013 |
13,50 Wh/kg | 37,12 W/g | 300.000 | Erste Anwendung siehe:[176] | |
| Elektrode aus „zerknüllten“ eindimensionalen Graphenschichten [47][46][177] | 2010 | 85,6 Wh/kg | 550 F/g | Die Elektroden mit zweidimensionaler Struktur formen Mesoporen mit großer Pseudokapazität. | ||
| Maßgeschneiderte dreidimensionale kristalline Graphitelektrode[178][179] | 2011 | 85 Wh/kg | >10.000 | 550 F/g | Chemisch aktiviertes Graphit mit dreidimensionaler kristalliner Elektrodenstruktur mit Meso/Makroporen | |
| Aktivierter Graphen-basierter Kohlenstoff mit Makro- und Mesoporen[180] | 2013 | 74 Wh/kg | Dreidimensionale Porenstruktur in graphenabgeleitetem Kohlenstoff mit Mesoporen, die in Makroporen integriert sind und eine Oberfläche von 3290 m2/g besitzen | |||
| Dreidimensionale poröse Graphen-Elektrode[181] | 2013 | 98 Wh/kg | 231 F/g | Dreidimensionales Graphen-basierter Elektrodenmaterial aus einlagigen gefalteten Graphenschichten mit kovalenten Bindungen | ||
| SWNT Komposit-Elektrode[182] | 2011 | 990 kW/kg | Komposit-Elektrode mit einwandigen Kohlenstoffnanoröhren mit einer maßgeschneiderten Porenstruktur in der Größenordnung der Meso- und Makroporen | |||
| Konjugierte mikroporöse Elektrode aus leitfähigem Polymer[183][184] | 2011 | 53 Wh/kg | 10,000 | Das “Aza-Fused π-Conjugated Microporous Framework” ist ein mikroporöses Polymer (CMP), in dem sich in seinen Doppelbindungen einige Elektronen als „Elektronenwolke“ frei bewegen können, und ist geeignet für eine große Pseudokapazität. | ||
| Nickelhydroxid Komposit-Elektrode[185] | 2012 | 50,6 Wh/kg | 3300 F/g | Asymmetrische Komposit-Elektrode, auf der Nickelhydroxid als Nanoflocken auf Kohlenstoffnanoröhren eingelagert sind, gekoppelt mit einer Kohlenstoff-Elektrode für einen Hybridkondensator mit 1,8 V Zellenspannung | ||
| Batterie-Elektroden Nano-Hybrid-Kondensator[186] | 2012 | 40 Wh/l | 7,5 kW/l | 10.000 | Li4Ti5O12 (LTO) eingelagert in Kohlenstoffnanofasern (CNF) gekoppelt mit einer Elektrode aus Aktivkohle | |
| Kohlenstoff-Aerogel-Kompositelektrode mit eingelagertem Nickel-Cobaltit[37] | 2012 | 53 Wh/kg | 2,25 kW/kg | 1700 F/g | Preiswerte und umweltfreundliche Nickel-Cobaltit-(NiCo2O4)Nanokristalle eingelagert in eine Kohlenstoff-Aerogel-Elektrode ergeben eine hohe Pseudokapazität | |
| Mangandioxid-Komposit-Elektrode mit interkaliertem Natrium[187] | 2013 | 110 Wh/kg | 1000 F/g | Elektrochemisch interkalierte Natrium-Ionen (Na+) in einer Mangandioxid-Elektrode MnO2 für schnellen Ionentransport mit hoher Pseudokapazität. | ||
| Graphen-basierte planare Mikro-Superkondensatoren für “on-chip” Energiespeicherung [188] | 2013 | 2,42 Wh/l | Integration von Superkondensator-Strukturen zur Entkopplung von Störfrequenzen. | |||
| Quanteneffekt-Superkondensatoren [29][189][190][191][192] |
2013 | 480 Wh/kg | Quantensuperkondensatoren weisen in ihren Elektroden sehr kleine Cluster (Nanocluster) aus dipolaren Metalloxiden in der Rutilstruktur auf. Die Energiespeicherung erfolgt überwiegend durch Beladen der Cluster mit Elektronen, wobei der Welle-Teilchen-Dualismus der Elektronen genutzt wird. |
Fußnote: Die Erforschung von neuen Elektrodenmaterialien macht Messmethoden erforderlich, die die Eigenschaften nur einer Elektrode anzeigen.[193] Durch die Benutzung einer Gegenelektrode, die die Messungen an der Testelektrode nicht beeinflusst, kann die Charakteristik einer neuentwickelten Elektrode erfasst werden. Die Energie- und die Leistungsdichte eines kompletten Superkondensators mit der neuentwickelten Elektrode beträgt meist nur etwa 1/3 des für die Elektrode gemessenen Wertes.
Markt
Das Marktvolumen für Super- bzw. Ultrakondensatoren im Jahre 2010 lag bei etwa 400 Mio. US-Dollar.[194] Verglichen mit dem Markt für Batterien im Jahre 2009 von 36,3 Milliarden US-Dollar, Akkumulatoren von 11,2 Milliarden US-Dollar (geschätzt von Frost & Sullivan)[195] und für Kondensatoren mit etwa 18 Milliarden US-Dollar im Jahre 2008[196] ist der Markt der Superkondensatoren noch ein Nischenmarkt.
Eine Analyse von Paumanok schätzt den Batteriemarkt auf 95 Milliarden US-Dollar für 2013[197] und sieht das Marktvolumen für Superkondensatoren hierzu im Verhältnis eher kleiner werden.
Von anderer Seite wird für Superkondensatoren ein Marktwachstum auf etwa 3,5 Milliarden US-Dollar im Jahr 2020 vorausgesagt,[198] also eine Verzehnfachung innerhalb eines Jahrzehnts für den Fall, dass die Kondensatoren insbesondere für die Rekuperation von Bremsenergie im privaten PKW-Bereich, aber auch für andere Bereiche der „grünen“ Energieeinsparung eingesetzt werden.
Der Marktpreis von Superkondensatoren für Großabnehmer betrug im Jahre 2006 etwa 0,01 US-Dollar pro Farad oder 2,85 US-Dollar pro Kilojoule.[199]
Literatur
- Héctor D. Abruña, Yasuyuki Kiya, Jay C. Henderson: Batteries and electrochemical capacitors. In: Physics Today. Nr. 12, 2008, S. 43–47 (PDF).
- F. Béguin, E. Raymundo-Piñero, E. Frackowiak: Carbons for Electrochemical Energy Storage and Conversion Systems. Chapter 8: Electrical Double-Layer Capacitors and Pseudocapacitors. CRC Press, 2009, ISBN 978-1-4200-5307-4, S. 329–375. (eBook, ISBN 978-1-4200-5540-5, doi:10.1201/9781420055405-c8)
- J. O’M. Bockris, M. A. V. Devanathan, K. Muller: On the Structure of Charged Interfaces. In: Proceedings of the Royal Society. Band 274, Nr. 1356, 1963, S. 55–79, doi:10.1098/rspa.1963.0114.
- B. E. Conway: Electrochemical Supercapacitors: Scientific Fundamentals and Technological Applications. Springer, Berlin 1999, ISBN 0-306-45736-9 (eingeschränkte Vorschau in der Google-Buchsuche).
- Farzad Ebrahimi (Hrsg.): Nanocomposites - New Trends and Developments. InTech, 2012, ISBN 978-953-510-762-0, doi:10.5772/3389 (Open-Access-Buch).
- Kim Kinoshita: Carbon: Electrochemical and Physicochemical Properties. 1 edition Auflage. Wiley-Interscience, New York 1988, ISBN 0-471-84802-6.
- K. W. Leitner, M. Winter, J. O. Besenhard: Composite supercapacitor electrodes. In: Journal of Solid State Electrochemistry. Band 8, Nr. 1, 2003, ISSN 1433-0768, S. 15–16, doi:10.1007/s10008-003-0412-x.
- Dagmar Oertel: Energiespeicher – Stand und Perspektiven. In: TAB Arbeitsbericht. Nr. 123, 2008, S. 86–92 (PDF – Abschnitt: Elektrochemische Kondensatoren).
- Volkmar M. Schmidt: Elektrochemische Verfahrenstechnik. Grundlagen, Reaktionstechnik, Prozessoptimierung. Wiley-VCH, Weinheim 2003, ISBN 3-527-29958-0, S. 539–639 (eingeschränkte Vorschau in der Google-Buchsuche – Kapitel 7: Elektrochemische Energietechnik).
- Yu M. Vol’fkovich, T. M. Serdyuk: Electrochemical Capacitors. In: Russian Journal of Electrochemistry. Band 38, Nr. 9, 2002, ISSN 1023-1935, S. 935–959, doi:10.1023/A:1020220425954.
- Jiujun Zhang, Lei Zhang, Hansan Liu, Andy Sun, Ru-Shi Liu: Electrochemical Technologies for Energy Storage and Conversion. Band 1. Wiley-VCH, Weinheim 2011, ISBN 978-3-527-32869-7, S. 317–376 (eingeschränkte Vorschau in der Google-Buchsuche – Kapitel 8: Electrochemical Supercapacitors).
Weblinks
Einzelnachweise
- ↑ a b c d e B. E. Conway: Electrochemical Supercapacitors: Scientific Fundamentals and Technological Applications. Springer, Berlin 1999, ISBN 0-306-45736-9, S. 1–8 (eingeschränkte Vorschau in der Google-Buchsuche). Siehe auch unter Brian E. Conway in Electrochemistry Encyclopedia: ELECTROCHEMICAL CAPACITORS Their Nature, Function, and Applications( abgerufen am 5. Januar 2014)
- ↑ a b c d e Marin S. Halper, James C. Ellenbogen: Supercapacitors: A Brief Overview. In: MITRE Nanosystems Group. März 2006, abgerufen am 14. Mai 2013 (englisch).
- ↑ a b c d e Adam Marcus Namisnyk and J. G. Zhu: A Survey of Electrochemical Super-Capacitor Technology. 2003 (PDF [abgerufen am 5. Januar 2014] Bachelor-Arbeit; University of Technology, Sydney; 2003).
- ↑ a b c d Zbigniew Stojek: The Electrical Double Layer and Its Structure. In: Fritz Scholz (Hrsg.): Electroanalytical Methods: Guide to Experiments and Applications. Springer, Berlin/Heidelberg 2010, ISBN 978-3-642-02914-1, S. 3–10 (online [abgerufen am 5. Januar 2014]).
- ↑ a b B.E. Conway, W.G. Pell, Double-layer and pseudocapacitance types of electrochemical capacitors and their applications to the development of hybrid devices, [1], abgerufen am 5. Januar 2014.
- ↑ a b Mustapha Jammal: Stand der Technik und Anwendung von Superkondensatoren. GRIN Verlag, 2010, ISBN 978-3-640-52396-2 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Elton Capacitor cells, abgerufen am 3. Januar 2014.
- ↑ Patent US2800616: Low voltage electrolytic capacitor. Veröffentlicht am 23. Juli 1957, Erfinder: H. I. Becker.
- ↑ J. Ho, T. R. Jow, S. Boggs: Historical Introduction to Capacitor Technology. (PDF) (abgerufen am 5. Januar 2014)
- ↑ A brief history of supercapacitors. (PDF; 1,5 MB) AUTUMN 2007 – Batteries & Energy Storage Technology, abgerufen am 5. Januar 2014.
- ↑ Patent US3288641: Electrical energy storage apparatus. Veröffentlicht am 29. November 1966, Erfinder: R. A. Rightmire.
- ↑ Patent US3536963: Electrolytic capacitor having carbon paste electrodes. Veröffentlicht am 27. Oktober 1970, Erfinder: D. L. Boos.
- ↑ Panasonic, Electric Double Layer Capacitor, Technical guide,1. Introduction,PDF
- ↑ DynaCap ELNA CO., LTD (abgerufen am 16. Mai 2013)
- ↑ a b c Joel Schindall: The Charge of the Ultra – Capacitors. ieee spectrum, Seite 2, November 2007, abgerufen am 5. Januar 2014.
- ↑ B. E. Conway: Transition from ‘Supercapacitor’ to ‘Battery’ Behavior in Electrochemical Energy Storage. In: Journal of The Electrochemical Society. Band 138, Nr. 6, Mai 1991, S. 1539–1548, doi:10.1149/1.2085829 (PDF).
- ↑ Patent US5369547: Energy Density Electrolytic-Electrochemical Hybrid Capacitor. Veröffentlicht am 29. November 1994, Erfinder: Evans.
- ↑ David A. Evans (Evans Company): High Energy Density Electrolytic-Electrochemical Hybrid Capacitor. In: Proceedings of the 14th Capacitor & Resistor Technology Symposium. 22. März 1994 (PDF, abgerufen am 5. Januar 2014)
- ↑ Capattery® Series Evans Capacitor Company 2007 ((abgerufen am 5. Januar 2014)
- ↑ David A. Evans: The Littlest Big Capacitor – an Evans Hybrid. Technical Paper – Evans Capacitor Company 2007 (abgerufen am 5. Januar 2014)
- ↑ FDK Historie 2000s. FDK Corporation, Corporate Information (abgerufen am 5. Januar 2014)
- ↑ a b c J. M. Miller (Maxwell Technologies Inc.): Energy Storage Technology, Markets and Applications, Ultracapacitor’s in Combination with Lithium-ion. IEEE Rock River Valley, IL, Section, 26. April 2007 (PDF), (abgerufen am 5. Januar 2014)
- ↑ a b c d e E. Frackowiak, F. Beguin: Carbon Materials For The Electrochemical Storage Of Energy In Capacitors. In: CARBON. 39, 2001, S. 937–950 (PDF) und E. Frackowiak, K. Jurewicz, S. Delpeux, F. Béguin: Nanotubular Materials For Supercapacitors. In: Journal of Power Sources. Volumes 97–98, Juli 2001, S. 822–825, doi:10.1016/S0378-7753(01)00736-4, abgerufen am 5. Januar 2014.
- ↑ Roy Peter Richner, Entwicklung neuartig gebundener Kohlenstoffmaterialien für elektrische Doppelschichtkondensatorelektroden, DISS.ETH Nr. 14413, 2001 e-collection.library.ethz.ch (abgerufen am 5. Januar 2014)
- ↑ a b B. P. Bakhmatyuk, B. Y. Venhryn, I. I. Grygorchak, M. M. Micov, S. I. Mudry: Intercalation Pseudo-Capacitance In Carbon Systems Of Energy Storage. In: Rev. Adv. Mater. Sci. Band 14, 2007, S. 151–156 (PDF [abgerufen am 5. Januar 2014]).
- ↑ a b c d e A. G. Pandolfo, A. F. Hollenkamp: Carbon properties and their role in supercapacitors. In: Journal of Power Sources. Band 157, Nr. 1, 2006, S. 11–27, doi:10.1016/j.jpowsour.2006.02.065.
- ↑ a b c d Patrice Simon, A. F. Burke: Nanostructured carbons: double-layer capacitance and more. In: The electrochemical society interface. Band 17, Nr. 1, 2008, S. 38 (PDF; 633 kB [abgerufen am 1. Februar 2015]). Referenzfehler: Ungültiges
<ref>-Tag. Der Name „Simon-Burke“ wurde mehrere Male mit einem unterschiedlichen Inhalt definiert. - ↑ K. Kinoshita: Carbon, Electrochemical and Physicochemical Properties. John Wiley & Sons, New York 1988, ISBN 0-471-84802-6.
- ↑ a b c Dagmar Oertel: Sachstandsbericht zum Monitoring »Nachhaltige Energieversorgung« Energiespeicher – Stand und Perspektiven. In: Arbeitsbericht Nr. 123. S. 86ff (Abschnitt: Elektrochemische Kondensatoren; PDF).
- ↑ Jorge Laine, Simon Yunes: Effect of the preparation method on the pore size distribution of activated carbon from coconut shell. In: Carbon. 30. Jahrgang, Nr. 4, 1992, S. 601–604, doi:10.1016/0008-6223(92)90178-Y.
- ↑ CHUNSHENG DU, NING PAN, Carbon Nanotube-Based Supercapacitors, NANOTECHNOLOGY LAW &BUSINESS , MARCH 2007, PDF
- ↑ U. Fischer, R. Saliger, V. Bock, R. Petricevic, J. Fricke: Carbon Aerogels as Electrode Material in Supercapacitors. In: Journal of Porous Materials. 4. Jahrgang, Nr. 4, 1997, S. 281–285, doi:10.1023/A:1009629423578.
- ↑ M. LaClair: Replacing Energy Storage with Carbon Aerogel Supercapacitors. In: Power Electronics, Feb 1, 2003, Cooper Electronic Technologies, Boynton Beach FL. (powerelectronics.com [abgerufen am 29. Januar 2013]).
- ↑ EJ Lerner: Less is more with aerogels: A laboratory curiosity develops practical uses. In: The Industrial Physicist, 2004
- ↑ M. LaClair: Replacing Energy Storage with Carbon Aerogel Supercapacitors. Power Electronics, 1. Februar 2003, Cooper Electronic Technologies, Boynton Beach FL
- ↑ Graphene aerogel takes world’s lightest material crown.
- ↑ a b Hsing-Chi Chien, Wei-Yun Cheng, Yong-Hui Wang, Shih-Yuan Lu: Ultrahigh Specific Capacitances for Supercapacitors Achieved by Nickel Cobaltite/Carbon Aerogel Composites. In: Advanced Functional Materials. Band 22, Nr. 23, 2012, S. 5038–5043, doi:10.1002/adfm.201201176.
- ↑ Volker Presser, Min Heon, Yury Gogotsi: Carbide-Derived Carbons – From Porous Networks to Nanotubes and Graphene. In: Advanced Functional Materials. Band 21, Nr. 5, 2011, S. 810–833, doi:10.1002/adfm.201002094.
- ↑ Y. Korenblit, M. Rose, E. Kockrick, L. Borchardt, A. Kvit, St. Kaskel, G. Yushin, High-Rate Electrochemical Capacitors Based on Ordered Mesoporous Silicon Carbide-Derived Carbon (PDF; 472 kB)
- ↑ SkelCap Ultracapacitors | Skeleton Technologies. Skeletontech.com, abgerufen am 29. Mai 2013.
- ↑ Michael Mullaney, Rensselaer Polytechnic Institute, 3-Aug-2007, Beyond batteries: Storing power in a sheet of paper
- ↑ J. J. Yoo, K. Balakrishnan, J. Huang, V. Meunier, B. G. Sumpter, A. Srivastava, M. Conway, A. L. M. Reddy, J. Yu, R. Vajtai, P. M. Ajayan: Ultrathin Planar Graphene Supercapacitors. In: Nano Letters. Band 11, Nr. 4, 2011, S. 1423–1427, doi:10.1021/nl200225j.
- ↑ University of Texas at Austin: Breakthrough In Energy Storage: New Carbon Material Shows Promise Of Storing Large Quantities Of Renewable Electrical Energy. ScienceDaily, 17. September 2008, abgerufen am 27. Januar 2014.
- ↑ PhysOrg, Jennifer Marcus, March 15, 2012 , Researchers develop graphene supercapacitor holding promise for portable electronics
- ↑ John R. Miller, R. A. Outlaw, B. C. Holloway: Graphene Double-Layer Capacitor with ac Line-Filtering Performance. In: Science. Band 329, Nr. 5999, 2010, S. 1637–1639, doi:10.1126/science.1194372.
- ↑ a b Prachi Patel: Elektroden aus zerknülltem Kohlenstoff. Technology Review, 9. Dezember 2010, abgerufen am 27. Januar 2014.
- ↑ a b physicsworld.com Graphene supercapacitor breaks storage record
- ↑ Chenguang Liu, Zhenning Yu, Bor Z. Jang, Aruna Zhamu, Bor Z. Jang: Graphene-Based Supercapacitor with an Ultrahigh Energy Density. In: Nano Letters. 10. Jahrgang, Nr. 12. American Chemical Society, 2010, S. 4863–4868, doi:10.1021/nl102661q.
- ↑ a b Wen Lu: Carbon Nanotube Supercapacitors. (PDF; 1,9 MB) ADA Technologies Inc.
- ↑ a b R. Signorelli, D. C. Ku, J. G. Kassakian, J. E. Schindall: Electrochemical Double-Layer Capacitors Using Carbon Nanotube Electrode Structures. In: Proceedings of the IEEE. Band 97, Nr. 11, 2009, S. 1837–1847, doi:10.1109/JPROC.2009.2030240 (Volltext [abgerufen am 29. Januar 2013]).
- ↑ B. Zhang, J. Liang, C. L. Xu, B. Q. Wei, D. B. Ruan, D. H. Wu: Electric double-layer capacitors using carbon nanotube electrodes and organic electrolyte. In: Materials Letters. Band 51, Nr. 6, 2001, S. 539–542, doi:10.1016/S0167-577X(01)00352-4 (PDF [abgerufen am 28. Juli 2013]).
- ↑ Qiao-Ling Chen, Kuan-Hong Xue, Wei Shen, Fei-Fei Tao, Shou-Yin Yin, Wen Xu: Fabrication and electrochemical properties of carbon nanotube array electrode for supercapacitors. In: Electrochimica Acta. Band 49, Nr. 24, 2004, S. 4157–4161, doi:10.1016/j.electacta.2004.04.010.
- ↑ Chunsheng Du, Ning Pan: Carbon Nanotube-Based Supercapacitors. In: Nanotechnology Law & Business. Band 4, 2007, S. 569–576.
- ↑ S. Arepalli, H. Fireman, C. Huffman, P. Moloney, P. Nikolaev, L. Yowell, C.D. Higgins, K. Kim, P.A. Kohl, S.P. Turano, and W.J. Ready: Carbon-Nanotube-Based Electrochemical Double-Layer Capacitor Technologies for Spaceflight Applications. In: JOM. 2005, S. 24–31 (gatech.edu [PDF]).
- ↑ A.C. Dillon: Carbon Nanotubes for Photoconversion and Electrical Energy Storage. In: Chem. Rev. 110. Jahrgang, Nr. 11, 2010, S. 6856–6872, doi:10.1021/cr9003314, PMID 20839769.
- ↑ a b Jian Li, Xiaoqian Cheng, Alexey Shashurin, Michael Keidar: Review of Electrochemical Capacitors Based on Carbon Nanotubes and Graphene. In: Graphene. 2012, 1, 1–13, doi:10.4236/graphene.2012.11001.
- ↑ S. Akbulut: Optimization of Carbon Nanotube Supercapacitor Electrode. (PDF; 5 MB) Graduate School of Vanderbilt University, Nashville TN August 2011.
- ↑ M. Jayalakshmi, K. Balasubramanian: Simple Capacitors to Supercapacitors – An Overview. (PDF; 901 kB) In: Int. J. Electrochem. Sci., 3, 2008, S. 1196–1217
- ↑ J. P. Zheng, P. J. Cygan, T. R. Jow: Hydrous Ruthenium Oxide as an Electrode Material for Electrochemical Capacitors. In: Journal of The Electrochemical Society. Band 142, Nr. 8, 1995, S. 2699–2703, doi:10.1149/1.2050077.
- ↑ J. P. Zheng, T. R. Jow: High energy and high power density electrochemical capacitors. In: Journal of Power Sources. Vol 62, Nr 2, October 1996, S. 155–159, doi:10.1016/S0378-7753(96)02424-X.
- ↑ P. Simon, Y.Gogotsi, Materials for electrochemical capacitors, nature materials (PDF; 1 MB), VOL 7, NOVEMBER 2008.
- ↑ H. Abruna: Batteries and electrochemical capacitors. (PDF; 511 kB) American Institute of Physics, Dezember 2008.
- ↑ Volkmar M. Schmidt: Elektrochemische Verfahrenstechnik. Grundlagen, Reaktionstechnik, Prozessoptimierung. Wiley-VCH, Weinheim 2003, ISBN 3-527-29958-0, S. 584 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Yu.M. Volfkovich, A.A. Mikhailin, D.A. Bograchev, V.E. Sosenkin, V.S. Bagotsky: Studies of Supercapacitor Carbon Electrodes with High Pseudocapacitance. (PDF; 990 kB) A. N. Frumkin Institute of Physical Chemistry and Electrochemistry, Russian Academy of Sciences, Moscow, Russia, Ujjal Kumar Sur (Ed.), ISBN 978-953-307-830-4.
- ↑ M. Morita, M. Araki, N. Yoshimoto: Pseudo-capacitance of Activated Carbon Fiber Coated by Polythiophenes. In: 2004 Joint International Meeting, E1 – Electrochemical Capacitor and Hybrid Power Sources. Electrochemical Society, 3.–8. Okt. 2004 (Abs# 676, PDF)
- ↑ E. Frackowiak, V. Khomenko, K. Jurewicz, K. Lota, F. Béguin: Supercapacitors based on conducting polymers/nanotubes composites. In: Journal of Power Sources. Band 153, Nr. 2, 2006, S. 413–418, doi:10.1016/j.jpowsour.2005.05.030.
- ↑ a b K. Naoi, P. Simon: New Materials and New Configurations for Advanced Electrochemical Capacitors. ECS, Vol. 17, No. 1, Spring 2008, PDF.
- ↑ H. Gualous et al.: Lithium Ion capacitor characterization and modelling. ESSCAP’08 – 3rd European Symposium on Supercapacitors and Applications, Rome/Italy 2008, PDF.
- ↑ Tetraethylammonium tetrafluoroborate – Compound Summary 2724277
- ↑ Matthias Dötterl: Hauptseminar Supercapacitors Superkondensatoren. (PowerPoint), 12. Dezember 2006, abgerufen 28. Juli 2013
- ↑ G. Bühler: ULTRACAPS – EIGENSCHAFTEN UND EINSATZGEBIETE. (PDF; 289 kB) In: JAHRESBERICHT 2000 des IMAB der TU Braunschweig, abgerufen am 23. Juli 2012.
- ↑ NESSCAP ULTRACAPACITOR – TECHNICAL GUIDE. (PDF; 337 kB) NESSCAP Co., Ltd. 2008, abgerufen am 23. Juli 2012.
- ↑ a b Product Guide – Maxwell Technologies BOOSTCAP Ultracapacitors (PDF; 267 kB) Maxwell Technologies, Inc. 2009, Doc. No. 1014627.1, abgerufen am 25. September 2012.
- ↑ Maxwell, K2 series, PDF
- ↑ APPLICATION NOTE – Energy Storage Modules Life Duration Estimation. (PDF; 150 kB) Maxwell Technologies, Inc. 2007, abgerufen am 30. Januar 2013.
- ↑ Gold capacitors Characteristics data. (PDF; 409 kB) In: Technical Guide of Electric Double Layer Capacitors, Edition 7.4, Panasonic Electronic Devices, 2011
- ↑ APowerCap
- ↑ AVX Kyocera, BestCap® (PDF; 869 kB)
- ↑ Cap-XX
- ↑ CDE Cornell Dubilier Supercapacitor
- ↑ Cooper Bussmann, PowerStor
- ↑ Elna, DYNACAP (PDF; 7,1 MB)
- ↑ Elton
- ↑ Evans Capacitor Company, Capattery
- ↑ Beijing HCC Energy Technology Co., HCAP
- ↑ FDK To Begin Mass Production of High-Capacity Li-Ion Capacitors. FDK, AFEC Asahi Kasei FDK Energy Device Co., Ltd., greencarcongress.com siehe auch EneCapTen afec.co.jp
- ↑ Illinois Capacitor Inc., Supercapacitor
- ↑ ioxus Inc., Supercapacitor
- ↑ JSR Micro, Ultimo
- ↑ Korchip, STARCAP
- ↑ Chaoyang Liyuan New Energy Co., Supercapacitor
- ↑ LSMtron, Ultracapacitor
- ↑ Maxwell Technologies, Ultracapacitor
- ↑ Murata Manufactoring Co., EDLC
- ↑ NEC Tokin, Supercapacitor
- ↑ Nesscap Energy Inc., Ultracapacitor, Pseudocapacitor
- ↑ Nichicon,EVerCAP
- ↑ Nippon Chemi-Con, NCC, ECC, UCC, DLCCAP
- ↑ Panasonic, Matsushita, Goldcap
- ↑ Samwha Electric Co., GreenCap
- ↑ Skeleton, SkelCap (PDF; 9,1 MB)
- ↑ Taiyo Yuden, PAS Capacitor, LIC Capacitor
- ↑ Vina Technology Co., Hy-Cap
- ↑ Wima Spezialvertrieb Elektronischer Bauelemente, SuperCaps
- ↑ YEC Yeon Long Technologies, Kapton capacitor
- ↑ Yunasco
- ↑ a b P. Van den Bossche u. a.: The Cell versus the System: Standardization challenges for electricity storage devices (PDF; 976 kB) EVS24 International Battery, Hybrid and Fuel Cell Electric Vehicle Symposium, Stavanger/Norway 2009.
- ↑ Normen-Bezugsquelle: Beuth Verlag
- ↑ Graham Pitcher If the cap fits .. (PDF; 184 kB). New Electronics. 26 March 2006.
- ↑ a b c d e R. Gallay, Garmanage, Technologies and applications of Supercapacitors (PDF; 3,2 MB), University of Mondragon, June 22th 2012.
- ↑ Ultracapacitor LED Flashlight Charges In 90 Seconds – Slashdot. Tech.slashdot.org, 10. Dezember 2008, abgerufen am 21. Oktober 2013.
- ↑ Light For Life Flashlight thefutureofthings.com
- ↑ Coleman FlashCell Cordless Screwdriver Recharges In Just 90 Seconds. OhGizmo!, 11. September 2007, abgerufen am 29. Mai 2013.
- ↑ Helium Bluetooth speakers powered by supercapacitors. Gizmag.com, abgerufen am 29. November 2013.
- ↑ David A. Johnson, P.E.: SuperCapacitors as Energy Storage. Discoversolarenergy.com, abgerufen am 29. Mai 2013.
- ↑ A. Stepanov, I. Galkin, Development of supercapacitor based uninterruptible power supply (PDF; 223 kB), Doctoral school of energy- and geo-technology, January 15–20, 2007. Kuressaare, Estonia
- ↑ Supercapacitor UPS. Marathon Power, abgerufen am 29. Mai 2013.
- ↑ a b SINAUTEC, Automobile Technology, LLC. Sinautecus.com, abgerufen am 29. Mai 2013.
- ↑ a b Maxwell Technologies Ultracapacitors (ups power supply) Uninterruptible Power Supply Solutions. Maxwell.com, abgerufen am 29. Mai 2013.
- ↑ International Energy Agency, Photovoltaic Power Systems Program, The role of energy storage for mini-grid stabilization, IEA PVPS Task 11, Report IEA-PVPS T11-02:2011, July 2011 iea-pvps-task11.org (PDF; 2 MB)
- ↑ J. R. Miller, JME, Inc. and Case Western Reserve University, Capacitors for Power Grid Storage, (Multi-Hour Bulk Energy Storage using Capacitors) (PDF; 867 kB)
- ↑ A 30 Wh/kg Supercapacitor for Solar Energy and a New Battery > JEOL Ltd. Jeol.com, 3. Oktober 2007, abgerufen am 24. Juli 2013.
- ↑ Nippon Chemi-Con, Stanley Electric and Tamura announce: Development of “Super CaLeCS”, an environment-friendly EDLC-powered LED Street Lamp. (PDF; 327 kB) Press Release Nippon Chemi-Con Corp., 30. März 2010.
- ↑ Beste Unterhaltung über den Wolken. In: Internationale Seilbahn Rundschau (ISR)
- ↑ Londoner Emirates Air Line: Teuerste Seilbahn der Welt mit fraglicher verkehrlicher Bedeutung. zukunft-mobilitaet.net
- ↑ yec.com.tw: super capacitor supplier list | YEC | This high-energy capacitor from a defibrillator can deliver a lethal 500 joules of energy. YEC, abgerufen am 29. Mai 2013.
- ↑ Cantec Systems, Power solutions
- ↑ High Energy Density Capacitors for Military Applications. (PDF; 4,4 MB) Evans Capacitor Company
- ↑ Back-up power for military applications- Batteries optional! Tecate Group
- ↑ BusBus-Hamburg
- ↑ Maxwell Ultracapacitor Transportation Solutions. Maxwell Technologies.
- ↑ a b J. R. Miller, A. F. Burke, Electrochemical Capacitors: Challenges and Opportunities for Real-World Applications, ECS, Vol. 17, No. 1, Spring 2008 (PDF)
- ↑ L. Lionginas, L. Povilas, Management of Locomotive Tractive Energy Resources (PDF; 792 kB)
- ↑ A. Jaafar, B. Sareni, X. Roboam, M. Thiounn-Guermeur: IEEE Xplore – Sizing of a hybrid locomotive based on accumulators and ultracapacitors. Ieeexplore.ieee.org, 3. September 2010, abgerufen am 29. Mai 2013 (10.1109/VPPC.2010.5729131).
- ↑ Fuel Cell Works Supplemental News Page. fuelcellworks.com, abgerufen am 29. Mai 2013. Fehler beim Aufruf der Vorlage:Cite web: Archiv im Parameter URL erkannt. Archive müssen im Parameter Archiv-URL angegeben werden.
- ↑ Bombardier, MITRAC Energy Saver Presentation PDF
- ↑ Freiburg: BZ auf Werksbesuch: Spanier fertigen neue Freiburger Straßenbahnen – badische-zeitung.de. 21. April 2014, abgerufen am 29. April 2014.
- ↑ Michael Fröhlich, Markus Klohr, Stanislaus Pagiela: Energy Storage System with UltraCaps on Board of Railway Vehicles. In: Proceedings – 8th World Congress on Railway Research. Mai 2008, Soul, Korea (PDF, siehe auch Vortrag: MITRAC Energy Saver (PDF; 517 kB)).
- ↑ SuperCap tests complete railwaygazette.com
- ↑ Rhein-Neckar Verkehr orders more supercapacitor trams. Railway Gazette, 5. April 2011, abgerufen am 29. Mai 2013.
- ↑ Siemens, Materialien für die Umwelt – Energiespeicher, Schnelle Stromdepots [2]
- ↑ Supercapacitors to be tested on Paris STEEM tram. Railway Gazette, 8. Juli 2009, abgerufen am 29. Mai 2013.
- ↑ Erlass des Präfekten (2009) (frz.) abgerufen 25. November 2013
- ↑ Genève tram trial assesses supercapacitor performance. Railway Gazette, 7. August 2012, abgerufen am 29. Mai 2013.
- ↑ Supercapacitor light metro train unveiled. Railway Gazette, 23. August 2012, abgerufen am 29. Mai 2013.
- ↑ Supercapacitor energy storage for South Island Line. Railway Gazette, 3. August 2012, abgerufen am 29. Mai 2013.
- ↑ Der Ultracapbus, ein alternatives Antriebssystem im Alltagstest. VAG Nürnberg, abgerufen am 24. Juli 2012
- ↑ Stefan Kerschl, Eberhard Hipp, Gerald Lexen: Effizienter Hybridantrieb mit Ultracaps für Stadtbusse. 14. Aachener Kolloquium Fahrzeug- und Motorentechnik 2005 (PDF)
- ↑ V.Härri, S.Eigen, B.Zemp, D.Carriero: Kleinbus „TOHYCO-Rider“ mit SAM-Superkapazitätenspeicher. Jahresbericht 2003 – Programm „Verkehr & Akkumulatoren“, HTA Luzern, Fachhochschule Zentralschweiz (PDF)
- ↑ TOHYCO Rider Fgyre. Ebookbrowse.com, abgerufen am 29. Mai 2013.
- ↑ Tyler Hamilton: Next Stop: Ultracapacitor Buses | MIT Technology Review. Technologyreview.com, 19. Oktober 2009, abgerufen am 29. Mai 2013.
- ↑ a b Superkondensatoren: Der bessere Stromspeicher fürs Elektroauto. In: Die Zeit, Nr. 10/2012.
- ↑ Green 'tribrid' minibus unveiled In: BBC, 5. Juni 2008. Abgerufen am 12. Januar 2013
- ↑ Launch of Europe’s First Tribrid Green Minibus, 30. Mai 2008. Abgerufen am 12. Januar 2013
- ↑ Tony Purnell, Peter Wright: Formula One 2011: Power-Train Regulation Framework. FIA, Version 1.3, 2007 (PDF)
- ↑ Christian Nimmervoll: Die große Analyse: KERS für Dummys. Motorsport-Total.com, 25. März 2009, abgerufen am 24. Juli 2012.
- ↑ Lern das auswendig, Spiegel-Gespräch mit Sebastian Vettel. In: Der Spiegel. Nr. 7, 2011, S. 112–115 (online).
- ↑ Toyota TS030 LMP1 hybrid revealed. Racecar Engineering, 24. Januar 2012, abgerufen am 30. Mai 2013.
- ↑ Die Hybridtechnik im Toyota TS030: Mit Superkondensatoren zum LeMans-Erfolg. sportauto.de
- ↑ Fred Jaillet: Post TOYOTA Racing Impresses In Le Mans Qualifying – TOYOTA Racing – FIA World Endurance Championship Team. Toyotahybridracing.com, 15. Juni 2012, abgerufen am 30. Mai 2013.
- ↑ A.F. Burke: Batteries and Ultracapacitors for Electric, Hybrid, and Fuel Cell Vehicles.
- ↑ A. Pesaran, J. Gonder: Recent Analysis of UCAPs in Mild Hybrids. (PDF; 688 kB) National Renewable Energy Laboratory, Golden CO, 6th Advanced Automotive Battery Conference, Baltimore MD, May 17–19, 2006.
- ↑ Cap-XX Supercapacitors for Automotive & Other Vehicle Applications (PDF; 1,1 MB), March 2012.
- ↑ AFS Trinity Unveils 150 mpg Extreme Hybrid (XH™) SUV (PDF; 1,6 MB) AFS Trinity Power Corporation. 13. Januar 2008; abgerufen 31. März 2013.
- ↑ A. Pesaran,T. Markel, M. Zolot, S. Sprik: Ultracapacitors and Batteries in Hybrid Vehicles. (PDF; 1 MB)
- ↑ Mazda präsentiert regeneratives Bremssystem mit Kondensator zur Energiespeicherung, 28. Nov 2011, grueneautos.com
- ↑ Mazda 2 mit Elektroantrieb startet in Japan im Oktober 2012, grueneautos.com
- ↑ Auto news, 2014 Mazda6 i-Eloop to net 40 mpg hwy, 28 mpg city autoblog.com
- ↑ i-Eloop im neuen Mazda 6: Ungewöhnliches Rekuperationssystem. In: Auto-Motor-Sport, Heft 17, 2012.
- ↑ M. Bodach, H. Mehlich, F. Hiller, S. König, D. Hrabal, J. De Roche: Zuverlässigkeit von Superkondensatoren im Hinblick auf Anwendungen im Automobil. In: ETG Fachbericht Internationaler ETG Kongress Karlsruhe 2007. VDE Verlag GmbH, ISBN 978-3-8007-3063-6. (siehe auch Vortragsfolien von M. Bodach, H. Mehlich: Zuverlässigkeitsaspekte bei der Anwendung von Supercaps.; PDF; 1,7 MB)
- ↑ Nippon Chemi-Con liefert elektrische Doppelschicht-Kondensatoren (DLCAP) für PKWs. (PDF; 169 kB) Press Release Nippon Chemi-Con Corp., 6. Dezember 2011.
- ↑ Grueneautos, 17. Sep 2011, Yo-Auto auf der IAA 2011: ë-Concept und ë-Crossover mit Hybridantrieb grueneautos.com und grueneautos.com
- ↑ A. E. Kramer: Billionaire Backs a Gas-Electric Hybrid Car to Be Built in Russia. In: The New York Times, 13. Dezember 2010.
- ↑ Francesco Lufrano, Pietro Staiti: A bibliometric analysis of the international literature in supercapacitors. In: Int. J. Electrochem. Sci. Band 4, 2009, S. 173–186 (PDF).
- ↑ Xiaowei Yang, Chi Cheng, Yufei Wang, Ling Qiu, Dan Li: Liquid-Mediated Dense Integration of Graphene Materials for Compact Capacitive Energy Storage. In: Science. Band 341, Nr. 6145, 2013, S. 534–537, doi:10.1126/science.1239089, PMID 23908233.
- ↑ Fastcap: Paradigm shift. FastCap Systems, abgerufen am 30. Mai 2013.
- ↑ Belle Dumé: Graphene supercapacitor breaks storage record. physicsworld.com 26. November 2010, abgerufen am 25. Juli 2013.
- ↑ New carbon material boosts supercapacitors. Rsc.org, 13. Mai 2011, abgerufen am 30. Mai 2013.
- ↑ Yanwu Zhu u. a.: Carbon-Based Supercapacitors Produced by Activation of Graphene. In: Science. Band 332, Nr. 6037, 2011, S. 1537–1541, doi:10.1126/science.1200770, PMID 21566159.
- ↑ TaeYoung Kim, Gyujin Jung, Seonmi Yoo, Kwang S. Suh, Rodney S. Ruoff , Activated Graphene-Based Carbons as Supercapacitor Electrodes with Macro- and Mesopores doi:10.1021/nn402077v
- ↑ Long Zhang u. a.: Porous 3D graphene-based bulk materials with exceptional high surface area and excellent conductivity for supercapacitors. In: Scientific Reports. Band 3, 2013, doi:10.1038/srep01408, PMID 23474952.
- ↑ K. Hata u. a.: High-power supercapacitor electrodes from single-walled carbon nanohorn/nanotube composite. In: ACS Nano, 5, Nr. 2, 2011, pp 811–819, doi:10.1021/nn1017457
- ↑ Microporous polymer material for supercapacitors with large capacitance, high energy and power densities and excellent cycle life
- ↑ Yan Kou, Yanhong Xu, Zhaoqi Guo, Donglin Jiang: Supercapacitive Energy Storage and Electric Power Supply Using an Aza-Fused π-Conjugated Microporous Framework. In: Angewandte Chemie. 123, 2011, S. 8912–8916, doi:10.1002/ange.201103493.
- ↑ Zhe Tang, Chun-hua Tang, Hao Gong: A High Energy Density Asymmetric Supercapacitor from Nano-architectured Ni(OH)2/Carbon Nanotube Electrodes. In: Advanced Functional Materials. Band 22, Nr. 6, 2012, S. 1272–1278, doi:10.1002/adfm.201102796.
- ↑ Nippon Chemi-Con announces: The advanced new technology Nano-hybrid Capacitor. (PDF; 1,1 MB) Press Release Nippon Chemi-Con Corp., 26. März 2010.
- ↑ Liqiang Mai u. a.: Fast Ionic Diffusion-Enabled Nanoflake Electrode by Spontaneous Electrochemical Pre-Intercalation for High-Performance Supercapacitor. In: Scientific Reports. Band 3, 2013, doi:10.1038/srep01718, PMID 23611904.
- ↑ Zhong-Shuai Wu, Xinliang Feng, Hui-Ming Cheng: Recent advances in graphene-based planar micro-supercapacitors for on-chip energy storage. In: National Science Review. 2013, S. nwt003, doi:10.1093/nsr/nwt003.
- ↑ K.-H. Heckner: Elektrochemische Energiespeicher und -wandler für dynamische Anforderungen. 6th Leibniz Conference Of Advanced Science, Lichtenwalde 18. Juni 2008 (Vortragsfolien; PDF; 3,1 MB).
- ↑ Patent WO2003003466: Quantum supercapacitor. Erfinder: Alexander Milhailovich.
- ↑ Patent WO2004004026: Verfahren zur Herstellung von Superkondensatoren. Veröffentlicht am 8. Januar 2004, Erfinder: Rolf Eisenring.
- ↑ Method And Device For Storing Electricity In Quantum Batteries – Patent Application. Faqs.org, abgerufen am 30. Mai 2013. Inventors: Rolf Eisenring (Oberengstringen, CH), IPC8 Class: AH01G430FI, USPC Class: 3613014, Class name: Electrostatic capacitors fixed capacitor stack, Publication date: 2009-08-06, Patent application number: 20090195961
- ↑ A. Raut, C. Parker, and J. Glass: A method to obtain a Ragone plot for evaluation of carbon nanotube supercapacitor electrodes. In: Journal of Materials Research Vol. 25, No. 8, Nr. 2010, doi:10.1557/JMR.2010.0192
- ↑ NanoMarkets forecasts supercapacitor market to reach $3B in 2016; decrease in transportation market share. Green Car Congress, 21. November 2010, abgerufen am 30. Mai 2013.
- ↑ Global Battery Markets Information – Battery University. Batteryuniversity.com, abgerufen am 30. Mai 2013.
- ↑ highbeam business, Electronic Capacitors SIC 3675, Industry report
- ↑ Dennis Zogbi: Supercapacitors the Myth, the Potential and the Reality. Paumanok Group, 4. März 2013.
- ↑ March 16, 2012: Ultracapacitor Market Forecast 2015–2020. Market Research Media, 16. März 2012, abgerufen am 30. Mai 2013.
- ↑ T2+2™ Market Overview (PDF; 61 kB), Ch. Ahern, Supercapacitors, December 10, 2009, Project Number NET0007IO