„Lazarus-Effekt“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
→Weblinks: Weblink entf.: Spiegel-Artikel bezieht sich ausschließlich auf Felsenratte und insbesondere dessen Merkmal "Lebendes Fossil", nicht allgemein auf Thema "Lazarus-Arten" |
→Weichtiere: - Vorlage "Belege fehlen"; unbelegte Aussagen durch belegte ers.+ erg. (IUCN 2000; IUCN 2018; Whelan&al2012_PLoSONE_7_8_e42499): Rhachistia aldabrae: "Only isolated individuals were found in the 1980s, and one in 1997. The species was then considered to be extinct until its rediscovery in 2014." |
||
| Zeile 436: | Zeile 436: | ||
===== Weichtiere ===== |
===== Weichtiere ===== |
||
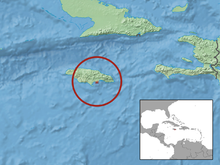
* [[Aldabra-Schnecke]] (''Rhachistia aldabrae''): Diese landlebende [[Landlungenschnecken]]-Art aus der Familie [[Cerastidae]] lebt nur auf dem [[Aldabra]]-[[Atoll]] ([[Seychellen]]). Nachdem von ihr in den 1980er Jahren noch vereinzelt frische [[Schneckenhaus|Schneckengehäuse]] gefunden sowie ein einzelnes im Jahr 1997, wurden trotz intensiver Suche zunächst keine Spuren ihres fortgesetzten Überlebens mehr entdeckt und sie galt als ausgestorben, bis sie 2014 wiederentdeckt wurde. Die Art wird als „vom Aussterben bedroht“ eingestuft (IUCN, 2018).<ref name="IUCN_168122_67485998">{{IUCN|Year=2018|ID=168122|ScientificName=Rhachistia aldabrae|YearAssessed=2017|AssessmentID=67485998|Assessor=Gerlach, J.|Download=2022-05-22}}</ref> |
|||
{{Belege fehlen|1=}} |
|||
* ''[[Leptoxis compacta]]'': Süßwasserbewohnende Schnecken-Art aus der Familie Pleuroceridae mit Verbreitungsgebiet in [[Alabama]] (USA). Von der IUCN wird die Art – mit Hinweis auf Aktualisierungsbedarf – als „ausgestorben“ geführt (IUCN, 2000).<ref name="IUCN_11774_3304833">{{IUCN|Year=2000|ID=11774|ScientificName=Leptoxis compacta|YearAssessed=2000|AssessmentID=3304833|Assessor=Bogan, A.E. (Mollusc Specialist Group)|Download=2022-05-22}}</ref> Die Art wurde Untersuchungen von Museumssammlungen zufolge wohl 1933 zum letzten Mal gesammelt. Im Jahr 2000 wurde sie formell für ausgestorben erklärt, 2011 aber im Cahaba River wiederentdeckt.<ref name="Whelan&al2012_PLoSONE_7_8_e42499">{{Literatur |Autor=Nathan V. Whelan, Paul D. Johnson, Phil M. Harris |Titel=Rediscovery of Leptoxis compacta (Anthony, 1854) (Gastropoda: Cerithioidea: Pleuroceridae) |Sammelwerk=PLoS ONE |Band=7 |Nummer=8 |Datum=2012 |ArtikelNr=42499 |DOI=10.1371/journal.pone.0042499 |Kommentar=Vollständige Artikel-Nr.: e42499}}</ref> |
|||
* [[Aldabra-Schnecke]] (''Rhachistia aldabrae''), landlebende [[Landlungenschnecken|Landlungenschnecke]] vom [[Aldabra-Atoll]], [[Seychellen]], 2009 für ausgestorben erklärt, jedoch 2014 wiederentdeckt.<!-- Beleg fehlt --> |
|||
* ''[[Leptoxis compacta]]'', Süßwasserschnecke aus Alabama, USA: keine Nachweise zwischen 1933 und 2011<!-- Beleg fehlt --> |
|||
===== Nesseltiere ===== |
===== Nesseltiere ===== |
||
Version vom 22. Mai 2022, 20:04 Uhr
Unter dem Lazarus-Effekt versteht man in der Paläontologie das vorübergehende Nichterscheinen von Taxa (beispielsweise im Rang von Familien) im Fossilbericht, häufig mit Bezug auf die Zeit von Massenaussterben. In der Naturschutzbiologie bezieht sich der Ausdruck auf die Wiederauffindung von Taxa (in der Regel im Rang von Arten oder Unterarten), die bereits als ausgestorben gelistet worden waren, also auf ihre Entfernung von der Liste ausgestorbener Arten.
Namensherkunft
Der naturwissenschaftliche Begriff wurde nach dem biblischen Charakter Lazarus des Neues Testaments benannt, der nach religiösem Glauben Tage nach seinem Tod eine Auferweckung durchlief,[1] also durch ein Wunder von den Toten wiederauferstand.[2][3]
Begriffsgeschichte und Bedeutung
Der Begriff wurde ursprünglich in der Paläontologie für vorübergehend im Fossilbericht fehlende Taxa definiert,[2] nachträglich aber in anderem Sinn auf rezente Arten oder Taxa, die wiederentdeckt wurden, nachdem sie einige Zeit als ausgestorben galten, übertragen.[4]
Paläontologische Konzepte
In der Paläontologie bezeichnet der Lazarus-Effekt ein vorübergehendes Verschwinden von Taxa aus dem Fossilbericht. Allerdings ist es im Zusammenhang mit dem „Lazarus-Effekt“ zu einer Vielzahl an Definitionen und Auslegungen gekommen, die zu erheblicher Begriffsverwirrung geführt haben. Viele Wissenschaftler beschränken die Verwendung des Begriffes auf die Zeitspannen während der Massenaussterben-Ereignisse, während einige andere damit ein Muster ansprechen, das sich auf bestimmte Zeitspannen bezieht, aber nicht auf Massenaussterben beschränkt ist. Entscheidend für die Bestimmung, was genau mit dem Begriff „Lazarus-Effekt“ bezeichnet werden soll, ist, ob der Fossilbericht als eine die angesprochenen evolutiven Abläufe angemessen darstellende Quelle angenommen werden soll oder ob der Fossilbericht für den angesprochenen Fall als unvollständig aufzufassen sein soll.[2]
Lazarus-Taxa als stratigraphisches Phänomen
Wird von einem unvollständigen Fossilbericht ausgegangen, dann wird mit dem Lazarus-Effekt die Unvollständigkeit der geologischen Überlieferung angesprochen, also ein stratigraphisches Phänomen.[2]
In Anlehnung an frühere Beobachtungen von Batten (1973) prägte David Jablonski 1983 den Begriff Lazarus-Effekt (englisch Lazarus effect, Fessa & Jablonski 1983[5]) am Beispiel einer Anzahl von Familien und vieler Gattungen, die kurz vor der Perm-Trias-Grenze (und dem damit verbundenen Massenaussterben) oder kurz vor der Kreide-Paläogen-Grenze (und dem damit verbundenen Massenaussterben) aus dem Fossilbericht verschwinden, kurz nach der jeweiligen Grenze dann aber wieder im Fossilbericht erscheinen.[5] 1986 entwickelte Jablonski das Konzept der Lazarus-Taxa (englisch Lazarus Taxa, Jablonski 1986) weiter.[2] Er beschrieb damit das Phänomen, dass einige Taxa vor einem Massenaussterbeerereignis aus dem Fossilbericht verschwinden (scheinbar aussterben), später aber wieder im Fossilbericht erscheinen, dass also für diese Taxa „Lücken“ im Fossilbericht während einer Zeit des Massenaussterbens entstehen.[6] Trotz des Nichterscheinens dieser Taxa in einer bestimmten Zeitspanne, also trotz dieser „Lücke“ in der geologischen Überlieferung während eines Massenaussterbens, kann ihr Fortbestehen während der Zeitspanne dieser „Lücke“ aus ihrem Erscheinen im Fossilbericht jüngerer und älterer Schichten geschlossen werden.[2] Der Lararus-Effekt (im Sinne von Jablonski, 1986) bezeichnet also im Fossilbericht das „Verschwinden und scheinbare Aussterben von Taxa, die später unversehrt wieder auftauchen“.[7]
Das Wissen um das Konzept der Lazarus-Taxa erlangt dadurch Bedeutung, dass ihr Vorkommen Hinweise auf die Qualität des Fossilberichts während eines Massensterbens geben kann.[8][2] Je mehr Lazarus-Taxa vorliegen und je größer die „Lücke“ in der geologischen Überlieferung während eines Massenaussterbens ist, desto unvollständiger ist der Fossilbericht.[8]
Lazarus-Taxa als biologisches Phänomen
Wird von einem adäquat vorliegenden Fossilbericht ausgegangen, dann wird mit dem Lazarus-Effekt ein echtes, mit dem Aussterben verbundenes Phänomen angesprochen, also ein biologisches Phänomen.[2] Grund für das Fehlen einiger Taxa während einer bestimmten Zeitspanne der geologischen Überlieferung kann eine tatsächliche Erholung nach einem Beinahe-Aussterben sein.[2] Diese biologische Auslegung ist als der stratigraphischen Interpretation untergeordnet zu betrachten und nur zu bevorzugen, wenn die stratigraphische Auslegung nicht dokumentiert werden kann.[2]
Abgrenzung zum Konzept der Elvis taxa
Bereits Batten (1973) und Erwin & Droser (1993) haben darauf hingewiesen, dass die verglichenen Taxa exakt und konsistent taxonomisch einander zugeordnet sein müssen, damit entschieden werden kann, ob bei einem Befund tatsächliche Lazarus-Taxa vorliegen oder aber davon zu unterscheidende Elvis-Taxa (englisch Elvis taxa, Erwin & Droser 1993).[2]
Das paläontologische Konzept der Elvis-Taxa betrifft Taxa im Fossilbericht, die einander ähnlich im Sinne von morphologisch konvergent, aber nicht miteinander stammesgeschichtlich verwandt sind.[8][2][9] Die Elvis taxa sind als taxonomische Artefakte aufzufassen.[8]
Beispiele für Lazarus-Taxa (im paläontologischen Sinn)
Ein Beispiel für Lazarus-Arten im Zusammenhang mit dem Massenaussterben an der Perm-Trias-Grenze sind Seeigel und andere Gruppen, die etwa in der Mitte des Trias, etwa 25 Millionen Jahre nach dem großen Massenaussterben, wieder im Fossilbericht erscheinen und als verhältnismäßig empfindlich auf Umweltveränderungen reagierende Organismen die Normalisierung der marinen Lebensbedingungen kennzeichnen.[10] Während des gleichen Massenaussterbenereignisses gab es auch unter Gastropoden, Bivalvien und articulaten Brachiopoden eine erhebliche Anzahl von Lazarus-Taxa.[11]
Rezent lebende Beispiele für Lazarus-Taxa (im paläontologischen Sinn)
Einen Sonderfall des Lazarus-Effekts im Sinne des Wiedererscheinens von Taxa nach einem längeren Hiatus im Fossilbericht stellt die Entdeckung lebender Exemplare ausgestorben geglaubter Taxa dar (nach Dawson & al., 2006).[12] Solche Entdeckungen wurden bei Säugetieren und anderen Wirbeltieren nur selten dokumentiert.[12]
- Chaco-Pekari (Catagonus wagneri): rezente Individuen der Art wurden in den 1920er Jahren im bolivianischen Teil des Gran Chaco als unbeschriebene dritte und scheinbar neuentdeckte Art der damals bekannten Vertreter der Familie Nabelschweine oder Pekaris entdeckt und konnten später vom Mammalogen Martin Eisentraut gesichtet werden.[13] Erst 1975 wurde diese dritte rezente Pekari-Art dann anhand von im paraguayanischen Teil des Gran Chaco entdeckten rezenten Individuen wissenschaftlich beschrieben, wobei diese Individuen jedoch der in der Paläontologie 1930 bereits erstbeschriebenen Art Catagonus wagneri zugeordnet werden konnten, die anhand von fossil und subfossil im unteren und mittleren Pleistozän Nordargentiniens erhaltenen Knochenresten bekannt war,[14][15][16][13] bereits zum Zeitpunkt ihrer Erstbeschreibung als ausgerottet galt[17] und nun also in gewissem Sinne in der rezenten Tierwelt „wiederentdeckt“ wurde.[14][15][16][13] 1985 wurde die Art durch Eisentraut auch für ihr zuvor schon gemeldetes Verbreitungsareal in Bolivien bestätigt. – Dieser Fall ist ein aufsehenerregendes Beispiel für den Nachweis einer Säugetierart mit beachtlicher Körpergröße in der rezenten Fauna, die der Wissenschaft zunächst nur fossil bis subfossil bekannt war.[13][16][18] Allerdings reagieren die vereinzelten Freilandpopulationen sehr empfindlich auf anthropogene Eingriffe und der Gesamtbestand der als „stark gefährdet“ eingestuften Art (IUCN, 2015[19]) wird auf nur noch wenige tausend Individuen geschätzt.[20]
- Laotische Felsenratte (Laonastes aenigmamus): Die Art gilt als besonders eindrückliches Beispiel für den „Lazarus-Effekt“ in der Gruppe rezenter Säugetiere. In diesem Fall wurde demnach nach einer zeitlichen Nachweis-„Lücke“ von rund 11 Millionen Jahren ein ehemals als ausgestorben betrachtetes Taxon (die sonst zuletzt aus den frühen Oligozän- und späten Miozän-Schichten fossil belegte Nagetier-Familie der Diatomyidae) in der Biota der Gegenwart wiederentdeckt.[21][22][23][24] 1996 wurden erstmals Kadaver der Art als angebotenes Nahrungsmittel in Süd-Laos von Wissenschaftlern entdeckt.[25] 2005 wurde anhand des Materials die Familie Laonastidae, die Gattung Laonastes und die Art L. aenigmamus wissenschaftlich beschrieben.[25][22] Lebende Exemplare konnten gefilmt und eingefangen werden.[23] 2006 wurde die Art in die Familie Diatomyidae gestellt.[21][22] 2007 wurde die umstrittene taxonomische Stellung der Art im Stammbaum der Säugetiere und damit die umstrittene Einordnung als Lazarus-Art mit molekularbiologischen Methoden überprüft und die Zugehörigkeit zur Familie Diatomyidae bestätigt. Aufgrund dieser anhand von morphologischen und molekularen Daten vorgenommenen Klassifikation wurde die Hypothese aufgestellt, dass es sich bei der Art um ein lebendes Fossil handelt.[22][21][23]
- Bergbilchbeutler (Burramys parvus): Diese Bilchbeutlerart wurde 1895 anhand von fossilem Material aus New South Wales beschrieben, das als dem Pleistozän zugehörig gedeutet wurde. Sie wurde für eine bis dahin unbekannte und ausgestorbene Beuteltier-Art gehalten. 1966 wurde dann in einer Skihütte auf dem Mount Hotham ein lebendes Individuum entdeckt, womit die fossil bekannte Art als auf alpines und subalpines Element der Rezentfauna wiederentdeckt wurde. – Kaum als rezent überlebendes Faunenelement „wieder“entdeckt, wurde die Art allerdings als „vom Aussterben bedroht“ (IUCN, 2008[26]) eingestuft. Denn aufgrund fehlender höher gelegener Rückzugsgebiete oder Korridore zum Ausweichen in den klimatisch kälteren Süden der Südhalbkugel wird für den erwarteten Fall des Eintretens der prognostizierten globalen Erwärmung vom sicheren Aussterben dieser in ihrem Verbreitungsgebiet stenök an Hochgebirge gebundenen Art in der Wildbahn ausgegangen.[27]
Zum Verbreitungsgebiet der rezenten Quastenflosser: Der Lebensraum der verbliebenen Populationen des Komoren-Quastenflossers liegt im tieferen Gewässer um zwei der vier Komoren-Hauptinseln, während es sich beim Erstfund an der Chalumna-Mündung in Südafrika und bei den vereinzelten Funden an der Ostküste Afrikas offenbar um zufällige „Verdriftungen“ durch die Meeresströmung handelt.[28] Es wird vermutet, dass Indonesien als Verbreitungsgebiet des Manado-Quastenflossers auch das eigentliche Reliktareal der Vorgänger der rezenten Quastenflosser war, von wo sie erst durch Meeresströmungen zu den Komoren „verdriftet“ wurden.[24]
- Quastenflosser oder Hohlstachlerartige (Coelacanthiformes): Diese zunächst nur aus dem Fossilbericht bekannte Gruppe der Knochenfische mit rezent überlebenden Vertretern innerhalb der Gattung Latimeria gehört zu den aufsehenerregendsten Beispielen von Lazarus-Taxa.[30] Die Ordnung der Quastenflosser galt lange Zeit mangels Funde aus dem Känozoikum als vor 50 oder über 65 Millionen Jahren ausgestorben. Ihre „Wiederentdeckung“ in der Rezentfauna im Jahr 1938 in Form eines in einer Tiefe von 80 Metern nahe der Flussmündung des Chalumna an der Küste Südafrikas gefangenen Exemplars stellte deshalb eine wissenschaftliche Sensation höchsten Ranges als „lebendes Fossil“ dar,[29][28][24] obwohl ihre Existenz in der lebenden Tierwelt zwar neu für die Wissenschaft war, nicht aber für in der Region einheimische Fischer, die die Tiere bereits als Beifang kannten.[28] Eine wissenschaftliche Sensation bestand durch die Entdeckung bereits allein dadurch, dass den Quastenflossern zur Zeit dieser Entdeckung als vermeintliche Vorfahren der Amphibien eine phylogenetisch entscheidende Rolle beim Landgang der Wirbeltiere zugewiesen wurde.[28][24] Die anhand eines bereits fortgeschritten zersetzten Kadavers angefertigte Erstbeschreibung wurde teilweise wissenschaftlich angefochten, konnte aber 1952 durch einen in der Nähe der Komoren getätigten weiteren Fund erhärtet werden.[28] 1988 konnte der Komoren-Quastenflosser (L. chalumnae) durch Tauchboote in so guter Qualität im Lebensraum gefilmt werden, dass erstmals Details seiner Lebensweise der in einer Tiefe von 120 bis 200 Metern in den Abhängen der vulkanischen Inseln lebenden Art dokumentiert wurden.[31][32] 1998 wurde dann vor der Nordküste der von den Komoren weit entfernt gelegenen und zu Indonesien gehörenden Insel Manado Tua vor Sulawesi (ehemals: Celebes) ein weiterer Quastenflosser gefangen,[31][28][24] der auf Basis seiner von L. chalumnae abweichenden Färbung und genetischen Merkmale als eigenständige Art, Manado-Quastenflosser (L. menadoensis), beschrieben wurde.[31][28][24] – Der Komoren-Quastenflosser wird allerdings inzwischen als „vom Aussterben bedroht“ eingestuft (IUCN, 2000[33]), der Manado-Quastenflosser als „gefährdet“ (IUCN, 2008).[34] Die hauptsächliche Ursache für die massive Gefährdung des Komoren-Quastenflosser soll nicht in der lokalen Fischerei bestehen, sondern in der nach 1952 entbrannten weltweiten Sammelbegierde von Museen, Forschungseinrichtungen, Naturalienhändlern und Kuriösitätensammlern, die hohe Preise für dieses bekannteste „lebende Fossil“ bieten, obwohl der fortlaufende Fang der Tiere aufgrund der bereits an über 200 Exemplaren erfolgten, intensiven Erforschung kaum mehr mit wissenschaftlichem Bedarf zu rechtfertigen ist.[28]
- Mallorca-Geburtshelferkröte (Alytes muletensis): 1979 (nominell: 1977) wurde die Art nach auf Mallorca gefundenen Knochenresten aus dem Pleistozän beschrieben und dafür die neue Gattung Baleaphryne in der Familie Scheibenzüngler geschaffen.[13][35] 1980 wurde an sehr unzugänglicher Stelle im Nordosten Mallorcas ein rezent lebender Bestand entdeckt, der als der aus dem Pleistozän beschriebenen Art zugehörig identifiziert wurde. Aufgrund des beobachteten Brutpflegeverhaltens der lebenden Männchen wurde die Art dabei aber in die von festlandbewohnenden Vertretern bekannte Gattung Alytes (Geburtshelferkröten) gestellt.[13] – Dieser Fall ist ein Beispiel für eine Froschlurchart mit Verbreitungsgebiet in Europa, die zunächst paläontologisch beschrieben, dann aber auch rezent nachgewiesen wurde.[13] An diesem Fall der als „stark gefährdet“ eingestuften Art (IUCN, 2020[36]) zeigt sich zudem exemplarisch, wie eingehende wissenschaftliche Studien in eine erfolgreiche Erhaltungszucht mündeten.[13]
Konzepte in der Naturschutzbiologie
Das nicht seltene Phänomen vorzeitiger Einstufungen von Arten als ausgestorben hat zu verschiedenen Begriffsbildungen geführt. Neben dem Begriff Lazarus-Effekt (englisch Lazarus effect im Sinne von Keith & Burgman, 2004[4]) existiert auch der Terminus Romeo-Irrtum (englisch Romeo error im Sinne von Collar, 1998[37]).[38] Die Phänomene Lazarus-Effekt und Romeo-Irrtum sind zwar beides Fälle einer irrtümlichen Einordnung in die Gefährdungskategorie „ausgestorben“, behandeln jedoch verschiedene Seiten der Problematik des Datenmangels im Bereich der Biodiversität, denn sie befassen sich mit unterschiedlichen Aspekten dieser Problematik und beschreiben unterschiedliche Folgen, die daraus entstehen.[39]
Lazarus-Effekt als Entfernung eines Taxons aus der Liste der ausgestorbenen Taxa
Der Lazarus-Wechsel bezieht sich auf die Zusammensetzung von Listen ausgestorbener Arten aufgrund von Änderungen im Wissen über die als ausgestorben geltenden Arten oder Populationen (etwa auf Basis von Verbesserungen im Wissen über ihre Taxonomie oder Verbreitung)[39] und behandelt die Entfernung eines Taxons aus der Liste der ausgestorbenen Taxa.[40][41][39][42]
In einer Übersichtsarbeit im Jahr 2011 wurden nach Auswertung der wissenschaftlichen Literatur 103 Arten von Säugetieren, 144 Vogelarten und 104 Amphibienarten identifiziert, die nach einem angenommenen Aussterben in den vorangegangenen 122 Jahren wiederentdeckt worden waren. Im Durchschnitt lagen zwischen der Meldung des Aussterbens und dem Wiederfund etwa 60 Jahre. Die meisten wiederentdeckten Arten leben in abgelegenen Regionen der Tropen. Fast 90 Prozent der wiederentdeckten Arten waren so selten, dass sie anschließend als vom Aussterben bedroht eingeschätzt werden mussten.[43]
Abgrenzung zum Konzept des Romeo-Irrtums
Im Gegensatz zum Lazarus-Effekt bezieht sich das Phänomen des Romeo-Irrtums auf die Auswirkungen auf die Artenschutzbemühungen[39] und behandelt das verfrühte Aufgeben eines Taxons durch den Natur- oder Artenschutz,[40][41][39][42] ist also begrifflich zu trennen sowohl von dem in der Paläontologie als Lazarus-Effekt bekannten Phänomen (im Sinne von Wignall & Benton, 1999[3]),[40][41][39][42] als auch von dem in der Naturschutzbiologie als Lazarus-Effekt bekannten Phänomen (im Sinne von Keith & Burgman 2004[4]).[40]
Beispiele für Tiere
Beim Lazarus-Effekt im Sinne der Wiederentdeckung von Arten, die in der Roten Liste der IUCN bereits als „ausgestorben“ aufgeführt worden waren, handelt es sich um ein recht häufiges Phänomen[44] mit hunderten beschriebenen Fällen allein im Bereich der Amphibien, Vögel und Säugetiere.[1][43] Die Rote Liste der IUCN gilt als maßgeblichste Grundlage, wie die Arten nach ihrem Aussterberisiko zu klassifizieren sind und welche Arten als rezent „ausgestorben“ einzuordnen sind.[45]
Grundlegend kann zum Verbreitungsspektrum der betroffenen Arten angemerkt werden, dass es sich bei einem Großteil der vom Aussterben bedrohten, im Aussterben befindlichen oder (gegebenenfalls auch nur scheinbar) ausgestorbenen Tierarten um inselbewohnende Endemiten handelt. Weltweit gilt, dass der Hauptgrund für das Aussterben von Tierarten auf Inseln in der Einführung invasiver Neozoen liegt.[46] Allerdings ist beispielsweise von der Avifauna belegt, dass der Anteil der inselbewohnenden an den ausgestorbenen Arten rückläufig ist, während der Anteil der festlandbewohnenden Arten zunimmt, möglicherweise, weil die meisten potenziellen Neozoen auf ursprünglich beutegreiferlosen Inseln bereits eingeführt worden sind und sich nun verstärkt die auch auf dem Festland stark wirkende, anthropogene Lebensraumzerstörung auswirkt.[45] Von aussterbenden inselbewohnenden Reptilientaxa ist mehrfach das Phänomen beobachtet worden, dass sie länger auf einer kleinen Rand- oder Nebeninsel eines Archipels als auf dessen Hauptinsel zu überdauern scheinen.[13]
Die wiederentdeckten Taxa innerhalb der Reptilien und Amphibien leben häufig stärker verborgen und sind oft schwerer aufzuspüren als Vwertreter anderer landbewohnenden Tiergruppen.[30]
Vögel
Den besten Grad an Dokumentation auf der Roten Liste weist die Organismen-Klasse der Vögel auf, für deren Erhaltungszustand beziehungsweise Gefährdungsstatus bereits mehrfach vollständige Bewertungen auf weltweiter Ebene von BirdLife International und IUCN veröffentlicht wurden.[45] In der Ornithologie kam es auch zur intensivsten Beschäftigung mit Fragen, die Rückstufungen in der Gefährdungskategorie betreffen, sowie zum Versuch einer differenzierten Behandlung der Thematik, die durch eine Vielzahl spektakulärer Wiederentdeckungen verschollener und als ausgestorben eingestufter Vogeltaxa veranschaulicht werden kann.[47]
- Elfenbeinspecht (Campephilus principalis): seit den 1920er Jahren mehrfach verloren gegangen geglaubte (1994 und 1996 auf der Roten Liste der IUCN als ausgestorben gelistet[48]) und wiederentdeckte Art. - Die letzte offizielle Sichtung erfolgte 1944, doch wurden erneut Hinweise auf ein mögliches Fortbestehen der Art gemeldet.[49] Die als „vom Aussterben bedroht“ (IUCN, 2020) geführte[48] und möglicherweise ausgestorbene Art gilt als Beispiel der charismatischen Megafauna (Flaggschiffart)[50][51] und hat im Zuge der Frage über ihr Aussterben sowohl im akademischen wie auch im Amateurbereich viel Aufmerksamkeit von Ornithologen erhalten.[50] Ihre zwischenzeitliche Wiederentdeckung war von Umweltskeptikern genutzt worden,[52][53] um die unter Ökologen vorherrschende Ansicht in Frage zu stellen, dass der Erde eine globale anthropogene Massenaussterben-Krise bevorsteht.[53] Ron Rohrbaugh (Cornell Lab of Ornithology), der im April 2004 die Sichtung eines Elfenbeinspechts in Arkansas gemeldet hatte, warnte im Jahr 2010 davor, aus dem Fehlen neuerer erhärtender Belege für seine und andere zurückliegenden Sichtungen der Vogelart voreilig die Ausrottung des Elfenbeinspechts zu schlussfolgern und begründete dies mit den drohenden tiefgreifenden negativen Folgen eines möglichen Romeo-Irrtums.[54] Andererseits wurde der Fall des Elfenbeinspechts, der nach seiner angeblichen Wiederentdeckung im Jahr 2004 trotz fünf Jahre andauernder intensiver Suche nicht mehr entdeckt wurde und für dessen Erhaltung ein hoher finanzieller Aufwand betrieben wurde, in der Wissenschaft aber auch als eindrückliches jüngeres Beispiel dafür genannt, dass aus dem Unterlassen der Aufführung einer ausgestorbenen Art in die Gefährdungskategorie „ausgestorben“ Kosten für den Naturschutz resultieren, insbesondere in Form eines vergeudeten Investierens von Ressourcen für Erhaltungsmaßnahmen in eine bereits ausgestorbene Art. Selbst wenn von diesen Erhaltungsmaßnahmen andere Arten profitieren sollten, könnten die Ressourcen in einem solchen Fall jedoch wohl effizienter eingesetzt werden. Für den Fall, dass die Art nach einiger Zeit doch als ausgestorben bestätigt wird, könnte es – ähnlich wie beim Lazarus-Effekt – zum Reputations- und Glaubwürdigkeitsverlust des Naturschutzes kommen.[44]
- Großschnabelweber (Ploceus megarhynchus): Die Wiederentdeckung dieser Art geschah 1889 und stellt damit den ersten dokumentierten Fall einer Wiederentdeckung dar.[43] Die Art wird seit 2021 als „stark gefährdet“ eingestuft (IUCN, 2021).[55]
- Chapmans Zwergamazone (Hapalopsittaca fuertesi): Die Art war seit 1911 nur von der Typserie sicher bekannt. Nach möglichen Sichtungen zwischen 1980 und 2000 erfolgte die erste bestätigte Sichtung und somit Wiederentdeckung 2002. Die Art ist seit 1994 als „stark gefährdet“ eingestuft (IUCN, 2021).[56]
- Gelbscheitelpipra (Lepidothrix vilasboasi): Die Art wurde seit 1957 nur von fünf am Typenfundort gesammelten Exemplaren bekannt, bis 2002 ein Männchen beobachtet und per Japannetz an einem 200 Kilometer entfernten Standort gefangen werden konnte. Seit 2021 als Least Concern („nicht gefährdet“), zuvor ab 1994 als Vulnerable („gefährdet“) und davor (1988) als „Threatened“ eingestuft (IUCN, 2021).[57]
- Glanzsittich (Neophema splendida): Seit 2004 als Least Concern („nicht gefährdet“) eingestuft (IUCN, 2016).[58] 1931 wiederentdeckt.
- Edwardsfasan (Lophura edwardsi): Seit 2014 als „vom Aussterben bedroht“ eingestuft (IUCN, 2018).[59] Keine Sichtungen zwischen 1923 und 1996.
- Bermuda-Sturmvogel (Pterodroma cahow): Die Art wurde 1620 zuletzt beobachtet, bis sie 1906 wiederentdeckt wurde.[13][60] 1951 wurden 18 Brutpaare auf suboptimal geeigneten Felseninseln mit einer Gesamtfläche von 1 Hektar in Castle Harbour entdeckt, deren Population mithilfe intensiven Schutzmanagements stetig anwuchs. Die Art wird als „stark gefährdet“ eingestuft (IUCN, 2018).[60]
- Neuseeländische Sturmschwalbe (Oceanites maorianus): Da nach der Sammlung von drei Exemplaren im 19. Jahrhundert keine weiteren Nachweise verzeichnet wurden,[61] galt die Art als seit 1850 ausgestorben[18] und wurde auch von der IUCN seit 1988 bis einschließlich 2000 offiziell als ausgetorben eingeordnet.[61] Seit 2000 wurde sie jedoch wieder verzeichnet[18] und seitdem als „vom Aussterben bedroht“ eingeordnet (IUCN, 2018).[61] – Der Fall gilt als besonders bemerkenswerter Forschungsgegenstand, da die Art möglicherweise dadurch überleben konnte, dass sie andere Nistgewohnheiten angenommen hat, als noch für das 19. Jahrhundert für die Art bekannt waren.[18]
Die über 150 Jahre lang nicht mehr nachgewiesene Neuseeländische Sturmschwalbe ist, wie der über 100 Jahre verschwundene Magentasturmvogel (Pterodroma magentae), der ebenfalls über 100 Jahre verwschwundene Macgillivray-Sturmvogel (Pseudobulweria macgillivrayi), der seit 1929 verschollene und möglicherweise 2006 wiederentdeckte Salomonensturmvogel (Pseudobulweria becki) und – besonders spektakulär – der fast 300 Jahre lang verschollene Bermuda-Sturmvogel, zudem ein Beispiel dafür, dass eine Anzahl auf Inseln brütender Meeresvögel vor ihrer Wiederentdeckung auffällig lange nicht mehr nachgewiesen worden waren. Da die Brutplätze auf Inseln von vielen Meeresvogelarten nachts aufgesucht werden und die dafür genutzten Nischen und Höhlen – auch bei sich tagsüber dort aufhaltenden Arten – leicht übersehen werden, bleiben ihre Brutplätze häufig unentdeckt, was auch für manche häufige Arten mit Populationsstärken von bis zu Zehntausenden Tieren gilt.[13]
- Langbein-Buschsänger (Megalurulus rufus): Singvogel-Art war historisch von vier, in den 1890er Jahren gesammelten Exemplaren bekannt und wurde lange Zeit für ausgestorben gehalten. Nach einer unbestätigten Meldung der Art im Jahr 1973 gelang die erste bestätigte Wiederentdeckung im Jahr 2003 im Wabu Forest Reserve (Fidschi), wo zwölf Pärchen entdeckt wurden. Die Art wird als „stark gefährdet“ eingestuft (IUCN, 2020).[62]
- Südinseltakahe (Porphyrio hochstetteri): Die Art wird als „stark gefährdet“ eingestuft (IUCN, 2020). Bei der „Wiederentdeckung“ der Art 1948 war ihr Vorkommen auf die Murchison Mountains (Fiordland-Nationalpark) begrenzt. In den 1980er Jahren wurde ein Aufzuchtprogramm begonnen und einige Exemplare konnten auf raubtierfreien „Festlandinseln“ freigelassen werden.[63] Die Art galt vor ihrer „Wiederentdeckung“ im Jahr 1948 als seit 1898 ausgestorben.
- Madagaskar-Schlangenhabicht (Eutriorchis astur): Zwischen 1930 und 1993 konnte die Art nicht sicher nachgewiesen werden. Sie wird als „stark gefährdet“ eingestuft (IUCN, 2016).[64]
- Banggai-Krähe (Corvus unicolor): Die Art war lange nur von zwei Museumsexemplaren unklarer Herkunft von den Banggai-Inseln bekannt. Ihr Überleben konnte aber nach einer unbestätigten Sichtung auf Peleng (1991) durch Suche auf dieser Insel in den Jahren 2004, 2006 und 2007 auf bestätigt und die Art somit wiederentdeckt werden. Seit 2005 wird die Art als „vom Aussterben bedroht“ eingeordnet (IUCN, 2017).[65]
- Flores-Zwergohreule (Otus alfredi): Die auf Flores endemische Art wurde nach ihrer ersten Sammlung im Jahr 1896 nicht mehr gesehen, bis im Jahr 1994 Exemplare gefangen wurden. Seit 2000 wird die Art als „stark gefährdet“ eingestuft (IUCN, 2016).[66]
- Vierfarben-Mistelfresser (Dicaeum quadricolor): Die Art gehört zu mehreren vorzeitig für ausgestorben erklärten Taxa auf der Insel Cebu[44][67][37][68] und wurde seit 1906 für ausgestorben erachtet,[69][70] dann aber 1992 – also nachdem sie seit 86 Jahre nicht nachgewiesen worden war[68][44] und seit mindestens 40 Jahren als ausgestorben galt[44][71] – in einem sehr kleinen Restwaldfragment wiederentdeckt.[69][70][67][37] – Es handelt sich beim Vierfarben-Mistelfresser zudem um den ersten Fall, für den das Phänomen des „Romeo-Irrtums“ beschrieben und verwendet wurde,[44][67][37][68] da die heute vom IUCN als „vom Aussterben bedroht“ (IUCN, 2021) eingestufte Art[72][67] nach Einschätzung der Wissenschaftler einen weitaus besseren Erhaltungszustand zeigen könnte, wenn die Schutzanstrengungen zwischenzeitlich nicht infolge der irrtümlichen Einordnung als „ausgestorben“ aufgegeben worden wären.[67][37][44]
- Cebuschama (Copsychus cebuensis): Rabor führte die Art 1959 als die einzige von zehn endemischen Vogel-Taxa auf der Insel Cebu auf, die noch vorgefunden wurde.[73] Nach Rabors Veröffentlichung wurde die endemische Avifauna der Insel 1960 von der Ornithologie weitestgehend regelrecht aufgegeben.[74] In den 1970er Jahren wurde der Cebuschama aufgrund der Annahme, dass seine letzte Sichtung 1956 geschehen sei, offiziell als ausgestorben aufgeführt.[75] 1995 führte die Rote Liste die Art dagegen wieder als existent und „gefährdet“ auf.[76]
- Príncipe-Drossel (Turdus xanthorhynchus): Die auf Príncipe (São Tomé und Príncipe) endemische Art wurde seit den 1920er Jahren nicht mehr verzeichnet, bis sie 1997 wiederentdeckt wurde. Seit 2011 wird die Art als „vom Aussterben bedroht“ eingeordnet (IUCN, 2021).[77]
- Bräunling (Motacilla bocagii): Die auf São Tomé endemische Art war nur aus sechs vor 1928 erfolgten Nachweisen bekannt, bis sie 1990 in den wiederentdeckt wurde. Die Art wird als „gefährdet“ eingestuft (IUCN, 2018).[78]
Neben dem Bräunling galten auch verschiedene andere endemische Vogelarten Sao Tomes, darunter der Einfarbgimpel, der Zwergolivenibis und der Newton-Würger, jahrzehntelang als verschollen.
- Antioquia-Buschammer (Atlapetes blancae): Die Art war nur von drei 1971 gesammelten Museumsexemplaren bekannt, bis sie 2018 in den kolumbianischen Anden wiederentdeckt wurde. Seit 2009 wird sie als „vom Aussterben bedroht“ eingeordnet (IUCN, 2021).[79]
- Godavarirennvogel (Rhinoptilus bitorquatus): Die lokal endemische Art war historisch nur aus wenigen Aufzeichnungen bekannt und galt als ausgestorben, bis sie 1986 wiederentdeckt wurde. Seit 2000 wird sie als „vom Aussterben bedroht“ eingeordnet (IUCN, 2017). Es existiert nur eine kleine, abnehmende Population, von der es aber seit 2009 keine bestätigten Sichtungen mehr gibt.[80]
- Schwarzbrauen-Mausdrossling (Malacocincla perspicillata): Für eine Einstufung in eine Gefährdungskategorie gab die IUCN 2016 und 2020 „ungenügende Datengrundlage“ an, denn die Art war bis dahin nur vom Typusexemplar unklaren Ursprungs bekannt.[81][82] 2020 wurde die Art nach 170 Jahren auf Borneo wiederentdeckt, gefangen und fotografiert.[81]
Säugetiere
Ähnlich wie bei den Vögeln liegt auch für die Säugetiere eine ganze Anzahl von Beispielen für bereits tot gehaltene und dann doch wiederentdeckte Taxa vor, sowohl im Rang von Arten, als auch im Rang von Unterarten oder auf Ebene von Populationen.[13]
- Java-Nashorn (Rhinoceros sondaicus): die ursprünglich vom früheren Ostbengalen (heute Bangladesch) im Westen bis nach Südwestchina, Indochina, Sumatra und Java im Osten verbreitete Art ist auch in ihrem heutigen Hauptverbreitungsareal (die dicht menschlich besiedelte Insel Java, bekanntester Zufluchtsort des Nashorns ist das Ujung-Kulon-Reservat) sehr selten (heute rund 50 Individuen) und galt in ihrem einstigen Festlandsareal, wo sie als taxonomisch umstrittene Unterart R. s. inermis geführt worden war, rund 40 Jahre lang als vollständig ausgerottet, bis sie Ende des 20. Jahrhunderts mit großer sensationeller Wirkung im Süden Vietnams in Form eines sehr kleinen Bestands wiederentdeckt wurde (heute rund 10 bis 15 Individuen).[84][13][85] – Dieser Fall gilt als Beispiel dafür, dass auch äußerst aufsehenerregende Großsäuger vom Lazarus-Effekt betroffen sein können.[13]
- Sumatra-Nashorn (Dicerorhinus sumatrensis): Die Art war bis ins frühe 20. Jahrhunderts im größten Teil Südostasiens weitverbreitet, bis zu den 1970er Jahren jedoch durch Bejagung auf der Malaiischen Halbinsel, auf Sumatra und auf Borneo mit Ausnahme kleiner Gebiete ausgerottet worden.[90] Weltweit überlebten nach Schätzungen, die auf Daten aus den Jahren 2005 bis 2009 beruhen, noch rund 200 bis 300 Individuen der gesamten Art,[90] nach neueren Schätzungen aus den Jahren 2013 und 2016 noch rund 100.[90][88][89] Es handelt sich bei diesen Tieren zugleich um die letzten lebenden Vertreter der 25 Millionen Jahren zurückreichenden eurasischen zweihörnigen Nashörner, zu denen im Quartär auch das Wollnashorn (Coelodonta antiquitatis) gehörte, und die die wohl ursprünglichste und bei weitem älteste noch existierenden Gruppe aus der im Eozän entstandenen Familie der Nashörner darstellen.[91][84][87] Die im indonesischen Teil Borneos beheimatete Teilpopulation der Art galt bereits seit 1986 als ausgestorben, als 2013 Belege für das Überleben von Tieren dieser Population bekannt wurden und weltweit auf große mediale Resonanz stießen.[92][93] 2013 erfolgte dann laut dem WWF die erste bestätigte Sichtung eines Exemplars in diesem Gebiet seit der vorangegangenen 40 Jahre.[89] – Am Beispiel dieses Falls wurde diskutiert, dass das Vorgehen des Artenschutzmanagements im Falle einer Wiederentdeckung sorgfältig erwogen werden muss.[30] Es wurde argumentiert, dass die Population im indonesischen Teil Borneos möglicherweise gerade aufgrund des Mangels an Aufmerksamkeit überleben konnte, der aus der jahrzehntelangen Einschätzung als ausgestorben resultierte.[90] Es wurde vermutet, dass durch die Bekanntmachung der Wiederentdeckung in einem solchen Fall die Aufmerksamkeit der Wilderei für die betroffene Population und damit der Bejagungsdruck erhöht wird, so dass das tatsächliche Aussterben der Population ausgelöst werden könne,[90] wenn nicht sofortige Erhaltungsmaßnahmen dagegen ergriffen würden.[90][30]
- Zwergwildschwein (Porcula salvania, Syn.: Sus salvania): Diese Art galt seit den 1950er Jahren als durch Lebensraumzerstörung ausgestorben.[94][95][96] 1971 kam es zur Wiederentdeckung, als ein Bekannter Gerald Durrells für dessen Jersey Zoo in Indien vier auf einem Markt zum Verkauf angebotene Zwergwildschweine aus dem Manas-Nationalpark in Assam ausfindig machte.[96][95] Später erfolgten weitere Entdeckungen von Beständen im Barnardi Wildlife Sanctuary. Der Gesamtrestbestand der Art betrug zu jener Zeit rund 150 Individuen.[94] Anfängliche Züchtungsversuche blieben erfolglos.[96] Durrells Engagement führte zu Maßnahmen, die Individuen der Wildbestände aufzufinden, einzufangen und in menschlicher Obhut zu züchten, um die Bestände der Art durch das Zucht- und Auswilderungsprogramm zu sichern.[95] 1995 wurde das Pygmy Hog Research and Breeding Centre bei Guwahati gegründet, das zu erfolgreicher Nachzucht führte, die jedoch auf die sehr begrenzte Anzahl von 2 männlichen und 4 weiblichen Gründertieren aus dem Manas National Park zurückgeht.[94][96] 2005 kam der Balipara Reserve Forest in Potasali nahe dem Nameri National Park als zusätzliche Zuchstation zur dezentralisierteren Anlage des Arterhaltungsbestandes dazu und es kam in der Folge zu erfolgreichen Auswilderungen von Nachzuchten in verschiedene Reservate.[94] Beim als „stark gefährdet“ (IUCN, 2019) eingestuften[97] Zwergwildschwein handelte oder handelt es sich um die weltweit seltenste Schweineart,[98] dem von seinem ursprünglichen Verbreitungsgebiet südlich des Himalajas von Uttar Pradesh im Westen bis Assam und Sikkim im Osten nur noch Reste in Schutzgebieten in Assam geblieben sind.[94] – Dieser Fall kann als Beispiel dafür genannt werden, dass die Wissenschaft informelle Datenquellen zum Vorkommen ausgestorben geglaubter Arten sorgfältig prüfen und berücksichtigen muss, um gegebenenfalls möglichst schnell Erhaltungsmaßnahmen einleiten zu können, da der Artenschutz sonst im Falle von unerwarteten Wiederentdeckungen unvorbereitet sein kann.[95]
- Juan-Fernández-Seebär (Arctocephalus philippii): 1824 für ausgestorben erklärt, 1965 wiederentdeckt.
- Galápagos-Seebär (Arctocephalus galapagoensis): im 19. Jahrhundert für ausgestorben erklärt, 1932 wiederentdeckt.
- Guadalupe-Seebär (Arctocephalus townsendi): 1894 für ausgestorben erklärt, 1949 wiederentdeckt.
- Antarktischer Seebär (Arctocephalus gazella): in den 1830er Jahren für ausgestorben erklärt, in den 1930er Jahren wiederentdeckt.
- Hörnchenbeutler (Gymnobelideus leadbeateri): Die 1867 beschriebene Art galt seit Beginn des 20. Jahrhunderts als ausgestorben, wurde 1961 wiederentdeckt und später in Australien aufgrund des im 20. Jahrhundert erfolgten und für die Zukunft erwarteten Lebensraumverlustes als gefährdet eingestuft. – Da es als wahrscheinlich gilt, dass die inzwischen zum Erhalt der Art erfolgten Änderungen in der Waldbewirtschaftung früher erfolgt wären, wenn die Art nicht verfrüht als ausgestorben eingestuft worden wäre, handelt es sich bei diesem Fall um ein Beispiel für den Romeo-Irrtum.[44] Gegenwärtig wird die Art als „vom Aussterben bedroht“ geführt (IUCN, 2016).[99]
- Bayerische Kurzohrmaus (Microtus bavaricus): Mitte der 1960er Jahre für ausgestorben erklärt, 2000 wiederentdeckt.
- Parmawallaby (Macropus parma): 1966 auf der Insel Kawau und sechs Jahre später auf dem australischen Festland wiederentdeckt.
- Dinagat-Borkenratte (Crateromys australis): keine Nachweise zwischen 1975 und 2012
- Presbytis hosei canicrus (auf Englisch zuweilen als „Dracula Monkey“ bezeichnet), Unterart des Hose-Langurs, galt seit 2005 als verschollen, wurde jedoch Anfang 2012 auf Borneo wiederentdeckt. Im April 2019 gelangen dem Tierfilmer Forrest Galante im Rahmen der Animal-Planet-Dokumentarserie Extinct or Alive die ersten Filmaufnahmen.
- Rotschopf-Baumratte (Santamartamys rufodorsalis) aus der Familie der Stachelratten, nur von zwei 1898 in Kolumbien erlegten Exemplaren bekannt; 2011 im Norden des Landes anhand eines Exemplars wieder nachgewiesen
- Neuguinea-Langohr (Pharotis imogene), Fledermausart aus Neuguinea, keine Sichtungen zwischen 1890 und 2012.
- Machu-Picchu-Inkaratte (Cuscomys oblativus), 1916 auf der Basis von zwei in Inka-Grabstätten entdeckten Schädeln aus dem 15. Jahrhundert beschrieben, 2009 wiederentdeckt.
- Schwarzschwanz-Luzon-Baumratte (Carpomys megalurus), 1895 auf der Basis von sechs Exemplaren beschrieben, 2008 wiederentdeckt.
- Der Vietnam-Kantschil (Tragulus versicolor) wurde zweimal wiederentdeckt: 1990 nach 84 Jahren und 2019 nach 30 Jahren.
- Das Wondiwoi-Baumkänguru (Dendrolagus mayri) wurde 2018 nach 90 Jahren wiederentdeckt.
- Die Zypern-Stachelmaus (Acomys nesiotes) galt ab 1980 als verschollen. 2007 wurden vier Exemplare bei Levkosia wiederentdeckt.
- Flachkopf-Mausohr (Myotis planiceps). Fledermausart aus Mexiko, keine Sichtungen zwischen 1996 und 2004.
Reptilien
- Barkudia-Skink (Barkudia insularisis): 1917 für ausgestorben erklärt, 2003 wiederentdeckt.
- La-Palma-Rieseneidechse (Gallotia auaritae): Die La-Palma-Rieseneidechse, ein Endemit auf La Palma,[90] war bereits seit Jahrhunderten nicht mehr auf der Inselgruppe gesichtet worden und wurde daher für seit dieser Zeit ausgestorben erachtet, als sie schließlich doch 2007 fotografiert werden konnte.[30][90] – Die Art ist ein Beispiel für das im Vergleich zu anderen landbewohnenden Taxa oftmals eher verbogene und schwer nachzuweisende Vorkommen von Lazarus-Arten unter den Reptilien und Amphibien.[30] Da ihre Bestände sehr geringe Individuenzahlen aufweisen, wurde sie jedoch nach ihrer Wiederentdeckung als „vom Aussterben bedroht (möglicherweise ausgestorben)“ eingestuft (IUCN, 2009).[100]
- El-Hierro-Rieseneidechse (Gallotia simonyi): Nachdem die Art zuerst auf der Insel El Hierro und um 1950 auch in ihrem kleinen Refugialraum, auf dem El Hierro im Westen vorgelagerten Salmor-Felsen (Roque Chico de Salmor), nicht mehr nachgewiesen wurde, wurde sie 1971 und 1976 für ausgestorben erklärt, wurde dann aber zeitnah in privatem Betreiben durch den Fund eines Kadavers aus Skelettresten und Hautfetzen wiederentdeckt und dann durch einen Lebendfang eines Pärchens auf El Hierro bestätigt. Der Lebendfang wurde zwar konfisziert, war aber fotografisch belegt, und die Art fand Aufnahme in die Naturschutzgesetzgebung Spaniens. Außer auf El Hierro existieren von dieser Art auch auf La Gomera, Teneriffa und La Palma subfossile und teilweise auch historische Knochenbelege. Für subfossile Skelettreste von La Gomera wurde 1985 die Unterart G. simonyi gomerana aufgestellt.[13] Die Art wird seit 1996 als „vom Aussterben bedroht“ eingestuft (IUCN, 2009).[101]
- Antigua-Schlanknatter: in den 1960er Jahren wiederentdeckt.
- Utila-Leguan: Schwarzleguanart, keine Sichtung seit 1901, im Jahr 1994 wiederentdeckt.
- Yunnan-Scharnierschildkröte (Cuora yunnanensis): diese Art galt seit mehr als 100 Jahren als ausgestorben, als sie 2004 lebend auf einem Markt in Kunming für die Wissenschaft unter großer medialer Resonanz wiederentdeckt.[13] Seit dem Jahr 1946 konnten trotz anderthalb Jahrzehnte langer Nachsuche lediglich 3 Individuen (sämtlich seit 2004 gefunden) der Art bestätigt werden (Stand: 1007). Es wird daher davon ausgegangen, dass nur extrem wenig Individuen überlebt haben können und alle verbliebenen Populationen äußerst klein und örtlich begrenzt sind.[102] Aufgrund der sehr hohen Preisgebote von Sammlern im illegalen Heimtierhandel sowie im Konsumhandel sind möglicherweise überlebende Tiere in besonderem Maße vom Sammlern bedroht.[102][13] Die Art ist daher als „vom Aussterben bedroht“ (IUCN, 2010) eingestuft.[102] Die Validität der drei entdeckten Tiere 2007 wurde durch DNA-Analyse bestätigt.
- Jamaika-Leguan (Cyclura collei): die über einen Meter lange Wirtelschwanzleguanart ist endemisch auf der Insel Jamaika[13] und kam einst an der südöstlichen Küste Jamaikas verbreitet in ihrem Habitat vor.[103] Ihre Bestände gingen seit Ende des 19. Jahrhunderts deutlich zurück.[103] Sie wurden durch verschiedene Neozoen dezimiert, bei denen es sich um anthropogen eingeführte Fressfeinde aus der Säugetierordnung der Raubtiere wie Mangusten, Hauskatzen und Haushund handelt, aber auch um eigelegeplündernde Ratten.[13][104] Seit Mitte der 1940er Jahre galten auch die letzten bekannten Jamaika-Leguan-Bestände (auf der Großen Ziegeninsel befindlich, einer kleinen Nebeninsel Jamaikas) als ausgestorben.[13][103] In den 1970er Jahren konnte jedoch ein lebendes Exemplar in den Hellshire Hills auf der Hauptinsel, an der Südküste Jamaikas, bestätigt werden[13][103] und 1990 eine Restpopulation von weniger als 50, hauptsächlich älteren adulten Individuen, entdeckt werden,[103] nachdem der Hund eines örtlichen Jägers ein lebendes Exemplar der Art in einer Gegend bei Kingston erbeutet hatte, wo seit 1940 keine Leguane mehr gesichtet worden waren.[104] 1994 konnten die ersten Exemplare der Art in US-amerikanische Zoos überführt und bis 1997 von Experten über 100 Tiere nachgezüchtet werden, die teilweise in einem speziellen Schutzgebiet ausgesetzt wurden.[104] Die Art bleibt dennoch seit 1996 als „vom Aussterben bedroht“ (IUCN, 2021) eingestuft.[103] – Dieser Fall eines von Noezoen bis an den Rand des Aussterbens dezimierten Inselendemiten gilt als ein Paradebeispiel für ein erfolgreich durchgeführtes Erhaltungszuchtprogramm.[13] 2021 gab die IUCN den Bestand wieder mit dank intensiver Schutzbemühungen auf 500 bis 600 geschätzte adulte Individuen angewachsen an.[103]
- Contomastix vittata (Departamento Chuquisaca, Cochabamba, Santa Cruz, Potosí (Bolivien); wurde vor über einem Jahrhundert zuletzt gesichtet, bis es in den frühen 2010er-Jahren wenige Exemplare in Gegenden wiederentdeckt wurde, die auf eine abnehmende Population schließen lassen) [105]
- Fernandina-Riesenschildkröte (Chelonoidis phantasticus). Nach dem Fund des einzelnen männlichen Exemplars im Jahr 1905, das als Holotyp für die Erstbeschreibung im Jahr 1907 diente, erfolgte zunächst kein Fund mehr auf der schwer zugänglichen Galapagosinsel Fernandina und die Art wurde als „vom Aussterben bedroht (möglicherweise ausgestorben)“ eingestuft (IUCN, 2017).[106] Offenbar litten ihre Bestände unter den häufigen vulkanischen Lavaströmen auf der Insel,[106] bei der es sich um einen aktiven Schildvulkan handelt.[107] Nach Anzeichen für die Existenz von Schildkröten auf der Insel im Jahr 1965 (wie Kot- und Fraßspuren) sowie nach späteren Indizien konnte das Überleben der Art, deren Vertreter wie für Galapagos-Riesenschildkröten üblich eine individuelle Lebenserwartung von mindestens 100 Jahren besitzen, nicht ausgeschlossen werden.[106] Im Februar 2019 soll dann ein einzelnes Weibchen der Art auf Fernandina aufgefunden und die Art somit wiederentdeckt worden sein.[107]
- Die Pinocchioechse (Anolis proboscis) galt zwischen 1953 und 2004 als verschollen.
Amphibien
Froschlurche




- Adenomus kandianus (Zentralprovinz (Sri Lanka)); im Jahr 1872 konnten zwei Exemplare gefunden werden, danach keine mehr, bis im Juni 2012 bekannt wurde, dass drei Jahre vorher, im Oktober 2009, die Art in der Zentralprovinz von Sri Lanka nach über 130 Jahren wiederentdeckt wurde[108][109]
- Amolops chakrataensis (Uttarakhand (Indien); nur ein Exemplar war bekannt, das im Jahr 1985 gesammelt wurde; 25 Jahre später konnte die Art wiederentdeckt werden) [110][111][112]
- Atelopus balios (Provinz Azuay, Cañar, Guayas (Ecuador); wurde zwischen April 1995 und Oktober 2010 nicht mehr gesichtet; im Oktober 2010 fand man ein Exemplar, im März 2011 fünf Männchen und im Juni 2012 ein weiteres Männchen) [113]
- Atelopus arsyecue (Sierra Nevada de Santa Marta, Kolumbien), 2019 konnten 30 Exemplare gefunden werden, nachdem diese Art 28 Jahre für ausgestorben gehalten wurde.
- Atelopus coynei (Provinz Pichincha, Imbabura, Carchi (Ecuador); wurde im September 1984 zuletzt gesichtet und galt als ausgestorben, bis die Art am 7. Februar 2012 fotografiert werden konnte) [114][115]
- Atelopus ignescens (Provinz Imbabura, Chimborazo, Bolívar (Ecuador); wurde seit 1988 nicht mehr gesehen und für ausgestorben erklärt; 2016 konnten doch wieder 27 Exemplare entdeckt werden) [116][117]
- Cardioglossa cyaneospila (Burundi, Demokratische Republik Kongo, Ruanda; die Art wurde zuletzt im Jahr 1949 in Burundi gesammelt und danach bis 2009 nicht mehr gefunden, als ein Foto auftauchte; im Jahr 2012 konnte dann ein einzelnes Exemplar im Bururi Forest Nature Reserve (Bururi (Burundi)) gesammelt werden) [118][119]
- Craugastor escoces (auf den Vulkanen Barva, Irazú und Turrialba (Provinz Alajuela, Costa Rica); wurde zuletzt um das Jahr 1986 gesichtet und im Jahr 2004 für ausgestorben erklärt; umfangreiche Suchaktionen blieben erfolglos, bis ein Weibchen am 19. September 2016 wiederentdeckt wurde) [120][121]
- Eleutherodactylus amadeus (Massif de la Hotte (Haiti); zuletzt im Jahr 1991 gesichtet, bis Anfang 2011 bekannt gegeben wurde, dass die Art wiederentdeckt wurde; jetzt im sehr begrenzten Verbreitungsgebiet sehr häufig) [122][123]
- Eleutherodactylus corona (Massif de la Hotte (Haiti); weniger als 10 Exemplare waren bekannt; die letzte Sichtung war im Jahr 1991, bis Anfang 2011 bekannt gegeben wurde, dass die Art wiederentdeckt wurde) [124][123]
- Eleutherodactylus dolomedes (Massif de la Hotte (Haiti); nur wenige Exemplare waren bekannt; die letzte Sichtung war vor 1992, bis Anfang 2011 bekannt gegeben wurde, dass die Art wiederentdeckt wurde) [125][123]
- Eleutherodactylus glandulifer (Massif de la Hotte (Haiti); im Jahr 1991 war die Art nur mäßig verbreitet, danach nicht mehr gesichtet, bis Anfang 2011 bekannt gegeben wurde, dass die Art wiederentdeckt wurde) [126][123]
- Eleutherodactylus parapelates (Massif de la Hotte (Haiti); wurde im Jahr 1984 oder 1996[123] zuletzt gesichtet, bis Anfang 2011 bekannt gegeben wurde, dass die Art wiederentdeckt wurde) [127][123]
- Eleutherodactylus thorectes (Massif de la Hotte (Haiti); einer der kleinsten Frösche der Welt; wurde im Jahr 1991 zuletzt gesichtet, bis Anfang 2011 bekannt gegeben wurde, dass die Art wiederentdeckt wurde) [128][123]
- Frankixalus jerdonii, Syn.: Polypedates jerdonii, Philautus jerdonii (Darjeeling (Westbengalen, Indien); wurde nur einmal im 1872 gesammelt, auch die IUCN-Liste gibt keine weiteren Informationen darüber; allerdings wurde die Art 137 Jahre später, also 2009, wiederentdeckt)[129][130][111]
- Nimba-Berg-Riedfrosch (Hyperolius nimbae) (Mount Nimba (Elfenbeinküste); diese Art aus der Familie der Riedfrösche (Hyperoliidae) galt von 1967 bis zu seiner Wiederentdeckung im Jahr 2010 als ausgestorben) [131][132]
- Omaniundu-Riedfrosch (Hyperolius sankuruensis) (im Süden der Demokratischen Republik Kongo; diese Art aus der Familie der Riedfrösche (Hyperoliidae) galt von 1979 bis zu seiner Wiederentdeckung im Jahr 2010 als ausgestorben) [133][132]
- Incilius holdridgei (Provinz Alajuela (Costa Rica); konnte zwischen 1987 und 2009 nicht gesichtet werden, galt seit 2004 als ausgestorben; es wird von weniger als 50 lebenden Exemplaren ausgegangen) [134][135]
- Indosylvirana aurantiaca, Syn.: Rana bhagmandlensis, Rana aurantiaca, Hylarana aurantiaca (südliche Westghats (Indien), Sri Lanka; laut [111] wurden nur zwei Exemplare von Hylarana bhagmandlensis = Rana bhagmandlensis im Jahr 1921 gesammelt; laut IUCN an gewissen Orten in den südwestlichen Ghats und in Sri Lanka reichlich vorhanden) [136]
- Indosylvirana temporalis, Syn.: Rana flavescens, Rana temporalis, Rana intermedius, Hylarana temporalis, Hylorana temporalis (Westghats (Indien), Sri Lanka; laut [111] wurde nur ein Exemplar von Hylarana intermedius = Rana intermedius im Jahr 1937 in Karnataka gesammelt; laut IUCN an gewissen Orten reichlich vorhanden) [137]
- Israelischer Scheibenzüngler (Latonia nigriventer, Syn.: Discoglossus nigriventer; alternative Trivialnamen auch: Palästinensischer Scheibenzüngler, Hulesee-Scheibenzüngler, Schwarzbäuchiger Scheibenzüngler): Diese für die in Israel gelegene Chulaebene endemische Art aus der Familie der Alytidae galt seit den 1950er Jahren als durch Lebensraumzerstörung ausgestorben, bis sie Anfang 2011 in der Chulaebene wiederentdeckt wurde.[30][90][138] Allerdings wird die Art als „vom Aussterben bedroht“ eingestuft (IUCN, 2021).[139] – Die Art ist ein Beispiel für das im Vergleich zu anderen landbewohnenden Taxa oftmals eher verbogene und schwer nachzuweisende Vorkommen von Lazarus-Arten unter den Reptilien und Amphibien.[30]
- Megophrys parva, Syn.: Xenophrys monticola (Sikkim (Indien); von Xenophrys monticola wurden im Jahr 1860 die einzigen zwei Exemplare gesammelt und auch zuletzt gesichtet, die Art wird aber mittlerweile der Art Megophrys parva zugeordnet (welche in ganz Südostasien vorkommt), allerdings ist diese Zuordnung noch fraglich) [140][111]
- Micrixalus elegans (Westghats (Indien); der Holotyp wurde 1937 gefunden, ist aber verloren gegangen; danach bis 2010 nicht wieder gesichtet, dürfte mittlerweile wieder recht häufig sein) [141][111][112]
- Micrixalus narainensis, Syn.: Philautus narainensis (Karnataka (Indien); der Holotyp wurde 1937 gefunden, ist mittlerweile aber wieder verloren gegangen; danach nie wieder gesichtet; im Jahr 2014 stellte man fest, dass diese Art und die ebenfalls vom Aussterben bedrohte Art Micrixalus kottigeharensis ident sind) [142][111]
- Micrixalus swamianus, Syn.: Philautus narainensis (Westghats (Indien); auch hier wurde nur ein einziges Exemplar im Jahr 1937 gefunden, der Holotyp, der aber mittlerweile ebenfalls wieder verloren gegangen ist; danach nie wieder gesichtet; im Jahr 2014 stellte man fest, dass diese Art und die ebenfalls vom Aussterben bedrohte Art Micrixalus kottigeharensis ident sind) [143][111]
- Micrixalus thampii (Silent-Valley-Nationalpark (Westghats, indien); nur zwei Exemplare waren bekannt, zuletzt wurde die Art im Jahr 1981 gesichtet, 30 Jahre später wiederentdeckt worden) [144][111][112]
- Nymphargus anomalus (Provinz Napo (Ecuador); laut [111] zwischen ihrer Entdeckung im Jahr 1971 und ihrer Wiederentdeckung im Jahr 2009 im Nationalpark Llanganates unauffindbar) [145][146]
- Pseudophilautus hypomelas, Syn.: Philautus hypomelas (Sri Lanka; wurde 1876 erstbeschrieben, danach keine Sichtung mehr bis zum Jahr 2010, als sie im zentralen Hochland von Sri Lanka nach über 130 Jahren wiederentdeckt wurde) [147][148]
- Pseudophilautus stellatus, Syn.: Philautus stellatus (Nuwara Eliya (Sri Lanka); der mittlerweile verlorene Holotyp wurde 1853 gesammelt, danach nie wieder gesichtet bis zum Jahr 2013, als diese Art nach 160 Jahren wiederentdeckt wurde) [149][150]
- Pleurodema marmoratum, Syn.: Phrynopus spectabilis (Argentinien, Bolivien, Chile, Peru; die in als ausgestorben angegebene Froschart Phrynopus spectabilis wurde mittlerweile der häufigen Art Pleurodema marmoratum zugeordnet) [151]
- Uperodon anamalaiensis, Syn.: Ramanella anamalaiensis (Tamil Nadu (Indien); nur der mittlerweile verloren gegangene Holotyp war bekannt, der 1937 gesammelt wurde; im Jahr 2010 wurde die Art aber wiedergefunden im Parambikulam Tiger Reserve (Kerala)) [152][153][112]
Schwanzlurche

- Ambystoma leorae (México (Bundesstaat) (Mexiko); dieser Breitkopfsalamander wurde im Jahr 1983 zuletzt beobachtet; seit 2017 gibt es aber wieder vermehrt Sichtungen) [154][155]
- Bolitoglossa jacksoni (Departamento Huehuetenango, Guatemala; dieser Salamander aus der Familie der Lungenlosen Salamander (Plethodontidae) wurde zwischen 1975 und 2017 nicht mehr gesichtet, galt schon als ausgestorben, bis er nach 42 Jahren in der Sierra de los Cuchumatanes wiederentdeckt wurde) [156][157]
- Chiropterotriton mosaueri (Hidalgo (Mexiko); diese Art aus der Familie der Lungenlosen Salamander (Plethodontidae), Unterfamilie Hemidactyliinae, Gattung Schwielensalamander (Chiropterotriton) galt von 1947 bis zu seiner Wiederentdeckung 73 Jahre später im Jahr 2010 als ausgestorben) [158][132]
Rundmäuler
- Eine nur in Oregon heimische Neunaugen-Art (Entosphenus minimus, Syn.: Lampetra minima), (Miller Lake, Oregon, USA), wurde seit 1958 für ausgestorben gehalten, jedoch in den späten 1990er Jahren wiederentdeckt.[159][160]
Fische
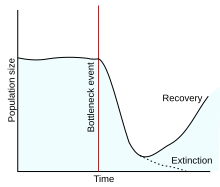
Eine andere, zwischenzeitlich für ausgestorben gehaltene, Unterart (C. n. shoshone) hat einen genetischen Flaschenhals überlebt und wurde wiederentdeckt (Lazarus-Effekt[161]), ist aber genetisch verarmt.[162]
- Owens Wüstenkärpfling (Cyprinodon radiosus): die Art wurde 1961 von verschiedenen Wissenschaftlern als ausgestorben betrachtet, 1964 jedoch an einer abgelegenen Stelle von Fish Slough (Kalifornien) wiederentdeckt.[162] 2013 wurde die Art von der IUCN als „stark gefährdet“ aufgeführt.[163]
- C. nevadensis shoshone: für diese Unterart des Nevada-Wüstenkärpflings hatten zahlreiche Untersuchungen keine Population mehr auffinden können, sie wurde jedoch 1986 wiederentdeckt. Der Bestand war allerdings zwischenzeitlich so stark reduziert worden, dass die überlebenden Individuen Nachfahren einer Population sind, die einen genetischen Flaschenhals durchlebt hat. Diese Unterart ist somit ein Beispiel von gefährdeten Taxa, bei denen zwar eine Restpopulation überlebt hat, die aber bereits einen Großteil ihrer ursprünglichen genetischen Variation eingebüßt hat.[162]
Beide genannten Wüstenkärpfling-Taxa sind Beispiele für zwischenzeitlich für ausgestorben gehaltene Fisch-Taxa, die jahrelang in prekär geringer Individuenanzahl überlebt haben, dann aber zur Überraschung der Wissenschaft entweder durch Fund an abgelegenen Stellen ihres Lebensraums oder durch Erfassung nach Bestandserholung wieder vorgefunden wurden.[162][161] Die mit rund 40 Arten vertretene Gattung der Wüstenkärpflinge (oder: Wüstenfische) (Cyprinodon) weist durch eine enge evolutive Verbindung zu den erdgeschichtlichen Entwicklungsphasen biologisch ungewöhnlich bemerkenswerte Adaptionen auf und enthält Reliktarten, deren Populationen in isolierten Teilarealen verbreitet und stark gefährdet sind.[164]
- Pondicherryhai (Carcharhinus hemiodon) (Küsten Indiens und Oman bis in die Inselgebiete Südostasiens um Vietnam, Indonesien und Neuguinea; im Jahr 1979 gelang das letzte Mal ein wissenschaftlicher Nachweis, bis im Januar 2016 ein Exemplar bei Sri Lanka wiederentdeckt wurde) [165][166]
- Notropis amecae (Río Ameca (Jalisco, Mexiko); galt seit 1969 als ausgestorben, eine kleine Population wurde aber im Jahr 2001 wiederentdeckt; sie werden gezüchtet und seit 2015 wiederangesiedelt) [167][168][169]
- Pseudogobiopsis tigrellus, Syn.: Gobius tigrellus (Mamberamo (Westneuguinea, Indonesien); diese Zwerggrundel wurde zwischen 1939 und 2000 nicht gesichtet) [170][171]
- Ptychochromoides itasy (Tsiribihina (Madagaskar); zwischen den späten 1970er-Jahren und 2010 nicht gesichtet) [172][173]
- Mangarahara-Buntbarsch (Ptychochromis insolitus): Das Vorkommen in der Natur dieser Art aus der Familie der Buntbarsche wurde im Jahr 2013 wiederentdeckt. Die Wiederentdeckung war nur durch ein gezieltes Programm mit internationaler Beteiligung und Freilandarbeit möglich und ist ein Beispiel für die zahlreichen Fälle, in denen die Wiederentdeckung der Lazarus-Arten einen erheblichen Suchaufwand erfordert.[174] Die Art wird als „vom Aussterben bedroht“ eingestuft (IUCN, 2016).[175]
- Rheocles pellegrini (westlich der Stadt Andapa (Madagaskar); zwischen den 1930er-Jahren und den 2000er-Jahren nicht gesichtet) [176]
- Tiefseesaibling, Bodensee-Tiefensaibling (Salvelinus profundus) (Bodensee (Österreich, Deutschland, Schweiz); wurde im Jahr 2008 für ausgestorben erklärt, weil er in den 1970er-Jahren zuletzt gesichtet wurde; zwischen 2010 und 2015 wurde die Art wiederentdeckt) [177][178]
- Siphateles bicolor isolata, Syn.: Gila bicolor isolata (Independence Valley fault system (Elko County, Nevada, USA); diese Unterart von Siphateles bicolor war im Jahr 1965 noch häufig, verschwand aber innerhalb eines Jahrzehnts; im Jahr 2000 wurde die Art wiederentdeckt, ist aber noch immer bedroht) [179][180][160]

- Stygichthys typhlops, brasilianischer Blindsalmler, lange nur vom Holotypus aus dem Jahre 1962 bekannt, 2004 wiederentdeckt.
- Ukliva-Strömer (Telestes ukliva) (im Abfluss des Cetina (Kroatien); wurde zwischen 1988 und 1997 für ausgestorben gehalten) [181][182]
Insekten
- Xylotoles costatus: Diese Bockkäfer-Art wurde 1996 für ausgestorben erklärt und von der IUCN auch bereits seit 1986 als „ausgestorben“ aufgeführt. Die Art wurde seitdem jedoch seitdem auf Pitt Island, einer Insel der Chatham-Inseln, wiederentdeckt. Es existiert allerdings lediglich eine einzelne Population auf einer Fläche von rund 200 Hektar mit geschätzt weniger als 200 adulten Individuen und die Art wurde als „stark gefährdet“ eingestuft (IUCN, 2004).[183]
- Baumhummer (Dryococelus australis): Diese Gespenstschrecken-Art von der Lord-Howe-Insel in Australien galt nach der Einschleppung von Ratten seit etwa 1920 oder 1930 als ausgestorben[18][184] und wurde auch von der IUCN (seit 1986) offiziell als ausgestorben gelistet.[184] 2001 wurde sie dann jedoch auf dem nahe gelegenen Felsinsel Ball’s Pyramid wiederentdeckt.[18][184] Allerdings wurde die Art nach ihrer Wiederentdeckung seit 2002 als „vom Aussterben bedroht“ eingestuft (IUCN, 2017), da ihr verbliebener Lebensraum auf Ball’s Pyramid auf weniger als einen Quadratkilometer beschränkt (bei einem beobachteten Bestand von höchstens 35 Individuen) und zufällige, auf ihn einwirkende Ereignisse zu einem Aussterben der Art führen können.[184] – Der Fall ist ein Beispiel dafür, dass die Wissenschaft bewerten muss, wie aussichtsreich die Wiederansiedlung einer Art ist, oder ob deren Aussterben als unabwendbar hinzunehmen ist.[18]
- Linsenfliege (Thyreophora cynophila): Die Fliegen-Art wurde als seit den 1840er Jahren ausgestorben betrachtet und 2007 als einzige Dipteren-Art auf einer Liste rezenter europäischer Arten, die weltweit als ausgestorben gelten, aufgeführt.[185][186] Sie wurde vermutlich durch im Jahr 2007 durchgeführte Fallenfänge in nahe von Madrid gelegenen Wäldern wiederentdeckt.[185] – Die Wiederentdeckung der Linsenfliege warf Bedenken hinsichtlich der künftigen Erhaltung ihrer Bestände auf. Anhand dieses Falles wurde exemplarisch auf die Problematik hingewiesen, dass zu den Hauptbedrohungen von wiederentdeckten Insektenarten der wahllose Fang durch Insektensammler zählt und daher Schutzmaßnahmen wie Beschränkungen oder Verbote ihres Fangs Vorrang haben sollten.[185]
- Megachile pluto: Diese Bienen-Art nistet offenbar nur in bewohnten Nestern der baumbewohnenden Termite Microcerotermes amboinensi.[187] , Die Art besitzt von allen lebenden Bienenarten die größte Körpergröße und weuist eine längere Nachweisgeschichte von „Wiederentdeckungen“ auf.[188] Nachdem sie 1981 zufällig nachgewiesen wurde, gab es keine sicheren, der Wissenschaft bekannten Sichtungen mehr und daher Befürchtungen, dass die Art ausgestorben sei, bis eine Expedition im Januar 2019 die Art auf den nördlichen Molukken nachweisen konnte.[189][188][190] Die Art wird als „gefährdet“ eingestuft (IUCN, 2014).[187]
- Pharohylaeus lactiferus, die australische Bienenart galt fast 100 Jahre lang als verschollen.[191]
Weichtiere
- Aldabra-Schnecke (Rhachistia aldabrae): Diese landlebende Landlungenschnecken-Art aus der Familie Cerastidae lebt nur auf dem Aldabra-Atoll (Seychellen). Nachdem von ihr in den 1980er Jahren noch vereinzelt frische Schneckengehäuse gefunden sowie ein einzelnes im Jahr 1997, wurden trotz intensiver Suche zunächst keine Spuren ihres fortgesetzten Überlebens mehr entdeckt und sie galt als ausgestorben, bis sie 2014 wiederentdeckt wurde. Die Art wird als „vom Aussterben bedroht“ eingestuft (IUCN, 2018).[192]
- Leptoxis compacta: Süßwasserbewohnende Schnecken-Art aus der Familie Pleuroceridae mit Verbreitungsgebiet in Alabama (USA). Von der IUCN wird die Art – mit Hinweis auf Aktualisierungsbedarf – als „ausgestorben“ geführt (IUCN, 2000).[193] Die Art wurde Untersuchungen von Museumssammlungen zufolge wohl 1933 zum letzten Mal gesammelt. Im Jahr 2000 wurde sie formell für ausgestorben erklärt, 2011 aber im Cahaba River wiederentdeckt.[194]
Nesseltiere
- Crambione cookii, Schirmqualle an den Küsten Australiens: keine Sichtungen zwischen 1896 und 1999
Beispiele für Pflanzen
- Nubische Wüstenpalme
- Quallenbaum
- Anogramma ascensionis
- Urweltmammutbaum
- Wollemie
- Bulbostylis neglecta (Sauergrasart von St. Helena, galt zwischen 1806 und 2008 als ausgestorben)
- Euphrasia arguta, (Augentrostart aus dem australischen Bundesstaat New South Wales, keine Funde zwischen 1904 und 2008)
- Asplenium dielmannii, (Streifenfarnart von der Hawaii-Insel Kauaʻi, keine Funde zwischen 1900 und 2002).
- Deparia kaalaana, (Frauenfarnart von der Hawaii-Insel Maui, keine Funde zwischen 1909 und 2013).
- Haloragodendron lucassii: die zur Familie der Tausendblattgewächse gehörende Art wurde nach 1926 nicht mehr nachgewiesen und daher in die Liste ausgestorbener Arten aufgenommen, dann aber 1986 in einem Vorort Sydneys wiederentdeckt.[195] – Der Fall gilt als ein Beispiel dafür, dass sich die Aufführung in der Liste ausgestorbener Arten (Gefährdungskategorie: EX) in einigen Fällen positiv in Form gesteigerter Suchbemühungen auswirkt,[196] denn die Art wurde wiederentdeckt, weil ein Amateur-Botaniker durch Erscheinen eines Buchs über ausgestorbene und gefährdete Pflanzen, in dem sich detailliertere Angaben zur Art befanden, zur Suche nach der Art angeregt worden war.[195]
Siehe auch
Einzelnachweise
- ↑ a b Simon A. Black: Chapter 11: Assessing Presence, Decline, and Extinction for the Conservation of Difficult-to-Observe Species. In: Francesco Maria Angelici, Lorenzo Rossi (Hrsg.): Problematic Wildlife II: New Conservation and Management Challenges in the Human-Wildlife Interactions. 1. Auflage. Springer, Cham 2020, ISBN 978-3-03042334-6, S. 359–392, hier S. 367, doi:10.1007/978-3-030-42335-3 (i–xiv, 1–649).
- ↑ a b c d e f g h i j k l Emmanuel Fara: What are Lazarus taxa? In: Geological Journal. Band 36, 3–4 (Special Issue: History of Biodiversity; Juli–Dezember 2001), 2001, S. 291–303, doi:10.1002/gj.879 (Erste Online-Veröffentlichung am 28. September 2001).
- ↑ a b P. B. Wignall, M. J. Benton: Lazarus taxa and fossil abundance at times of biotic crisis. In: Journal of the Geological Society. Band 156, Nr. 3, 1999, S. 453–456, doi:10.1144/gsjgs.156.3.0453 (Online-Veröffentlichung am 1. Juni 1999).
- ↑ a b c David A. Keith, Mark A. Burgman: The Lazarus effect: can the dynamics of extinct species lists tell us anything about the status of biodiversity? In: Biological Conservation. Band 117, Nr. 1, Mai 2004, S. 41–48, doi:10.1016/S0006-3207(03)00261-1.
- ↑ a b Karl W. Flessa, David Jablonski: Extinction is Here to Stay. In: Paleobiology. Band 9, Nr. 4, 1983, S. 315–321, JSTOR:2400573.
- ↑ Douglas H. Erwin, Mary L. Droser: Elvis taxa. In: PALAIOS. Band 8, Nr. 6, 1. Dezember 1993, S. 623–624, doi:10.2307/3515039. Dort mit Verweis auf: D. Jablonski: Causes and consequences of mass extinctions: a comparative approach. In: E. K. Elliott (Hrsg.): Dynamics of extinction. Wiley, New York 1986, S. 183–229. Und auf: R. L. Batten: The vicissitudes of the gastropods during the interval of Guadalupian-Ladinian time. In: A. Logan, L. V. Hills (Hrsg.): The Permian and Triassic Systems and Their Mutual Boundary (= Memoir. Band 2). Canadian Society of Petroleum Geologists, 1973, S. 596–607.
- ↑ Emmanuel Fara: What are Lazarus taxa? In: Geological Journal. Band 36, 3–4 (Special Issue: History of Biodiversity; Juli–Dezember 2001), 2001, S. 291–303, doi:10.1002/gj.879 (Erste Online-Veröffentlichung am 28. September 2001). Dort mit Verweis auf: D. Jablonski: Causes and consequences of mass extinctions: a comparative approach. In: E. K. Elliott (Hrsg.): Dynamics of extinction. Wiley, New York 1986, S. 183–229.
- ↑ a b c d Douglas H. Erwin, Mary L. Droser: Elvis taxa. In: PALAIOS. Band 8, Nr. 6, 1. Dezember 1993, S. 623–624, doi:10.2307/3515039.
- ↑ Simon A. Black: Chapter 11: Assessing Presence, Decline, and Extinction for the Conservation of Difficult-to-Observe Species. In: Francesco Maria Angelici, Lorenzo Rossi (Hrsg.): Problematic Wildlife II: New Conservation and Management Challenges in the Human-Wildlife Interactions. 1. Auflage. Springer, Cham 2020, ISBN 978-3-03042334-6, S. 359–392, hier S. 367, doi:10.1007/978-3-030-42335-3 (i–xiv, 1–649). Dort mit Verweis auf: Douglas H. Erwin, Mary L. Droser: Elvis taxa. In: PALAIOS. Band 8, Nr. 6, 1. Dezember 1993, S. 623–624, doi:10.2307/3515039 (Online-Veröffentlichung am).
- ↑ Douglas H. Erwin: The Mother of Mass Extinctions. In: Scientific American. Band 275, Nr. 1, Juli 1996, S. 72–78, JSTOR:24993272.
- ↑ Douglas H. Erwin, Mary L. Droser: Elvis taxa. In: PALAIOS. Band 8, Nr. 6, 1. Dezember 1993, S. 623–624, doi:10.2307/3515039. Mit Verweis auf: D. H. Erwin: The great Paleozoic Crisis. Columbia University Press, New York 1993 (327 S.).
- ↑ a b Mary R. Dawson, Laurent Marivaux, Chuan-kui Li, K. Christopher Beardand, Grégoire Métais: Laonastes and the "Lazarus Effect" in Recent Mammals. In: Science. Band 311, Nr. 5766, 10. März 2006, S. 1456–1458, doi:10.1126/science.1124187: „The Lazarus effect refers to the reappearance of taxa after a lengthy hiatus in the fossil record [...]. The discovery of living examples of taxa that were previously thought to be extinct is a very special case of the Lazarus effect, one that has only rarely been documented among mammals and other vertebrates.“
- ↑ a b c d e f g h i j k l m n o p q r s t u v w Wolfgang Böhme, Darius Stiels: Totgesagte leben länger: Wiederentdeckungen ausgestorben geglaubter Landwirbeltiere. In: Koenigiana. Band 1, Nr. 1, 2007, ISSN 2627-0005, S. 21–39.
- ↑ a b Ralph M. Wetzel, Robert E. Dubos, Robert L. Martin, Philip Myers: Catagonus, an "Extinct" Peccary, Alive in Paraguay. In: Science. Band 189, Nr. 4200, 1. August 1975, S. 379–381, doi:10.1126/science.189.4200.379, JSTOR:1740567.
- ↑ a b Ralph M. Wetzel: The Chacoan peccary, Catagonus wagneri (Rusconi). In: Bull. Cernegie Mus. Nat. Hist. (Bulletin of Carnegie Museum Of Natural History). Band 3, 1977, ISSN 0145-9058, S. 1–36 (biodiversitylibrary.org).
- ↑ a b c M. Eisentraut: Über das Vorkommen des Chaco-Pekari, Catagonus wagneri, in Bolivien. In: Bonn. zool. Beitr. Band 37, Nr. 1, S. 43–47 (biodiversitylibrary.org).
- ↑ Diether Zscheile, Karin Zscheile: Zootierhaltung: Säugetiere. Begründet von W. Puschmann, fortgeführt und neu bearbeitet von D. Zscheile und K. Zscheile. 6. Auflage. Verlag Europa-Lehrmittel (Edition Harri Deutsch), Haan-Gruiten 2018, ISBN 978-3-8085-5745-7, hier S. 707 (994 Seiten).
- ↑ a b c d e f g Alberto Castaño Camacho: Lazarus Species: hope for conservation? Sometimes, species that were decleared extint are rediscovered, as if they came back to life. In: latinamericanpost.com. 26. Dezember 2017, abgerufen am 21. Mai 2022.
- ↑ Catagonus wagneri in der Roten Liste gefährdeter Arten der IUCN 2015. Eingestellt von: Altrichter, M., Taber, A., Noss, A., Maffei, L. & Campos, J., 2011. Abgerufen am 14. Mai 2022.
- ↑ Christian Matschei: Seltene Tiere im Zoo - Säugetiere. Schüling Verlag, Münster 2017, ISBN 978-3-86523-288-5, hier S. 16 (239 Seiten).
- ↑ a b c Mary R. Dawson, Laurent Marivaux, Chuan-kui Li, K. Christopher Beard, Grégoire Métais: Laonastes and the "Lazarus Effect" in Recent Mammals. In: Science. Band 311, Nr. 5766, 10. März 2006, S. 1456–1458, doi:10.1126/science.1124187.
- ↑ a b c d Dorothée Huchon, Pascale Chevret, Ursula Jordan, C. William Kilpatrick, Vincent Ranwez, Paulina D. Jenkins, Jürgen Brosius, Jürgen Schmitz: Multiple molecular evidences for a living mammalian fossil. In: Proceedings of the National Academy of Sciences of the USA (PNAS). Band 104, Nr. 18, 1. Mai 2007, S. 7495–7499, doi:10.1073/pnas.0701289104.
- ↑ a b c Ein lebendes Fossil. Norbert Frie Presse- und Informationsstelle: Westfaelische Wilhelms-Universität Münster. In: idw-online.de (Informationsdienst Wissenschaft (idw)). 10. Mai 2007, abgerufen am 6. Mai 2022. Dort mit Verweis auf: Dorothée Huchon, Pascale Chevret, Ursula Jordan, C. William Kilpatrick, Vincent Ranwez, Paulina D. Jenkins, Jürgen Brosius, Jürgen Schmitz: Multiple molecular evidences for a living mammalian fossil. In: Proceedings of the National Academy of Sciences of the USA (PNAS). Band 104, Nr. 18, 1. Mai 2007, S. 7495–7499, doi:10.1073/pnas.0701289104.
- ↑ a b c d e f g E. Thenius: „Lebende Fossilien“ im Organismenreich: Paläontologie und Molekularbiologie als wichtigste Grundlagen. In: Denisia. Nr. 20, 2007, ISSN 1608-8700, S. 75–96 (zobodat.at [PDF] Zugleich: Kataloge der oberösterreichischen Landesmuseen, Neue Serie, 66).
- ↑ a b Paulina D. Jenkins, C. William Kilpatrick, Mark F. Robinson, Robert J. Timmins: Morphological and molecular investigations of a new family, genus and species of rodent (Mammalia: Rodentia: Hystricognatha) from Lao PDR. In: Systematics and Biodiversity. Band 2, Nr. 4, 2005, S. 419–454, doi:10.1017/S1477200004001549.
- ↑ Burramys parvus in der Roten Liste gefährdeter Arten der IUCN 2008. Eingestellt von: Menkhorst, P., Broome, L. & Driessen, M., 2008. Abgerufen am 14. Mai 2022.
- ↑ Michael Archer, Hayley Bates, Suzanne J. Hand, Trevor Evans, Linda Broome, Bronwyn McAllan, Fritz Geiser, Stephen Jackson, Troy Myers, Anna Gillespie, Chris Palmer, Tahneal Hawke, Alexis M. Horn: The Burramys Project: a conservationist's reach should exceed history's grasp, or what is the fossil record for? In: Phil. Trans. R. Soc. B. Band 374, Nr. 1788, 4. November 2019, 20190221, doi:10.1098/rstb.2019.0221.
- ↑ a b c d e f g h i Evžen Kůs, Václav Pfleger: Seltene und bedrohte Tiere: Die große farbige Enzyklopädie. Gondrom, Bindlach 2001, ISBN 3-8112-1830-1, hier S. 137 (160 S.).
- ↑ a b W. E. Engelmann: Klasse Knochenfische (Osteichthyes). In: Wolf-Eberhard Engelmann (Hrsg.): Zootierhaltung: Tiere in menschlicher Obhut: Fische. 1. Auflage. Harri Deutsch, Frankfurt am Main 2005, ISBN 3-8171-1352-8, S. 219–224, hier S. 224 (890 Seiten).
- ↑ a b c d e f g h Simon A. Black: Chapter 11: Assessing Presence, Decline, and Extinction for the Conservation of Difficult-to-Observe Species. In: Francesco Maria Angelici, Lorenzo Rossi (Hrsg.): Problematic Wildlife II: New Conservation and Management Challenges in the Human-Wildlife Interactions. 1. Auflage. Springer, Cham 2020, ISBN 978-3-03042334-6, S. 359–392, hier S. 368, doi:10.1007/978-3-030-42335-3 (i–xiv, 1–649).
- ↑ a b c W. E. Engelmann, J. Kormann: 17: Ordnung Hohlstachlerartige (Coelacanthiformes). In: Wolf-Eberhard Engelmann (Hrsg.): Zootierhaltung: Tiere in menschlicher Obhut: Fische. 1. Auflage. Harri Deutsch, Frankfurt am Main 2005, ISBN 3-8171-1352-8, S. 225–227, hier S. 225 (890 Seiten).
- ↑ E. Thenius: „Lebende Fossilien“ im Organismenreich: Paläontologie und Molekularbiologie als wichtigste Grundlagen. In: Denisia. Nr. 20, 2007, ISSN 1608-8700, S. 75–96 (zobodat.at [PDF] Zugleich: Kataloge der oberösterreichischen Landesmuseen, Neue Serie, 66). Dort mit Verweis auf: H. Fricke: Coelacanths: The fish that time forgot. In: National Geographic. Band 173, Nr. 6, Juni 1988, ISSN 0027-9358, S. 824–838.
- ↑ Latimeria chalumnae in der Roten Liste gefährdeter Arten der IUCN 2000. Eingestellt von: Musick, J.A., 2000. Abgerufen am 17. Mai 2022.
- ↑ Latimeria menadoensis in der Roten Liste gefährdeter Arten der IUCN 2008. Eingestellt von: Erdmann, M., 2008. Abgerufen am 17. Mai 2022.
- ↑ B. Sanchíz, R. Adrover: Anfibios fósiles del Pleistoceno de Mallorca. In: Doñana, Acta vertebrata. Band 4, 1/2 (Dezember 1977), 1979, ISSN 0210-5985, S. 5–25 (csic.es – Veröffentlichungsjahr: 1979 (sic!)).
- ↑ Alytes muletensis in der Roten Liste gefährdeter Arten der IUCN 2020. Eingestellt von: IUCN SSC Amphibian Specialist Group, 2020. Abgerufen am 14. Mai 2022.
- ↑ a b c d e N.J. Collar: Extinction by assumption; or, the Romeo Error on Cebu. In: Oryx. Band 32, Nr. 4, Oktober 1998, S. 239–244, doi:10.1046/j.1365-3008.1998.d01-51.x (Erste Online-Veröffentlichung am 28. Juni 2008).
- ↑ J. Michael Scott, Fred L. Ramsey, Martjan Lammertink, Kenneth V. Rosenberg, Ron Rohrbaugh, John A. Wiens, J. Michael Reed: When is an “Extinct” Species Really Extinct? Gauging the Search Efforts for Hawaiian Forest Birds and the Ivory-Billed Woodpecker. In: Avian Conservation and Ecology - Écologie et conservation des oiseaux. Band 3, Nr. 2, 2008, S. Art. 3, doi:10.5751/ACE-00254-030203 (Erste Online-Veröffentlichung: 28. November 2008).
- ↑ a b c d e f Fernanda Schmidt Silveira, Angelo Alberto Schneider, Luis Rios de Moura Baptista: The role of a local rediscovery in the evaluation of the conservation status of a plant species: Testing the hypothesis of the biodiversity knowledge gap. In: Journal for Nature Conservation. Band 48, April 2019, S. 91–98, doi:10.1016/j.jnc.2018.10.004.
- ↑ a b c d Ben Collen, Samuel T. Turvey: Chapter 9: Probabilistic methods for determining extinction chronologies. In: Samuel T. Turvey (Hrsg.): Holocene Extinctions. Oxford University Press, Oxford & New York 2009, ISBN 978-0-19-953509-5, S. 181–191, hier S. 189, doi:10.1093/acprof:oso/9780199535095.001.0001 (i–xii, 1–352, Erste Online-Veröffentlichung im September 2009, DOI des Kapitels: 10.1093/acprof:oso/9780199535095.003.0009): „Scientists are sensibly reluctant to state with certainty if a species is extinct, so as not to facilitate the Romeo effect (giving up on a species too early; Collar 1998) or the Lazarus effect (bringing species back from the dead; Wignall and Benton 1999; Keith and Burgman 2004)“
- ↑ a b c Ben Collen, Andy Purvis, Georgina M. Mace: BIODIVERSITY RESEARCH: When is a species really extinct? Testing extinction inference from a sighting record to inform conservation assessment. In: Diversity Distrib. (Diversity and Distributions). Band 16, Nr. 5, September 2010, S. 755–764, doi:10.1111/j.1472-4642.2010.00689.x (Erste Online-Veröffentlichung am 12. Juli 2010): „Scientists are reluctant to state with certainty if a species is extinct, so as not to facilitate the Romeo effect (giving up on a species too early; Collar, 1998) or the Lazarus effect (bringing species back from being named extinct; Keith & Burgman, 2004).“
- ↑ a b c Jonathon C. Dunn, Graeme M. Buchanan, Richard J. Cuthbert, Mark J. Whittingham, Philip J.K. McGowan: Mapping the potential distribution of the Critically Endangered Himalayan Quail Ophrysia superciliosa using proxy species and species distribution modelling. In: Bird Conservation International. Band 25, Nr. 4, Dezember 2015, S. 466–478, doi:10.1017/S095927091400046X (Erste Online-Veröffentlichung am 5. Februar 2015; Lizenz: Creative Commons Attribution 3.0 Unported (CC BY 3.0)): „For example, giving up prematurely may doom the species to extinction (the ‘Romeo error’; Collar 1998) and re-appearances (the ‘Lazarus effect’; Keith and Burgman 2004 ) may waste conservation resources if costly and extensive surveys are undertaken.“
- ↑ a b c Brett R. Scheffers, Ding Li Yong, J. Berton C. Harris, Xingli Giam, Navjot S. Sodhi: The World's Rediscovered Species: Back from the Brink? In: PLoS ONE. Band 6, Nr. 7, 2011, S. e22531, doi:10.1371/journal.pone.0022531 (8 Seiten (als PDF), Erste Online-Veröffentlichung am 27. Juli 2011).
- ↑ a b c d e f g h H.R. Akçakaya, David A. Keith, Mark Burgman, Stuart H.M. Butchart, Michael Hoffmann, Helen M.Regan, Ian Harrison, Elizabeth Boakes: Inferring extinctions III: A cost-benefit framework for listing extinct species. In: Biological Conservation. Band 214, Oktober 2017, S. 336–342, doi:10.1016/j.biocon.2017.07.027.
- ↑ a b c S. H. M. Butchart, A. J. Stattersfield, T. M. Brooks: Going or gone: Defining 'Possibly Extinct' species to give a truer picture of recent extinctions. In: Bull. B. O. C. (Bulletin of the British Ornithologists' Club). 126A, 2006, ISSN 0007-1595, S. 7–24 (academia.edu).
- ↑ J. C. Z. Woinarski, M. F. Braby, A. A. Burbidge, D.Coates, S. T. Garnett, R. J. Fensham, S. M. Legge, N. L. McKenzie, J. L. Silcock, B. P. Murphy: Reading the black book: The number, timing, distribution and causes of listed extinctions in Australia. In: Biological Conservation. Band 239, Nr. 108261, November 2019, doi:10.1016/j.biocon.2019.108261.
- ↑ Wolfgang Böhme, Darius Stiels: Totgesagte leben länger: Wiederentdeckungen ausgestorben geglaubter Landwirbeltiere. In: Koenigiana. Band 1, Nr. 1, 2007, ISSN 2627-0005, S. 21–39. Dort mit Verweis auf: S. H. M. Butchart, A. J. Stattersfield, T. M. Brooks: Going or gone: Defining 'Possibly Extinct' species to give a truer picture of recent extinctions. In: Bull. B. O. C. (Bulletin of the British Ornithologists' Club). 126A, 2006, ISSN 0007-1595, S. 7–24 (academia.edu). Sowie auf: S. H. M. Butchart, N. J. Collar, M. J. Crosby, J. A. Tobias: "Lost" and poorly known birds: targets for birders in Asia. In: BirdingASIA. Band 3, Juni 2005, S. 41–49 (academia.edu orientalbirdclub.org). Und auf: Joseph A. Tobias, Stuart H. M. Butchart, Nigel J. Collar: Lost and found: a gap analysis for the Neotropical avifauna. In: Neotropical Birding. 2006, S. 3–22.
- ↑ a b c Campephilus principalis in der Roten Liste gefährdeter Arten der IUCN 2020. Eingestellt von: BirdLife International, 2020. Abgerufen am 20. April 2022.
- ↑ Kate Neafsey: Lessons from the ivory-billed woodpecker. In: news.cornell.edu Cornell Chronicle (hauseigene Wochenzeitung der Cornell University). 22. Dezember 2009, abgerufen am 17. April 2022.
- ↑ a b David L. Roberts, Chris S. Elphick, J. Michael Reed: Identifying Anomalous Reports of Putatively Extinct Species and Why It Matters. In: Conservation Biology. Band 24, Nr. 1, Februar 2010, S. 189–196, JSTOR:40419644.
- ↑ David S. Wilcove: Rediscovery of the Ivory-billed Woodpecker. In: Science. Band 308, Nr. 5727, 3. Mai 2005, S. 1422–1423, doi:10.1126/science.1114507.
- ↑ David L. Roberts: Extinct or Possibly Extinct? In: Science. Band 312, Nr. 5776, 19. Mai 2006, S. 997–998, doi:10.1126/science.312.5776.997c.
- ↑ a b David S. Wilcove: Rediscovery of the Ivory-billed Woodpecker. In: Science. Band 308, Nr. 5727, 3. Mai 2005, S. 1422–1423, doi:10.1126/science.1114507. Dort mit Verweis auf: Henry Fountain: The Basics; Extinct? Prove It. In: nytimes.com. 1. Mai 2005, abgerufen am 17. April 2022.
- ↑ Peter Cashwell: Along Those Lines: The Boundaries that Create Our World. Paul Dry Book, Philadelphia, Pennsylvania 2014, ISBN 978-1-58988-092-4, We're Not Lost, S. 213–225, hier S. 221 (237 S.).
- ↑ Ploceus megarhynchus in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: BirdLife International, 2021. Abgerufen am 21. Mai 2022.
- ↑ Hapalopsittaca fuertesi in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: BirdLife International, 2021. Abgerufen am 21. Mai 2022.
- ↑ Lepidothrix vilasboasi in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: BirdLife International, 2021. Abgerufen am 21. Mai 2022.
- ↑ Neophema splendida in der Roten Liste gefährdeter Arten der IUCN 2016. Eingestellt von: BirdLife International, 2016. Abgerufen am 21. Mai 2022.
- ↑ Lophura edwardsi in der Roten Liste gefährdeter Arten der IUCN 2018. Eingestellt von: BirdLife International, 2018. Abgerufen am 21. Mai 2022.
- ↑ a b Pterodroma cahow in der Roten Liste gefährdeter Arten der IUCN 2018. Eingestellt von: BirdLife International, 2018. Abgerufen am 21. Mai 2022.
- ↑ a b c Fregetta maoriana in der Roten Liste gefährdeter Arten der IUCN 2018. Eingestellt von: BirdLife International, 2018. Abgerufen am 21. Mai 2022.
- ↑ Megalurulus rufus in der Roten Liste gefährdeter Arten der IUCN 2020. Eingestellt von: BirdLife International, 2020. Abgerufen am 21. Mai 2022.
- ↑ Porphyrio hochstetteri in der Roten Liste gefährdeter Arten der IUCN 2020. Eingestellt von: BirdLife International, 2020. Abgerufen am 21. Mai 2022.
- ↑ Eutriorchis astur in der Roten Liste gefährdeter Arten der IUCN 2016. Eingestellt von: BirdLife International, 2016. Abgerufen am 21. Mai 2022.
- ↑ Corvus unicolor in der Roten Liste gefährdeter Arten der IUCN 2017. Eingestellt von: BirdLife International, 2016. Abgerufen am 21. Mai 2022.
- ↑ Otus alfredi in der Roten Liste gefährdeter Arten der IUCN 2016. Abgerufen am 21. Mai 2022.
- ↑ a b c d e John R. Platt: Why Don’t We Hear About More Species Going Extinct? The extinction crisis threatens life all over the planet, but scientists are cautious about declaring a species extinct too quickly. In: therevelator.org. 28. Mai 2019, abgerufen am 10. April 2022. Dort mit Verweis auf: N.J. Collar: Extinction by assumption; or, the Romeo Error on Cebu. In: Oryx. Band 32, Nr. 4, Oktober 1998, S. 239–244, doi:10.1046/j.1365-3008.1998.d01-51.x (Erstmals online veröffentlicht am 28. Juni 2008).
- ↑ a b c S. H. M. Butchart, A. J. Stattersfield, T. M. Brooks: Going or gone: Defining 'Possibly Extinct' species to give a truer picture of recent extinctions. In: Bull. B. O. C. (Bulletin of the British Ornithologists' Club). 126A, 2006, ISSN 0007-1595, S. 7–24 (academia.edu): „However, extinction — the disappearance of the last individual of a species — is very difficult to detect (Diamond 1987).“ Dort mit Verweis auf: N.J. Collar: Extinction by assumption; or, the Romeo Error on Cebu. In: Oryx. Band 32, Nr. 4, Oktober 1998, S. 239–244, doi:10.1046/j.1365-3008.1998.d01-51.x (Erste Online-Veröffentlichung am 28. Juni 2008). Und auf: Guy C. L. Dutson, Perla M. Magsalay, Rob J. Timmins: The rediscovery of the Cebu Flowerpecker Dicaeum Quadricolor, with notes on other forest birds on Cebu, Philippines. In: Bird Conservation International. Band 3, Nr. 3, September 1993, S. 235–243, doi:10.1017/S0959270900000927 (Erste Online-Veröffentlichung am 11. Mai 2010).
- ↑ a b Guy C. L. Dutson, Perla M. Magsalay, Rob J. Timmins: The rediscovery of the Cebu Flowerpecker Dicaeum Quadricolor, with notes on other forest birds on Cebu, Philippines. In: Bird Conservation International. Band 3, Nr. 3, September 1993, S. 235–243, doi:10.1017/S0959270900000927 (Erste Online-Veröffentlichung am 11. Mai 2010).
- ↑ a b Perla Magsalay, Thomas Brooks, Guy Dutson, Rob Timmins: Extinction and conservation on Cebu. In: Nature. Band 373, 1995, ISSN 1476-4687, S. 294, doi:10.1038/373294a0 (Veröffentlichung am 26. Januar 1995).
- ↑ S. H. M. Butchart, A. J. Stattersfield, T. M. Brooks: Going or gone: Defining 'Possibly Extinct' species to give a truer picture of recent extinctions. In: Bull. B. O. C. (Bulletin of the British Ornithologists' Club). 126A, 2006, ISSN 0007-1595, S. 7–24 (academia.edu): „However, extinction — the disappearance of the last individual of a species — is very difficult to detect (Diamond 1987).“ Dort mit Verweis auf: Perla Magsalay, Thomas Brooks, Guy Dutson, Rob Timmins: Extinction and conservation on Cebu. In: Nature. Band 373, 1995, ISSN 1476-4687, S. 294, doi:10.1038/373294a0 (Veröffentlichung am 26. Januar 1995).
- ↑ Dicaeum quadricolor in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: BirdLife International, 2020. Abgerufen am 20. April 2022.
- ↑ D. S. Rabor: The Impact of Deforestation on Birds of Cebu, Philippines, with New Records for That Island. In: The Auk. Band 76, Nr. 1, 1959, S. 37–43, doi:10.2307/4081841, JSTOR:4081841: „Ten endemic forms (see list below) have been recognized for Cebu. All presumably were forest birds. We were able to find only one of these, the Black Shama, Copsychus cebuensis. [...] Copsychus cebuensis Steere. Black Shama.-Collected by: Steere Expedition, Bourns and Worcester, McGregor, and Empeso. Lives in original forests, dense thickets, and dense second growth mixed with thickets. Its adaptation to second growth and thickets will help much in its survival on the island. F. Empeso collected a single specimen, a male with the testes enlarged, on July 16, 1956, in dense second growth mixed with thickets.“
- ↑ N.J. Collar: Extinction by assumption; or, the Romeo Error on Cebu. In: Oryx. Band 32, Nr. 4, Oktober 1998, S. 239–244, doi:10.1046/j.1365-3008.1998.d01-51.x (Erste Online-Veröffentlichung am 28. Juni 2008): „In retrospect it is apparent that after c. 1960 Cebu was effectively written off the biological map, with no ornithological interest other than shorebird counts and P.M. Magsalay's work on Rabor's one known forest survivor, the black shama Copsychus cebuensis.“
- ↑ Paul F. Donald: Facing Extinction: The World's Rarest Birds and the Race to Save Them. T & AD Poyser, London 2010, ISBN 978-0-7136-7021-9, hier S. 221. Dort mit Verweis auf: Warren B. King: Red data book: Volume 2: Aves. IUCN, Morges 1978 ("1978-1979").
- ↑ Perla Magsalay, Thomas Brooks, Guy Dutson, Rob Timmins: Extinction and conservation on Cebu. In: Nature. Band 373, 1995, ISSN 1476-4687, S. 294, doi:10.1038/373294a0 (Veröffentlichung am 26. Januar 1995): „The latest Red Data Book lists the island's two endemic species, the Cebu flowerpeeker and the black shama (Copsychus cebuensis), as 'threatened'.“
- ↑ Turdus xanthorhynchus in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: BirdLife International, 2020. Abgerufen am 21. Mai 2022.
- ↑ Amaurocichla bocagii in der Roten Liste gefährdeter Arten der IUCN 2018. Eingestellt von: BirdLife International, 2018. Abgerufen am 21. Mai 2022.
- ↑ Atlapetes blancae in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: BirdLife International, 2021. Abgerufen am 21. Mai 2022.
- ↑ Rhinoptilus bitorquatus in der Roten Liste gefährdeter Arten der IUCN 2017. Eingestellt von: BirdLife International, 2016. Abgerufen am 21. Mai 2022.
- ↑ a b Panji Gusti Akbar, Teguh Willy Nugroho, Muhammad Suranto, Muhammad Rizky Fauzan, Oddy Ferdiansyah, Joko Said Trisiyanto, Ding Li Yong: Missing for 170 years-the rediscovery of Black-browed Babbler Malacocincla perspicillata on Borneo. In: BirdingASIA. Band 34, 31. Dezember 2021, S. 13–14, doi:10.5281/zenodo.4562229.
- ↑ Malacocincla perspicillata in der Roten Liste gefährdeter Arten der IUCN 2016. Eingestellt von: BirdLife International, 2016. Abgerufen am 21. Mai 2022.
- ↑ Rhinoceros sondaicus in der Roten Liste gefährdeter Arten der IUCN 2020. Eingestellt von: Ellis, S. & Talukdar, B., 2019. Abgerufen am 12. Mai 2022.
- ↑ a b c Evžen Kůs, Václav Pfleger: Seltene und bedrohte Tiere: Die große farbige Enzyklopädie. Gondrom, Bindlach 2001, ISBN 3-8112-1830-1, hier S. 56 f. (160 S.).
- ↑ Diether Zscheile, Karin Zscheile: Zootierhaltung: Säugetiere. Begründet von W. Puschmann, fortgeführt und neu bearbeitet von D. Zscheile und K. Zscheile. 6. Auflage. Verlag Europa-Lehrmittel (Edition Harri Deutsch), Haan-Gruiten 2018, ISBN 978-3-8085-5745-7, hier S. 677 f. (994 Seiten).
- ↑ Dicerorhinus sumatrensis in der Roten Liste gefährdeter Arten der IUCN 2020. Eingestellt von: Ellis, S. & Talukdar, B., 2019. Abgerufen am 18. Mai 2022.
- ↑ a b Benoît Goossens, Milena Salgado-Lynn, Jeffrine J. Rovie-Ryan, Abdul H. Ahmad, Junaidi Payne, Zainal Z. Zainuddin, Senthilvel K. S. S. Nathan, Laurentius N. Ambu: Genetics and the last stand of the Sumatran rhinoceros Dicerorhinus sumatrensis. In: Oryx. Band 47, Nr. 3, 2013, S. 340–344, doi:10.1017/S0030605313000045.
- ↑ a b c Diether Zscheile, Karin Zscheile: Zootierhaltung: Säugetiere. Begründet von W. Puschmann, fortgeführt und neu bearbeitet von D. Zscheile und K. Zscheile. 6. Auflage. Verlag Europa-Lehrmittel (Edition Harri Deutsch), Haan-Gruiten 2018, ISBN 978-3-8085-5745-7, hier S. 679 (994 Seiten).
- ↑ a b c Nashorn wiederentdeckt: WWF entdeckt ausgestorben geglaubte Nashorn-Art in Kalimantan/Indonesien. In: wwf.de. 23. März 2016, abgerufen am 19. Mai 2022 (Mit einem Nachtrag vom 6. April 2016).
- ↑ a b c d e f g h i E. Meijaard, V. Nijmand: Secrecy considerations for conserving Lazarus species. In: Biological Conservation. Band 175, Juli 2014, S. 21–24, doi:10.1016/j.biocon.2014.03.021.
- ↑ Diether Zscheile, Karin Zscheile: Zootierhaltung: Säugetiere. Begründet von W. Puschmann, fortgeführt und neu bearbeitet von D. Zscheile und K. Zscheile. 6. Auflage. Verlag Europa-Lehrmittel (Edition Harri Deutsch), Haan-Gruiten 2018, ISBN 978-3-8085-5745-7, hier S. 676 (994 Seiten).
- ↑ E. Meijaard, V. Nijmand: Secrecy considerations for conserving Lazarus species. In: Biological Conservation. Band 175, Juli 2014, S. 21–24, doi:10.1016/j.biocon.2014.03.021. Dort mit Verweis auf: 'Extinct' Sumatran rhino spotted in Indonesian forest - video. In: theguardian.com. 8. Oktober 2013 (Quelle: Reuters). Und auf: Associated Press, Sumatran rhino footprints believed found on Borneo, URL: http://bigstory.ap.org/article/sumatran-rhino-footprints-believed-foundborneo, 28. März 2013.
- ↑ Sumatran rhino footprints believed found on Borneo. In: phys.org. 28. März 2013, abgerufen am 19. Mai 2022 (Quelle: Associated Press).
- ↑ a b c d e Diether Zscheile, Karin Zscheile: Zootierhaltung: Säugetiere. Begründet von W. Puschmann, fortgeführt und neu bearbeitet von D. Zscheile und K. Zscheile. 6. Auflage. Verlag Europa-Lehrmittel (Edition Harri Deutsch), Haan-Gruiten 2018, ISBN 978-3-8085-5745-7, hier S. 694 f. (994 Seiten).
- ↑ a b c d Simon A. Black: Chapter 11: Assessing Presence, Decline, and Extinction for the Conservation of Difficult-to-Observe Species. In: Francesco Maria Angelici, Lorenzo Rossi (Hrsg.): Problematic Wildlife II: New Conservation and Management Challenges in the Human-Wildlife Interactions. 1. Auflage. Springer, Cham 2020, ISBN 978-3-03042334-6, S. 359–392, hier S. 367 f., doi:10.1007/978-3-030-42335-3 (i–xiv, 1–649).
- ↑ a b c d Jane Goodall, Thane Maynard, Gail E. Hudson: Hope for animals and their world: how endangered species are being rescued from the brink. Grand Central, New York 2009, ISBN 978-0-446-54338-5, Pygmy Hog.
- ↑ Porcula salvania in der Roten Liste gefährdeter Arten der IUCN 2019. Eingestellt von: Meijaard, E., Narayan, G. & Deka, P., 2016. Abgerufen am 16. Mai 2022.
- ↑ Evžen Kůs, Václav Pfleger: Seltene und bedrohte Tiere: Die große farbige Enzyklopädie. Gondrom, Bindlach 2001, ISBN 3-8112-1830-1, hier S. 63 (160 S.).
- ↑ a b Gymnobelideus leadbeateri in der Roten Liste gefährdeter Arten der IUCN 2016. Eingestellt von: Woinarski, J. & Burbidge, A.A., 2014. Abgerufen am 20. April 2022.
- ↑ Gallotia auaritae in der Roten Liste gefährdeter Arten der IUCN 2009. Eingestellt von: Jose Antonio Mateo Miras, Iñigo Martínez-Solano, 2008. Abgerufen am 16. Mai 2022.
- ↑ Gallotia simonyi in der Roten Liste gefährdeter Arten der IUCN 2009. Eingestellt von: Jose Antonio Mateo Miras, Valentin Pérez-Mellado, Iñigo Martínez-Solano, 2008. Abgerufen am 21. Mai 2022.
- ↑ a b c Cuora yunnanensis in der Roten Liste gefährdeter Arten der IUCN 2010. Eingestellt von: van Dijk, P.P., Blanck, T. & Lau, M., 2009. Abgerufen am 13. Mai 2022.
- ↑ a b c d e f g Cyclura collei in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: Grant, T.D. & Pasachnik, S.A., 2021. Abgerufen am 14. Mai 2022.
- ↑ a b c Evžen Kůs, Václav Pfleger: Seltene und bedrohte Tiere: Die große farbige Enzyklopädie. Gondrom, Bindlach 2001, ISBN 3-8112-1830-1, hier S. 117 (160 S.).
- ↑ Contomastix vittata in der Roten Liste gefährdeter Arten der IUCN.
- ↑ a b c Chelonoidis phantasticus in der Roten Liste gefährdeter Arten der IUCN 2017. Eingestellt von: Rhodin, A.G.J., Gibbs, J.P., Cayot, L.J., Kiester, A.R. & Tapia, W., 2015. Abgerufen am 13. Mai 2022.
- ↑ a b Jill Langlois: 100 Jahre ausgestorben: Comeback einer Galapagos-Schildkröte. Seit 1906 war kein lebendes Exemplar der Fernandinha-Riesenschildkröte mehr gesehen worden. In: nationalgeographic.de. 26. Februar 2019, abgerufen am 13. Mai 2022 (Ursprünglich in englischer Sprache publiziert auf NationalGeographic.com).
- ↑ Adenomus kandianus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Extinct toad rediscovered after hiding for 133 years in Sri Lanka
- ↑ Amolops chakrataensis in der Roten Liste gefährdeter Arten der IUCN.
- ↑ a b c d e f g h i j Lost! Amphibians of India
- ↑ a b c d India's 5 Lost Frogs Rediscoverd
- ↑ Atelopus balios in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Atelopus coynei in der Roten Liste gefährdeter Arten der IUCN.
- ↑ My frog is ALIVE! – Atelopus coynei
- ↑ Atelopus ignescens in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Boy finds ‘extinct’ frog in Ecuador and helps revive species
- ↑ Cardioglossa cyaneospila in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Photos: the aye-aye of frogs rediscovered after 62 years
- ↑ Craugastor escoces in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Heredia Robber Frog rediscovered – Craugastor escoces
- ↑ Eleutherodactylus amadeus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ a b c d e f g Haiti earthquake: Rediscovered frog species offer signs of hope - gallery
- ↑ Eleutherodactylus corona in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Eleutherodactylus dolomedes in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Eleutherodactylus glandulifer in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Eleutherodactylus parapelates in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Eleutherodactylus thorectes in der Roten Liste gefährdeter Arten der IUCN.
- ↑ 'Extinct' tree frog rediscovered in India after 137 years
- ↑ Philautus jerdonii in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Hyperolius nimbae in der Roten Liste gefährdeter Arten der IUCN.
- ↑ a b c 'Lost' frogs found after decades
- ↑ Hyperolius sankuruensis in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Incilius holdridgei in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Reconsidering Extinction: Rediscovery of Incilius holdridgei (Anura: Bufonidae) in Costa Rica After 25 Years – Incilius holdridgei
- ↑ Indosylvirana aurantiaca in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Indosylvirana temporalis in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Zafrir Rinat: Long Thought Extinct, Hula Painted Frog Found Once Again in Israeli Nature Reserve. Rare find is akin to the Dead Sea Scrolls of nature conservation. In: haaretz.com. 17. November 2011, abgerufen am 16. Mai 2022.
- ↑ Latonia nigriventer in der Roten Liste gefährdeter Arten der IUCN 2021. Eingestellt von: IUCN SSC Amphibian Specialist Group, 2020. Abgerufen am 16. Mai 2022.
- ↑ Megophrys parva in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Micrixalus elegans in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Micrixalus narainensis in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Micrixalus swamianus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Micrixalus thampii in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Nymphargus anomalus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Anifibios del Ecuador (spanisch)
- ↑ Pseudophilautus hypomelas in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Not seen in over 130 years, ‘extinct’ frog rediscovered in Sri Lanka
- ↑ Pseudophilautus stellatus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Starry frog rediscovered after thought extinct for 160 years (photos)
- ↑ Pleurodema marmoratum in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Uperodon anamalaiensis in der Roten Liste gefährdeter Arten der IUCN.
- ↑ The Sixth Extinction – Possibly Extinct Amphibians ( des vom 16. November 2018 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Ambystoma leorae in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Observaciones – Ambystoma leorae. iNaturalist, abgerufen am 13. Januar 2019 (spanisch).
- ↑ Bolitoglossa jacksoni in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Brilliantly colored ‘lost’ salamander rediscovered after 42 years
- ↑ Chiropterotriton mosaueri in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Entosphenus minimus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ a b Robert R. Miller, James D. Williams, Jack E. Williams: Extinctions of North American Fishes During the Past Century. (PDF) Fisheries 14 (6), 1989, S. 22–38, abgerufen am 6. Januar 2019.
- ↑ a b H.R. Akçakaya, David A. Keith, Mark Burgman, Stuart H.M. Butchart, Michael Hoffmann, Helen M.Regan, Ian Harrison, Elizabeth Boakes: Inferring extinctions III: A cost-benefit framework for listing extinct species. In: Biological Conservation. Band 214, Oktober 2017, S. 336–342, doi:10.1016/j.biocon.2017.07.027. Dort mit Verweis auf: Robert R. Miller, James D. Williams, Jack E. Williams: Extinctions of North American Fishes During the past Century. In: Fisheries. Band 14, Nr. 6, 1989, S. 22–38, doi:10.1577/1548-8446(1989)014<0022:EONAFD>2.0.CO;2.
- ↑ a b c d Robert R. Miller, James D. Williams, Jack E. Williams: Extinctions of North American Fishes During the past Century. In: Fisheries. Band 14, Nr. 6, 1989, S. 22–38, doi:10.1577/1548-8446(1989)014<0022:EONAFD>2.0.CO;2.
- ↑ Cyprinodon radiosus in der Roten Liste gefährdeter Arten der IUCN 2013. Eingestellt von: NatureServe, 2011. Abgerufen am 8. Mai 2022.
- ↑ K. Breitfeld, W. E. Engelmann: 43 Ordnung Zahnkärpflingsartige (Cyprinodontiformes). In: Wolf-Eberhard Engelmann (Hrsg.): Zootierhaltung: Tiere in menschlicher Obhut: Fische. 1. Auflage. Harri Deutsch, Frankfurt am Main 2005, ISBN 3-8171-1352-8, S. 477–504, hier S. 486 (890 Seiten).
- ↑ Carcharhinus hemiodon in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Malaka Rodrigo: ‘Extinct’ shark spotted in Menik Ganga In: The Sunday Times vom 14. Februar 2016
- ↑ Notropis amecae in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Zoogoneticus tequila. Goodeid Working Group, abgerufen am 6. Januar 2019.
- ↑ Mexico Fish Ark Project. Chester Zoo, abgerufen am 6. Januar 2019.
- ↑ Gobius tigrellus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Helen Larson: Review of the gobiid fish genera Eugnathogobius and Pseudogobiopsis (Gobioidei: Gobiidae: Gobionellinae), with descriptions of three new species. The Raffles Bulletin of Zoology 57 (1), 2009, S. 127–181, abgerufen am 6. Januar 2019.
- ↑ Ptychochromoides itasy in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Helen Larson: Mad Fishes 2010. Toronto Zoo, abgerufen am 6. Januar 2019.
- ↑ H.R. Akçakaya, David A. Keith, Mark Burgman, Stuart H.M. Butchart, Michael Hoffmann, Helen M.Regan, Ian Harrison, Elizabeth Boakes: Inferring extinctions III: A cost-benefit framework for listing extinct species. In: Biological Conservation. Band 214, Oktober 2017, S. 336–342, doi:10.1016/j.biocon.2017.07.027. Dort mit Verweis auf: Brian Zimmerman: In search of the Mangarahara cichlid. In: Newsletter of the IUCN SSC/WI Freshwater Fish Specialist Group. 4 (Saving Freshwater Fishes and Habitats), März 2014, S. 17–22 (http://www.iucnffsg.org/wp-content/uploads/2013/05/ FFSG-Newsletter-March-2014-Small.pdf [PDF]).
- ↑ Ptychochromis insolitus in der Roten Liste gefährdeter Arten der IUCN 2016. Eingestellt von: Ravelomanana, T., Sparks, J.S. & Loiselle, P.V., 2016. Abgerufen am 19. Mai 2022.
- ↑ Rheocles pellegrini in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Salvelinus profundus in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Eawag: Überraschendes aus den Tiefen der Schweizer Seen, 9. Januar 2019.
- ↑ Siphateles bicolor in der Roten Liste gefährdeter Arten der IUCN.
- ↑ Siphateles bicolor isolata
- ↑ Telestes ukliva in der Roten Liste gefährdeter Arten der IUCN.
- ↑ D. Zanella, M. Mrakovčić, P. Mustafić, M. Ćaleta: Recovery of Telestes ukliva, an endemic species from the Cetina River, Croatia (Cypriniformes, Cyprinidae). Journal of Fish Biology 73 (1), 2008, S. 311–316, abgerufen am 13. Januar 2019.
- ↑ Xylotoles costatus in der Roten Liste gefährdeter Arten der IUCN 2004. Eingestellt von: McGuinness, C.A., 2004. Abgerufen am 22. Mai 2022.
- ↑ a b c d Dryococelus australis in der Roten Liste gefährdeter Arten der IUCN 2017. Eingestellt von: Rudolf, E. & Brock, P., 2017. Abgerufen am 21. Mai 2022.
- ↑ a b c Daniel Martín-Vega, Arturo Baz, Verner Michelsen: Back from the dead: Thyreophora cynophila (Panzer, 1798) (Diptera: Piophilidae) ‘globally extinct’ fugitive in Spain. In: Systematic Entomology. Band 35, Nr. 4, Oktober 2010, S. 607–613, doi:10.1111/j.1365-3113.2010.00541.x.
- ↑ Rowan Hooper: Zoologger: Horror fly returns from the dead. In: newscientist.com. 22. September 2010, abgerufen am 22. Mai 2022 (englisch).
- ↑ a b Megachile pluto in der Roten Liste gefährdeter Arten der IUCN 2014. Eingestellt von: Kuhlmann, M., 2013. Abgerufen am 22. Mai 2022.
- ↑ a b Ruby Prosser Scully: World’s biggest bee rediscovered after decades on ‘most wanted’ list. In: newscientist.com. 21. Februar 2019, abgerufen am 22. Mai 2022 (englisch).
- ↑ Clay Bolt: Rediscovering Wallace’s Giant Bee. In: rewild.org. 22. Februar 2019, abgerufen am 22. Mai 2022 (englisch).
- ↑ Daniel Lingenhöhl: Bienengigant nach 38 Jahren wiederentdeckt. Neben Wallaces Riesenbiene wirkt unsere Honigbiene wie ein Zwerg. Doch seit 1981 hatte niemand mehr diesen Giganten gesehen - bis jetzt. In: spektrum.de. 21. Februar 2019, abgerufen am 22. Mai 2022.
- ↑ J.B. Dorey. 2021. Missing for almost 100 years: the rare and potentially threatened bee, Pharohylaeus lactiferus (Hymenoptera, Colletidae). Journal of Hymenoptera Research 81: 165-180; doi:10.3897/jhr.81.59365
- ↑ Rhachistia aldabrae in der Roten Liste gefährdeter Arten der IUCN 2018. Eingestellt von: Gerlach, J., 2017. Abgerufen am 22. Mai 2022.
- ↑ Leptoxis compacta in der Roten Liste gefährdeter Arten der IUCN 2000. Eingestellt von: Bogan, A.E. (Mollusc Specialist Group), 2000. Abgerufen am 22. Mai 2022.
- ↑ Nathan V. Whelan, Paul D. Johnson, Phil M. Harris: Rediscovery of Leptoxis compacta (Anthony, 1854) (Gastropoda: Cerithioidea: Pleuroceridae). In: PLoS ONE. Band 7, Nr. 8, 2012, 42499, doi:10.1371/journal.pone.0042499 (Vollständige Artikel-Nr.: e42499).
- ↑ a b H.R. Akçakaya, David A. Keith, Mark Burgman, Stuart H.M. Butchart, Michael Hoffmann, Helen M.Regan, Ian Harrison, Elizabeth Boakes: Inferring extinctions III: A cost-benefit framework for listing extinct species. In: Biological Conservation. Band 214, Oktober 2017, S. 336–342, doi:10.1016/j.biocon.2017.07.027. Dort mit Verweis auf: J. H. Leigh, R. Boden, J. D. Briggs: Extinct and Endangered Plants. World Wildlife Fund MacMillan, Melbourne 1984.
- ↑ H.R. Akçakaya, David A. Keith, Mark Burgman, Stuart H.M. Butchart, Michael Hoffmann, Helen M.Regan, Ian Harrison, Elizabeth Boakes: Inferring extinctions III: A cost-benefit framework for listing extinct species. In: Biological Conservation. Band 214, Oktober 2017, S. 336–342, doi:10.1016/j.biocon.2017.07.027. Dort mit Verweis auf: Robin Moore: In Search of Lost Frogs: The Quest to Find the world's Rarest Amphibians. Bloomsbury Natural History, 2014, ISBN 978-1-4081-8633-6, S. 256.
Weblinks
- Daniel Lingenhöhl: Biodiversität - Manchmal kommen sie wieder. Spektrum.de, 22. Oktober 2010, abgerufen am 15. November 2018.