„COVID-19“ – Versionsunterschied
| [ungesichtete Version] | [ungesichtete Version] |
Gerbil (Diskussion | Beiträge) →Herkunft: + Beleg zum Hund |
Infos aus doi:10.1001/jama.2020.2648 (Bericht CCDC) und wenige Infos des Berichts der WHO-China joint mission eingetragen, CFR bislang auskommentiert, vgl. Disk. |
||
| Zeile 80: | Zeile 80: | ||
=== Anteil bestimmter Bevölkerungsgruppen === |
=== Anteil bestimmter Bevölkerungsgruppen === |
||
Eine Mitte Februar 2020 veröffentliche Auswertung der englischsprachigen und chinesischen Fachartikel kommt zu dem Ergebnis, dass alle Bevölkerungsgruppen infiziert werden können. Von den Infizierten waren 72 % 40 Jahre alt oder älter, 64 % waren männlich. 40 % der Patienten hatten [[Krankheitsverlauf|chronische Erkrankungen]] wie [[Diabetes mellitus]] und [[Arterielle Hypertonie|Bluthochdruck]].<ref name="Cheng_Infection_20200218" /> |
Eine Mitte Februar 2020 veröffentliche Auswertung der englischsprachigen und chinesischen Fachartikel kommt zu dem Ergebnis, dass alle Bevölkerungsgruppen infiziert werden können. Von den Infizierten waren 72 % 40 Jahre alt oder älter, 64 % waren männlich. 40 % der Patienten hatten [[Krankheitsverlauf|chronische Erkrankungen]] wie [[Diabetes mellitus]] und [[Arterielle Hypertonie|Bluthochdruck]].<ref name="Cheng_Infection_20200218" /> Dies bestätigt der Bericht der von der WHO in China durchgeführten ''gemeinschaftlichen Mission'' (engl. ''WHO-China joint mission''), der weiterhin noch [[Herz-Kreislauf-Erkrankung]]en, chronische [[Atemwegserkrankung]]en und [[Krebs (Medizin)|Krebs]] nennt.<ref name="WHO_cjm" /> |
||
Außerdem haben Personen über 60 Jahre ein höheres Risiko, einen schweren Krankheitsverlauf zu erleiden.<ref name="WHO_cjm" /> Die chinesische Seuchenschutzbehörde CCDC ([[Chinese Center for Disease Control and Prevention]]) hat alle bis zum 11. Februar 2020 vorliegenden Daten zu COVID-19-Krankheitsfällen in China ausgewertet und auch international publiziert. Bei den 44.672 bestätigten Fällen ergibt sich die folgende Altersgruppenverteilung: 3 % 80 Jahre und älter, 87 % 30–79 Jahre, 8 % 20–29 Jahre, 1 % 10–19 Jahre und 1 % jünger als 10 Jahre. Bei den infizierten Personen im Alter von 70 bis 79 Jahren und noch stärker bei den Personen, die 80 Jahre und älter sind, ist die Wahrscheinlichkeit, an COVID-19 zu versterben, höher als der Durchschnitt.<ref name="Wu_JAMA_20200224" /><!-- 8;0 % overall case-fatality rate (CFR) bzw. 14,8 % im Vgl. zu 2,3 % --> |
|||
=== Anteil schwerer Verläufe und Sterblichkeit === |
=== Anteil schwerer Verläufe und Sterblichkeit === |
||
| Zeile 107: | Zeile 109: | ||
In einem Informationsblatt des deutschen [[Auswärtiges Amt|Außenministeriums]] wird erwähnt, dass aus China Berichte „von [[Infektionskette]]n über die 4. Generationen hinaus“ vorliegen.<ref>{{Internetquelle |url=https://www.auswaertiges-amt.de/blob/2294930/c4ff6708cd7c37bac1cb198f53400b56/ncov-data.pdf |titel=Gesundheitsdienst, Stand 27. Januar 2020 |hrsg=Auswärtiges Amt |format=PDF |abruf=2020-01-27}}</ref> |
In einem Informationsblatt des deutschen [[Auswärtiges Amt|Außenministeriums]] wird erwähnt, dass aus China Berichte „von [[Infektionskette]]n über die 4. Generationen hinaus“ vorliegen.<ref>{{Internetquelle |url=https://www.auswaertiges-amt.de/blob/2294930/c4ff6708cd7c37bac1cb198f53400b56/ncov-data.pdf |titel=Gesundheitsdienst, Stand 27. Januar 2020 |hrsg=Auswärtiges Amt |format=PDF |abruf=2020-01-27}}</ref> |
||
== Klinische und laborchemische Krankheitszeichen == |
== Klinische Erscheinungen == |
||
=== Klinische und laborchemische Krankheitszeichen === |
|||
[[Datei:Symptoms of coronavirus disease 2019.png|mini|Schematische Darstellung der gängigen Krankheitssymptome verursacht durch das SARS-CoV2 (Beschriftung in englischer Sprache)]] |
[[Datei:Symptoms of coronavirus disease 2019.png|mini|Schematische Darstellung der gängigen Krankheitssymptome verursacht durch das SARS-CoV2 (Beschriftung in englischer Sprache)]] |
||
Da dieser Virustyp erst im Januar 2020 nachgewiesen wurde, ändern sich die Erkenntnisse über die Krankheit möglicherweise noch. Eine Abgrenzung zu anderen Viruserkrankungen wie [[Influenza]] ist schwierig. Nach einer [[Inkubationszeit]] von bis zu 14 Tagen<ref name="RKI_FAQ" /> können [[Fieber]], [[Myalgie|Muskelschmerzen]] und trockener [[Husten]] auftreten. Häufig manifestiert sich die Krankheit auch mit allgemeinem, schwerem Krankheitsgefühl und auch Rückenschmerzen.<ref name="Chan_Lancet_20200124" /> [[Symptom]]e der oberen Atemwege, wie Husten, [[Rhinitis|Schnupfen]], Halskratzen, sind möglich, einige Betroffene leiden auch an [[Durchfall]].<ref name="RKI_FAQ" /> Im weiteren Verlauf kann sich eine schwere Atemnot aufgrund einer Infektion der unteren Atemwege bis zur [[Lungenentzündung]] entwickeln.<ref name="Huang_Lancet_20200124" /> Diese kann mit Brustschmerzen im Sinne einer [[Pleuritis]] einhergehen. Die Mehrheit der Patienten zeigte die für schwere Virusinfekte typische Kombination aus einer Verminderung der Anzahl der [[Leukopenie|gesamten weißen Blutzellen]], einer Verminderung der [[Lymphopenie|Lymphozyten]]-Anzahl und einer Erhöhung laborchemischer Entzündungsparameter (wie [[C-reaktives Protein|CRP]] und [[Blutkörperchensenkungsgeschwindigkeit|BSG]]). Bildgebend zeigten sich in der [[Computertomographie]] der Lunge beidseitige, milchglasartige Verschattungen als Zeichen einer Bronchopneumonie.<ref name="Huang_Lancet_20200124" /> |
Da dieser Virustyp erst im Januar 2020 nachgewiesen wurde, ändern sich die Erkenntnisse über die Krankheit möglicherweise noch. Eine Abgrenzung zu anderen Viruserkrankungen wie [[Influenza]] ist schwierig. Nach einer [[Inkubationszeit]] von bis zu 14 Tagen<ref name="RKI_FAQ" /> können [[Fieber]], [[Myalgie|Muskelschmerzen]] und trockener [[Husten]] auftreten. Häufig manifestiert sich die Krankheit auch mit allgemeinem, schwerem Krankheitsgefühl und auch Rückenschmerzen.<ref name="Chan_Lancet_20200124" /> [[Symptom]]e der oberen Atemwege, wie Husten, [[Rhinitis|Schnupfen]], Halskratzen, sind möglich, einige Betroffene leiden auch an [[Durchfall]].<ref name="RKI_FAQ" /> Im weiteren Verlauf kann sich eine schwere Atemnot aufgrund einer Infektion der unteren Atemwege bis zur [[Lungenentzündung]] entwickeln.<ref name="Huang_Lancet_20200124" /> Diese kann mit Brustschmerzen im Sinne einer [[Pleuritis]] einhergehen. Die Mehrheit der Patienten zeigte die für schwere Virusinfekte typische Kombination aus einer Verminderung der Anzahl der [[Leukopenie|gesamten weißen Blutzellen]], einer Verminderung der [[Lymphopenie|Lymphozyten]]-Anzahl und einer Erhöhung laborchemischer Entzündungsparameter (wie [[C-reaktives Protein|CRP]] und [[Blutkörperchensenkungsgeschwindigkeit|BSG]]). Bildgebend zeigten sich in der [[Computertomographie]] der Lunge beidseitige, milchglasartige Verschattungen als Zeichen einer Bronchopneumonie.<ref name="Huang_Lancet_20200124" /> |
||
Die Mehrheit der Krankenhauseinweisungen der ersten Patienten erfolgte nach rund einwöchiger symptomatischer Krankheit aufgrund einer Verschlechterung des Zustandes. In den Fällen, in denen eine [[intensivmedizin]]ische Behandlung notwendig wurde, ergab sich deren Notwendigkeit nach rund zehn Tagen nach Symptombeginn.<ref name="Huang_Lancet_20200124" /> In einer epidemiologischen Studie von 99 hospitalisierten Fällen fanden bei 13 Patienten eine [[Beatmung#Nichtinvasive Beatmung (NIV)|nicht-invasive Beatmung]], bei vier Patienten eine invasive [[Beatmung]], bei neun Patienten eine [[Dialyse]] aufgrund eines [[Nierenversagen]]s und bei drei Patienten eine extrakorporale Lungenunterstützung ([[ECMO]]) Anwendung.<ref name="DOI10.1016/S0140-6736(20)30211-7">{{Literatur |Autor=Nanshan Chen, Min Zhou, Xuan Dong, Jieming Qu, Fengyun Gong, Yang Han, Yang Qiu, Jingli Wang, Ying Liu, Yuan Wei, Jia'an Xia, Ting Yu, Xinxin Zhang, L. i. Zhang |Titel=Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study |Sammelwerk=[[The Lancet]] |Datum=2020-01-30 |DOI=10.1016/S0140-6736(20)30211-7}}</ref> |
Die Mehrheit der Krankenhauseinweisungen der ersten Patienten erfolgte nach rund einwöchiger symptomatischer Krankheit aufgrund einer Verschlechterung des Zustandes. In den Fällen, in denen eine [[intensivmedizin]]ische Behandlung notwendig wurde, ergab sich deren Notwendigkeit nach rund zehn Tagen nach Symptombeginn.<ref name="Huang_Lancet_20200124" /> In einer epidemiologischen Studie von 99 hospitalisierten Fällen fanden bei 13 Patienten eine [[Beatmung#Nichtinvasive Beatmung (NIV)|nicht-invasive Beatmung]], bei vier Patienten eine invasive [[Beatmung]], bei neun Patienten eine [[Dialyse]] aufgrund eines [[Nierenversagen]]s und bei drei Patienten eine extrakorporale Lungenunterstützung ([[ECMO]]) Anwendung.<ref name="DOI10.1016/S0140-6736(20)30211-7">{{Literatur |Autor=Nanshan Chen, Min Zhou, Xuan Dong, Jieming Qu, Fengyun Gong, Yang Han, Yang Qiu, Jingli Wang, Ying Liu, Yuan Wei, Jia'an Xia, Ting Yu, Xinxin Zhang, L. i. Zhang |Titel=Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study |Sammelwerk=[[The Lancet]] |Datum=2020-01-30 |DOI=10.1016/S0140-6736(20)30211-7}}</ref> Im Bericht der chinesischen Seuchenschutzbehörde CCDC erfolgt die Klassifizierung als leichter Krankheitsverlauf, wenn keine oder nur eine leichte Lungenentzündung vorliegt, für einen schweren Krankheitsverlauf sind Pneumonie (Lungenentzündung), [[Dyspnoe]] (Atemnot), eine [[Atemfrequenz]] von ≥ 30 Atemzüge pro Minute, eine [[Sauerstoffsättigung]] des Blutes ≤ 93 % und weitere klinische Anzeichen typisch, bei einem kritischen Krankheitsverlauf ist mit [[Respiratorische Insuffizienz|Atemversagen]], [[Schock (Medizin)#Septischer Schock|septischem Schock]] und/oder Multiorganversagen zu rechnen.<ref name="Wu_JAMA_20200224" /> |
||
Ein wesentlicher Unterschied zum SARS-Coronavirus ist der, dass Patienten schon einige Tage vor Einsetzen der Krankheitssymptome infektiös sein können (beim SARS-Coronavirus waren die Patienten hingegen erst nach Auftreten der Symptome infektiös). Die Infektion lässt sich daher schwerer erkennen und schwieriger eindämmen. Bei [[Quarantäne]]maßnahmen reicht es deswegen nicht aus, nur die klinisch auffälligen Personen zu isolieren.<ref name="DEAEB_20200127" /> |
Ein wesentlicher Unterschied zum SARS-Coronavirus ist der, dass Patienten schon einige Tage vor Einsetzen der Krankheitssymptome infektiös sein können (beim SARS-Coronavirus waren die Patienten hingegen erst nach Auftreten der Symptome infektiös). Die Infektion lässt sich daher schwerer erkennen und schwieriger eindämmen. Bei [[Quarantäne]]maßnahmen reicht es deswegen nicht aus, nur die klinisch auffälligen Personen zu isolieren.<ref name="DEAEB_20200127" /> |
||
=== Krankheitsverlauf bzw. Dauer der Erkrankung === |
=== Krankheitsverlauf bzw. Dauer der Erkrankung === |
||
Die Auswertung von 44.415 Fällen durch die CCDC zeigt bei 81 % der bestätigten Fälle einen leichten, bei 14 % einen schweren und bei 5 % einen kritischen [[Krankheitsverlauf]].<ref name="Wu_JAMA_20200224" /> Bei einem leichten Krankheitsverlauf (dem häufigsten Fall) klingen die Krankheitszeichen, sofern überhaupt welche bestehen, laut [[Weltgesundheitsorganisation|WHO]] in der Regel innerhalb von zwei Wochen ab.<ref name="WHO_speech_20200224" /> Bei Menschen mit einem schweren Krankheitsverlauf dauere es zwischen drei und sechs Wochen, bis sie sich von der Krankheit erholen.<ref name="WHO_speech_20200224" /> |
|||
== Nachweismethoden == |
== Nachweismethoden == |
||
| Zeile 180: | Zeile 183: | ||
==== Allgemeinbevölkerung ==== |
==== Allgemeinbevölkerung ==== |
||
Das Robert Koch-Institut hat am 28. Januar 2020 Hinweise für die Allgemeinbevölkerung gegeben, wie man das Risiko für eine Ansteckung wesentlich verringern kann, sie sind nicht spezifisch für COVID-19, sondern gelten auch für Influenza und andere Atemwegsinfektionen. Hierbei wird in erster Linie auf folgende Punkte hingewiesen: |
Das Robert Koch-Institut hat am 28. Januar 2020 Hinweise für die Allgemeinbevölkerung gegeben, wie man das Risiko für eine Ansteckung wesentlich verringern kann, sie sind nicht spezifisch für COVID-19, sondern gelten auch für Influenza und andere Atemwegsinfektionen. Hierbei wird in erster Linie auf folgende Punkte hingewiesen: |
||
* auf eine gute Händehygiene achten: u. a. Hände mit Seife [[Händewaschen|waschen]]: vor dem Essen, vor und nach Kontakt zu anderen Menschen, nach Niesen/Husten; |
* auf eine gute Händehygiene achten: u. a. Hände mit Seife [[Händewaschen|waschen]]: vor dem Essen, vor und nach Kontakt zu anderen Menschen, nach dem Toilettengang, nach Niesen/Husten; |
||
* einen Mindestabstand von ein bis zwei Metern zu krankheitsverdächtigen Personen halten; |
* einen Mindestabstand von ein bis zwei Metern zu krankheitsverdächtigen Personen halten; |
||
* korrekte Hustenetikette: möglichst in die Armbeuge husten oder niesen, nicht in die Hand; |
* korrekte Hustenetikette: möglichst in die Armbeuge husten oder niesen, nicht in die Hand; |
||
| Zeile 537: | Zeile 540: | ||
|datum=2020-02-20 |
|datum=2020-02-20 |
||
|abruf=2020-02-25}} |
|abruf=2020-02-25}} |
||
</ref> |
|||
<ref name="WHO_cjm"> |
|||
{{Internetquelle |
|||
|url=https://www.who.int/docs/default-source/coronaviruse/who-china-joint-mission-on-covid-19-final-report.pdf |
|||
|titel=Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19) |
|||
|titelerg=16–24 February 2020 |
|||
|hrsg=[[Weltgesundheitsorganisation]] (WHO) |
|||
|datum=2020-02-28 |
|||
|format=PDF; 1,6 MB |
|||
|abruf=2020-03-02}} |
|||
</ref> |
</ref> |
||
<ref name="who_lab_testing"> |
<ref name="who_lab_testing"> |
||
| Zeile 587: | Zeile 600: | ||
|sprache=en |
|sprache=en |
||
|abruf=2020-02-26}} |
|abruf=2020-02-26}} |
||
</ref> |
|||
<ref name="Wu_JAMA_20200224"> |
|||
{{Literatur |
|||
|Autor=Zunyou Wu, Jennifer M. McGoogan, CCDC |
|||
|Titel=Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China |
|||
|Sammelwerk=[[Journal of the American Medical Association]] |
|||
|Datum=2020-02-24 |
|||
|Sprache=en |
|||
|DOI=10.1001/jama.2020.2648}} |
|||
</ref> |
</ref> |
||
<ref name="Zhou_Nature_20200203"> |
<ref name="Zhou_Nature_20200203"> |
||
Version vom 2. März 2020, 22:41 Uhr
| SARS-CoV-2 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||
| Systematik | ||||||||||||||||||
| ||||||||||||||||||
| Taxonomische Merkmale | ||||||||||||||||||
| ||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||
| Severe Acute Respiratory Syndrome Coronavirus 2 | ||||||||||||||||||
| Kurzbezeichnung | ||||||||||||||||||
| SARS-CoV-2 | ||||||||||||||||||
| Links | ||||||||||||||||||
|
SARS-CoV-2 (Sars-CoV-2; vormals 2019-nCoV, 2019-novel Corona virus, „neuartiges Coronavirus 2019“ sowie Wuhan-Virus[4]) ist die Bezeichnung eines im Januar 2020 in der chinesischen Stadt Wuhan, Provinz Hubei, neu identifizierten Coronavirus. Das Virus verursacht die Erkrankung namens COVID-19 (oder Covid-19, für Corona virus disease 2019)[5] und ist Auslöser der Coronavirus-Epidemie 2019/2020, die von der WHO als „gesundheitliche Notlage von internationaler Tragweite“ eingestuft wurde. In der Öffentlichkeit wird das Virus meist (nach der Virus-Familie) als Coronavirus oder gelegentlich (nach der Krankheit) als Covid-19-Virus bezeichnet.[6]
Entdeckungsgeschichte
Im Dezember 2019 wurde in der Stadt Wuhan eine Häufung von schweren Lungenentzündungen unklarer Ursache festgestellt. Am 30. Dezember 2019 informierte der chinesische Arzt Li Wenliang in einer WeChat-Gruppe seine Arztkollegen über sieben Patienten, die mit Verdacht auf eine Infektion mit dem SARS-Virus im Zentralkrankenhaus Wuhan behandelt wurden.[7] Die chinesische Seuchenschutzbehörde CCDC (Chinese Center for Disease Control and Prevention) entsandte am 31. Dezember 2019 ein Team in die Stadt.[8] Am selben Tag wurde das China-Büro der Weltgesundheitsorganisation (WHO) durch die chinesischen Behörden offiziell darüber informiert, dass im Dezember 2019 in Wuhan mehrere Personen an einer schweren Lungenentzündung erkrankt waren und dass als deren Ursache ein bis dahin uncharakterisierter, infektiöser Erreger vermutet wurde. Bis zum 3. Januar 2020 wurden der WHO insgesamt 44 Erkrankte gemeldet, darunter mehrere Schwerkranke. Da mehrere Erkrankte auf dem örtlichen „Südchinesischen Markt für Fische und Meeresfrüchte“ (chinesisch 武汉华南海鲜批发市场, Pinyin Wǔhàn huánán hǎixiān pīfā shìchǎng – „Wuhan Huanan Großhandelsmarkt für Fische und Meeresfrüchte“) als Verkäufer oder Händler arbeiteten, wurde in diesem Markt der primäre Infektionsort vermutet.[9][10]
Am 7. Januar 2020 gab der mit der Virusidentifizierung befasste, leitende chinesische Virologe Xu Jianguo (徐建国) bekannt, dass es sich bei dem Krankheitserreger um ein bis dahin unbekanntes Coronavirus handle. Dies hätten Untersuchungen von Blutproben und Rachenabstrichen von 15 Erkrankten ergeben. In einer Stellungnahme der WHO am 9. Januar 2020 wurde diese Erkenntnis bestätigt.[11][12] Am 13. Januar 2020 wurde die komplette Genomsequenz eines Isolats des neuen Coronavirus in der NCBI-GenBank hinterlegt (GenBank-Nummer MN908947).[13] Nahezu gleichzeitig wurde ein erstes Nachweisverfahren publiziert.[14][15][16]
Benennung
Die vom 13. Januar 2020 bis zum 11. Februar 2020 von der WHO verwendete Bezeichnung „2019-nCoV“ galt laut WHO als „vorläufig“.[17] Das erste sequenzierte Virusisolat wurde in der Erstbeschreibung als WH-Human-1 coronavirus (WHCV) bezeichnet (WH = Wuhan) und als Wuhan seafood market pneumonia virus isolate Wuhan-Hu-1 in die NCBI Taxonomie-Datenbank (die für Virusnamen und -klassifikationen nicht maßgebend ist) aufgenommen. Das Virus wurde dort danach – ebenfalls vorläufig – als Wuhan seafood market pneumonia virus geführt; als Synonyme wurden 2019-nCoV und Wuhan coronavirus erwähnt.[18] Namensvorschläge, das Virus in Anlehnung an MERS-CoV (Middle East respiratory syndrome coronavirus) nach dem Ort seiner Erstidentifikation, der Stadt Wuhan, als Wuhan respiratory syndrome coronavirus (WRS-CoV) zu benennen, wurden von der WHO nicht aufgegriffen. Ein von Fachleuten genannter Grund waren Beschwerden in der Vergangenheit, als Viren ihren Namen nach einzelnen Ländern oder Regionen erhalten hatten[19] (beispielsweise das Marburg-Virus). Die WHO hatte daher 2015 Empfehlungen herausgegeben, wie neue Krankheitserreger und Erkrankungen zu benennen seien. Eine Benennung nach dem Entdeckungsort wurde dabei explizit für unerwünscht erklärt.[20] In der NCBI Taxonomie-Datenbank aufgeführte Synonyme sind 2019-nCoV, COVID-19, COVID-19 virus, Wuhan coronavirus und Wuhan seafood market pneumonia virus (Stand 16. Februar 2020).[21]
Am 11. Februar 2020 gab die WHO bekannt, die durch das Virus verursachte Erkrankung als „COVID-19“ bzw. „Covid-19“ (Corona virus disease 2019) benannt zu haben.[5][22] Am selben Tag wurde von der Coronavirus Study Group (CSG) des International Committee on Taxonomy of Viruses (ICTV) auf dem Preprint-Server bioRxiv für das Virus die Bezeichnung SARS-CoV-2 (Severe Acute Respiratory Syndrome Coronavirus 2) vorgeschlagen.[1] Dem widersprach eine Woche später eine Gruppe chinesischer Virologen, die stattdessen als Bezeichnung „Humanes Coronavirus 2019“ (human coronavirus 2019, HCoV-19) vorschlug. Als Begründung nannten sie die Ähnlichkeit dieser Virusbezeichnung mit der Bezeichnung der von der WHO als COVID-19 benannten Krankheit und die Gefahr der Verwechslung von SARS-CoV-2 mit SARS-CoV in der Öffentlichkeit. Sie betonten, dass sich „2019-nCoV“ von dem SARS-Virus in biologischer und epidemiologischer Hinsicht unterscheidet, ebenso wie die klinischen Symptome von COVID-19 und SARS verschieden sind.[23] Zur Unterscheidung wird der Erreger von SARS auch als SARS-CoV-1 bezeichnet.[24]
Merkmale
Molekulargenetik und Phylogenetik
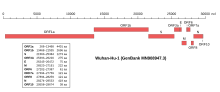
Das Virusgenom besteht, wie in Coronaviren üblich, aus einzelsträngiger RNA (ssRNA) mit positiver Polarität. Das Isolat Wuhan-Hu-1 (NCBI GenBank-Nummer MN908947[25]) umfasst 29.903 nt (Nukleotide) mit zwei 265 nt bzw. 229 nt langen untranslatierten Bereichen am 5′-Ende bzw. am 3′-Ende.[13] Die putativen (vermuteten) Gene könnten für zehn Proteine codieren: ein 7096 Aminosäuren (AS) langes ORF1ab-Polyprotein (Replikase-Komplex), ein 1273 AS langes Oberflächen-Glykoprotein (S für englisch spikes, vergleiche Peplomer), ein 75 AS langes Hüllprotein (E für engl. envelope, vergleiche Virushülle), ein 222 AS langes Membran-Glykoprotein (M), ein 419 AS langes Nukleokapsid-Phosphoprotein (N) und weitere fünf Proteine (ORF3a, ORF6, ORF7a, ORF8 und ORF10).[13] Die Abfolge der Gene entspricht jener des SARS-Virus und der aller Coronaviren.[26]
Mit Stand 16. Februar 2020 gab es mehr als 40 vollständige Genomanalysen von SARS-CoV-2-Isolaten. Die Genomgröße liegt zwischen 29.825 und 29.903 nt.[25] Der GC-Gehalt (der Anteil der Nukleinbasen Guanin und Cytosin) liegt bei 38,0 Mol-Prozent.[27][28] Die beiden Virusisolate HKU-SZ-002a (NCBI GenBank-Nummer MN938384[25]) und HKU-SZ-005b (NCBI GenBank-Nummer MN975262[25]) stammen von Patienten einer Familie aus Shenzhen und unterscheiden sich lediglich durch zwei Nukleotide. Die Genomanalyse dieser beiden Isolate ergab, dass sie nahe verwandt mit den bei Fledermäusen (englisch bat) auftretenden SARS-ähnlichen Coronaviren bat-SL-CoVZXC21 (NCBI GenBank-Nummer MG772934) und bat-SL-CoVZC45 (NCBI GenBank-Nummer MG772933) sind, zu letzterem besteht eine Übereinstimmung in der Nukleotidabfolge von 89 %. Das Genom der beiden Fledermaus-Coronaviren wurde 2018 sequenziert, bat-SL-CoVZC45 wurde bei der Chinesischen Hufeisennase (Rhinolophus sinicus)[29] aus der Familie der Hufeisennasen (Rhinolophidae) gefunden, die Wirtstiere wurden in Zhoushan in der ostchinesischen Provinz Zhejiang in den Jahren 2015 und 2017 untersucht.[28]
Ein weiteres Virusisolat (WIV04, NCBI GenBank-Nummer MN996528[25]) von SARS-CoV-2 aus der bronchoalveolären Spülflüssigkeit eines der ersten Patienten zeigt ebenfalls phylogenetisch größte Ähnlichkeit mit einem bei einer anderen Fledermausart (Java-Hufeisennase, wissenschaftlich Rhinolophus affinis, englisch intermediate horseshoe bat, verbreitet in Indonesien (Java), Indien, Vietnam, China)[29] in China isolierten Coronavirus BatCoV RaTG13, die Genomsequenzen stimmen zu 96,2 % überein.[30][24] Auch eine am 27. Januar 2020 publizierte genetische Analyse verwies auf Fledermäuse als mutmaßlicher Ursprungswirt des Virus.[31] Am 29. Januar 2020 wurde in der Fachzeitschrift The Lancet eine genetische Analyse von zehn Virusproben publiziert, die bei neun Erkrankten gewonnen worden waren. Demnach war die Genomsequenz aller zehn Proben zu 99,98 Prozent identisch, was darauf hinweist, dass die neu entdeckte Coronavirusvariante erst vor Kurzem auf den Menschen übergegangen ist.[32][33][34] Die Genomsequenz stimmt zu 88 bzw. 87 % Prozent mit den Genomsequenzen der bei Fledermäusen auftretenden bat-SL-CoVZC45 und bat-SL-CoVZXC21 überein. Die zehn Proben zeigen hingegen nur rund 79 Prozent Übereinstimmung in der Genomsequenz zu SARS-CoV und rund 50 Prozent zu MERS-CoV. Die Ergebnisse der phylogenetischen Untersuchungen werden auch als phylogenetischer Baum veranschaulicht.[28][32] Eine darauf basierende Darstellung ist im Artikel Betacoronavirus zu finden.
Der Aufbau des Genoms sowohl der SARS-CoV-2-Isolate wie auch der genannten Fledermaus-Coronaviren ist typisch für Viren der Lineage B (Untergattung Sarbecovirus, englisch SARS-like Betacoronavirus) der Gattung Betacoronavirus. Aufgrund der genetischen Distanzen zu SARS-CoV und zu MERS-CoV wurde SARS-CoV-2 zunächst als eine in Bezug auf den Menschen neue, ihn infizierende Betacoronavirus-Spezies angesehen.[28][32] Aufgrund der großen genetischen Übereinstimmung mit dem ursprünglichen SARS-Coronavirus hatte am 11. Februar 2020 die Coronavirus Study Group des ICTV jedoch vorgeschlagen, das neue Virus derselben Spezies Severe acute respiratory syndrome-related coronavirus zuzuordnen wie das bisherige.[1]
Das S-Protein (S für englisch spikes) ist für die Bindung an die Wirtszelle verantwortlich, funktionell wird es in die S1-Domäne und die S2-Domäne unterschieden. Die S1-Domäne vermittelt die Bindung an den Oberflächenrezeptor der Wirtszelle, die S2-Domäne vermittelt die Fusion der Zellmembran, durch Endozytose erfolgt dann der Eintritt des Virus in die Zelle. Das S-Gen von SARS-CoV-2 zeigt mit 75 % eine eher geringe Übereinstimmung in der Nukleotidsequenz mit den beiden Fledermausisolaten bat-SL-CoVZC45 und bat-SL-CoVZXC21 im Vergleich zur Genomanalyse. Insbesondere die Nukleotidsequenz, die für die S1-Domäne codiert, unterscheidet sich von diesen deutlich (68 % Übereinstimmung) und weist eine größere Ähnlichkeit mit der entsprechenden Nukleotidsequenz von SARS-CoV auf. Daraus lässt sich schließen, dass SARS-CoV und das neuartige Coronavirus den gleichen Zellrezeptor nutzen, das Angiotensin-konvertierende Enzym 2 (ACE2).[32] Dies konnte experimentell bewiesen werden, vergleiche Abschnitt Pathogenese.
Morphologie

Die in einer Zellkultur über mehrere Tage vermehrten Viren können nach Abtrennung durch Ultrazentrifugation für die Untersuchung im Transmissionselektronenmikroskop (TEM) vorbereitet werden, dabei wird eine Negativkontrastierung verwendet. Das TEM-Bild zeigt Virionen von kugelförmiger bis pleomorpher Gestalt mit einem Durchmesser von 60 bis 140 Nanometer (nm). Auf der Oberfläche sind 9 bis 12 nm lange Spikes zu erkennen. Die Morphologie entspricht der anderer bekannter Vertreter der Familie der Coronaviridae. Die Wirtszellen, die im lichtmikroskopischen Bild einen cytopathischen Effekt aufweisen, können nach Fixierung und anschließendem Ultradünnschnitt (Dicke von 80 nm) ebenfalls mit dem TEM untersucht werden. Hier zeigen sich neben Virionen auch Einschlusskörperchen, die mit Viren gefüllte membrangebundene Vesikel im Cytoplasma enthalten.[8]
Herkunft
Fachleute vermuteten bereits zu Beginn der Epidemie, dass als Hauptwirt ein anderes Säugetier oder Geflügel infrage komme. Der Übergang vom Tier auf den Menschen könne jedoch über einen noch nicht identifizierten Zwischenwirt erfolgt sein.[35]
Am 28. Februar 2020 gab die Regierung Hongkongs bekannt, erstmals einen Hund positiv auf das Virus getestet zu haben, der im Haushalt seiner infizierten Halter lebte.[36] Die WHO bestätigte, die SARS-CoV-2-Proben seien „schwach positiv“[37] getestet worden. Chinesische Forscher verwiesen in diesem Zusammenhang im Journal of Medical Virology auf Schlangen wie den Vielgebänderten Krait (Bungarus multicinctus) und die Chinesische Kobra (Naja atra),[38][39] die auf dem Großmarkt neben anderen lebenden Wildtieren (sogenannten „Ye Wei“) wie Fledermäusen oder Kaninchen angeboten werden.[40] Diese Hypothese wurde von anderen Virologen für unwahrscheinlich erklärt, da es bisher keine Evidenz dafür gäbe, dass Coronaviren auch Reptilien infizieren können. Bisher seien Coronaviren ausschließlich bei Säugetieren und Vögeln gefunden worden.[35] Nachdem in Malaiischen Schuppentieren (englisch Sunda pangolins) ein Coronavirus mit hoher genetischer Übereinstimmung zum SARS-CoV-2 gefunden wurde, geraten diese zunehmend in Verdacht, der Ursprung der neuen Epidemie zu sein, zumal diese trotz Verbots in China gehandelt werden.[22][24][41] Aufgrund der Ähnlichkeit der Bindungsstelle (englisch receptor binding domain, RBD) des Spike-Proteins an den menschlichen Rezeptor ACE2 gilt inzwischen (Stand 17. Februar 2020) die Java-Hufeisennase (Rhinolophus affinis), in der das Virus-Isolat BatCoV RaTG13 gefunden wurde, als noch aussichtsreicherer Kandidat für den Ursprung des Virus, auch wenn nicht klar ist, ob die Übertragung direkt erfolgte.[24]
Virulenz und Pathogenese
Risikogruppe
Für Beschäftigte, die durch ihre berufliche Tätigkeit mit Infektionserregern in Kontakt kommen können, gilt in Deutschland die Biostoffverordnung (BioStoffV). Der bei der Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA) eingerichtete Ausschuss für Biologische Arbeitsstoffe (ABAS) hat SARS-CoV-2 am 19. Februar 2020 vorläufig in die Risikogruppe 3 nach der BioStoffV eingeordnet (zweithöchste Stufe).[42] Grundsätzlich erfolgt die Einstufung in Risikogruppen in den Technischen Regeln für biologische Arbeitsstoffe (TRBA), die von der BAuA veröffentlicht werden, für Viren ist dies die TRBA 462: Einstufung von Viren in Risikogruppen. Beim Auftreten neuartiger, noch nicht zugeordneter Krankheitserreger erfolgt zunächst eine vorläufige Einstufung durch den ABAS. In der Begründung wird auf die Ähnlichkeit von SARS-CoV-2 mit dem SARS-CoV-1 hingewiesen, der die SARS-Epidemie 2002/2003 ausgelöst hat und auch die Ähnlichkeit in geringerem Umfang mit dem MERS-CoV wird erwähnt. Diese beiden Viren wurden ebenfalls der Risikogruppe 3 zugeordnet. Der ABAS nennt die „derzeit fehlenden Möglichkeiten zu Impfprävention und Therapie sowie die großen Verbreitungsmöglichkeit in der Bevölkerung“ als Begründung für die vorläufige Zuordnung zur Risikogruppe 3.[43]
Außerdem werden Empfehlungen zur Arbeit mit dem Virus bei der Diagnostik im Labor gegeben: Nicht gezielte Tätigkeiten (vergleiche § 5 BioStoffV) – ausgehend vom Untersuchungsmaterial, also beispielsweise die Probenvorbereitung, Probenaufbereitung und die Inaktivierung, um den Nachweis mittels RT-PCR (siehe Abschnitt Nachweismethoden) durchzuführen – können unter den Bedingungen der Schutzstufe 2 durchgeführt werden. Dabei sind alle Tätigkeiten, bei denen mit Aerosolbildung zu rechnen ist, in einer mikrobiologischen Sicherheitswerkbank der Klasse II durchzuführen. Außerdem ist die entsprechende persönliche Schutzausrüstung zu tragen. Gezielte Tätigkeiten nach § 5 BioStoffV dürfen nur in Laboratorien der Schutzstufe 3 durchgeführt werden, dies betrifft z. B. die Vermehrung des Virus in einer Zellkultur.[43] Die US-amerikanische Seuchenkontrollbehörde Centers for Disease Control and Prevention (CDC) hatte zuvor ähnliche Empfehlungen herausgegeben.[44]
Übertragungsweg
Am 20. Januar 2020 gab die chinesische Gesundheitskommission bekannt, dass eine Mensch-zu-Mensch-Übertragung möglich sei,[4][45] insbesondere wenn zwei Personen engen Kontakt zueinander haben (weniger als 1,8 m Abstand[46] bzw. weniger als 1 – 2 m Abstand[12]). Es wird angenommen, dass sich das Virus wie andere Erreger von Atemwegserkrankungen durch Tröpfcheninfektion verbreitet.[43][46][12] Das Virus wurde bisher im Sekret des Nasen- und Rachenraumes, im Sputum, dem Stuhl, der Tränenflüssigkeit und dem Blut nachgewiesen.[28][47][48] Chinesische Forscher schließen aufgrund von quantitativen Analysen von RT-PCR-Untersuchungen des Nasenrachenraums, dass das Virus wie Influenza auch durch Aerosole übertragbar ist.[49][42] Bei 17 untersuchten Patienten mit Krankheitssymptomen war die Viruslast in der Nase höher als im Rachen, das Auftreten gerade in den oberen Atemwegen unterscheidet SARS-CoV-2 damit von dem SARS-verursachenden Virus.[49]
Ob eine Übertragung auch durch das Berühren kontaminierter Oberflächen und Gegenstände stattfindet, ist unklar.[46] Eine Auswertung von 22 Studien, die sich mit der Persistenz von medizinisch relevanten Coronaviren (wie SARS-CoV und MERS-CoV) auf Oberflächen beschäftigen, zeigt, dass diese Viren bei Raumtemperatur bis zu neun Tage lang auf Oberflächen aus Metall, Glas oder Plastik überdauern können. Durchschnittlich bleiben sie vier bis fünf Tage infektiös. Allerdings werden sie durch geeignete Desinfektionsmittel inaktiviert (vergleiche Abschnitt Hygienemaßnahmen). Nach Aussage der beteiligten Wissenschaftler sollten diese Erkenntnisse auf SARS-CoV-2 übertragbar sein.[50][51]
In einer Studie mit neun Patientinnen, die im letzten Schwangerschaftsdrittel eine SARS-Cov2-Infektion erlitten hatten, zeigten sich nach der Geburt per Kaiserschnitt alle neun Kinder virusfrei. Daraus schlossen die Studienautoren, dass eine Übertragung des Virus im Mutterleib nicht stattfinde.[52] Die chinesischen Gesundheitsbehörden erfassten bis zum 6. Februar 2020 nur neun Säuglinge, bei denen ein positiver Virusnachweis erbracht wurde. Die Studienautoren zogen als mögliche Ursache dieser geringen Zahl eine mögliche hohe Zahl von Verläufen mit geringen Symptomen unter Kindern wie auch ein Defizit des Meldesystems in Betracht.[53]
Basisreproduktionszahl
Die Auswertung der Daten der ersten 425 Fälle in Wuhan ergab eine Basisreproduktionszahl von 2,2,[54] was bedeutet, dass jeder Infizierte im Durchschnitt 2,2 andere Personen angesteckt hatte. Eine Modellrechnung mit chinesischen und ausländischen Patientendaten vom 31. Dezember 2019 bis zum 28. Januar 2020 ergab einen Wert von 2,68.[55] Im Vergleich hierzu wurde für SARS eine Basisreproduktionsrate von 2,3 bis 2,6 berechnet.[56] Eine vergleichende Auswertung von 12 Studien, die bis zum 7. Februar 2020 veröffentlicht wurden, kommt zu dem Ergebnis, dass die Basisreproduktionszahl höher liegt, als bisher von der WHO angenommen, deren Schätzung bei 1,4 bis 2,5 liegt.[45] Die Wissenschaftler aus Schweden, China und Deutschland ermitteln, dass die Basisreproduktionszahl im Mittel bei 3,28, im Median bei 2,79 liegt und somit höher als der Wert bei SARS ist, den sie mit 2 bis 5 angeben.[57]
Anteil bestimmter Bevölkerungsgruppen
Eine Mitte Februar 2020 veröffentliche Auswertung der englischsprachigen und chinesischen Fachartikel kommt zu dem Ergebnis, dass alle Bevölkerungsgruppen infiziert werden können. Von den Infizierten waren 72 % 40 Jahre alt oder älter, 64 % waren männlich. 40 % der Patienten hatten chronische Erkrankungen wie Diabetes mellitus und Bluthochdruck.[45] Dies bestätigt der Bericht der von der WHO in China durchgeführten gemeinschaftlichen Mission (engl. WHO-China joint mission), der weiterhin noch Herz-Kreislauf-Erkrankungen, chronische Atemwegserkrankungen und Krebs nennt.[58]
Außerdem haben Personen über 60 Jahre ein höheres Risiko, einen schweren Krankheitsverlauf zu erleiden.[58] Die chinesische Seuchenschutzbehörde CCDC (Chinese Center for Disease Control and Prevention) hat alle bis zum 11. Februar 2020 vorliegenden Daten zu COVID-19-Krankheitsfällen in China ausgewertet und auch international publiziert. Bei den 44.672 bestätigten Fällen ergibt sich die folgende Altersgruppenverteilung: 3 % 80 Jahre und älter, 87 % 30–79 Jahre, 8 % 20–29 Jahre, 1 % 10–19 Jahre und 1 % jünger als 10 Jahre. Bei den infizierten Personen im Alter von 70 bis 79 Jahren und noch stärker bei den Personen, die 80 Jahre und älter sind, ist die Wahrscheinlichkeit, an COVID-19 zu versterben, höher als der Durchschnitt.[59]
Anteil schwerer Verläufe und Sterblichkeit
Die WHO gab mit ihrem Situation Report – 18 vom 7. Februar 2020 beispielsweise für China bei 31.211 bestätigt infizierten Personen 4.821 Patienten (15,4 %) mit schweren Krankheitsverläufen bekannt.[60] Genaue Angaben der Sterblichkeit sind im Moment jedoch nicht möglich. Aufgrund bisher noch unbekannter weniger symptomatischer Fälle kann die Letalität einerseits geringer ausfallen. Auf der anderen Seite können die Patienten, die noch nicht genesen sind, noch versterben und damit kann die Letalität höher ausfallen. Auch für den Anteil der schweren Verläufe gilt dies. Bei Diagnosestellung muss noch nicht bekannt sein, ob der Patient schwer erkrankt oder sogar stirbt. Im Folgenden werden einige Studien zitiert, die Hinweise auf die Letalität geben.
Eine von der WHO zitierte[61] Studie von Mike Famulare, Institute for Disease Modeling, schätzt die tatsächliche Sterblichkeitsrate für COVID-19-Infizierte, sprich die statistische Wahrscheinlichkeit, dass eine infizierte Person unabhängig von individuellen Merkmalen stirbt, als zwischen 0,4 und 2,6 % ein, wobei der wahrscheinlichste Wert mit 0,94 % angegeben wird.[62]
Bei einer epidemiologischen Betrachtung von 99 hospitalisierten Fällen waren bis zum 25. Januar 2020 11 % gestorben, 31 % entlassen und 58 % noch im Krankenhaus.[63] Diese Studie ist ein erster Hinweis darauf, dass die Letalität hospitalisierter Patienten bei ca. 11 % liegt.
In einer am 2. Februar 2020 vorab veröffentlichten Studie wurde die Letalität der bestätigten Fälle geschätzt. Hierbei wurde sowohl die Zeit zwischen dem Einsetzen der ersten Krankheitszeichen und der Diagnosestellung (5,1 Tage, 95 % KI: 3,5-7,5) als auch die Zeit zwischen dem Einsetzen der ersten Krankheitszeichen und dem Tod (15,2 Tage, 95 % KI: 13,1-17,7) berücksichtigt. Im 1. Szenario wurde die Epidemie auf Grundlage des Indexpatienten vom 8. Dezember 2019 kalkuliert und eine Letalität von 4,6 % (95 % KI: 3,1-6,6) berechnet. Im 2. Szenario wurde anhand der in andere Länder exportierten Fälle eine Epidemie simuliert und eine Letalität von 7,7 % (95 % KI: 4,9-11,3 %) ermittelt. Die Autoren weisen darauf hin, dass die tatsächliche Letalität durch nicht diagnostizierte Fälle entsprechend niedriger ausfallen könne.[64]
Eine Fallstudie aus einem Krankenhaus in Wuhan beschreibt 138 Patienten mit radiologisch und virologisch gesicherter Pneumonie durch SARS-CoV-2 vom 1. Januar bis zum 2. Februar 2020. Rund ein Viertel dieser Patienten musste intensivmedizinisch behandelt werden. Der häufigste Grund für die Intensivtherapie war ein akutes Atemnotsyndrom, welches in rund der Hälfte der Fälle eine invasive Beatmung notwendig machte. Die Intensivpatienten waren mit im Median 66 Jahren signifikant älter als der Rest der Patienten mit im Median 51 Jahren. Zum Studienendpunkt waren rund 65 % der Patienten noch im Krankenhaus. Unter den Patienten befanden sich 40 Krankenhausmitarbeiter, die sich bei der Arbeit angesteckt hatten, sowie 17 Patienten des Krankenhauses, die in der Einrichtung angesteckt wurden. Die Mehrheit der Patienten erhielt Oseltamivir und Antibiotika. 4,3 % der Patienten verstarben bis zum Studienendpunkt. Rund die Hälfte erhielt Kortikosteroide. Die Studienautoren beschrieben diese antivirale Therapie aus ihrer Beobachtung als nicht effektiv.[65]
Die von der WHO in China durchgeführte gemeinschaftliche Mission (engl. WHO-China joint mission) hat dazu Daten aus Wuhan und anderen Regionen ermittelt und kommt am 24. Februar 2020 zu dem Schluss, dass in Wuhan 2 – 4 % der Infizierten verstarben, in den anderen chinesischen Regionen 0,7 %.[66]
Inkubationszeit
Die Inkubationszeit kann laut Informationen des Robert Koch-Instituts (RKI) bis zu 14 Tage betragen.[12] Darüber hinaus gibt es Berichte chinesischer Forscher, welche die mögliche Inkubationszeit auf bis zu 24 Tage ausdehnen.[67] Eine Analyse der ersten 425 in Wuhan gemeldeten Fälle ergibt eine Inkubationszeit von im Mittel 5,2 Tagen und ein Durchschnittsalter von 59 Jahren. Die Autoren gehen davon aus, dass bereits Mitte Dezember 2019 im Umfeld des Fischmarktes Übertragungen von Mensch zu Mensch stattfanden.[54] Eine statistische Auswertung mehrerer Berichte von Infektionen in einem Haushalt oder in anderer enger räumlicher Begrenzung (sogenannte Cluster) ergibt eine Inkubationszeit von im Median 5 – 6 Tagen.[68]
Eine Ansteckung anderer Menschen während der Inkubationszeit ist trotz beschwerdefreien Gesundheitszustands möglich. Tests auf die Viruslast im Blut bei einzelnen Patienten legen den Verdacht nahe, dass manche Patienten auch während der Ausheilung bei klinischer Besserung weiterhin vorübergehend infektiös sein können.[69] Der Bericht dieser Publikation, welcher auf der Annahme einer asymptomatischen chinesischen Indexpatientin beruhen, wurde durch die Recherche der Fachzeitschrift Science widerlegt und vom RKI in Zweifel gezogen.[70] In einer Gruppe von 126 aus Wuhan nach Deutschland Evakuierten zeigten sich zwei Patienten in der RT-PCR des Rachenabstrichs positiv, welche keine oder nur sehr unspezifische Beschwerden aufwiesen.[71] Ebenso ist ein Fall eines subjektiv asymptomatischen zehnjährigen Jungen in Shenzhen beschrieben, dessen Blutbild und Entzündungszeichen im Labor unauffällig waren. In der weiteren Untersuchung zeigten sich jedoch radiologische Befunde vereinbar mit einer Pneumonie, und im Rachenabstrich ließ sich Virus-RNA nachweisen.[28]
Darüber hinaus existiert ein weiterer Fallbericht aus Guangzhou von zwei asymptomatisch Infizierten mit Virusnachweis im Nasenrachenraum. Die Autoren wiesen explizit auf die Verbreitungsgefahr des Virus durch beschwerdefreie Patienten in frühen Infektionsstadien hin.[72] Messungen der Viruslast im Sekret des Nasenrachenraums ergeben eine ähnlich hohe Viruslast zwischen beschwerdefreien und symptomatisch kranken Patienten.[49] Aufgrund von quantitativen Virusuntersuchungen im Sekret des Nasenrachenraums bei Patienten mit sehr leichten Symptomen schlossen die Forscher der Virologie der Charité und des Instituts für Mikrobiologie der Bundeswehr, dass auch bereits bei sehr milden Erkrankungssymptomen eine hohe Infektionsfähigkeit besteht.[73][22] Auch das Robert Koch-Institut berichtet über einzelne Fälle, bei denen sich Betroffene möglicherweise bei infizierten Personen angesteckt haben, die noch keine oder keine spezifischen Symptome gezeigt hatten.[12] Zum gleichen Ergebnis kommt eine chinesische Fallstudie, die sechs Patienten einer Familie betrachtet. Patientin 1 hat ihre fünf Verwandten mit SARS-CoV-2 angesteckt, ohne selbst Symptome zu zeigen. Wegen der Krankheitsfälle in der Familie wurde auch sie isoliert und ärztlich überwacht. Der Virusnachweis durch RT-PCR bei ihr war nach 17 Tagen negativ, nach 19 Tagen positiv und nach 25 bzw. 30 Tagen wieder negativ.[67] Es sind mehrere Patienten nachgewiesen, die nach klinischer Ausheilung und negativer PCR-Testung erneut eine nachweisbare Viruslast entwickelten. Ob es sich um eine Wiederinfektion oder eine Reaktivierung des Virus handelt ist unklar.[74][75]
Pathogenese
Das Virus dringt wie bei SARS über den ACE2-Rezeptor in die menschliche Zelle ein.[30] Im Versuch mit HeLa-Zellen, die ACE2 des Menschen, der Chinesischen Hufeisennase (Rhinolophus sinicus), einer Schleichkatzenart (engl. civet), des Hausschweins und der Maus exprimieren, konnte SARS-CoV-2 das jeweilige ACE2-Protein als Rezeptor nutzen, um in die Zelle einzudringen, nur bei dem Maus-ACE2 gelang dies nicht, ebenso wenig bei HeLa-Zellen, die kein ACE2 bildeten. An Rezeptoren, die von anderen Coronaviren genutzt werden, findet keine Bindung von SARS-CoV-2 statt.[30]
In einem Informationsblatt des deutschen Außenministeriums wird erwähnt, dass aus China Berichte „von Infektionsketten über die 4. Generationen hinaus“ vorliegen.[76]
Klinische Erscheinungen
Klinische und laborchemische Krankheitszeichen

Da dieser Virustyp erst im Januar 2020 nachgewiesen wurde, ändern sich die Erkenntnisse über die Krankheit möglicherweise noch. Eine Abgrenzung zu anderen Viruserkrankungen wie Influenza ist schwierig. Nach einer Inkubationszeit von bis zu 14 Tagen[12] können Fieber, Muskelschmerzen und trockener Husten auftreten. Häufig manifestiert sich die Krankheit auch mit allgemeinem, schwerem Krankheitsgefühl und auch Rückenschmerzen.[28] Symptome der oberen Atemwege, wie Husten, Schnupfen, Halskratzen, sind möglich, einige Betroffene leiden auch an Durchfall.[12] Im weiteren Verlauf kann sich eine schwere Atemnot aufgrund einer Infektion der unteren Atemwege bis zur Lungenentzündung entwickeln.[77] Diese kann mit Brustschmerzen im Sinne einer Pleuritis einhergehen. Die Mehrheit der Patienten zeigte die für schwere Virusinfekte typische Kombination aus einer Verminderung der Anzahl der gesamten weißen Blutzellen, einer Verminderung der Lymphozyten-Anzahl und einer Erhöhung laborchemischer Entzündungsparameter (wie CRP und BSG). Bildgebend zeigten sich in der Computertomographie der Lunge beidseitige, milchglasartige Verschattungen als Zeichen einer Bronchopneumonie.[77]
Die Mehrheit der Krankenhauseinweisungen der ersten Patienten erfolgte nach rund einwöchiger symptomatischer Krankheit aufgrund einer Verschlechterung des Zustandes. In den Fällen, in denen eine intensivmedizinische Behandlung notwendig wurde, ergab sich deren Notwendigkeit nach rund zehn Tagen nach Symptombeginn.[77] In einer epidemiologischen Studie von 99 hospitalisierten Fällen fanden bei 13 Patienten eine nicht-invasive Beatmung, bei vier Patienten eine invasive Beatmung, bei neun Patienten eine Dialyse aufgrund eines Nierenversagens und bei drei Patienten eine extrakorporale Lungenunterstützung (ECMO) Anwendung.[63] Im Bericht der chinesischen Seuchenschutzbehörde CCDC erfolgt die Klassifizierung als leichter Krankheitsverlauf, wenn keine oder nur eine leichte Lungenentzündung vorliegt, für einen schweren Krankheitsverlauf sind Pneumonie (Lungenentzündung), Dyspnoe (Atemnot), eine Atemfrequenz von ≥ 30 Atemzüge pro Minute, eine Sauerstoffsättigung des Blutes ≤ 93 % und weitere klinische Anzeichen typisch, bei einem kritischen Krankheitsverlauf ist mit Atemversagen, septischem Schock und/oder Multiorganversagen zu rechnen.[59]
Ein wesentlicher Unterschied zum SARS-Coronavirus ist der, dass Patienten schon einige Tage vor Einsetzen der Krankheitssymptome infektiös sein können (beim SARS-Coronavirus waren die Patienten hingegen erst nach Auftreten der Symptome infektiös). Die Infektion lässt sich daher schwerer erkennen und schwieriger eindämmen. Bei Quarantänemaßnahmen reicht es deswegen nicht aus, nur die klinisch auffälligen Personen zu isolieren.[34]
Krankheitsverlauf bzw. Dauer der Erkrankung
Die Auswertung von 44.415 Fällen durch die CCDC zeigt bei 81 % der bestätigten Fälle einen leichten, bei 14 % einen schweren und bei 5 % einen kritischen Krankheitsverlauf.[59] Bei einem leichten Krankheitsverlauf (dem häufigsten Fall) klingen die Krankheitszeichen, sofern überhaupt welche bestehen, laut WHO in der Regel innerhalb von zwei Wochen ab.[66] Bei Menschen mit einem schweren Krankheitsverlauf dauere es zwischen drei und sechs Wochen, bis sie sich von der Krankheit erholen.[66]
Nachweismethoden
Vorgehensweise bei der Diagnostik
Das Virus ist mittels RT-PCR (Reverse-Transkriptase-Polymerase-Kettenreaktion) im Sputum, im Trachealsekret, in der bronchoalveolären Spülflüssigkeit und im Nasenrachen-Abstrich direkt nachzuweisen. Die Laboruntersuchung führt in Deutschland das Konsiliarlabor für Coronaviren an der Charité in Berlin durch, mittlerweile sind mehr als 20 Labore in Deutschland dazu in der Lage.[78] Diese Untersuchung wird durch das Robert Koch-Institut (RKI) nach zwei Kriterien empfohlen (die Falldefinitionen wurden am 14. Februar 2020 geändert, auf der Website des RKI ist ein Flussschema zur Verdachtsabklärung zu finden):[79]
- für Personen mit unspezifischen Allgemeinsymptomen oder akuten respiratorischen Symptomen jeder Schwere und Kontakt zu einem bestätigtem COVID-19-Fall bis maximal 14 Tage vor Erkrankungsbeginn
und / oder - für Personen mit akuten respiratorischen Symptomen jeder Schwere mit oder ohne Fieber und Aufenthalt in Risikogebieten bis maximal 14 Tage vor Erkrankungsbeginn (die Risikogebiete werden auf der RKI-Website genannt und aktualisiert, vergleiche Abschnitt Weblinks)
Diese Personengruppen werden vom RKI als begründeter Verdachtsfall eingestuft.[79] Vor dem 14. Februar beinhaltete die Falldefinition Personen mit Verdacht auf Pneumonie und Aufenthalt im Risikogebiet bzw. Kontaktpersonen.[80]
Das RKI weist darauf hin, dass Ärzte SARS-CoV-2 bzw. COVID-19 in ihre Differentialdiagnose einbeziehen sollen, wenn sich der Patient zuvor in Regionen mit einzelnen Infektions-Clustern (diese gelten nicht als Risikogebiete) aufgehalten hat oder Kontakt zu bisher unbestätigten COVID-19-Fällen bestand (beide Kriterien bis maximal 14 Tage vor Erkrankungsbeginn) oder wenn er Symptome einer durch Viren verursachten Pneumonie unklarer Ursache zeigt. In diesen Fällen sollte beim Auftreten von Atemwegsinfektionen eine ambulante Diagnostik erfolgen und der Patient bis zum Vorliegen der Testergebnisse als Kontaktperson eingestuft werden, vergleiche Abschnitt Management von Kontaktpersonen.[79][81] (Stand: 1. März 2020)
Bis zur Entwicklung eines indirekten Nachweises (Antikörpernachweis)[34][82] soll das Blutserum betroffener Personen aufbewahrt werden.[79] (Stand: 1. März 2020)
Der begründete Verdachtsfall wird dem zuständigen Gesundheitsamt gemeldet und zusammen mit diesem entschieden, ob eine ambulante oder eine stationäre Versorgung möglich ist, je nach Schwere der Erkrankung. Bei einer stationären Einweisung wird der RT-PCR-Test durchgeführt. Bei positivem Befund wird das zuständige Gesundheitsamt informiert, dass nun ein laborbestätigter COVID-19-Fall vorliegt, und stationär wird mit der Therapie begonnen.[79] Ist der Befund zwar negativ, besteht aber ein anhaltend hoher Verdacht auf eine Infektion mit dem neuartigen Coronavirus, empfiehlt das Robert Koch-Institut, die Diagnostik zu wiederholen. Bei erneut negativem Befund gilt die COVID-19-Infektion als ausgeschlossen. Lässt sich die Diagnostik von vornherein nicht durchführen, muss erneut mit dem Konsiliarlaboratorium Rücksprache gehalten werden.[83] Auch bei einem zunächst ambulant versorgten begründeten Verdachtsfall erfolgt die ambulante Diagnostik, bei positivem Ergebnis liegt hier ebenfalls ein laborbestätigter COVID-19-Fall vor, der dem Gesundheitsamt zu melden ist.[79]
Radiologen aus Changsha berichteten aus einer Fallserie von 167 Patienten über fünf Patienten, bei denen zum Zeitpunkt einer durch Computertomographie gesicherten Lungenentzündung die RT-PCR für das Virus negativ ausfiel und der Virusnachweis erst nach mehrmaligen Tests im Verlauf der Erkrankung gelang.[84]
RT-PCR
Die Nachweismethode der Charité ist die real-time quantitative Reverse-Transkriptase-Polymerase-Kettenreaktion (abgekürzt als qRT-PCR oder RT-qPCR). Sie basiert auf der Detektion von zwei Nukleotidsequenzen, bezeichnet als E Gen und RdRp Gen. Das erste Gen codiert für die Virushülle (E für engl. envelope ‚Hülle‘), das zweite Gen für die RNA-abhängige RNA-Polymerase (RdRP für engl. RNA-dependent RNA polymerase). Für das Primerdesign wurden das SARS-assoziierte Coronavirus und weitere, bei Fledermausarten vorkommende SARS-assoziierte Coronaviren (SARS-CoV) verwendet. Die erste Version des real-time RT-PCR-Assays ist erstellt worden, bevor die Genomsequenz von SARS-CoV-2 veröffentlicht wurde. Nach deren Veröffentlichung wurden die Primer ausgewählt, die auch für den Nachweis von SARS-CoV-2 geeignet sind. Das erste Assay (E Gen) dient als Screening, da es mehrere Virusspezies der Untergattung Sarbecovirus (aus der Gattung Betacoronavirus) nachweist. Verläuft diese Untersuchung positiv, so ist ein Bestätigungs-Assay (RdRp Gen) durchzuführen. Falls auch hier ein positives Ergebnis erhalten wird, schließt sich als drittes ein Charakterisierungs-Assay an (ebenfalls RdRp Gen). Die letzten beiden Assays verwenden eine Gensonde, die für SARS-CoV-2 spezifisch ist, beim zweiten Assay ist zusätzlich eine Sonde enthalten, die zur Nukleotidsequenz sowohl des RNA-Teilstücks des SARS-CoV als auch des SARS-CoV-2 passt.[16][85]
Die molekularbiologische Nachweismethode, die im Konsiliarlabor an der Charité verwendet wird, wurde schnell und effektiv entwickelt, eine erste Version war bereits am 13. Januar 2020 verfügbar. Dazu haben chinesische Wissenschaftler bereitwillig unveröffentlichte Befunde beigetragen. Von internationalen Forschungsnetzen kamen grundlegende Daten, und die globale Sektion des Europäischen Virus-Archivs (European Virus Archive – Global, EVAg) lieferte notwendige Produkte (SARS-CoV RNA und RNA-Transkripte) für die Assays.[85] Auch weitere Gruppen von Wissenschaftlern haben ihre entwickelten Methoden veröffentlicht. Dabei handelt es sich um PCR-Protokolle oder Auflistungen geeigneter Primer und deren für die RT-PCR verwendete Stoffmengenkonzentration, beispielsweise von den Centers for Disease Control and Prevention (CDC) in den USA, den CDC in China oder der Universität Hongkong. Sie unterscheiden sich darin, welche Gene der Virus-RNA nachgewiesen werden.[86] Für die Durchführung der qRT-PCR werden 90 Minuten bis drei Stunden benötigt.[87] Anstelle der real-time quantitative-Variante können die Produkte der Reverse-Transkriptase-PCR auch mittels Agarose-Gelelektrophorese nachgewiesen werden.[28]
Weitere Methoden
Genomanalyse
Laboratorien mit Ausstattung für eine Genomanalyse (DNA-Sequenzierung des Genoms) können SARS-CoV-2 auch auf diese Weise identifizieren.[88] Vollständige Genomanalysen von SARS-CoV-2-Isolaten zum Vergleich sind beispielsweise in der Gendatenbank des National Center for Biotechnology Information (NCBI) oder über die GISAID Plattform[89] verfügbar (vergleiche Abschnitt Molekulargenetik).
Nukleinsäurenachweise

Nach Aussage der Weltgesundheitsorganisation (WHO) ist ein vereinfachtes molekularbiologisches Verfahren, die Nucleic Acid Amplification Technology (NAAT) in der Entwicklung, die Assays dafür werden momentan validiert (Stand: 17. Januar 2020). Die NAAT-Methode beruht ebenfalls auf der RT-PCR, das fertig zusammengestellte Assay bietet jedoch den Vorteil, einfacher in der Handhabung zu sein und ließe sich von entsprechend ausgestatteten Routine-Laboratorien verwenden.[88]
Am 5. Februar 2020 gab die US-amerikanische Behörde CDC bekannt, ein derartiges Assay (test kit) für die Anwendung in akkreditierten Diagnoselaboratorien zur Verfügung zu stellen. Das Assay wird als Centers for Disease Control and Prevention (CDC) 2019-Novel Coronavirus (2019-nCoV) Real-Time Reverse Transcriptase (RT)-PCR Diagnostic Panel bezeichnet und ist für den Nachweis sowohl des neuartigen Coronavirus wie auch SARS-ähnlicher Coronaviren in Proben der oberen und unteren Atemwege von Patienten vorgesehen. Zuvor erfolgte eine beschleunigte Zulassung durch die Gesundheitsbehörde Food and Drug Administration (FDA), somit darf das Assay auch außerhalb von Forschungseinrichtungen verwendet werden.[90] Ein Testkit ermöglicht die Untersuchung von 700 – 800 Proben, 100 dieser Packungen gehen an US-amerikanische Labore, weitere 100 an internationale Laboratorien, die beispielsweise im Auftrag der WHO Untersuchungen durchführen.[91] Die Untersuchung dauert von der Probevorbereitung bis zum Vorliegen der Ergebnisse etwa vier Stunden.[87]
Schnelltests
Ende Januar 2020 hatte Xinhua, die Nachrichtenagentur der Regierung der Volksrepublik China gemeldet, dass die chinesische Behörde National Medical Products Administration (NMPA) am 26. Januar vier Testkits eines neuen Testverfahrens zugelassen habe. Das Assay ist von dem Biotechnologieunternehmen Sansure Biotech aus Changsha entwickelt worden. Mit Hilfe der dafür geeigneten Laborautomatisierung sollen Testergebnisse bereits nach 30 Minuten vorliegen.[87][92] Die staatliche Nachrichtenagentur teilte weiterhin mit, dass eine in Wuxi in der östlichen Provinz Jiangsu ansässige Firma in Zusammenarbeit mit dem National Institute for Viral Disease Control and Prevention eine Schnellmethode entwickelt habe. Mit dem Testkit soll das Virus innerhalb von 8 – 15 Minuten nachgewiesen werden, die Firma könne täglich so viele Testkits produzieren, dass damit die Untersuchung von 4.000 Proben möglich sei und das Verfahren soll bereits in der Provinz Hubei eingesetzt worden sein.[93] Die Xinhua-Meldungen enthalten keinen Hinweis auf die dabei verwendeten molekularbiologischen Methoden. Weiterhin wird an der chinesischen Tianjin-Universität in Zusammenarbeit mit einer Pekinger Biotechnologiefirma ein Schnellverfahren entwickelt, bei dem nach 15 Minuten Resultate vorliegen sollen. Es befindet sich im Probeeinsatz (Stand Februar 2020).[87]
Forscher der Hong Kong University of Science and Technology meldeten Anfang Februar 2020 die Entwicklung eines tragbaren Gerätes, mit dem das neuartige Coronavirus innerhalb von 40 Minuten nachweisbar sein soll. Für das im Vergleich zur herkömmlichen qRT-PCR schnellere Verfahren werden modifizierte Chip-Thermocycler verwendet.[87] Auch Forscher des Institute for Health Innovation & Technology (iHealthtech) an der National University of Singapore berichteten im Februar 2020 darüber, eine Schnellmethode zu entwickeln. Sie basiert auf der seit 2018 verwendeten enVision-Technologie, mit der Nukleinsäuren innerhalb von 30 bis 60 Minuten nachgewiesen werden. Es wird geschätzt, dass bis zur Marktreife des neuen Testverfahrens noch mehrere Monate benötigt werden.[94]
Das Biotechnologieunternehmen Qiagen N.V. entwickelte am Standort in Hilden ebenfalls einen Schnelltest, der auf einem bereits international für die Diagnostik von Krankheitserregern zugelassenen Verfahren basiert, mit dem sich u. a. SARS-assoziierte Viren und EHEC nachweisen lassen.[95] Das Verfahren wurde um den Nachweis der im SARS-CoV-2-Genom vorhandenen Gene ORF1b und E erweitert und die Ergebnisse wurden mit denen der RT-PCR-Methode verglichen.[96] Das Unternehmen arbeitet mit der WHO zusammen, um eine Validierung zu erreichen.[95] Das tragbare Diagnosegerät ist für den Einsatz in Arztpraxen oder an Flughäfen geeignet. Als Probenmaterial ist ein Abstrich aus dem Rachenraum oder eine Blutprobe geeignet,[95] Testergebnisse liegen innerhalb von 60 Minuten vor.[96] In Deutschland ist die vorläufige Zulassung durch das Bundesinstitut für Arzneimittel und Medizinprodukte beantragt.[97] Die Diagnosegeräte werden zur Zeit in französischen und chinesischen Krankenhäusern getestet (Stand Februar 2020).[96] Zwei weitere Diagnostik-Firmen in Deutschland entwickeln ebenfalls Schnelltests.[97]
Antikörpernachweis
Auch der Antikörpernachweis als serologische Untersuchung wird nach Angabe der WHO derzeit entwickelt (Stand: 17. Januar 2020). Dadurch wird es ein Assay (beispielsweise ein Immunassay wie ELISA) geben, mit dem Antikörper aus Patienproben (Blutserum) durch Antigen-Antikörper-Reaktion nachweisbar sind. Die WHO und das Robert Koch-Institut (RKI) in Deutschland rufen dazu auf, Serumproben von bestätigten oder Verdachtsfällen in der Akutphase zu sammeln und zu asservieren.[80] Die WHO empfiehlt, die erste Probe in der ersten Krankheitswoche und die zweite Probe drei bis vier Wochen später zu nehmen. Damit lässt sich eine Serokonversion überprüfen.[88][98]
In einem chinesischen Forschungslabor wurden im Januar 2020 erste ELISA-Tests durchgeführt, als Antigen wurde das Nukleokapsidprotein (N) eines Fledermaus-Coronavirus mit Ähnlichkeit zu SARS-CoV-2 verwendet. Damit ließen sich in Serumproben eines Patienten die Antikörper Immunglobulin G (IgG) und Immunglobulin M (IgM) nachweisen und deren Titer über mehrere Tage während des Krankheitsverlaufes bestimmen. In einem zweiten Test wurden Serumproben, die 20 Tage nach den ersten Symptomen entnommen wurden, untersucht. Alle Patientenseren, aber nicht die Seren von Gesunden zeigten eine stark positive IgG-Reaktion, einige Patientenseren zeigten zusätzlich eine IgM-Reaktion, was auf eine aktuelle Immunantwort, also eine momentane Infektion hindeutet.[30]
Zellkultur
Die Vermehrung des Virus zu Forschungszwecken in einer Zellkultur ist unter anderem in China, Australien, Frankreich, Deutschland und den USA gelungen.[8][82][99][100][101] Die chinesischen Wissenschaftler verwenden hierbei Epithelzellen des menschlichen Atemtrakts, die das mehrschichtige mukoziliäre Epithelgewebe (Flimmerepithel) simulieren, ebenso werden die Zelllinien Vero E6 und Huh-7 eingesetzt.[8][30]
Behandlung
Derzeit steht keine spezifische Behandlung zur Verfügung, allenfalls können Symptome gelindert werden; möglicherweise sind aber einige bereits existierende Virostatika, die zum Beispiel gegen MERS-CoV und HIV eingesetzt werden, auch bei einer Infektion mit SARS-CoV-2 wirksam.[102][103][104] Dazu gehören Proteasehemmer wie Indinavir, Saquinavir, Remdesivir, Lopinavir/Ritonavir und Interferon-beta.[105][106] Die Nationale Gesundheitskommission der VR China empfiehlt eine Kombination der HIV-Proteaseinhibitoren Lopinavir und Ritonavir mit inhalativ verabreichtem Interferon Alpha. In den Vereinigten Staaten wurde das Nukleotidanalogon Remdesivir, das eigentlich gegen Ebolafieber entwickelt wurde, eingesetzt. Ein Wirkungsnachweis steht noch aus.[107]
Neben Remdesivir sind in China zur Zeit noch Favipiravir und Chloroquin, ein Wirkstoff gegen Malaria, in der Erprobung am Menschen.[108] Die klinischen Studien für Remdesivir finden in China und weiteren Staaten statt, Favipiravir – ein Wirkstoff, der gegen das Influenzavirus verwendet wird – wird an 70 Patienten in Shenzhen erprobt und hat am 16. Februar 2020 kurzfristig als wirksames Virustatikum für fünf Jahre unter dem Namen Favilavir die Zulassung erhalten und wird ab sofort produziert.[109] Chloroquin wurde in Krankenhäusern in Peking und der Provinz Guangdong an mehr als 100 Patienten getestet und steht mit Umifenovir (Handelsname Arbidol) – ein in Russland und China zugelassener Influenza-Wirkstoff – auf der empfohlenen Medikationsliste (Stand 20. Februar 2020).[110] Chloroquin hat sich in einer klinischen Studie in China als wirksam erwiesen (Stand 27. Februar 2020).[111] Erste Ergebnisse der Studie wurden in der Fachzeitschrift BioScienceTrends veröffentlicht, danach ist die Behandlung mit Chloroquin „wirksamer“ als die Behandlung mit Placebos.[112] Das chloroquinhaltige Prophylaxepräparat Resochin wurde von der Herstellerfirma Bayer im Juli 2019 vom Markt genommen, weil der Wirkstoff nicht mehr in der erforderlichen Qualität geliefert wurde.[113]
Aktuell rufen die Kliniken bereits genesene Patienten zu Blutspenden auf, um mit daraus gewonnenem antikörperreichem Plasma Akutfälle zu therapieren und wertvolle Erkenntnisse zur Entwicklung eines Impfstoffes zu erhalten.[114][115]
In einem Diagnose- und Behandlungsschema für Triagezentren aus Wuhan kommt bei Verdachtspatienten das Virostatikum Umifenovir und eine antibiotische Behandlung mit Linezolid, Nemonoxacin oder Fluorchinolonen zum Einsatz. Die antibiotische Behandlung wird mit einer zu erwartenden bakteriellen Zweitinfektion des durch den Virusinfekt geschädigten Lungengewebes begründet. Die Autoren betonen den Stellenwert des Therapiebeginns vor Eintreffen des RT-PCR-Tests aufgrund klinischer, laborchemischer und apparativer Untersuchungsbefunde. Patienten ohne Nachweis einer Verminderung der Lymphozytenzahl im Blut, ohne virale Pneumonie, ohne Dyspnoe (Atemnot) und ohne Reduktion der Sauerstoffsättigung unter <93 % sollten ohne RT-PCR-Testung in die Heimversorgung entlassen werden. Für diese Patienten ist die orale Gabe von Azithromycin oder Amoxicillin vorgesehen. Patienten mit Pneumonien anderer Genese sollen regulär und nach Möglichkeit ambulant behandelt werden. Schwangere Frauen und Menschen über 65 Jahre sollen als besondere Risikogruppen eher stationär behandelt werden. Die Studienautoren begründen ihr Vorgehen mit der Überforderung des Gesundheitswesens in Wuhan. Die Behandlung möglichst vieler Patienten zu Hause berge Risiken, sei aber notwendig, um die vielen kritischen Fälle zu versorgen.[116]
Vorbeugung
Entwicklung von Impfstoffen
Bereits unmittelbar nach Veröffentlichung der RNA-Sequenz des Virus wurde in mehreren Laboren damit begonnen, einen Impfstoff gegen das Virus zu entwickeln.[117] Die internationale Impfstoffinitiative CEPI (Coalition for Epidemic Preparedness Innovations) plante, bis Mitte Juni 2020 erste Tests mit bis dahin entwickelten Impfstoffen durchzuführen. Dafür erhielten mehrere potentiell geeignete Unternehmen finanzielle Unterstützungen.[22] In Deutschland betraf dies u. a. die Tübinger Biotechnologiefirma CureVac, die an der schnellen Impfstoffentwicklung arbeitete.[118] Das Robert Koch-Institut verwies darauf, dass derzeit klinische Studien mit Impfstoffen gegen MERS-CoV laufen würden.[12] Allerdings sind klinische Studien lediglich der erste Schritt, es würde bei erfolgreichem Studienverlauf voraussichtlich frühestens in mehreren Monaten ein Impfstoff zur Verfügung stehen, der allerdings in einer ersten Phase sicher nicht für die gesamte Bevölkerung bereitgestellt werden könnte.[119]
Hygienemaßnahmen
Allgemeinbevölkerung
Das Robert Koch-Institut hat am 28. Januar 2020 Hinweise für die Allgemeinbevölkerung gegeben, wie man das Risiko für eine Ansteckung wesentlich verringern kann, sie sind nicht spezifisch für COVID-19, sondern gelten auch für Influenza und andere Atemwegsinfektionen. Hierbei wird in erster Linie auf folgende Punkte hingewiesen:
- auf eine gute Händehygiene achten: u. a. Hände mit Seife waschen: vor dem Essen, vor und nach Kontakt zu anderen Menschen, nach dem Toilettengang, nach Niesen/Husten;
- einen Mindestabstand von ein bis zwei Metern zu krankheitsverdächtigen Personen halten;
- korrekte Hustenetikette: möglichst in die Armbeuge husten oder niesen, nicht in die Hand;
- den Kontakt und damit eine potentielle Infektion zu (Hoch-)Risiko-Gruppen, vornehmlich älteren Personen (> 60 Jahre), die meist multimorbid sind, zu deren Schutz zu verringern oder ganz zu vermeiden.[120]
Atemschutzmasken werden hingegen in erster Linie für Kranke selbst oder für Pflegende empfohlen, die engen Kontakt mit Erkrankten haben. Ob das Tragen eines Mund-Nasen-Schutzes in der Öffentlichkeit das Risiko, sich selbst anzustecken, wesentlich reduziert, ist nicht wissenschaftlich belegt.[12]
Das Sciencemediacentre Germany – ein disziplinübergreifender Fachinformationsdienst – hat eine darüberhinausgehende umfangreiche Verhaltens- und Vorsorgeplanung für die Bevölkerung zusammengestellt, damit für einen pandemieartigen Ereignisfall individuelle Vorkehrungen geplant und getroffen werden können (Stand: 24. Februar 2020).
Medizinisches Personal

Das Robert Koch-Institut hat am 24. Januar 2020 erste Hinweise gegeben, welche Hygienemaßnahmen zur Vermeidung einer Übertragung des Erregers durch Tröpfchen auf medizinisches Personal notwendig sind. Mit Änderung der Falldefinitionen am 14. Februar 2020 wurden auch die Hygienemaßnahmen präzisiert: Es sind Schutzkittel und langärmelige, wasserdichte Einwegschürze, Schutzhandschuhe, Schutzbrille und Atemschutzmaske (mindestens vom Standard FFP2) zu tragen. Diese Angaben gelten auch bei der stationären Versorgung.[79][121] Der Patient muss einen Mund-Nasen-Schutz tragen und wird bei der Verdachtsabklärung in der Arztpraxis sofort in einen separaten Raum geführt und dort untersucht.[79] Zu den empfohlenen Hygienemaßnahmen gehört die konsequente Einhaltung der Basishygiene, besonders der Händehygiene.[121]
Zur chemischen Desinfektion der Hände und Flächen sind Desinfektionsmittel geeignet, die die Wirkungsbereiche „begrenzt viruzid“, „begrenzt viruzid PLUS“ oder „viruzid“ abdecken.[121][122] Eine Auswertung von 22 Studien, die sich mit der Persistenz und Inaktivierung von medizinisch relevanten Coronaviren (wie SARS-CoV und MERS-CoV) unter anderem in Gesundheitseinrichtungen beschäftigen, zeigt, dass für die Oberflächendesinfektion Mittel auf der Basis von Ethanol, Wasserstoffperoxid oder Natriumhypochlorit in entsprechender Konzentration wirksam sind.[50] Neben den Hygienemaßnahmen durch das medizinische Personal zählen außerdem die Unterbringung des Patienten in einem Isolierzimmer mit Vorraum oder Schleuse[79] und das Abstellen eventuell vorhandener raumlufttechnischer Anlagen, über die ein Luftaustausch mit anderen Räumen möglich ist, zu den Präventionsmaßnahmen.[121]
Management von Kontaktpersonen durch öffentliche Behörden
Die Nachverfolgung von Kontaktpersonen erfolgt im Rahmen des Infektionsschutzes im Einklang mit der Einschätzung der Situation des Geschehens durch das lokal zuständige Gesundheitsamt. Das Robert Koch-Institut unterscheidet zwischen Kontaktpersonen mit höherem Infektionsrisiko (Kategorie I), Kontaktpersonen mit geringerem Infektionsrisiko (Kategorie II) und Kontaktpersonen der Kategorie III, dabei handelt es sich um medizinisches Personal mit geeigneter Schutzausrüstung, das Kontakt (Abstand weniger als zwei Meter) zu bestätigten COVID-19-Fällen hat (Stand: 28. Februar 2020).[123]
In Deutschland wird Personen der Kategorie I unter Abwägung der Möglichkeiten und nach Risikobewertung des Gesundheitsamtes eine häusliche Absonderung mit regelmäßiger Gesundheitsüberwachung (bis zum 14. Tag nach dem letzten Kontakt mit dem bestätigten Infektionsfall) empfohlen, dabei sollen die Kontaktpersonen ein Tagebuch führen, in dem die Körpertemperatur, Symptome und mögliche weitere Kontaktpersonen notiert werden. Das Gesundheitsamt meldet sich täglich, um sich über den Gesundheitszustand informieren zu lassen. Die Kontaktpersonen werden über das COVID-19-Krankheitsbild informiert und sollen namentlich registriert werden. Falls während der häuslichen Quarantäne Symptome auftreten, die auf eine SARS-CoV-2-Infektion hindeuten, wird die Kontaktperson als Verdachtsfall angesehen und nach Rücksprache mit dem Gesundheitsamt eine diagnostische Abklärung veranlasst.[123]
Personen der Kategorie II wird eine häusliche Absonderung auf freiwilliger Basis nahegelegt, eine namentliche Registrierung ist optional. Auch hier gilt, dass bei Eintreten von Symptomen unverzüglich das Gesundheitsamt zu informieren ist. Bei der häuslichen Absonderung ist u. a. die Kontaktperson zeitlich und räumlich von anderen Haushaltsmitgliedern zu trennen und auf die Hygiene (Händewaschen, Hustenetikette) zu achten.[123]
Das Management von Personen der Kategorie III dient dazu, nosokomiale Übertragungen des Virus zu vermeiden. Dabei gilt, dass das medizinische Personal durch die Verwendung der persönlichen Schutzausrüstung (PSA) vor Infektionen geschützt ist, aber darüber hinaus durch Schulungen und organisatorische Maßnahmen verhindert werden soll, dass es zu Virusübertragungen im Arbeitsbereich kommt. Nach Möglichkeit soll das medizinische Personal, das COVID-19-Patienten versorgt, nicht mit der Versorgung anderer Patienten beauftragt werden. Das medizinische Personal soll sensibilisiert werden und sich selbst auf Symptome überwachen, die Ergebnisse wie auch die verwendete PSA sollen in einem Tagebuch notiert werden.[123]
Impfung gegen andere Infektionen
Die Berliner Senatsgesundheitsverwaltung empfahl Ende Februar 2020 allen Menschen über 60 Jahre und chronisch Kranken, ihren Impfstatus zu überprüfen und gegebenenfalls die Impfung gegen Pneumokokken und Keuchhusten (Pertussis) durchführen oder auffrischen zu lassen. Denn eine Primärinfektion mit Pneumokokken oder Keuchhusten birgt ein hohes Risiko eines schweren Verlaufs bei einer Ansteckung mit SARS-CoV. Da Menschen über 60 Jahren und chronisch Kranke durch SARS-CoV besonders gefährdet sind, seien sie vorsorglich zu schützen.[124][125]
Epidemiologie
Nachdem der WHO bis zum 3. Januar 2020 insgesamt 44 Erkrankte gemeldet worden waren, verstarb am 9. Januar 2020 (Ortszeit) erstmals einer der Erkrankten, ein 61-jähriger Mann,[126] und am 15. Januar 2020 verstarb ein zweiter Erkrankter (im Alter von 69 Jahren) an den Folgen der Virusinfektion.[127]
Am 13. Januar 2020 wurde der erste Erkrankungsfall außerhalb Chinas bekannt. Es handelte sich um eine aus Wuhan am 8. Januar 2020 nach Bangkok (Thailand) eingereiste 61-jährige Frau.[128][129]
Am 20. Januar 2020 berichteten die chinesischen Behörden über einen starken Anstieg der Neuerkrankungen mit 139 neuen Fällen am 18./19. Januar 2020, davon einige auch außerhalb Wuhans in Shenzhen und Peking. Ein weiterer durch das Virus verursachter Todesfall und der erste Fall aus Südkorea wurden gemeldet.[130] Die chinesischen Behörden bestätigten zudem, dass sich Infektionen durch Mensch-zu-Mensch-Übertragung ereignet hatten.[12][28]
An den folgenden Tagen wurden der WHO täglich neue Erkrankungen aus China gemeldet, die Anzahl der Erkrankten erhöhte sich bis zum 26. Januar 2020 weltweit auf mehr als 2000 und die Anzahl der Todesfälle auf mehr als 50.[131] Auch an den folgenden Tagen erhöhten sich die gemeldeten Fallzahlen sprunghaft, so dass am 31. Januar 2020 bereits fast 10.000 Infizierte und mehr als 200 Todesfälle,[131] am 10. Februar mehr als 40.000 Infizierte und mehr als 900 Todesfälle[131] und am 22. Februar mehr als 77.000 Infizierte und mehr als 2.300 Todesfälle[131] der WHO gemeldet worden waren.
Am 27. Januar 2020 wurden erstmals auch in Deutschland Infektionen nachgewiesen.[132] Zunächst bei einem 33-jährigen Mann aus dem Landkreis Landsberg am Lech, der von einer Chinesin – der Indexpatientin – infiziert worden war, die sich vom 19. bis 22. Januar auf Dienstreise in dem Unternehmen Webasto SE in Bayern aufgehalten hatte. Zunächst hatte es geheißen, bei ihr seien Anzeichen für eine Infektion erst während des Rückflugs nach China aufgetreten;[69] tatsächlich hatte sie aber bereits zuvor aufgrund erster Symptome fiebersenkende Mittel eingenommen.[70] Bereits am Abend des 28. Januar wurde bekannt gegeben, dass sich auch drei Kollegen des 33-Jährigen mit SARS-CoV-2 infiziert hatten.[133] An den folgenden Tagen wurde das Virus bei mehreren Kontaktpersonen der Indexpatientin und bei Angehörigen der in Bayern infizierten Personen nachgewiesen, darunter ein fünfjähriges Kind.[118][134] Ab dem 22. Februar 2020 stieg die Anzahl der Infektionsfälle in Italien deutlich an.[131]
Am Abend des 30. Januar 2020 erklärte die Weltgesundheitsorganisation (WHO) die Epidemie zu einer Gesundheitlichen Notlage internationaler Tragweite.[135] Am 9. Februar 2020 überstieg die Zahl der registrierten Todesfälle mit über 800 die Gesamtzahl der Todesfälle bei der SARS-Pandemie 2002/2003.[45]
Meldepflicht und ICD-10-Einordnung
In Deutschland ist laut Infektionsschutzgesetz (§ 6) das Auftreten einer bedrohlichen übertragbaren Erkrankung an das zuständige Gesundheitsamt zu melden. Mit Wirkung vom 1. Februar 2020 wurde mittels Verordnung durch das Bundesministerium für Gesundheit (Verordnungsermächtigung nach § 15 IfSG) eine Ausdehnung der Meldepflicht beschlossen. Demnach sind sowohl der Verdacht einer Erkrankung, die Erkrankung und der Tod als auch der laborchemische Nachweis einer akuten Infektion mit dem neuartigen Coronavirus meldepflichtig. Die Meldung des Verdachts hat nur zu erfolgen, wenn der Verdacht sowohl durch das klinische Bild als auch durch einen wahrscheinlichen epidemiologischen Zusammenhang begründet ist. Diese Verordnung gilt bis zum 1. Februar 2021,[veraltet] sofern nicht mit Zustimmung des Bundesrates etwas anderes verordnet wird.[136]
Am 17. Februar 2020 wurde die Krankheit durch die WHO in die Internationale statistische Klassifikation der Krankheiten und verwandter Gesundheitsprobleme in der aktuellen, international gültigen Ausgabe ICD-10-WHO aufgenommen (Schlüsselnummer U07.1). Auch für die in Deutschland geltende ICD-10-GM (German Modification) wurde ein sekundärer Kode (Ausrufezeichenschlüsselnummer) vergeben (U07.1!) und die Krankheit als COVID-19 Coronavirus-Krankheit-2019 bezeichnet.[137] Weiterhin erfolgte eine entsprechende Ergänzung für die Todesursachenkodierung in der ICD-10-GM.[12]
Weblinks
- COVID-19 (Coronavirus SARS-CoV-2). Übersichtsseite des Robert Koch-Instituts (RKI). In: rki.de. Robert Koch-Institut, 28. Februar 2020 (wird laufend aktualisiert).
- Antworten auf häufig gestellte Fragen zum Coronavirus SARS-CoV-2. In: rki.de. Robert Koch-Institut, 28. Februar 2020 (wird laufend aktualisiert).
- COVID-19 (Coronavirus SARS-CoV-2): Risikogebiete. In: rki.de. Robert Koch-Institut, 27. Februar 2020 (wird laufend aktualisiert).
- Antworten auf häufig gestellte Fragen zum neuartigen Coronavirus (SARS-CoV-2). In: infektionsschutz.de. Bundeszentrale für gesundheitliche Aufklärung, 28. Februar 2020 (wird wöchentäglich aktualisiert).
- Kann das neuartige Coronavirus über Lebensmittel und Spielzeug übertragen werden? Aktualisierte Fragen und Antworten des BfR vom 24. Februar 2020. In: bfr.bund.de. Bundesinstitut für Risikobewertung, 24. Februar 2020, abgerufen am 29. Februar 2020.
- Aktuelle Informationen zum Coronavirus. In: bundesgesundheitsministerium.de. Bundesministerium für Gesundheit (Deutschland), 29. Februar 2020 (wird laufend aktualisiert).
- Coronavirus. In: sozialministerium.at. Bundesministerium für Soziales, Gesundheit, Pflege und Konsumentenschutz (Österreich), 29. Februar 2020 (wird laufend aktualisiert).
- Neues Coronavirus. In: bag.admin.ch. Bundesamt für Gesundheit (Schweiz), 29. Februar 2020 (wird laufend aktualisiert).
- Q & A on COVID-19. In: ecdc.europa.eu. Europäisches Zentrum für die Prävention und die Kontrolle von Krankheiten, 16. Februar 2020, abgerufen am 29. Februar 2020 (englisch).
- Weltgesundheitsorganisation: Coronavirus disease (COVID-19) outbreak. In: who.int. (englisch, wird laufend aktualisiert).
- Terra X: Das neue Coronavirus wissenschaftlich geprüft. In: zdf.de. 30. Januar 2020.
- The Novel Coronavirus Pneumonia Emergency Response Epidemiology Team: Vital Surveillances: The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19) – China, 2020. In: Website Chinese Center for Disease Control and Prevention (CCDC) weekly. 21. Februar 2020, abgerufen am 1. März 2020 (englisch).
Einzelnachweise
- ↑ a b c Alexander E. Gorbalenya, Susan C. Baker, Ralph S. Baric, Raoul J. de Groot, Christian Drosten, Anastasia A. Gulyaeva, Bart L. Haagmans, Chris Lauber, Andrey M Leontovich, Benjamin W. Neuman, Dmitry Penzar, Stanley Perlman, Leo L.M. Poon, Dmitry Samborskiy, Igor A. Sidorov, Isabel Sola, John Ziebuhr: Severe acute respiratory syndrome-related coronavirus: The species and its viruses – a statement of the Coronavirus Study Group. In: bioRxiv. 11. Februar 2020, S. 1–20, doi:10.1101/2020.02.07.937862 (englisch, biorxiv.org).
- ↑ Alissa Eckert, MS, Dan Higgins, MAM: ID#: 23312. In: Centers for Disease Control and Prevention (Hrsg): Public Health Image Library (PHIL). 2020, Abgerufen am 26. Februar 2020.
- ↑ National Institute of Allergy and Infectious Diseases: New Images of Novel Coronavirus SARS-CoV-2 Now Available. In: nih.gov. 13. Februar 2020. Vgl. Novel Coronavirus 2019. In: flickr.com. Februar 2020. Abgerufen am 26. Februar 2020.
- ↑ a b Nicky Phillips, Smriti Mallapaty, David Cyranoski: How quickly does the Wuhan virus spread? In: Nature. 21. Januar 2020, doi:10.1038/d41586-020-00146-w (englisch).
- ↑ a b Novel Coronavirus (2019-nCoV). (PDF; 1,0 MB) Situation Report – 22. WHO, 11. Februar 2020, abgerufen am 13. Februar 2020.
- ↑ Fast 100 weitere Tote durch Covid-19 in China. Süddeutsche Zeitung, 12. Februar 2020, abgerufen am 13. Februar 2020 (Direkt aus dem dpa-Newskanal).
- ↑ Stephanie Hegarty: The Chinese doctor who tried to warn others about coronavirus. BBC News, 6. Februar 2020, abgerufen am 6. Februar 2020 (englisch).
- ↑ a b c d Na Zhu, Dingyu Zhang, Wenling Wang, Xingwang Li, Bo Yang, Jingdong Song, Xiang Zhao, Baoying Huang, Weifeng Shi, Roujian Lu, Peihua Niu, Faxian Zhan, Xuejun Ma, Dayan Wang, Wenbo Xu, Guizhen Wu, George F. Gao, Wenjie Tan for the China Novel Coronavirus Investigating and Research Team: A Novel Coronavirus from Patients with Pneumonia in China, 2019. In: The New England Journal of Medicine. 24. Januar 2020, doi:10.1056/NEJMoa2001017 (englisch).
- ↑ Pneumonia of unknown cause – China. Website der WHO, 5. Januar 2020, abgerufen am 14. Januar 2020 (englisch).
- ↑ New virus surging in Asia rattles scientists. nature.com, 20. Januar 2020, abgerufen am 28. Januar 2020 (englisch).
- ↑ WHO Statement Regarding Cluster of Pneumonia Cases in Wuhan, China. WHO, 9. Januar 2020, abgerufen am 14. Januar 2020 (englisch).
- ↑ a b c d e f g h i j k Antworten auf häufig gestellte Fragen zum Coronavirus SARS-CoV-2. In: Website des Robert Koch-Instituts. 25. Februar 2020, abgerufen am 26. Februar 2020.
- ↑ a b c F. Wu, S. Zhao, B. Yu, Y.-M. Chen, W. Wang, Y. Hu, Z.-G. Song, Z.-W. Tao, J.-H. Tian, Y.-Y. Pei, M. L. Yuan, Y.-L. Zhang, F.-H. Dai, Y. Liu, Q.-M. Wang, J.-J. Zheng, L. Xu, E. C. Holmes, Y.-Z. Zhang: Wuhan seafood market pneumonia virus isolate Wuhan-Hu-1, complete genome. In: Website Nucleotide des National Center for Biotechnology Information (NCBI). Abgerufen am 4. Februar 2020.
- ↑ WHO: Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. Auf: who.int vom 14. Januar 2020.
- ↑ Karola Neubert: Erster Test für das neuartige Coronavirus in China ist entwickelt. In: Website Informationsdienst Wissenschaft (idw). 16. Januar 2020, abgerufen am 9. Februar 2020.
- ↑ a b Victor M. Corman, Tobias Bleicker, Sebastian Brünink, Christian Drosten, Olfert Landt, Marion P. G. Koopmans, Maria Zambon, Malik Peiris: Diagnostic detection of 2019-nCoV by real-time RT-PCR (protocol-v2-1). Hrsg.: Charité Virologie, Berlin. 17. Januar 2019, S. 1–13 (PDF, 1, MB [abgerufen am 1. Februar 2020]).
- ↑ Novel Coronavirus (2019-nCoV). ( vom 28. Januar 2020 im Internet Archive)
- ↑ Taxonomy ID: 2697049 Wuhan seafood market pneumonia virus. ( vom 3. Februar 2020 im Internet Archive)
- ↑ Ching-Tse Cheng: WHO declines to name new pneumonia after 'China' or 'Wuhan'. Taiwan News, 14. Januar 2020, abgerufen am 14. Januar 2020 (englisch).
- ↑ WHO issues best practices for naming new human infectious diseases. Weltgesundheitsorganisation, 8. Mai 2015, abgerufen am 6. Februar 2020 (englisch).
- ↑ Taxonomy Browser Severe acute respiratory syndrome coronavirus 2, Taxonomy ID: 2697049. In: Website National Center for Biotechnology Information (NCBI). Abgerufen am 16. Februar 2020 (englisch).
- ↑ a b c d Lars Fischer, Alina Schadwinkel: Verursacht das Coronavirus Engpässe bei Medikamenten? Stammt das Virus aus dem Pangolin? Website Spektrum.de, 10. Februar 2020, abgerufen am 15. Februar 2020.
- ↑ Shibo Jiang, Zhengli Shi, Yuelong Shu, Jingdong Song, George F. Gao, Wenjie Tan, Deyin Guo: A distinct name is needed for the new coronavirus. In: The Lancet. 19. Februar 2020, doi:10.1016/S0140-6736(20)30419-0 (englisch).
- ↑ a b c d Kristian G. Andersen, Andrew Rambaut, W. Ian Lipkin, Edward C. Holmes, Robert F. Garry: The Proximal Origin of SARS-CoV-2, auf: virologica.org, Quelle: ARTIC Network, 17. Februar 2020
- ↑ a b c d e NCBI Database Nucleotide, txid2697049 (Severe acute respiratory syndrome coronavirus 2). In: Website Nucleotide des National Center for Biotechnology Information (NCBI). Abgerufen am 16. Februar 2020.
- ↑ Matthew Frieman, Ralph Baric: Mechanisms of Severe Acute Respiratory Syndrome Pathogenesis and Innate Immunomodulation. In: Microbiology and Molecular Microbiology Reviews. Band 72, Dezember 2008, S. 672–685, doi:10.1128/MMBR.00015-08, PMID 19052324 (englisch, open access).
- ↑ Wuhan seafood market pneumonia virus. In: Website Genome des National Center for Biotechnology Information (NCBI). Abgerufen am 16. Februar 2020.
- ↑ a b c d e f g h i Jasper Fuk-Woo Chan, Shuofeng Yuan, Kin-Hang Kok, Kelvin Kai-Wang To, Hin Chu, Jin Yang, Fanfan Xing, Jieling Liu, Cyril Chik-Yan Yip, Rosana Wing-Shan Poon, Hoi-Wah Tsoi, Simon Kam-Fai Lo, Kwok-Hung Chan, Vincent Kwok-Man Poon, Wan-Mui Chan, Jonathan Daniel Ip, Jian-Piao Cai, Vincent Chi-Chung Cheng, Honglin Chen, Christopher Kim-Ming Hui, Kwok-Yung Yuen: A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster. In: The Lancet. 24. Januar 2020, doi:10.1016/S0140-6736(20)30154-9 (englisch).
- ↑ a b Hufeisennasenfledermäuse, auf: Schutzgemeinschaft Deutscher Wald, Oberursel vom 16. Dezember 2015
- ↑ a b c d e Peng Zhou, Xing-Lou Yang, Xian-Guang Wang, Ben Hu, Lei Zhang, Wei Zhang, Hao-Rui Si, Yan Zhu, Bei Li, Chao-Lin Huang, Hui-Dong Chen, Jing Chen, Yun Luo, Hua Guo, Ren-Di Jiang, Mei-Qin Liu, Ying Chen, Xu-Rui Shen, Xi Wang, Xiao-Shuang Zheng, Kai Zhao, Quan-Jiao Chen, Fei Deng, Lin-Lin Liu, Bing Yan, Fa-Xian Zhan, Yan-Yi Wang, Geng-Fu Xiao, Zheng-Li Shi: A pneumonia outbreak associated with a new coronavirus of probable bat origin. In: Nature. 3. Februar 2020, doi:10.1038/s41586-020-2012-7 (englisch, dieser Artikel wurde am 23. Januar 2020 vorab ohne Peer-Review auf bioRxiv veröffentlicht).
- ↑ D. Paraskevis, E. G. Kostaki, G. Magiorkinis, G. Panayiotakopoulos, G. Sourvinos, S. Tsiodras: Full-genome evolutionary analysis of the novel corona virus (2019-nCoV) rejects the hypothesis of emergence as a result of a recent recombination event. In: bioRxiv. 27. Januar 2020, doi:10.1101/2020.01.26.920249 (englisch).
- ↑ a b c d Roujian Lu, Xiang Zhao, Juan Li, Peihua Niu, Bo Yang, Honglong Wu, Wenling Wang, Hao Song, Baoying Huang, Na Zhu, Yuhai Bi, Xuejun Ma, Faxian Zhan, Liang Wang, Tao Hu, Hong Zhou, Zhenhong Hu, Weimin Zhou, Li Zhao, Jing Chen, Yao Meng, Ji Wang, Yang Lin, Jianying Yuan, Zhihao Xie, Jinmin Ma, William J Liu, Dayan Wang, Wenbo Xu, Edward C Holmes, George F Gao, Guizhen Wu, Weijun Chen, Weifeng Shi, Wenjie Tan: Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. In: The Lancet. 29. Januar 2020, doi:10.1016/S0140-6736(20)30251-8 (englisch).
- ↑ Genom-Analysen klären Herkunft von 2019-nCoV. In: Website Deutsches Ärzteblatt. 30. Januar 2020, abgerufen am 9. Februar 2020.
- ↑ a b c 2019-nCoV: Erste Bilder vom Virus und Erkenntnisse zum klinischen Verlauf. In: Website Deutsches Ärzteblatt. 27. Januar 2020, abgerufen am 11. Februar 2020.
- ↑ a b Ewen Callaway, David Cyranoski: Why snakes probably aren’t spreading the new China virus – One genetic analysis suggests reptilian reservoir — but researchers doubt that the coronavirus could have originated in animals other than birds or mammals. In: Nature. 23. Januar 2020, doi:10.1038/d41586-020-00180-8 (englisch).
- ↑ Weltorganisation für Tiergesundheit (OIE): Immediate notification. Tai Hang, Islands District, Hong Kong. Auf: oie.int vom 29. Februar 2020.
- ↑ Noah Higgins-Dunn: A dog in Hong Kong tests positive for the coronavirus, WHO officials confirm. 28. Februar 2020, abgerufen am 29. Februar 2020 (englisch).
- ↑ Wei Ji, Wei Wang, Xiaofang Zhao, Junjie Zai, Xingguang Li: Homologous recombination within the spike glycoprotein of the newly identified coronavirus may boost cross‐species transmission from snake to human. In: Journal of Medical Virology. 22. Januar 2020, doi:10.1002/jmv.25682 (englisch).
- ↑ Researchers trace coronavirus outbreak in China to snakes. In: Website EurekAlert! 22. Januar 2020, abgerufen am 26. Januar 2020 (englisch).
- ↑ Coronavirus: How worried should we be? BBC News, 27. Januar 2020, abgerufen am 27. Januar 2020 (englisch).
- ↑ David Cyranoski: Did pangolins spread the China coronavirus to people? In: Nature. 7. Februar 2020, doi:10.1038/d41586-020-00364-2 (englisch).
- ↑ a b Informationen der BAuA: Neuartiges Virus SARS-CoV-2 (bislang 2019-nCoV) durch den ABAS in Risikogruppe 3 eingestuft und Empfehlungen zur Labordiagnostik gegeben. In: Website der Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA). 19. Februar 2020, abgerufen am 23. Februar 2020.
- ↑ a b c Beschluss 1/2020 des ABAS vom 19.2.2020 und Begründung zur vorläufigen Einstufung des Virus SARS-CoV-2 in Risikogruppe 3 und Empfehlungen zu nicht gezielten Tätigkeiten (Labordiagnostik) und gezielten Tätigkeiten mit SARS-CoV-2. (PDF; 140 kB) In: Website der Bundesanstalt für Arbeitsschutz und Arbeitsmedizin. 19. Februar 2020, abgerufen am 23. Februar 2020.
- ↑ Interim Laboratory Biosafety Guidelines for Handling and Processing Specimens Associated with Coronavirus Disease 2019 (COVID-19). In: Website der US-amerikanischen Centers for Disease Control and Prevention (CDC). 16. Februar 2020, abgerufen am 23. Februar 2020 (englisch).
- ↑ a b c d Zhangkai J. Cheng, Jing Shan: 2019 Novel coronavirus: where we are and what we know. In: Infection. 18. Februar 2020, doi:10.1007/s15010-020-01401-y (englisch).
- ↑ a b c How COVID-19 Spreads. In: Website der US-amerikanischen Centers for Disease Control and Prevention (CDC). 17. Februar 2020, abgerufen am 23. Februar 2020 (englisch).
- ↑ Michelle L. Holshue, Chas DeBolt et al. for the Washington State 2019-nCoV Case Investigation Team: First Case of 2019 Novel Coronavirus in the United States. In: The New England Journal of Medicine. 31. Januar 2020, doi:10.1056/NEJMoa2001191 (englisch).
- ↑ Dongyu Guo: Evaluation of coronavirus in tears and conjunctival secretions ofpatients with SARS-CoV-2 infection. Journal of Medical Virology, 18. Februar 2020, doi:10.1002/jmv.25725
- ↑ a b c Lirong Zou, Feng Ruan, Mingxing Huang, Lijun Liang, Huitao Huang, Zhongsi Hong, Jianxiang Yu, Min Kang, Yingchao Song, Jinyu Xia, Qianfang Guo, Tie Song, Jianfeng He, Hui-Ling Yen, Malik Peiris, Jie Wu: SARS-CoV-2 Viral Load in Upper Respiratory Specimens of Infected Patients. In: The New England Journal of Medicine. 19. Februar 2020, doi:10.1056/NEJMc2001737 (englisch).
- ↑ a b Günter Kampf, Daniel Todt, Stephanie Pfaender, Eike Steinmann: Persistence of coronaviruses on inanimate surfaces and its inactivation with biocidal agents. In: The Journal of Hospital Infection. 6. Februar 2020, doi:10.1016/j.jhin.2020.01.022 (englisch).
- ↑ Meike Drießen: Wie lang Coronaviren auf Flächen überleben und wie man sie inaktiviert. In: Website Informationsdienst Wissenschaft (idw). 7. Februar 2020, abgerufen am 8. Februar 2020.
- ↑ Huijun Chen, Juanjuan Guo, Chen Wang, Fan Luo, Xuechen Yu, Wei Zhang, Jiafu Li, Dongchi Zhao, Dan Xu, Qing Gong, Jing Liao, Huixia Yang, Wei Hou, Yuanzhen Zhang: Clinical characteristics and intrauterine vertical transmission potential of COVID-19 infection in nine pregnant women: a retrospective review of medical records. In: The Lancet. 12. Februar 2020, doi:10.1016/S0140-6736(20)30360-3 (englisch).
- ↑ Min Wei, Jingping Yuan, Yu Liu, Tao Fu, Xue Yu, Zhi-Jiang Zhang: Novel Coronavirus Infection in Hospitalized Infants Under 1 Year of Age in China. In: Journal of the American Medical Association. 14. Februar 2020, doi:10.1001/jama.2020.2131 (englisch).
- ↑ a b Li Q, Guan X, Wu P, Wang X, Zhou L, Tong Y, Ren R, Leung KSM, Lau EHY, Wong JY, Xing X, Xiang N, Wu Y, Li C, Chen Q, Li D, Liu T, Zhao J, Li M, Tu W, Chen C, Jin L, Yang R, Wang Q, Zhou S, Wang R, Liu H, Luo Y, Liu Y, Shao G, Li H, Tao Z, Yang Y, Deng Z, Liu B, Ma Z, Zhang Y, Shi G, Lam TTY, Wu JTK, Gao GF, Cowling BJ, Yang B, Leung GM, Feng Z.: Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus–Infected Pneumonia. In: The New England Journal of Medicine. 29. Januar 2020, doi:10.1056/NEJMoa2001316 (englisch).
- ↑ Joseph T. Wu, Kathy Leung, Gabriel M. Leung: Nowcasting and forecasting the potential domestic and international spread of the 2019-nCoV outbreak originating in Wuhan, China: a modelling study. In: The Lancet. 31. Januar 2020, doi:10.1016/S0140-6736(20)30260-9 (englisch).
- ↑ Tao Liu, Jianxiong Hu, Jianpeng Xiao, Guanhao He, Min Kang, Zuhua Rong, Lifeng Lin, Haojie Zhong, Qiong Huang, Aiping Deng, Weilin Zeng, Xiaohua Tan, Siqing Zeng, Zhihua Zhu, Jiansen Li, Dexin Gong, Donghua Wan, Shaowei Chen, Lingchuan Guo, Yan Li, Limei Sun, Wenjia Liang, Tie Song, Jianfeng He, Wenjun Ma: Time-varying transmission dynamics of Novel Coronavirus Pneumonia in China. In: bioRxiv. 13. Februar 2020, doi:10.1101/2020.01.25.919787 (englisch).
- ↑ Ying Liu, Albert A. Gayle, Annelies Wilder-Smith, Joacim Rocklöv: The reproductive number of COVID-19 is higher compared to SARS coronavirus. In: Journal of Travel Medicine. 13. Februar 2020, S. taaa021, doi:10.1093/jtm/taaa021 (englisch).
- ↑ a b Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19). (PDF; 1,6 MB) 16–24 February 2020. Weltgesundheitsorganisation (WHO), 28. Februar 2020, abgerufen am 2. März 2020.
- ↑ a b c Zunyou Wu, Jennifer M. McGoogan, CCDC: Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China. In: Journal of the American Medical Association. 24. Februar 2020, doi:10.1001/jama.2020.2648 (englisch).
- ↑ Novel Coronavirus (2019-nCoV). (PDF; 0,9 MB) Situation Report – 18. WHO, 7. Februar 2020, abgerufen am 8. Februar 2020.
- ↑ Coronavirus disease 2019 (COVID-19) Situation Report – 30. WHO, 19. Februar 2020, abgerufen am 1. März 2020 (englisch).
- ↑ Mike Famulare: 2019-nCoV: preliminary estimates of the confirmed-case-fatality-ratio and infection-fatality-ratio, and initial pandemic risk assessment. Institute for Disease Modeling, 19. Februar 2020 (github.io [abgerufen am 27. Februar 2020]).
- ↑ a b Nanshan Chen, Min Zhou, Xuan Dong, Jieming Qu, Fengyun Gong, Yang Han, Yang Qiu, Jingli Wang, Ying Liu, Yuan Wei, Jia'an Xia, Ting Yu, Xinxin Zhang, L. i. Zhang: Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. In: The Lancet. 30. Januar 2020, doi:10.1016/S0140-6736(20)30211-7.
- ↑ Sung-mok Jung, Andrei R. Akhmetzhanov, Katsuma Hayashi, Natalie M. Linton, Yichi Yang, Baoyin Yuan, Tetsuro Kobayashi, Ryo Kinoshita, Hiroshi Nishiura: Real time estimation of the risk of death from novel coronavirus (2019-nCoV) infection: Inference using exported cases. In: medRxiv. 2. Februar 2020, doi:10.1101/2020.01.29.20019547 (englisch).
- ↑ D. Wang, B. Hu, C. Hu et al.: Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus–Infected Pneumonia in Wuhan, China. In: Journal of the American Medical Association. 7. Februar 2020, doi:10.1001/jama.2020.1585 (englisch).
- ↑ a b c Tedros Adhanom Ghebreyesus: WHO Director-General's opening remarks at the media briefing on COVID-19 - 24 February 2020. In: Website Weltgesundheitsorganisation (WHO). 24. Februar 2020, abgerufen am 26. Februar 2020 (englisch).
- ↑ a b Yan Bai, Lingsheng Yao, Tao Wei, Fei Tian, Dong-Yan Jin, Lijuan Chen, Meiyun Wang: Presumed Asymptomatic Carrier Transmission of COVID-19. In: Journal of the American Medical Association. 21. Februar 2020, doi:10.1001/jama.2020.2565 (englisch).
- ↑ Coronavirus disease 2019 (COVID-19). (PDF; 1,1 MB) Situation Report – 30. WHO, 19. Februar 2020, abgerufen am 23. Februar 2020.
- ↑ a b Camilla Rothe, Mirjam Schunk, Peter Sothmann, Gisela Bretzel, Guenter Froeschl, Claudia Wallrauch, Thorbjörn Zimmer, Verena Thiel, Christian Janke, Wolfgang Guggemos, Michael Seilmaier, Christian Drosten, Patrick Vollmar, Katrin Zwirglmaier, Sabine Zange, Roman Wölfel, Michael Hoelscher: Transmission of 2019-nCoV Infection from an Asymptomatic Contact in Germany. In: The New England Journal of Medicine. 30. Januar 2020, doi:10.1056/NEJMc2001468 (englisch).
- ↑ a b Kai Kupferschmidt: Study claiming new coronavirus can be transmitted by people without symptoms was flawed. In: Science. 3. Februar 2020 (englisch, sciencemag.org).
- ↑ Sandra Ciesek et al.: Evidence of SARS-CoV-2 Infection in Returning Travelers from Wuhan, China. NEJM, 18. Februar 2018 doi:10.1056/NEJMc2001899
- ↑ Jing Liu : Asymptomatic cases in a family cluster with SARS-CoV-2 infection. Lancet, 19. Februar 2020, doi:10.1016/S1473-3099(20)30114-6
- ↑ 2019-nCoV offenbar schon bei sehr leichten Symptomen übertragbar. In: Website Deutsches Ärzteblatt. 4. Februar 2020, abgerufen am 5. Februar 2020.
- ↑ Haibo Xu et al. : Positive RT-PCR Test Results in Patients Recovered From COVID-19. JAMA, 27. Februar 2020, doi:10.1001/jama.2020.2783
- ↑ Nach Genesung tauchte SARS-CoV-2 wieder auf. In: Website Ärztezeitung. 28. Februar 2020, abgerufen am 28. Februar 2020.
- ↑ Gesundheitsdienst, Stand 27. Januar 2020. (PDF) Auswärtiges Amt, abgerufen am 27. Januar 2020.
- ↑ a b c Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, Zhang L, Fan G, Xu J, Gu X, Cheng Z, Yu T, Xia J, Wei Y, Wu W, Xie X, Yin W, Li H, Liu M, Xiao Y, Gao H, Guo L, Xie J, Wang G, Jiang R, Gao Z, Jin Q, Wang J, Cao B: Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. In: The Lancet. 24. Januar 2020, doi:10.1016/S0140-6736(20)30183-5 (englisch).
- ↑ Diese Institute bieten den SARS-CoV-2 PCR Test an. In: Website Gesellschaft für Virologie e.V. (GfV). Abgerufen am 25. Februar 2020.
- ↑ a b c d e f g h i COVID-19: Verdachtsabklärung und Maßnahmen – Orientierungshilfe für Ärztinnen und Ärzte. (PDF; 112 kB) In: Website des Robert Koch-Instituts. 26. Februar 2020, abgerufen am 1. März 2020.
- ↑ a b 2019-nCoV: Verdachtsabklärung und Maßnahmen – Orientierungshilfe für Ärztinnen und Ärzte. (PDF; 59 kB) In: Website des Robert Koch-Instituts. 23. Januar 2020, abgerufen am 26. Januar 2020.
- ↑ SARS-CoV-2 / COVID-19 in die Differentialdiagnose einbeziehen. In: Website des Robert Koch-Instituts. 24. Februar 2020, abgerufen am 1. März 2020.
- ↑ a b Jef Akst: Australian Lab Cultures New Coronavirus as Infections Climb. In: Website The-Scientist. 29. Januar 2020, abgerufen am 4. Februar 2020 (englisch).
- ↑ Kathrin Strobel: Was tun bei Verdacht auf Coronavirus 2019-nCoV? In: medical-tribune.de. Medical Tribune Deutschland, 28. Januar 2020, abgerufen am 28. Januar 2020.
- ↑ Xingzhi Xie, Zheng Zhong, Wei Zhao, Chao Zheng, Fei Wang, Jun Liu: Chest CT for Typical 2019-nCoV Pneumonia: Relationship to Negative RT-PCR Testing. In: Radiology. 12. Februar 2020, S. 1–11, doi:10.1148/radiol.2020200343 (englisch).
- ↑ a b Victor M. Corman, Olfert Landt, Marco Kaiser, Richard Molenkamp, Adam Meijer, Daniel K. W. Chu, Tobias Bleicker, Sebastian Brünink, Julia Schneider, Marie Luisa Schmidt, Daphne G. J. C. Mulders, Bart L. Haagmans, Bas van der Veer, Sharon van den Brink, Lisa Wijsman, Gabriel Goderski, Jean-Louis Romette, Joanna Ellis, Maria Zambon, Malik Peiris, Herman Goossens, Chantal Reusken, Marion P. G. Koopmans, Christian Drosten: Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. In: Eurosurveillance. Band 25, Nr. 3, 23. Januar 2020, ISSN 1560-7917, S. 1–8, doi:10.2807/1560-7917.ES.2020.25.3.2000045.
- ↑ Novel Coronavirus (2019-nCoV) technical guidance: Laboratory testing for 2019-nCoV in humans. In: Website WHO. Weltgesundheitsorganisation (WHO), 2020, abgerufen am 5. Februar 2020 (englisch).
- ↑ a b c d e Coronavirus outbreak: New test kit can detect the virus in just 15 minutes. In: Website MSN. 10. Februar 2020, abgerufen am 16. Februar 2020 (englisch).
- ↑ a b c Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. In: Website WHO. Weltgesundheitsorganisation (WHO), 17. Januar 2020, abgerufen am 5. Februar 2020 (englisch).
- ↑ Global Initiative on Sharing All Influenza Data (GISAID). In: Website der GISAID (Bundesrepublik Deutschland als Host (Datenbankanbieter)). Abgerufen am 5. Februar 2020 (englisch).
- ↑ CDC Tests for 2019-nCoV. In: Website der US-amerikanischen Centers for Disease Control and Prevention (CDC). 5. Februar 2020, abgerufen am 10. Februar 2020 (englisch).
- ↑ Stephanie Soucheray: CDC sends out nCoV test kits as Wisconsin confirms case. In: Website der University of Minnesota. CIDRAP – Center for Infectious Disease Research and Policy, 5. Februar 2020, abgerufen am 10. Februar 2020 (englisch).
- ↑ New test kits for coronavirus approved in China. In: Website Xinhua. 30. Januar 2020, abgerufen am 10. Februar 2020 (englisch).
- ↑ China's Jiangsu develops rapid test kit for coronavirus. In: Website Xinhua. 31. Januar 2020, abgerufen am 16. Februar 2020 (englisch).
- ↑ Dean Koh: iHealthtech researchers working on Wuhan novel coronavirus (2019-nCoV) detection kit. In: Website mobi health news der National University of Singapore. 6. Februar 2020, abgerufen am 16. Februar 2020 (englisch).
- ↑ a b c Hildener Unternehmen entwickelt Schnelltest für Corona-Virus. In: Website WDR. 5. Februar 2020, abgerufen am 28. Februar 2020.
- ↑ a b c Pressemitteilung: QIAGEN announces worldwide shipments of QIAstat-Dx test kits for SARS-CoV-2. In: Website Qiagen. 26. Februar 2020, abgerufen am 28. Februar 2020 (englisch).
- ↑ a b Maike Telgheder: Diagnose Coronavirus: Die Industrie entwickelt Schnelltests. In: Website Handelsblatt. 26. Februar 2020, abgerufen am 28. Februar 2020.
- ↑ Hinweise zur Testung von Patienten auf Infektion mit dem neuartigen Coronavirus SARS-CoV-2. In: Website des Robert Koch-Instituts (RKI). 20. Februar 2020, abgerufen am 25. Februar 2020.
- ↑ Institut Pasteur isolates strains of coronavirus 2019-nCoV detected in France. In: Website EurekAlert! 31. Januar 2020, abgerufen am 4. Februar 2020 (englisch).
- ↑ Erstmals nCoV in Deutschland in Zellkultur isoliert. In: Website Institut für Mikrobiologie der Bundeswehr. 31. Januar 2020, abgerufen am 3. Februar 2020.
- ↑ CDC Grows 2019-nCoV Virus in Cell Culture. In: Website der US-amerikanischen Centers for Disease Control and Prevention (CDC). 6. Februar 2020, abgerufen am 10. Februar 2020 (englisch).
- ↑ Zhijian Xu, Cheng Peng, Yulong Shi, Zhengdan Zhu, Kaijie Mu, Xiaoyu Wang, Weiliang Zhu: Nelfinavir was predicted to be a potential inhibitor of 2019 nCov main protease by an integrative approach combining homology modelling, molecular docking and binding free energy calculation. In: bioRxiv. 28. Januar 2020, S. 2020.01.27.921627, doi:10.1101/2020.01.27.921627 (englisch).
- ↑ Jon Cohen: Can an anti-HIV combination or other existing drugs outwit the new coronavirus? In: Science. 27. Januar 2020, doi:10.1126/science.abb0659 (englisch).
- ↑ Xin Liu, Xiu-Jie Wang: Potential inhibitors for 2019-nCoV coronavirus M protease from clinically approved medicines. In: bioRxiv. 29. Januar 2020, doi:10.1101/2020.01.29.924100 (englisch).
- ↑ Catharine I. Paules, Hilary D. Marston, Anthony S. Fauci: Coronavirus Infections – More Than Just the Common Cold. In: Journal of the American Medical Association. 23. Januar 2020, doi:10.1001/jama.2020.0757, PMID 31971553 (englisch).
- ↑ 上海药物所和上海科技大学联合发现一批可能对新型肺炎有治疗作用的老药和中药. Chinese Academy of Sciences, 25. Januar 2020 (chinesisch).
- ↑ Fu-Sheng Wang, Chao Zhang: What to do next to control the 2019-nCoV epidemic? In: The Lancet. Band 395, Nr. 10222, 8. Februar 2020, S. 391–393, doi:10.1016/S0140-6736(20)30300-7 (englisch).
- ↑ Wang Xiaoyu: Drugs with potential against coronavirus in human trials. In: Website China Daily. 15. Februar 2020, abgerufen am 16. Februar 2020 (englisch).
- ↑ Zhang Yangfei: First antiviral drug approved to fight coronavirus. In: Website China Daily. 17. Februar 2020, abgerufen am 17. Februar 2020 (englisch).
- ↑ Wang Xiaoyu: Progress seen in epidemic fight. In: Website China Daily. 20. Februar 2020, abgerufen am 19. Februar 2020 (englisch).
- ↑ Coronavirus: Zaghafte Erfolge bei Medikamentensuche. Wiener Zeitung, 27. Februar 2020, abgerufen am 27. Februar 2020.
- ↑ Alexandra Negt: Malariamittel gegen Coronavirus. Apotheke adhoc, 26. Februar 2020, abgerufen am 28. Februar 2020.
- ↑ Alexandra Negt: Bayer: Resochin geht außer Vertrieb. Apotheke adhoc, 1. November 2019, abgerufen am 28. Februar 2020.
- ↑ Wang Xiaodong: Plasma therapy could lead to development of vaccine for novel coronavirus pneumonia. In: Website China Daily. 17. Februar 2020, abgerufen am 18. Februar 2020 (englisch).
- ↑ Zhang Zhihao: More plasma needed from recovered coronavirus patients, experts say. In: Website China Daily. 17. Februar 2020, abgerufen am 18. Februar 2020 (englisch).
- ↑ Jinnong Zhang, Luqian Zhou, Yuqiong Yang, Wei Peng, Wenjing Wang, Xuelin Chen: Therapeutic and triage strategies for 2019 novel coronavirus disease in fever clinics. In: The Lancet Respiratory Medicine. 13. Februar 2020, doi:10.1016/S2213-2600(20)30071-0 (englisch).
- ↑ Jon Cohen: Scientists are moving at record speed to create new coronavirus vaccines—but they may come too late. In: Science. 27. Januar 2020, doi:10.1126/science.abb0612 (englisch).
- ↑ a b Sechste Infektion bestätigt: Kind in Bayern an Coronavirus erkrankt. In: Website tagesschau.de. 31. Januar 2020, abgerufen am 9. Februar 2020.
- ↑ Florian Schumann: Deutscher Coronavirus-Experte: „Wir müssen uns auf eine Pandemie einstellen“. In: Website Der Tagesspiegel. 13. Februar 2020, abgerufen am 15. Februar 2020.
- ↑ Prof. Dr. Christian Drosten Direktor des Instituts für Virologie, Charité – Universitätsmedizin Berlin: „Wie gefährlich wird das neue Coronavirus?“
- ↑ a b c d Empfehlungen des Robert Koch-Institutes für die Hygienemaßnahmen und Infektionskontrolle bei Patienten mit bestätigter Infektion durch SARS-CoV-2. In: Website des Robert Koch-Instituts. 14. Februar 2020, abgerufen am 1. März 2020.
- ↑ Liste der vom Robert Koch-Institut geprüften und anerkannten Desinfektionsmittel und -verfahren. In: Website des Robert Koch-Instituts. 6. September 2018, abgerufen am 8. Februar 2020.
- ↑ a b c d Kontaktpersonennachverfolgung bei respiratorischen Erkrankungen durch das neuartige Coronavirus (COVID-19, Virusname SARS-CoV-2). In: Website des Robert Koch-Instituts. 28. Februar 2020, abgerufen am 1. März 2020.
- ↑ Gesundheitssenatorin begrüßt Ausweitung des Risikogebiets durch Robert-Koch-Institut. In: berlin.de. 26. Februar 2020, abgerufen am 29. Februar 2020.
- ↑ Coronavirus: Wann gilt der Katastrophenfall - und was folgt? In: rbb24.de. 26. Februar 2020, abgerufen am 29. Februar 2020.
- ↑ Amy Qin, Javier C. Hernández: China Reports First Death From New Virus. The New York Times, 10. Januar 2020, abgerufen am 14. Januar 2020 (englisch).
- ↑ Novel Coronavirus – China. WHO, 12. Januar 2020, abgerufen am 19. Januar 2020 (englisch).
- ↑ Wuhan pneumonia outbreak: First case reported outside China. BBC News, 14. Januar 2020, abgerufen am 14. Januar 2020 (englisch).
- ↑ Neue Lungenkrankheit auch in Thailand. Deutsche Welle, 13. Januar 2020, abgerufen am 14. Januar 2020.
- ↑ China coronavirus: Number of cases jumps as virus spreads to new cities. 20. Januar 2020, abgerufen am 20. Januar 2020 (englisch).
- ↑ a b c d e Novel Coronavirus (2019-nCoV) situation reports; Coronavirus disease (COVID-2019) situation reports. WHO (englisch, abgerufen im Januar bis Februar 2020).
- ↑ Pressemitteilung: Bestätigter Coronavirus-Fall in Bayern – Infektionsschutzmaßnahmen laufen. In: Website Bayerisches Staatsministerium für Gesundheit und Pflege. 27. Januar 2020, abgerufen am 9. Februar 2020.
- ↑ Coronavirus: Drei weitere Fälle in Bayern. In: Website tagesschau.de. 29. Januar 2020, abgerufen am 9. Februar 2020.
- ↑ Pressemitteilung: 7. Fall in München Klinik Schwabing in stabilem Zustand. In: Website Bayerisches Staatsministerium für Gesundheit und Pflege. 27. Januar 2020, abgerufen am 9. Februar 2020.
- ↑ WHO ruft wegen Coronavirus weltweite Notlage aus. Süddeutsche Zeitung, 30. Januar 2020, abgerufen am 30. Januar 2020.
- ↑ Verordnung über die Ausdehnung der Meldepflicht nach § 6 Absatz 1 Satz 1 Nummer 1 und § 7 Absatz 1 Satz 1 des Infektionsschutzgesetzes auf Infektionen mit dem erstmals im Dezember 2019 in Wuhan/Volksrepublik China aufgetretenen neuartigen Coronavirus („2019-nCoV“). Bundesministerium der Justiz und für Verbraucherschutz, Bundesamt für Justiz (Deutschland), 30. Januar 2020, abgerufen am 1. Februar 2020.
- ↑ ICD-10 (WHO und GM): U07.1 kodiert COVID-19, Coronavirus-Krankheit-2019. Deutsches Institut für Medizinische Dokumentation und Information (DIMDI), 17. Februar 2020, abgerufen am 29. Februar 2020.

![Aufnahme von Virionen mit den namensgebenden „Kronen“.[3]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/76/Novel_Coronavirus_SARS-CoV-2.jpg/200px-Novel_Coronavirus_SARS-CoV-2.jpg)